Фкд правой лобной доли что это такое
Хотя отдельные фокальные дисплазии включают участки полимикрогирии (ПМГ), большинство из них обычно не являются полимикрогирии с гистологической точки зрения, поэтому предпочтительнее неоднозначное определение фокальная корковая дисплазия, включающее аномалии как миграции, так и организации, а в отдельных случаях нарушения пролиферации и дифференцировки нейробластов. Значительное число сообщений в литературе об эпилепсии появилось за последние 20 лет (см. Janota и Polkey, 1992, Guerrini и Filippi, 2005). Очаговые дисплазии могут быть обнаружены в любой области коры. Нередко встречается оперкулярная дисплазия (Ambrosetto, 1992, Sebire et al., 1996).
Действительно, многие случаи локализованной кортикальной дисплазии избирательно поражают эту область. В области корковой дисплазии кора уплотнена, а извилины увеличены. Гистологическая картина варьирует от простой дезорганизации пластинок или колонок с субкортикальными гетеротопическими нейронами до более сложных аномалий с гигантскими нейронами и клетками, подвергшимися баллонной дистрофии, а также гигантскими многоядерными астроцитами (Taylor et al; 1971, Tassi et al., 2002; Alonso-Nanclares et al., 2005).
Классификация этих мальформаций с патологической точки зрения остатеся предметом дискуссий (Palmini et al., 2004). Выделено по меньшей мере два типа, известные как тейлоровская и не-тейлоровская кортикальная дисплазия. В недавней классификации (Tassi et al., 2002) выделено три типа: архитектоническая дисплазия, при которой нарушается корковая структура, но гигантские нейроны или аномальные клетки отсутствуют; цитоархитектоническая дисплазия, где в дополнение к патологически организованной коре имеются гигантские и/или дисморфические нейроны; и тейлоровский тип дисплазии, при котором также присутствуют «баллонные клетки», напоминающие повреждения при туберозном склерозе.
Эти клетки окрашиваются как нейрональными, так и глиальными маркерами и являются следствием раннего нарушения клеточной дифференцировки. Кортикальные дисплазии могут поражать любую часть коры и рассматриваются в качестве основной причины очаговой эпилепсии, часто трудно поддающейся лечению. Тейлоровский тип обычно преобладает в лобных и теменных долях, тогда как другие типы чаще встречаются в височных долях (Kuzniecky et al., 1994). Основным клиническим проявлением являются очаговые судороги (Hamiwka et al; 2005, Fauser et al., 2006) часто, но не всегда устойчивые к медикаментозному лечению (см. главу 15). У четырех детей сообщалось о небольших участках корковой дисплазии, которые могли отвечать за очаговый корковый миоклонус и фокальные двигательные судороги (Kuzniecky et al., 1986). Подобные повреждения были обнаружены в случае с эпилептическим статусом (Desbiens et al., 1993).

Большие нейроны неправильно расположены в пределах коры.
Отдельные нейроны с характерной периферической конденсацией хроматина.
В недавних исследованиях микроанатомии, молекулярного патогенеза и патофизиологии этих повреждений описана подробная структура с демонстрацией присущего им эпилептогенного потенциала (Bentivoglio et al., 2003; Alonso-Nanclares et al., 2005; Crino, 2005).
Визуализация данной патологии основывается на MPT исследовании, но выявление может оказаться непростым и потребовать новейших методов МР. Тем не менее, значительная часть случаев может остаться нераспознанной. Тейлоровский тип дисплазии может иметь отличительные МР признаки в виде особенно высокого сигнала в белом веществе под повреждением, иногда распространяющегося до желудочка (так называемая трансмантийная корковая дисплазия) (Barkovich et al., 1997). Архитектонические и цитоархитектонические дисплазии чаще проявляются истонченной корой на MPT (Tassi et al., 2002).
Фокальная кортикальная дисплазия может сопровождаться опухолями дисэмбриогенеза (ганглиоглиомами и нейроэпителиальными опухолями) в этой же области мозга.
Хирургическое лечение эпилепсии в результате очаговой дисплазии возможно в значительной доле случаев и способно купировать судороги (Tassi et al., 2002; Cascino et al., 2004; Fauser et al., 2004, 2006; Hamiwka et al., 2005).
Большинство случаев кортикальной дисплазии относятся к спорадическим, но встречаются и семейные случаи (Kuzniecky et al., 1994).
Некоторые редкие синдромы проявляются напоминающей пахигирию корой в сочетании с внемозговыми аномалиями: врожденный нефроз у мужских сиблингов (Robain и Deonna, 1983; Palm et al., 1986), семейная лимфэдема и агенезия червя мозжечка (Hourihane et al., 1993), врожденная короткая кишка (Nezelof et al., 1976), и семейная пахигирия с диссеминированной кальцификацией мозга и атаксией (Harbord et al., 1990).
Основной интерес при очаговой корковой дисплазии заключается в перспективах хирургического лечения. Этот вопрос будет обсуждаться в отдельной статье на сайте.
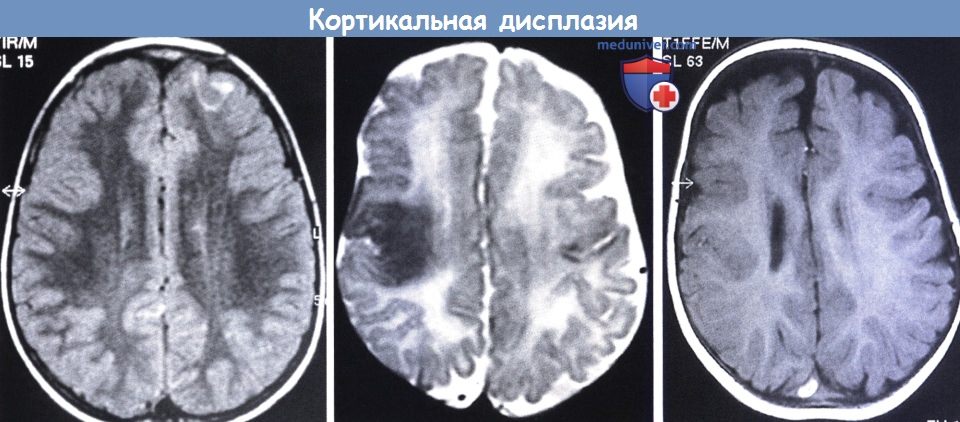
Т2-взвешенная МРТ: определяются области патологической коры в правой лобной доле с высоким сигналом в подлежащей аномальной коре.
После резекции патологического участка был достигнут контроль над судорогами, (в центре) МРТ:
(другой мальчик с судорогами) заметны диспластические участки в возрасте шести месяцев, которые в 18 месяцев стали более очевидными (справа).
— Вернуться в оглавление раздела «Неврология.»
Редактор: Искандер Милевски. Дата публикации: 29.11.2018
Фкд правой лобной доли что это такое
Примечание. * — Манна—Уитни U-тест; ** — без гемисферных; ^ — точный тест Фишера; ^^ — Хи-квадрат; *** — IA — полное прекращение всех приступов; **** — другое — все остальные варианты, начиная с IB и тяжелее. МРТ — магнитно-резонансная томография; ЭКОГ — электрокортикография.
Среди прогностически незначимых факторов оказались: срок заболевания от момента первых приступов до операции — фактор, который постоянно, из работы в работу, упоминается в качестве одного из определяющих в плане прогноза благоприятного исхода, а также тип приступов, среди которых с позитивным исходом обычно связывают фокальные припадки. Наши данные это не подтверждают.
Обсуждение
В отличие от ряда сообщений, содержащих сведения о демографии детей с кортикальными дисплазиями [5, 6], среди наших пациентов также, как и в кооперативном исследовании [7], первые приступы проявились раньше у детей с I типом (медиана — 11 мес). У пациентов со II типом она составила 3 года, и это в большей степени соответствует сведениям Европейского банка данных по изучению исходов хирургического лечения эпилепсии, в котором у 1157 пациентов с КД медиана тоже оказалась равной трем годам.
В остальном наши результаты соответствуют большинству из опубликованных [8—12] и указывают, что пациенты со II типом дисплазии имеют наилучшие шансы благоприятного результата. Это следует учитывать в первую очередь, рассматривая целесообразность хирургического лечения эпилепсии у пациентов с ФКД. В связи с этим возникает ряд вопросов, связанных с достоверностью электро-клинических (ЭЭГ и семиология приступов) и нейровизуализационных (МРТ) признаков этих дисплазий, а также с их локализацией и распространенностью (фокальные и мультилобарные, в критических и функционально менее значимых областях); соответствием фокуса эпилептической активности анатомическим границам диспластичной коры (по МРТ и во время операции); ролью и значением интраоперационной ЭКОГ. И наконец, неясно, как быть с детьми, у которых предполагаются другие типы дисплазии, особенно I тип? Существует ли для них «окно» и некая совокупность признаков и обстоятельств, при которых им все же можно эффективно помочь?
Формирование топического диагноза у больных с ФКД всегда начинается с ЭЭГ и электро-клинической картины приступов, однако исчерпывающую информацию эти сведения дают не более чем в половине случаев [6, 7, 13—16]. Причинами служат возрастные особенности (у детей, в частности, у малышей до 1,5 лет, эпилепсия, имея в основе очаговую причину и фокальное начало, нередко проявляется генерализованными приступами или в виде спазмов с генерализованным иктальным паттерном на ЭЭГ), локализация (при поражении медиобазальной или орбитофронтальной коры и быстром распространении эпилептической активности на обширную поверхность мозгового плаща, порой и на противоположное полушарие), размеры (небольшие, скрытые в глубине борозд ФКД могут вообще никак не проявляться в скальповой ЭЭГ) и т.д. Перечисленные проблемы могут быть отчасти преодолены с помощью МЭГ и инвазивной ЭЭГ (см. рис. 4, 6): МЭГ — благодаря тому, что она более чувствительна к локальной корковой активности по сравнению со скальповой ЭЭГ, а также регистрирует в основном тангенциально ориентированные диполи нейронов коры (в межполушарной щели и в глубине мозговых борозд такое расположение нейронов преобладает) [17, 18], инвазивной ЭЭГ — потому, что она регистрирует активность непосредственно с коры, «не зашумленную» артефактами с покровов свода, и с гораздо лучшим пространственным разрешением, нежели со скальпа.
Рис. 6 (а—б). Пример резекции фокальной кортикальной дисплазии I типа лобно-центральной области слева.
Девочка, 5 лет, праворукая, болеющая эпилепсией с 8 мес. На момент операции — очень частые и резистентные к антиэпилептическому лечению эпилептические спазмы и асимметричные тонические приступы, а также начальные признаки задержки в развитии. Учитывая обширность изменений в лобно-центральных отделах доминантного полушария и неопределенность их границ, операцию ограничили частичной резекцией мальформации в пределах премоторной коры при ориентировке в основном по данным магнитоэнцефалографии и интраоперационной электрокортикографии. После непродолжительного и незначительного уменьшения частоты приступов они возобновились и сохранялись вплоть до последнего осмотра спустя 14 месяцев. Исход IVB. а — слева — интериктальная электроэнцефалография, мультирегиональная эпилептиформная активность (нередко — вплоть до гипсаритмии); б — слева — иктальная электроэнцефалография. Тонический приступ с предшествующей ему редукцией и десинхронизацией активности; диффузный разряд пик-волн, совпадающий с началом клинических проявлений, и последующая диффузная низкоамплитудная быстроволновая активность с включением пиков (fast activity). Справа — дооперационные магнитно-резонансные томограммы в режимах T2 и T2-FLAIR, на которых в коре средней и нижней лобных извилин слева отмечается усиление сигнала и нечеткость ее границ с белым веществом, а также линейный участок повышенного сигнала, распространяющийся от левой прецентральной извилины до тела бокового желудочка (стрелка) и симулирующий «трансмантийный тяж», совпадающий с топографией магнитоэнцефалографических источников инициальных разрядов длительных последовательностей, в том числе иктальных (см. также в).
Рис. 6 (в—г). Пример резекции фокальной кортикальной дисплазии I типа лобно-центральной области слева.
в — результаты локализации источников эпилептиформной активности во сне по данным магнитоэнцефалографии. Зелеными точками отмечены источники интериктальных разрядов как одиночных, так и входящих в состав длительных последовательностей, красными — источники начала длительных последовательностей разрядов, на фоне которых у пациентки возникли два тонических приступа. Следует отметить, что эта же зона первой включалась в генерацию многочисленных и длительных интериктальных последовательностей без клинических проявлений; г — слева — вид операционной раны к моменту завершения субпиального опорожнения коры средней и медиальной лобных извилин кпереди от прецентральной борозды (кора нижней лобной извилины сохранена с учетом доминантности полушария); справа — иммуногистохимический препарат — видны выраженные нарушения корковой архитектоники по смешанному типу (экспрессия NeuN, ×100).
Важно указать также, что ни один из разнообразных патологических паттернов ЭЭГ, как интериктальной, так и иктальной, не может считаться специфическим для ФКД, не говоря уж о том, чтобы предположить их морфологический тип. Одним из немногих более или менее типичных признаков ФКД II типа в интериктальной ЭЭГ считаются вспышки ритмической активности на фоне локального и нерегулярного замедления биоэлектрической активности (см. рис. 5) [19, 20], но такой паттерн встречается далеко не у всех. Ранее мы сообщали о попытке сопоставить находки в ЭЭГ с морфологией ФКД [21]. В случаях со II типом КД начало приступов лишь в 40% совпало с локальной ритмической активностью, порой с предшествующим электродекрементом, а у детей с I типом дисплазии (несколько более частым и, что важнее, синхронным, с манифестацией приступов) оказалось только диффузное уплощение ритмики (см. рис. 6). Зоны интериктальной и приступной активности совпали менее чем у половины.
МРТ в этом отношении информативнее, хотя нельзя не отметить, что в небольшом числе инициально МРТ-негативных наблюдений именно ЭЭГ и электро-клиническая картина приступов стали основанием для пересмотра их изображений и выявления пропущенной поначалу патологии. Привлекательны попытки использования морфометрии и математической обработки изображений с целью выявления малых и недоступных визуальной оценке изменений сигнала [22], однако наиболее важными условиями являются соблюдение протокола МРТ и экспертный уровень ее интерпретации [23].
Описание МРТ признаков кортикальных дисплазий выходит за рамки настоящей работы, а подробности заинтересованный читатель может найти в ряде монографий и других публикациях [5, 14, 24—26].
Здесь же ограничимся общими положениями о том, что зоны с I типом дисплазии на МРТ чаще всего просто не видны, и их приходится обычно угадывать по неспецифическим и косвенным признакам (по уменьшению объема белого вещества и редко встречающемуся и незначительному повышению интенсивности на томограммах, выполненных в режиме T2) (см. рис. 6). Гораздо увереннее распознается II тип по утолщению и гиперинтенсивности на томограммах, выполненных в режимах T2 и FLAIR корковой пластинки, а также по «смазанности» границ между корой и белым веществом в пораженной зоне. Наличие в подкорковом белом веществе конически сужающегося по направлению к боковому желудочку трансмантийного «тяжа» с высокой вероятностью указывает на тип IIb (см. рис. 2—5). Следует отметить, что в большинстве случаев ФКД II типа, особенно типа IIb, МРТ дает весьма четкое представление и об их анатомических границах. Еще важнее то, что на операции ткани мальформаций II типа обычно визуально отличаются от нормального мозга консистенцией, изредка — даже окраской и сосудистым рисунком мягкой оболочки (см. рис. 2, 3, 5), чего мы ни разу не видели у больных с I типом, при котором мозг всегда выглядит обычно.
Любопытно и на первый взгляд даже обескураживает отсутствие сколько-нибудь очевидной связи между результатами операций и феноменом остаточной эпилептической активности при ЭКОГ. Мы использовали этот метод в большинстве случаев с корт-эктомией, и хотя в финале на момент визуально уже иссеченной мальформации порой регистрировали признаки остаточной эпилептической активности в смежных участках внешне здоровой коры, а иногда и за пределами ее обнаженной части, на результате это сказалось не у всех. В половине этих случаев приступы исчезли. Резекция мальформации в пределах анатомических границ оказалась важнее. В этой связи значение ЭКОГ не следует переоценивать (см. табл. 5). Ограничения ЭКОГ известны: во-первых, она обычно лимитирована небольшими промежутками времени (до 5—6 мин) и ограничена территорией обнаженной коры; во-вторых, она требует общей анестезии, искажающей картину биоэлектрической активности мозга, и содержит артефакты, обусловленные хирургической травмой. Не случайно интраоперационную ЭКОГ, десятилетиями считавшуюся стандартом в хирургии эпилепсии, в последнее время практически вытеснила дооперационая инвазивная ЭЭГ [2, 27]. Интраоперационные исследования резервируются на те случаи, когда анатомическая мишень, против ожидавшегося, не распознается, или на ситуации, в которых, кроме очевидного эпилептогенного поражения (каверномы, нейроглиальные опухоли, глиотические рубцы), есть основания для поиска дисплазии в смежных с ними участках коры. Такую ФКД на МРТ обычно не видно.
Располагая только опцией имплантации субдуральных электродов, мы применяли инвазивную ЭЭГ в основном при ФКД в функционально критических зонах мозга с целью картирования функции и уточнения топографии фокуса эпилептической активности в зоне интереса, реже — у больных с несколькими фокусами эпилептической активности и семиотически разными приступами, и во всех случаях получили важную и исчерпывающую информацию. Предлагая это исследование, необходимо учитывать риск осложнений, вероятность которых достигает 7—15%, начиная с гематом и кончая ликвореей, менингитом и остеомиелитом [28—31]. Не менее двух из отдаленных хирургических осложнений у наших пациентов (остеомиелит и резорбция костных лоскутов) связаны с этим исследованием.
Несмотря на высокую стоимость, стандартом инвазивных исследований в наши дни считается стереотаксическая ЭЭГ с помощью множественных многоконтактных погружных электродов. Благодаря ей, кортикография возможна практически в любой зоне (субдуральные электроды непросто, а иногда невозможно безопасно разместить в таких областях, как базальная, медиальная или инсулярная кора), при этом — с высокой точностью и с минимальным риском осложнений [32, 33].
У больных с ФКД проблема осложнений, в особенности нового неврологического дефицита, его вероятности и приемлемости, — центральная, причем как в выборе хирургической опции, как и в показаниях к операции в целом. Безусловно, на этом как-то сказывается доминантность пораженного полушария (больные с левосторонними очагами составили чуть более трети от всех наших пациентов), однако при прочих равных условиях морфологический тип дисплазии — значимый фактор, который нужно иметь в виду. Так, в 4 из 5 случаев настоящей серии, в которых операция привела к стойким неврологическим нарушениям, имелись мальформации I типа. В то же время новый дефицит (геми- или монопарезы) развился лишь в половине из 19 резекций, которые произведены нами у детей с мальформациями в такой критической области, как перироландическая. У большинства имелись ФКД II типа (см. табл. 1, рис. 1), и почти у всех эти нарушения позже постепенно уменьшились или исчезли, а остальные и вовсе выписались без последствий (см. рис. 2, 5).
Феномен смещения функции в сторону от зон с дисплазиями II типа, расположенных в критических областях, упоминается в ряде работ [34—36]. Это логично, поскольку они обусловлены нарушением миграции и запрограммированного апоптоза нервных клеток [37], а период эмбрионального развития, к которому относят их формирование и в который происходит специализация функции коры (в том числе ее сенсомоторных отделов), приходятся почти на один и тот же период гестации (7—12 нед).
Есть сведения о том, что в эпилептогенезе мальформаций типа IIb ведущую роль играют дисморфические гигантские нейроны, а территории с баллонными клетками не эпилептогенны, и, чтобы не рисковать функцией, их можно оставить интактными [38, 39]. В то же время нужно учесть, что, чередуясь, эти различные клеточные формы образуют, в сущности, анатомическую мишень — фрагмент коры, который, отличаясь от нормального мозга по консистенции, имеет границу, которую удается довольно уверенно «уловить» во время субпиальной диссекции и кортэктомии (см. рис. 2, 5).
В случаях с дисплазиями I типа тератогенное воздействие на развивающийся мозг и организующуюся кору приходится позже, ближе к III триместру, а иногда и постнатально, когда ее специализированные участки (зрительная и сенсомоторная кора) уже организованы и функционально сформированы. Кроме того, территория, охваченная такими формами дисплазии, редко ограничивается одной-двумя извилинами. Чаще поражается и становится эпилептогенной обширная зона какого-либо из регионов, которая в немалом числе случаев охватывает несколько смежных долей полушария, без очевидных границ на ЭЭГ и МРТ. Судьба таких детей, в особенности, когда поражен задний (теменно-затылочно-задневисочный) регион полушария, трагична. Обычно они начинают болеть с первых месяцев жизни, чаще в форме эпилептических спазмов, которые не поддаются антиэпилептическому лечению и очень быстро запускают процесс эпилептической энцефалопатии. В таких ситуациях, обсудив неврологический дефицит с родителями и семьей, вместо декортикации разумнее прибегнуть к дисконнекции этих отделов в пределах их анатомических границ, а при еще более обширном поражении — вплоть до гемисферотомии.
В последние годы появился ряд сообщений о роли в происхождении пороков развития мозга соматически патогенных вариантов регуляции мультимолекулярных сигнальных комплексов TORC1 и RORC2, которые регулируют рост и выживание клеток (так называемая механическая мишень рапамицина — mTOR) [40, 41]. В этом смысле ФКД II, особенно IIb, сильно отличаются от дисплазий I типа, которые и «фокальными» в полном смысле этого слова почти никогда не бывают, и во многих отношениях, включая гистологическое строение, ближе к такому состоянию, как туберозный склероз и, возможно, представляют собой его так называемые «forme fruste» варианты (единичная гамартома без других фенотипических признаков этого комплекса). Продолжается дискуссия в отношении принципов классификации кортикальных дисплазий [42—44].
Заключение
Обсуждая прогноз и вероятность благоприятного результата хирургического лечения кортикальной дисплазии с полным прекращением приступов, следует исходить, прежде всего, из предполагаемого типа мальформации. Топографически фокальная кортикальная дисплазия II типа и эпилептогенная зона близко соответствуют друг другу, а мальформации типа IIb чаще всего имеют достаточно отчетливые визуальные границы. Это важные предпосылки для излечивающей резекции и успешности операции, в том числе, когда фокальная кортикальная дисплазия расположена вблизи от функционально критических зон коры, которые, как правило, сформированы и организованы атипично и смещены в сторону от мальформации.
Видимо, есть смысл пересмотреть стандарт проведения резекционных операций и их электрофизиологического сопровождения у больных с кортикальными дисплазиями I типа, сместив акцент с интраоперационной электрокортикографии в сторону дооперационной инвазивной электроэнцефалографии, резервируя электрокортикографию для больных с предположительно III типом мальформаций и на те случаи, когда анатомические границы мальформации, против ожидаемого, визуально не распознаются.
У детей с I типом фокальной кортикальной дисплазии шансов на прекращение приступов путем ограниченных секторальных кортэктомий немного. При этих формах морфологические изменения и эпилептогенная зона обычно обширны, а их границы неопределенные. В части подобных случаев, особенно с катастрофическим течением заболевания, когда операция все же неизбежна, несмотря на вынужденный новый неврологический дефицит следует рассматривать возможности расширенных резекций (лобэктомии) или дисконнекций.
Хирургическое лечение эффективно более чем у половины детей с фармакорезистентной эпилепсией, обусловленной дисплазией коры головного мозга. Рациональный отбор пациентов и их обследование требуют взаимодействия и коллегиального участия команды специалистов, включая эпилептологов, психологов, рентгенологов, физиологов и нейрохирургов. Обследование и лечение таких больных необходимо концентрировать в центрах, располагающих оборудованием, инфраструктурой и штатом соответствующих специалистов.
Участие авторов:
Концепция и дизайн исследования — Меликян А.Г., Воробьев А.Н., Власов П.А.
Сбор и обработка материала — Меликян А.Г., Воробьев А.Н., Власов П.А., Шишкина Л.В., Коптелова А.М., Айвазян С.О., Шульц Е.И., Корсакова М.Б., Козлова А.Б., Демин М.О., Буклина С.Б.
Статистическая обработка данных — Агрба С.Б.
Написание текста — Меликян А.Г.
Редактирование — Меликян А.Г., Власов П.А., Шишкина Л.В., Коптелова А.М., Шульц Е.И., Козлова А.Б., Буклина С.Б., Шевченко А.М.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.






