Антибиотики нового поколения: за и против
Антибиотики – это вещества биологического или полусинтетического происхождения. Применяются в лечебной практике для борьбы с болезнетворными микробами, вирусами. До появления этих медпрепаратов статус неизлечимых болезней был у брюшного тифа, дизентерии, пневмонии, туберкулеза. Сегодня лечение заболеваний инфекционного характера возможно с применением 1-6 поколения антибиотиков.
На этот момент фармакологическая индустрия выпускает более 2000 разновидностей лекарственных средств подобного типа. Медики описали действие около 600 позиций, а во врачебной практике используются порядка 120-160 препаратов.
Важно! При любом заболевании принимать антибиотики рекомендуется после консультации с врачом. В противном случае может развиться антибиотикорезистентность (снижение чувствительности патогенных микроорганизмов к антибактериальным средствам).
Классификация антибиотиков
Все антибактериальные средства можно разделить на 5 категорий по характеристикам и спектру применения. Рассмотрим эту классификацию подробнее:
Спектр действия
Различают антибактериальные средства:
По составу
Антибактериальные препараты делят на 6 групп:
Поколения препаратов. У передовых антимикробных препаратов насчитывается уже шесть генераций. Например, пенициллин был первым средством природного происхождения, тогда как третья или шестая генерация – это уже улучшенная версия, которая включает в состав сильнейшие ингибиторы. Зависимость прямая: чем новее генерация, тем эффективнее воздействие препаратов на патогенную микрофлору.
По способу приема. Пероральные – принимают через рот. Это различные сиропы, таблетки, растворимые капсулы, суспензии. Парентеральные – вводятся внутривенно или внутримышечно. Они быстрее дают эффект, чем пероральные лекарства. Ректальные препараты вводятся в прямую кишку.
Важно! Принимать антибиотики допускается только после консультации с врачом, иначе разовьется антибиотикорезистентность.
Антибактериальные средства нового поколения
Отличие последних генераций антибиотиков от их ранних версий в более совершенной формуле действующего вещества. Активные компоненты точечно устраняют только патологические реакции в клетке. Например, кишечные антибиотики нового поколения не нарушают микрофлору ЖКТ. При этом они борются с целой «армией» возбудителей инфекций.
Новейшие антибактериальные препараты делятся на пять групп:
Рассмотрим несколько известных противомикробных средств импортного и российского производства.
Амоксициллин – импортный противомикробный препарат из группы пенициллинов. Используется во врачебной практике для лечения бактериальной инфекции. Эффективен при кишечных инфекциях, гайморите, ангине, болезни Лайма, дизентерии, сепсисе.
Авелокс – медпрепарат последней генерации из группы фторхинолонов. Отличается сильнейшим воздействием на бактериальные и атипичные возбудители. Не вредит почкам и ЖКТ. Используется при острых, хронических заболеваниях.
Цефалоспорины – антибиотики третьего поколения. К этой группе относят Цефтибутен, Цефтриаксон и другие. Используются для лечения пиелонефрита, пневмонии. В целом это безопасные средства с малым количеством побочных действий. Однако их нужно принимать только после консультации с врачом. Медпрепаратов много, а какой именно выбрать – порекомендует специалист.
Дорипрекс – импортный противомикробный препарат синтетического происхождения. Показал хорошие результаты при лечении пневмонии, запущенных интраабдоминальных инфекций, пиелонефритах.
Инваз – антибактериальное средство из группы карбапенемов. Выпускается в ампулах для парентерального способа применения. Показывает быстрый эффект при лечении бактериальных расстройств кожи, мягких тканей, инфекциях мочевыводящих путей, пневмонии, септицемиях.
Аугметин – полусинтетический пенициллин третьей генерации с добавлением усиливающих ингибиторов. Педиатрами признается лучшим комплексным медпрепаратом для лечения детских гайморита, бронхита, тонзиллита и других инфекций дыхательных путей.
Цефамандол – антибактериальное средство российского производства. Относится к группе цефалоспоринов третьего поколения. Используется для лечения кишечных инфекций, возбудителей инфекций половых органов. Как противомикробное средство обширного диапазона воздействия применяется при простудных заболеваниях.
Лучшие антибактериальные препараты широкого диапазона действия
Противомикробные средства новой генерации обычно синтезируют из природного сырья и стабилизируют в лабораториях. Это помогает усилить эффект лекарства на патогенную микрофлору.
Какие препараты самые сильные? Врачи относят к таким антибактериальные средства широкого спектра воздействия. Приведем ниже краткий список препаратов по названиям:
Резюме
Мы рассмотрели российские и импортные антибиотики широкого спектра действия, кратко описали классификацию препаратов. Ответим на вопрос: какие антибактериальные средства выбрать?
Важно понимать, противомикробные лекарства для обширного применения обладают токсичностью, поэтому негативно влияют на микрофлору. Кроме того, бактерии мутируют, а значит препараты теряют свою эффективность. Поэтому антибактериальные средства с новейшей структурой будут в приоритете, чем их ранние аналоги.
Самолечение антибиотиками опасно для здоровья. При инфекционном заболевании первым делом нужно обратиться к врачу. Специалист установит причину болезни и назначит эффективные антибактериальные средства. Самолечение «наугад» приводит к развитию антибиотикорезистентности.
НОВЫЕ ФТОРХИНОЛОНЫ: новые возможности лечения внебольничной пневмонии
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетлив
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетливая тенденция к увеличению смертности от пневмонии во всех развитых странах мира. Причина может быть связана прежде всего с ростом резистентности основных возбудителей внебольничных инфекций дыхательных путей ко многим антибактериальным препаратам. Этим объясняется интерес клиницистов к новым антибактериальным средствам, к которым отмечается меньший уровень резистентности бактерий.
Этиология внебольничной пневмонии непосредственно связана с нормальной микрофлорой «нестерильных» верхних отделов дыхательных путей (полости рта, носа, рото- и носоглотки). Из множества видов микроорганизмов, колонизующих верхние отделы дыхательных путей, лишь некоторые, обладающие повышенной вирулентностью, проникая в нижние дыхательные пути, способны вызывать воспалительную реакцию даже при минимальных нарушениях защитных механизмов. Такими типичными бактериальными возбудителями внебольничной пневмонии являются следующие перечисленные ниже микроорганизмы.
Streptococcus pneumoniae — самый частый возбудитель внебольничной пневмонии у лиц всех возрастных групп (30-50%). Наиболее остро в настоящее время стоит проблема распространения среди пневмококков пенициллинрезистентных штаммов. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований распространения резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью — около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией β-лактамаз, а с модификацией мишени действия антибиотика в микробной клетке — пенициллинсвязывающих белков, поэтому ингибитор-защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно ассоциируется с устойчивостью к цефалоспоринам I-II поколений, макролидам, тетрациклинам, ко-тримоксазолу.
Haemophilus influenzae — второй по частоте возбудитель (10-20%), особенно у лиц, страдающих хроническими обструктивными болезнями легких, а также у курильщиков; высокой природной активностью в отношении гемофильной палочки обладают аминопенициллины, амоксициллин/клавуланат, цефалоспорины II-IV поколений, карбапенемы, фторхинолоны. Основной механизм резистентности H. influenzae связан с продукцией β-лактамаз.
Staphylococcus aureus — нечастый возбудитель пневмонии (около 5%), наиболее опасен для пожилых людей, наркоманов, алкоголиков, после перенесенного гриппа. Препаратами выбора при стафилококковых пневмониях являются оксациллин, также активны амоксициллин/клавуланат, цефалоспорины, фторхинолоны.
Klebsiella pneumoniae — редкий возбудитель внебольничной пневмонии (менее 5%), встречается, как правило, у больных с тяжелыми сопутствующими заболеваниями (сахарный диабет, застойная сердечная недостаточность, цирроз печени и др.). Наиболее высокой природной активностью в отношении этого возбудителя обладают цефалоспорины III-IV поколений, карбапенемы, фторхинолоны.
Определенное значение в этиологии пневмонии имеют также два других микроорганизма, характеризующихся особыми биологическими свойствами и внутриклеточной локализацией в макроорганизме — Micoplasma pneumoniae и Chlamidia pneumoniae. В отношении этих микроорганизмов клинически неэффективны все β-лактамные антибиотики. Наибольшей природной активностью обладают макролиды и тетрациклины, несколько менее активны ранние фторхинолоны.
В настоящее время в качестве основных средств стартовой терапии внебольничной пневмонии в амбулаторной практике обычно рекомендуются аминопенициллины (ампициллин, амоксициллин), защищенные аминопенициллины (амоксициллин/клавуланат), пероральные цефалоспорины II поколения (цефуроксим аксетил), макролиды (эритромицин, кларитромицин, рокситромицин, азитромицин, спирамицин, мидекамицин). При тяжелом течении пневмонии у госпитализированных больных целесообразно применение парентеральных цефалоспоринов III поколения или фторхинолонов. Клиническая эффективность всех указанных препаратов примерно одинакова, однако при лечении внебольничной пневмонии ни один из этих антибиотиков не может считаться идеальным.
Аминопенициллины характеризуются высокой природной активностью в отношении S. pneumoniae (амоксициллин более высокой, чем ампициллин), однако о проблемах, связанных с возрастающим распространением пенициллинрезистентных пневмококков, упоминалось выше. Имеются данные, что амоксициллин пока сохраняет клиническую эффективность в отношении штаммов пневмококка с промежуточной чувствительностью, а также в отношении устойчивых штаммов. Однако можно предположить снижение клинической эффективности амоксициллина при выделении штаммов пневмококка с высоким уровнем резистентности. Аминопенициллины неэффективны при пневмонии, вызванной S. aureus и K. pneumoniae.
Назначение амоксициллина/клавуланата и цефуроксима аксетила предусмотрено большинством международных и отечественных стандартов лечения внебольничной пневмонии ввиду высокой активности против пневмококков, гемофильной палочки, стафилококков. Однако в отношении пенициллинрезистентных пневмококков мы сталкиваемся с теми же проблемами, что и у аминопенициллинов.
Следует подчеркнуть, что все пенициллины и цефалоспорины неактивны в отношении микоплазм, а также хламидий, и поэтому клинически неэффективны при атипичных пневмониях.
Макролидные антибиотики проявляют высокую природную активность в отношении пневмококков, стафилококков, микоплазм, хламидий и низкую — в отношении гемофильной палочки. Однако в последние годы во всех регионах мира, в том числе и в нашей стране, отмечается неуклонная тенденция повышения устойчивости пневмококков к макролидам. Резистентность пневмококков обычно ассоциируется с неуспехом терапии макролидами. Следует отметить, что новые полусинтетические макролиды не имеют преимуществ перед эритромицином, когда речь идет об устойчивых штаммах пневмококков. В последние годы значение макролидов при внебольничной пневмонии пересматривается. По всей видимости, эти препараты могут быть рекомендованы только в случае нетяжелой пневмонии при подозрении на атипичную этиологию.
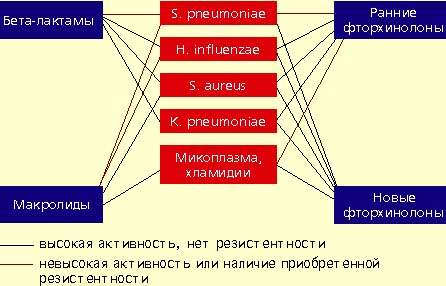 |
| Антимикробная активность бета-лактамов, макролидов и фторхинолонов в отношении наиболее значимых возбудителей внебольничной пневмонии |
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних фторхинолонов (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из-за их слабой природной активности в отношении основного возбудителя пневмонии — S. pneumoniae. Значения минимальных подавляющих концентраций (МПК) ранних фторхинолонов в отношении пневмококков составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия фторхинолонами при пневмококковой пневмонии не приносила успеха.
Определенные перспективы лечения внебольничной пневмонии связаны с появлением в последние годы препаратов нового поколения фторхинолонов, которые характеризуются более высокой активностью в отношении S. pneumoniae. Современная классификация фторхинолонов представлена в таблице.
Первым препаратом нового поколения фторхинолонов является левофлоксацин, представляющий собой левовращающий изомер офлоксацина. Левофлоксацин характеризуется более высокой активностью против пневмококков (МПК = 2 мкг/мл) по сравнению с офлоксацином и ципрофлоксацином, причем препарат сохраняет активность и в отношении пенициллинрезистентных штаммов S. pneumoniae. Левофлоксацин — это первый и пока единственный антибактериальный препарат, который официально рекомендован в США для лечения пневмонии, вызванной пенициллинрезистентными пневмококками. Среди новых фторхинолонов только левофлоксацин выпускается в двух лекарственных формах — для приема внутрь и для внутривенного введения. Поэтому левофлоксацин может применяться не только в амбулаторной практике, но и при тяжелых пневмониях у госпитализированных больных. В большом количестве клинических исследований показана высокая эффективность левофлоксацина при внебольничной пневмонии в дозе 500 мг, вводимой однократно в сутки. К несомненным достоинствам левофлоксацина можно отнести его хорошую переносимость.
Вторым препаратом нового поколения фторхинолонов, внедренным в клиническую практику, был спарфлоксацин. Он зарегистрирован в нашей стране и выпускается только в пероральной форме. Однако наряду с доказанной высокой клинической эффективностью следует отметить ряд нежелательных эффектов, отмеченных при его применении. Прежде всего речь идет о существенной фототоксичности спарфлоксацина (т. е. повышенной чувствительности кожи к ультрафиолету); по некоторым данным, частота возникновения этого нежелательного явления составляет более 10%. Фототоксичность характерна для всех препаратов класса фторхинолонов, однако при использовании других препаратов этой группы (например, левофлоксацина, офлоксацина, ципрофлоксацина) это побочное явление возникает гораздо реже. К другим достаточно серьезным нежелательным явлениям, связанным с приемом спарфлоксацина, относится удлинение интервала QT на ЭКГ, что может сопровождаться появлением желудочковых аритмий, иногда опасных для жизни. Клиническое значение этого феномена до конца не ясно, однако известен факт отзыва с рынка препарата этого класса (грепафлоксацина) именно по данной причине. Таким образом, спарфлоксацин, по всей видимости, не может быть рекомендован для рутинного применения в амбулаторной практике при пневмонии, учитывая наличие других, более безопасных препаратов этой группы.
Последним зарегистрированным в нашей стране новым фторхинолоном является моксифлоксацин. Пока он существует только для перорального приема, однако в следующем году ожидается появление в клинической практике парентеральной лекарственной формы. Моксифлоксацин характеризуется очень высокой природной активностью в отношении пневмококков (МПК = 0,25 мкг/мл), в том числе пенициллинрезистентных штаммов, а также более высокой активностью (по сравнению с ранними фторхинолонами) в отношении микоплазм и хламидий. Моксифлоксацин в суточной дозе 400 мг (однократно) показал высокую клиническую эффективность и хорошую переносимость при внебольничной пневмонии. В контролируемых исследованиях не отмечено клинически значимого удлинения интервала QT и существенной фототоксичности.
Ряд перспективных препаратов нового поколения фторхинолонов в настоящее время проходят стадию клинического изучения. В 2001 году ожидается разрешение клинического применения в России еще двух препаратов этой группы — гемифлоксацина и гатифлоксацина.
Почему нельзя пить алкоголь при приеме антибиотиков
В данной статье вы узнаете, что будет если пить антибиотики и алкоголь.
Взаимодействие, совместимость и последствия от совместного приема.
Подробности на сайте.
Последствия смешивания антибиотиков и алкоголя
Почему не следует пить алкоголь с антибиотиками?
Что будет, если выпить алкоголь и антибиотики?
Упоминание антибиотиков и алкоголя в одной фразе рисует в воображении фатальные последствия. Обычно они касаются острых побочных эффектов. Однако некоторые люди даже на время лечения не могут отказаться от привычного бокала вина за ужином. Подвергают ли они опасности свое здоровье? В данной статье мы ответим на этот вопрос и расскажем, что делать, если в желудке одновременно оказались антибиотики с алкоголем.
Как влияют алкогольные напитки на организм?
Основу любого такого напитка составляет этанол. Разница заключается в его содержании. Например, в водке его в 10 раз больше, чем в пиве. Употребление алкоголя в больших количествах негативно сказывается на организме. С мочой и потом выводится не более десятой части объема поступившего этанола, остальные 90% расщепляются и всасываются.
Этанол вредит мембранным липидам клеток. Их вязкость снижается, а рецепторы становятся недостаточно восприимчивыми к необходимым медиаторам. Для предотвращения такого влияния желудок пытается обезвредить этанол. Для этого слизистая оболочка вырабатывает гораздо больше слизи, чем в обычном пищеварительном режиме. С одной стороны, это замедляет всасывание нежелательного вещества, с другой – вызывает раздражение слизистой и тормозит усвоение нутриентов и других лекарств.
Нельзя исключить и комплекс патологий, именуемый алкогольной болезнью печени. При злоупотреблении этанолом развивается клеточная дистрофия, препятствующая нормальному функционированию органа.
Как влияют антибиотики на организм?
Препараты этой группы неспроста принимают только по назначению врача. Принцип их действия заключается в уничтожении или подавлении роста бактерий, причем всех (как полезных, так и вредных).
• Аппарат клеточного синтеза. Это не позволяет бактериям выстраивать защитные пептидные стенки.
• ДНК-гиразу. Это предотвращает репликацию генетической информации и тормозит размножение патогенных микроорганизмов.
• Аппарат биосинтеза белка (рибосомы) — без него бактерии погибают.
Современная фармакология старается делать антибиотики более избирательными. Но их употребление ведет к нарушению баланса микрофлоры. Страдают и полезные бактерии, формирующие своеобразный щит в кишечнике. Поэтому только специалист может сопоставить эффект от лечения с возможными потерями. Также ряд антибактериальных препаратов обладает свойством гепатотоксичности. Они повреждают клетки печени, вызывая холестаз (нарушение оттока желчи) или некроз (отмирание тканей).
Можно ли пить алкоголь при приеме антибиотиков?
Мы выяснили, что алкоголь и антибиотики обладают гепатотоксическим действием. Получается, если их совмещать, атака на клетки печени многократно усилится. Это первая причина, по которой нельзя пить спиртное во время антибактериальной терапии. Но есть и другие.
Небольшая порция пива или вина печень не разрушит. Однако для активизации защитной реакции слизистой желудка ее достаточно. Лекарственные средства в таких условиях должным образом всасываться не будут. При взаимодействии антибиотиков даже со слабым алкоголем эффект от антибактериальной терапии будет минимальным, если не нулевым. Поэтому подобного сочетания лучше не допускать.
Какие антибиотики лучше не совмещать с алкоголем?
Антибактериальные препараты образуют довольно крупную фармакологическую группу. Входящие в нее лекарства обладают разной степенью активности. Поэтому применение одних вместе с алкоголем — нежелательно, а других — условно не запрещается.
К первым относятся антибиотики, обладающие высоким гепатотоксичным действием:
Существуют разные точки зрения на взаимодействие этанола с тетрациклинами. Одни считают, что при таком сочетании лекарство нейтрализуется, другие полагают, что оно усиливает негативное влияние на печень.
Некоторые антибактериальные препараты нельзя пить с алкоголем из-за возможных побочных эффектов. Особенно это касается метронидазола.
Последствия употребления алкоголя с антибиотиками
Если человек не злоупотребляет спиртным, действия на печень от однократного сочетания антибиотика и этанола он не почувствует. Однако реакции могут последовать со стороны других систем:
• Пищеварительной. Боль в желудке объясняется раздражением слизистой, а избыточная секреция слизи может вызвать диарею.
• Нервной. Антибиотики сами по себе пагубно влияют на нейроны. При взаимодействии с этанолом, возбуждающим нервную систему, не исключены судороги.
• Сердечно-сосудистой. Фторхинолоны повышают риск нарушения кровотока, что усиливает нагрузку на сердце. А каждая дополнительная порция пива или вина (не говоря уже о более крепких напитках) эту нагрузку умножает.
Аллергикам вообще запрещено смешивать любые лекарства с алкоголем, так как реакция организма может быть непредсказуемой. Даже врач не всегда может предсказать исход.
Почему нельзя пить алкоголь во время приема антибиотиков?
Мы выяснили, что основные причины заключаются в опасности для печени и возможности возникновения побочных эффектов. Но пациенты часто задают вопрос: меняется ли интенсивность действия лекарственного средства под действием этанола?
В целом она снижается. Пока организм сопротивляется всасыванию компонентов спирта, он неосознанно защищается и от медикаментов. Чем крепче алкогольный напиток, тем меньше вероятность полного всасывания лекарства.
Если совмещать этанол с метронидазолом, возникает синергетический эффект. Однако он касается не самого действия препарата, а его побочных эффектов:
• нарушения сердечного ритма;
Встречаются и вопросы о возможной передозировке. Ее можно не бояться — в составе антибактериальных препаратов спирт отсутствует. Подобные предположения возникают из-за невнимательного изучения состава лекарственных средств.
Как избежать нежелательных последствий?
Самое простое решение — не смешивать вещества. Курс антибактериальной терапии длится недолго, так что можно потерпеть и не прикасаться к спиртным напиткам. Однако бактериальная инфекция может настигнуть в самый неожиданный момент, например, накануне свадьбы или юбилея. В такой ситуации важно:
• Посоветоваться с врачом на предмет совместимости назначенного препарата с алкоголем.
• Даже при отсутствии противопоказаний не злоупотреблять — ограничиться 1-2 бокалами некрепкого напитка.
• При наличии ограничений не преступать их.
• Выждать между последним приемом лекарства и употреблением спиртного не менее двух суток (лучше — трех).
Не нужно прерывать курс антибиотиков ради алкогольной вечеринки. Это сведет на нет все достигнутые результаты — придется начинать лечение заново. Получится, что в первый курс терапии микрофлора страдала зря, а со вторым — подвергнется лишней угрозе.
Что делать в случае смешения?
Невнимательность, настойчивость окружающих, сознательное игнорирование указаний врача — все это может привести к ситуации, когда в организме одновременно окажутся антибактериальный препарат и алкоголь. Это не значит, что человеку тут же станет плохо (хотя такое не исключено).
За состоянием нужно понаблюдать. Если острых реакций нет, можно обойтись без медицинской помощи:
• принудительно очистить желудок;
• принять активированный уголь или другой энтеросорбент;
• выпить большое количество воды.
По возможности нужно сообщить лечащему врачу, что очередная доза препарата была выведена из организма, записать время последнего приема и время очищения желудка. Только медик может решить, стоит ли корректировать дозу.
Не лишним будет сдать анализ крови, чтобы убедиться, не повлияло ли сочетание алкоголя и антибиотика на основные показатели. Однако если вскоре после употребления возникли ярко выраженные симптомы со стороны нервной, сердечно-сосудистой или пищеварительной системы, лучше вызвать Скорую помощь. Особенно это касается людей, страдающих диабетом и аллергией, поскольку их организмы особенно чувствительны и могут отреагировать самым неожиданным образом.












