Мелатонин – при диабете и ожирении показан
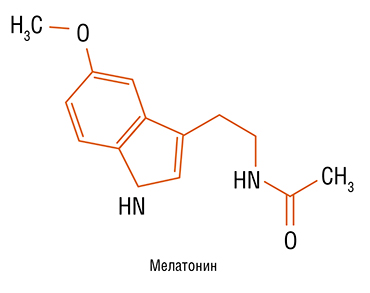
Верно говорят: мал золотник, да дорог. Гормон мелатонин представляет собой очень маленькую молекулу и синтезируется в организме из аминокислоты триптофана в очень малом количестве. Однако эта древнейшая сигнальная молекула принимает участие в регуляции множества сторон жизнедеятельности нашего организма, включая сон, кровообращение, работу эндокринной и лимфатической систем и иммунитет. Последние исследования говорят о том, что мелатонин можно успешно использовать не только в качестве снотворного средства при нарушениях суточного ритма, но и для лечения ожирения и сахарного диабета 2-го типа. И одним из самых перспективных препаратов для этой цели может стать инновационная разработка новосибирского НИИ клинической и экспериментальной лимфологии
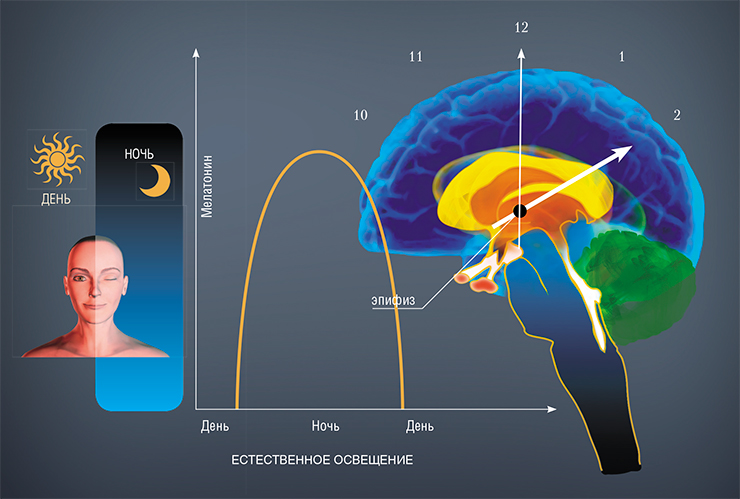
Французский философ и ученый Рене Декарт недаром называл этот маленький, размером с горошину орган головного мозга «седалищем души». Функции эпифиза еще во многом остаются загадкой, хотя мы знаем, что эта эндокринная железа действительно влияет на эмоциональное, психическое состояние человека и животного.
Функциональная роль эпифиза связана с его основным гормоном – мелатонином. Эпифизарный мелатонин поступает в кровь и разносится по всему организму, где участвует в регуляции самых разных биологических процессов. К примеру, он индуцирует процессы торможения в центральной нервной системе и способствует наступлению сна, регулирует суточный ритм температуры тела, активирует иммунную систему, повышает функцию антиоксидантной системы организма и т. д. Снижение продукции мелатонина с возрастом может быть фактором повышенного окислительного повреждения клеток у пожилых людей, что способствует развитию таких «возрастных» заболеваний, как болезни Альцгеймера и Паркинсона (Peschke, 2008).
До 80 % мелатонина в сыворотке крови имеет эпифизарное происхождение. Но мелатонин вырабатывается не только в эпифизе, но и в периферических тканях, в первую очередь в желудочно-кишечном тракте, включая кишечник, поджелудочную железу и печень. Так, в слизистой оболочке толстой кишки синтезируется в 400 раз больше мелатонина, чем в эпифизе, при этом его содержание регулируется в основном приемом и характером пищи, а не чередованием света и темноты (Мелатонин: перспективы применения в клинике, 2012).
Биологическое действие внеэпифизарного мелатонина реализуется, по-видимому, непосредственно там, где он синтезируется. Учитывая необыкновенную распространенность гормона в организме, можно предполагать, что он играет ключевую роль в местной координации клеточных функций. Такое широкое распространение мелатонина отражает его важную роль как межклеточного нейроэндокринного регулятора и координатора многих сложных и взаимосвязанных биологических процессов
Важная особенность эпифизарного мелатонина заключается в том, что его продукция имеет суточный ритм, достигая пика в темное время суток, а в светлое синтез мелатонина блокируется.
Так как самым очевидным эффектом этого «ночного» гормона является его снотворное действие, препараты мелатонина часто назначают при различных нарушениях сна из-за рассогласования биологических ритмов. Последнее случается в самых разных жизненных ситуациях: при сменной и ночной работе, дальних перелетах, работе в Арктике и Антарктике, неправильном режиме дня, а также сне при включенном свете. Кроме того, так как мелатонин обладает свойствами антидепрессанта, его назначают для улучшения настроения.
Но в этой статье мы остановимся на гораздо менее известных эффектах мелатонина, связанных с его влиянием на углеводный и жировой обмен, лимфатическую и иммунную системы, процессы жизнедеятельности и смерти клеток.
Регулятор обмена веществ
Мелатонин воздействует на функцию этих клеток через мембранные рецепторы (MT1 и МТ2), которые также имеются у клеток в некоторых структурах мозга и во многих периферических органах. Таким образом происходит синхронизация производства инсулина и чередования светлого и темного времени суток. Кроме того, установлено, что мелатонин способствует воспроизводству бета-клеток в поджелудочной железе, улучшает чувствительность тканей к инсулину и уменьшает окислительный стресс в экспериментальных моделях сахарного диабета 2-го типа (Peschke et al., 2006; Peschke, 2008).
Мелатонин воздействует на клетки через мембранные рецепторы МТ1 и МТ2, активность которых снижается при ночном освещении, а также через рецепторы в ядре клеток, влияя таким образом на уровень активации ряда генов, в том числе в органах, определяющих суточные ритмы организма (эпифизе, сетчатке глаза, гипоталамусе и др.). И сам гормон, и его метаболиты (6-гидроксимелатонин) могут также беспрепятственно проникать в цитоплазму клетки через клеточную мембрану, где связывают свободные радикалы кислорода, защищая от оксидативного повреждения макромолекулы (белки, жиры, ядерную и митохондриальную ДНК) во всех субклеточных структурах (Carpentieri et al. 2012; Bouroutzika et al. 2020)
Таким образом, этот гормон играет важную роль в регуляции уровня глюкозы в крови и секреции инсулина, поэтому неудивительно, что и сахарный диабет 2-го типа, и сопутствующие ему патологии – алиментарное (первичное) ожирение и метаболический синдром – развиваются на фоне нарушения/снижения продукции мелатонина (BährI et al., 2012; Hardeland, 2012). У больных сахарным диабетом 2-го типа нормальный циркадный ритм мелатонина, как правило, отсутствует, а его уровень в целом понижен.
Причина подобных нарушений может быть различной. С одной стороны, возникновение такой патологии может быть связано с определенными вариантами генов, кодирующими рецепторы мелатонина, из-за чего чувствительность к этому гормону падает (Tosini et al., 2014). С другой стороны, сахарный диабет 2-го типа часто начинается на фоне рассогласования суточных ритмов из-за ночного освещения, что приводит к частичной или полной блокаде синтеза мелатонина в эпифизе.
Сейчас во всем мире, особенно в развитых странах, наблюдается буквально эпидемия сахарного диабета 2-го типа и связанных с ним сердечно-сосудистых осложнений, смертность от которых выше, чем от онкологических болезней. Согласно данным Минздрава РФ, риск развития диабета сегодня угрожает каждому десятому россиянину. И мелатонин может занять свое место в ряду эффективных фармакологических средств для борьбы с подобными нарушениями.
Печень Прометея
Нашим первым шагом по выяснению механизмов действия мелатонина при сахарном диабете 2-го типа стало изучение его влияния на печень, которая играет основную роль в поддержании постоянства внутренней среды организма. Именно печень выполняет функции «метаболического мозга», координируя потоки разнообразных соединений и адаптируя метаболизм к текущим потребностям нашего организма, и она же является одним из главных органов-мишеней для любых метаболических нарушений.
Развитие метаболического синдрома и сахарного диабета 2-го типа также сопровождается нарушениями функций печени. Мы изучили эти изменения на модельном объекте – лабораторных мышах линии BKS.Cg-Dock7 m +/+Lepr db /J, генетически предрасположенных к развитию ожирения и диабета, для которых характерен пониженный уровень секреции эпифизарного мелатонина.
У взрослых животных этой линии были обнаружены отчетливые структурные перестройки, свидетельствующие о развитии у них неалкогольной жировой болезни печени. Микроскопические исследования выявили накопление в клетках печени жира и гликогена («животного крахмала»), нарушение клеточных структур, ответственных за синтез белка, и митохондрий – «клеточных электростанций», а также застой лимфы, особенно у самцов (Michurina et al., 2016).
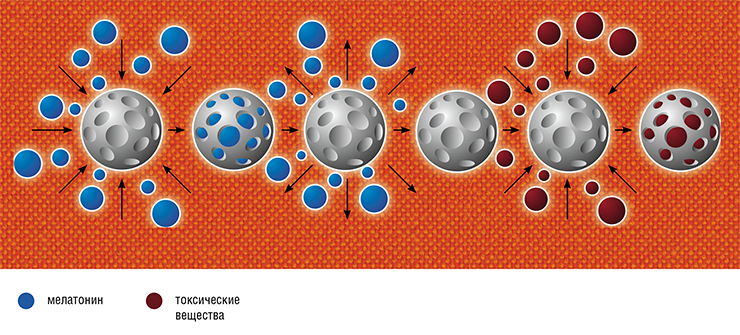
На последнее стоит обратить особое внимание, так как лимфатическая система, сосуды которой пронизывают все органы и ткани, – это тот дренаж, по которому идет отток жидкости из межклеточного пространства. С этой жидкостью из ткани выводятся продукты обмена веществ, в том числе токсические. Застой лимфы свидетельствует о значительной нагрузке на эту систему и способствует развитию кислородного голодания тканей печени, что наряду с повреждением митохондрий приводит к усилению программируемой гибели (апоптозу) клеток.
Может ли дополнительный прием мелатонина повлиять на все эти структурные изменения? Известно, что мелатонин улучшает состояние митохондрий (Srinivasan et al., 2011); под регулирующим влиянием этого гормона находятся и транспортные пути для лимфы и лимфоидных клеток. Таким образом, можно обоснованно предположить, что при ожирении и сахарном диабете препараты мелатонина позволят добиться коррекции печеночной патологии.
Мелатонин и иммунная система
Еще одна важнейшая система организма, которая страдает при сахарном диабете 2-го типа, – иммунная. Основными рабочими элементами этой системы являются иммунные клетки (макрофаги, дендритные клетки, различные типы лимфоцитов, включая Т-киллеры), которые образуются и созревают в красном костном мозге и тимусе. Попадая в кровь, такие клетки разносятся по всем органам и тканям, где осуществляют надзор за состоянием внутренней среды организма, уничтожая чужеродные молекулы, патогенные вирусы и бактерии, а также злокачественные клетки.
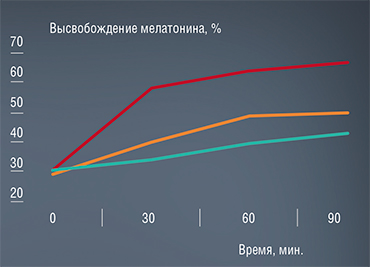
В нашем эксперименте крыс содержали на диете, в которую входили продукты с высоким содержанием жира, что привело к увеличению у них массы тела, повышению содержания триглицеридов и общего холестерина в сыворотке крови, а также жира в печени.
Заметно пострадала и иммунная система упитанных животных. В их селезенке изменилась численность иммунных клеток, в том числе понизилось содержание антигенпрезентирующих клеток и активированных лимфоцитов, обеспечивающих быстрый иммунный ответ на конкретные патогены. Количество активированных лимфоцитов упало и в лимфоузлах печени, а в крови увеличилось число лейкоцитов. В лимфоцитах крови изменился баланс активности окислительно-восстановительных ферментов, что говорит о нарушении энергетического обмена и снижении функциональной активности этих клеток.
Инъекции мелатонина животным в течение двух недель привели к нормализации практически всех этих показателей, включая вес тела.
Комплекс М – «продвинутый» мелатонин
Таким образом, все имеющиеся на сегодня данные говорят о том, что, хотя в лечении сахарного диабета 2-го типа и ожирения мелатонин пока не используется, это новое терапевтическое направление имеет полное право на существование. При этом результаты экспериментальных работ в этой области, когда мелатонин применялся в «чистом виде», до сих пор неоднозначны и противоречивы, несмотря на их многочисленность. Может быть, это связано с тем, что мелатонин, введенный путем инъекции или с пищей, быстро выводится из организма, тогда как эпифиз выделяет гормон постепенно, в течение темного времени суток.
В новосибирском НИИ клинической и экспериментальной лимфологии – филиале ФИЦ ИЦиГ СО РАН разработан и синтезирован новый препарат мелатонина – «Комплекс М». Он представляет собой оригинальную композицию из носителя – пористого оксида алюминия с преимущественным размером пор 10–100 нм, кремнийсодержащего полимера полиметилсилоксана, относящегося к силиконовым соединениям, и гормона мелатонина, содержание которого в препарате составляет 0,15 % (Патент № 2015100920 /05(001238) от 11.01.2016).
В НИИКЭЛ – филиале ФИЦ ИЦиГ СО РАН в течение ряда лет разрабатываются оригинальные лекарственные препараты на основе пористых носителей (модифицированных сорбентов), поры которых служат «микроконтейнерами» для активных фармацевтических субстанций.
Как известно, сорбенты могут фиксировать на своей поверхности различные молекулы, поэтому сорбционная терапия традиционно применяется для выведения токсических продуктов из организма. Однако ее можно использовать и для целевой доставки лекарственных средств. Сорбент не разрушается при прохождении по желудочно-кишечному тракту, поэтому удерживаемый на поверхности носителя фармацевтический агент выходит из него постепенно, в течение длительного времени (Бородин и др., 2014). Это позволяет избежать передозировки, а также снижает риск побочных эффектов и интоксикаций.
Разработки новых препаратов в НИИКЭЛ базируются на сырье отечественного производства, при котором используются технологии получения безопасных для человека пористых материалов, исключающие применение высоких температур и органических растворителей
Поверхность пор носителя характеризуется набором как гидрофильных участков за счет матрицы из оксида алюминия, так и гидрофобных за счет полиметилсилоксана. Это создает условия, способствующие многоточечному связыванию на их поверхности различных средне- и высокомолекулярных соединений. Благодаря таким физико-химическим особенностям препарата мелатонин высвобождается из него постепенно, что позволяет добиться эффекта «протезирования» мелатонин-продуцирующей функции эпифиза.
С другой стороны, на пористом носителе могут адсорбироваться различные токсические соединения. Благодаря достаточно высокой сорбционной емкости препарат проявляет детоксицирующий эффект, а также противоотечный за счет регуляции баланса тканевой жидкости.
Во время доклинических испытаний при содержании мышей С57Bl/6J при круглосуточном освещении, которое подавляет синтез мелатонина в эпифизе, были получены обнадеживающие результаты. В этом случае введение «Комплекса М» можно рассматривать как своего рода заместительную терапию.
Так, ежедневное введение водной суспензии «Комплекса М» самцам мышей этой линии уже через неделю привело к значительному увеличению мышечной силы и выносливости животных. В то же время прием обычного мелатонина в аналогичной дозе не оказал такого эффекта. Эти результаты говорят о перспективности применения «Комплекса М» у людей, чья деятельность связана с тяжелыми физическими нагрузками: спортсменов, военнослужащих, вахтовиков и др.
Также выяснилось, что препарат благоприятно влияет на состояние селезенки – многофункционального органа, выполняющего кроветворные, иммунные и обменные функции, а также депонирующего кровь. Усиление кровотока в венозных сосудах и ряд структурных изменений этого органа в ответ на прием «Комплекса М» свидетельствуют об активации его иммунных функций. Кроме того, введение этого препарата повышало корково-мозговой индекс тимуса (вилочковой железы), что может указывать на стимуляцию дифференцировки T-клеток иммунной системы.
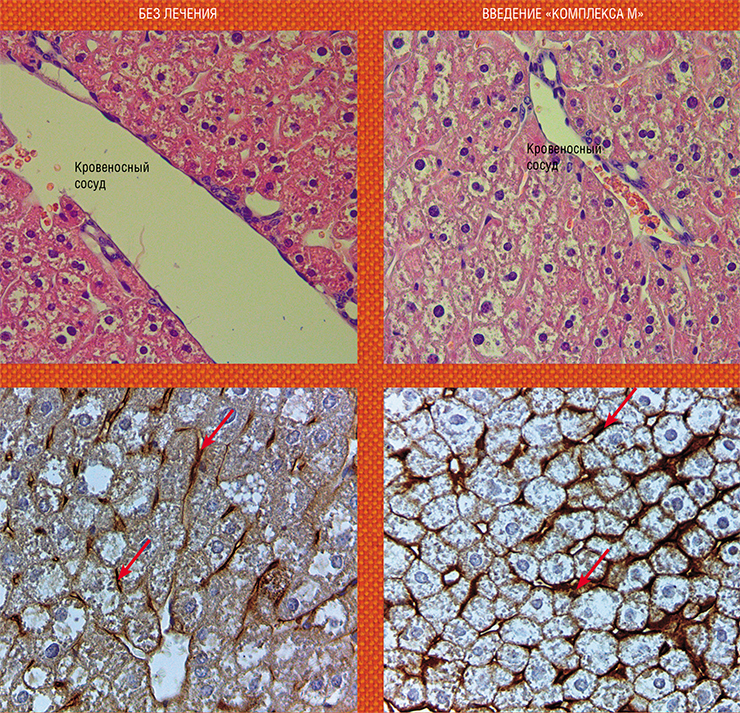
Успешным оказалось и лечение мышей с генетически детерминированным развитием ожирения и сахарного диабета, о которых говорилось выше. Внутрижелудочное введение «Комплекса М» взрослым особям привело к нормализации у них структурно-функциональных показателей циркуляции крови и лимфы, а также к улучшению состояния клеток печени и усилению регенеративного потенциала этого органа.
Наглядной иллюстрацией положительного действия «Комплекса М» на таких животных могут служить молекулярные особенности запрограммированной гибели клеток печени. Как уже говорилось выше, плохое снабжение клеток кислородом у мышей этой линии негативно сказывается на структуре и функциях митохондрий – основных внутриклеточных участников апоптоза. Изучение ультраструктурного состояния этих внутриклеточных органелл и динамики продукции двух белков, регулирующих клеточное «самоубийство», – антиапоптотического Bcl‑2 и проапоптотического Bad – показало, что у взрослых самцов активируется так называемая митохондриальная «ветвь» апоптоза. Введение «Комплекса М» привело к преобладанию «защитника» Bcl‑2 над «клеточным убийцей» Bad, что говорит о восстановлении клеточной защиты в печени (Мичурина 2019; Michurina et al., 2016).
Таким образом, можно утверждать, что как сам мелатонин, так и новый препарат мелатонина «Комплекс М» обладают мощными антиоксидантными, иммуномодулирующими, лимфотропными, гепатопротекторными и гиполипидемическими свойствами. И в этом смысле они являются перспективными средствами для коррекции нарушений липидного обмена и иммунного статуса при ожирении и нарушении светового режима, а также в комплексном лечении сахарного диабета 2-го типа.
При этом «Комплекс М» обладает более выраженным терапевтическим действием по сравнению с обычными препаратами мелатонина. Он не только безопасен, но и проявляет детоксикационные свойства за счет пористой структуры носителя.
Препарат, разработанный новосибирскими специалистами, успешно прошел лабораторно-экспериментальные испытания. Однако трудно сказать, когда он появится на прилавках аптек. Официальные доклинические и клинические испытания нового лекарственного средства – процедура всегда дорогостоящая, а в мире к тому же идет пандемия нового вирусного заболевания. И это, кстати, лишний повод напомнить о роли мелатонина в поддержании здоровья больных сахарным диабетом 2-го типа, так как такие пациенты входят в группу риска.
Арушанян Э. Б., Наумов С. С. Противовоспалительные возможности мелатонина // Клиническая медицина. 2013. Т. 91, № 7. С. 18–22.
Арушанян Э. Б., Щетинин Е. В. Мелатонин как универсальный модулятор любых патологических процессов // Патологическая физиология и экспериментальная терапия. 2016. Т. 60, № 1. С. 79–88.
Бородин Ю. И., Труфакин В. А., Мичурина С. В., Шурлыгина А. В. Структурно-временная организация печени, лимфатической, иммунной, эндокринной систем при нарушении светового режима и введении мелатонина. Новосибирск: Изд. дом «Манускрипт», 2012. 208 с.
Коненков В. И. КлимонтовВ. В., Мичурина С. В и др. Мелатонин при сахарном диабете: от патофизиологии к перспективам лечения // Сахарный диабет. 2013. № 2. С. 11–16.
Мичурина С. В., Васендин С. В., Ищенко Ю. И. Физиологические и биологические эффекты мелатонина: некоторые итоги и перспективы изучения // Российский физиологический журнал им. И.М. Сеченова. 2018. Т. 104, № 3. С. 257–271.
Мичурина С.В., Летягин А. Ю., Шурлыгина А. В. и др. Гепато-иммуно-эпифизарная ось межсистемных взаимодействий. Мелатонин и структурно-функциональные изменения печени и иммунной системы при ожирении и сахарном диабете 2 типа. Новосибирск: Изд. дом «Манускрипт», 2019. 304 с.
Мелатонин диабетикам можно ли
Кафедра фармакологии Ставропольской государственной медицинской академии
Мелатонин и сахарный диабет (обзор современных экспериментальных данных)
Журнал: Проблемы эндокринологии. 2012;58(3): 35-40
Арушанян Э. Б. Мелатонин и сахарный диабет (обзор современных экспериментальных данных). Проблемы эндокринологии. 2012;58(3):35-40.
Arushanian É B. Melatonin and diabetes mellitus (an overview of current experimental data). Problemy Endokrinologii. 2012;58(3):35-40.
Кафедра фармакологии Ставропольской государственной медицинской академии
Секретируемый эпифизом и апудоцитами желудочно-кишечного тракта мелатонин участвует в регуляции углеводного обмена, модулируя активность α- и Β-клеток островков Лангерганса поджелудочной железы через специфические мелатониновые рецепторы (МР1 и МР2). Уровни мелатонина и инсулина находятся в реципрокных отношениях, а дефицит мелатонина, очевидно, является одним из факторов патогенеза сахарного диабета. Мелатонин обеспечивает антидиабетическую защиту посредством различных клеточных и системных механизмов.
Кафедра фармакологии Ставропольской государственной медицинской академии
На протяжении нескольких десятилетий в биологической науке и медицине удерживается стойкий интерес к биологическим свойствам мелатонина (МТ). В последние годы появилось много сведений о его участии в поддержании энергетического гомеостаза и генеза сахарного диабета. В данном обзоре сделана попытка обобщения современных знаний в этой области.
Биологические особенности мелатонина
В середине ХХ века МТ был впервые выделен из эпифиза животных и позднее идентифицирован в качестве специфического эпифизарного гормона. Благодаря совместным усилиям разных специалистов во многом были выяснены процессы его формирования и необычайно широкий диапазон биологических эффектов МТ. Эти сведения подробно освещены в серии обзоров [1—3] и вкратце сводятся к двум главным положениям.
Во-первых, синтез МТ в пинеалоцитах проходит несколько этапов. Исходным веществом служит триптофан, который через серотонин и N-ацетилсеротонин превращается в конечный гормон. Ключевыми ферментами его синтеза являются N-ацетилтрансфераза и гидроксииндол-О-метилтрансфераза. МТ секретируется преимущественно в ликвор, откуда поступает в сосудистое русло и разносится кровью по всему организму. В различных мозговых структурах и периферических органах эффекты гормона реализуются посредством специфических рецепторов (преимущественно типа МР1 и МР2).
Во-вторых, образование эпифизарного МТ независимо от видовых особенностей животных максимально выражено в темный и минимально в светлый периоды суток. Это позволило считать эпифиз важной хронотропной железой, обеспечивающей за счет тесных морфофункциональных связей с водителем суточного ритма (супрахиазматическими ядрами гипоталамуса) циркадианные колебания различных физиологических функций. За МТ закрепилась репутация естественного хронобиотика и универсального адаптогенного гормона.
Описанные представления сформировались на основе многолетнего изучения физиологии эпифиза и секретируемых им биологически активных соединений (не только индольной, но и пептидной природы). Между тем уже в 70-е годы ХХ века иммуногистохимическая техника позволила установить существование МТ в различных периферических тканях. Содержащие его энтерохромаффинные клетки — апудоциты — наиболее полно представлены в различных структурах желудочно-кишечного тракта (ЖКТ), в том числе в поджелудочной железе и гепато-биллиарной системе.
Как и в эпифизе, этот МТ синтезируется при участии тех же ферментов. Его общее количество в органах ЖКТ в десятки раз превосходит уровень МТ эпифизарного происхождения в плазме. После удаления эпифиза исчезают суточные колебания содержания гормона в плазме, но за счет апудоцитов в дневные часы он продолжает в определенном количестве сохраняться в сосудистом русле [4—6].
Эффекты регионального МТ, подобно эпифизарному, реализуются посредством специфических МР, идентифицированных во всех органах ЖКТ. Однако если в слизистой желудка и в поджелудочной железе плотность МР1 обнаруживает четкий суточный ритм с максимальными значениями в темный период, то у МР2 подобная ритмика отсутствует [7—8].
Широкая распространенность в организме позволила считать, что внеэпифизарный МТ играет ключевую роль паракринной сигнальной молекулы, регионально координирующей клеточные функции. Циркулирующий в крови МТ может действовать как типичный гормон, достигая далеко расположенных клеток-мишеней [9, 10].
Учитывая изложенное, а также тот факт, что МТ является мощным эндогенным «поглотителем» свободных радикалов, иммуномодулятором и антитоксикантом (см. ниже), он, по-видимому, способен обеспечивать в организме универсальную протективную миссию, участвуя в любых патологических процессах. Как показывают приводимые ниже данные, МТ контролирует обмен углеводов и жиров, деятельность поджелудочной железы, проявления метаболического синдрома и сахарного диабета, наряду с другими факторами определяя надежность энергетического гомеостаза в целом.
Влияние мелатонина на углеводный обмен
Уже в первых работах, посвященных биологии эпифиза, была обоснована возможность его участия в регуляции энергетического метаболизма, хотя конкретные данные весьма противоречивы. Функциональные свойства как самой железы, так и ее гормона позволяют указать на несколько вероятных причин противоречий. К ним, очевидно, следует отнести видовые особенности животных, дозу и схему введения МТ, гендерные и возрастные различия, исходное функциональное состояние организма.
Действительно, по одним наблюдениям повторное введение МТ крысам (парентерально, 10 мг/кг, 18 дней) существенно не влияло на гликемию и антиоксидантный статус животных; по другим — при его пероральном введении (с водой, 4 мкг/мл, 12 нед) отмечалось снижение массы тела и уровня глюкозы в плазме, а у самцов (в отличие от самок) — и содержания инсулина в крови. У крыс разного пола содержание триацилглицерина в крови и гликогена в миокарде менялось разнонаправленно [11, 12]. При добавлении МТ к изолированным островкам поджелудочной железы наблюдались более однозначные сдвиги: МТ заметно угнетал секрецию инсулина β-клетками и усиливал экспрессию и секрецию глюкагона α-клетками. По данным опытов in vivo, его пероральное введение крысам провоцировало гипергликемию с ростом концентрации глюкагона в плазме [13].
Результаты некоторых работ, выполненных на ведущих дневной образ жизни животных и людях, не во всем совпадают с такими выводами. Так, введение МТ (0,1 мг/кг) коровам существенно повышало уровень общего холестерина и триглицеридов, но концентрации глюкозы и инсулина в плазме менялись незначительно. В то же время однократный прием (1 мг) МТ пожилыми женщинами снижал толерантность к глюкозе и повышал чувствительность к инсулину [14, 15].
Особенно следует подчеркнуть значение видовой принадлежности животных [16, 17]. Действительно, хотя суточная кривая содержания МТ в крови животных, ведущих ночной и дневной образ жизни, имеет одинаковую конфигурацию с пиком в полночь, у первых активность выше в темный период суток, а у вторых пик уровня МТ совпадает со снижением активности.
Еще одним важным условием проявления эффектов МТ служит исходное функциональное состояние организма. Это требует обязательного учета исходного метаболического фона при назначении МТ.
Так, у крыс, подвергаемых регулярной физической нагрузке, в отличие от нетренируемых, развивалась гипогликемия, возрастал уровень лактата в плазме, а в печени и мышцах увеличивалось содержание гликогена. На этом фоне повторное введение МТ (0,5 или 2 мг/кг) нормализовало указанные сдвиги [18]. У крыс, которых кормили богатой жирами пищей, повышение массы тела сочеталось с устойчивым подъемом в крови концентрации инсулина, глюкозы, триглицеридов, адипонектина, причем эти сдвиги также нивелировались, если животные одновременно получали с водой МТ (25 мкг/мл, в течение 11 нед). Существенно, что у крыс с ожирением в несколько раз увеличивалось содержание МТ в плазме [19]. Учет указанных факторов позволяет более определенно говорить о вкладе МТ в регуляцию углеводного обмена и эндокринной функции поджелудочной железы.
Мелатонин и экспериментальный сахарный диабет
При стрептозотоциновом диабете у крыс гипергликемия сочетается с ухудшением толерантности к углеводной нагрузке, снижением активности глюкокиназы и глюкозо-6-фосфатдегидрогеназы в печени и ухудшением антиоксидантного статуса. Предварительное введение МТ (5 мг/кг, 15 дней) предупреждало появление указанных сдвигов [20]. У крыс линии Goto-Kakizaki с диабетом, аналогичным сахарному диабету 2-го типа у человека, наблюдается гиперинсулинемия и гиперлипидемия, снижение концентрации глюкагона и активности тирозинкиназы рецептора инсулина. Однако и в этой ситуации установлен отчетливый антидиабетический эффект МТ [13, 21, 22].
С этими данными совпадают результаты исследований in vitro. Например, в островковом аппарате Лангерганса мышей с аллоксановым диабетом неизменно развиваются дегенеративные изменения. Если таким животным предварительно вводили МТ (ежедневно по 0,15 мг/кг в течение 2 нед), то число и структура выделенных β-клеток не отличались от таковых у контрольных и, что особенно показательно, у старых мышей. С другой стороны, у эпифизэктомированных крыс наблюдается снижение плотности островков и гибель их клеточных элементов [23, 24]. Добавление МТ в инкубационную среду гепатоцитов, полученных от мышей с алиментарным диабетом, увеличивало в них синтез гликогена, причем этот эффект устранялся антагонистом МТ лузиндолом [25]. Интересно, что МТ облегчал приживление трансплантата островков Лангерганса у мышей с диабетом [26].
Результаты пока немногочисленных исследований на людях в принципе совпадают с экспериментальными данными и подтверждают защитные антидиабетические свойства МТ. В развитии метаболического синдрома, ассоциированного с сахарным диабетом 2-го типа и кардиоваскулярными расстройствами, как известно, ключевую роль играет резистентность к инсулину. У больных с этой патологией зачастую нарушено соотношение между уровнями МТ и инсулина в плазме, что позволило предположить роль эпифизарной недостаточности в патогенезе метаболического синдрома [27]. Назначение МТ пожилым пациентам с инсулиннезависимым диабетом (5 мг/сут в течение 1 мес) улучшало клиническое состояние и ослабляло проявления оксидативного стресса (повышение активности эритроцитарной супероксиддисмутазы и снижение уровня малонового диальдегида) [28].
Участие МТ в регуляции метаболизма углеводов и его вклад в патогенез сахарного диабета реализуется, очевидно, несколькими путями, но главную роль, по всей вероятности, играет прямое вмешательство в функцию клеточных элементов островков Лангерганса через специфические рецепторы, присутствующие на поверхности мембран β- и α-клеток как грызунов, так и человека. При этом в β-клетках обнаружена мРНК МР2, а в α-клетках — МР1 [29].
Добавление МТ к изолированным островкам человека повышает в клетках содержание свободных ионов кальция, мобилизуя его запасы из эндоплазматического ретикулума и тем самым модулируя клеточные функции. Стимуляция α-клеток при МР1, по-видимому, служит основной причиной усиления секреции глюкагона. В то же время за счет включения цГМФ-сигнального пути через МР2 тормозится выработка инсулина β-клетками [30—34].
У мышей с нокаутом гена МР1 резко нарушается метаболизм глюкозы и растет резистентность к инсулину. Потому есть все основания приравнивать состояние таких животных к сахарному диабету 2-го типа у человека [35].
У экспериментальных животных присутствуют два подтипа МР1 — МР1А и МР1В, причем на β-клетках панкреатической ткани плотность вторых выше, и их генетические вариации в большей степени сказываются на секреции инсулина. Это справедливо и для поджелудочной железы людей, что позволяет считать нарушения мелатонинергической системы серьезным фактором риска сахарного диабета [36—38].
Таким образом, накопленные к настоящему моменту сведения не оставляют сомнений в роли МТ в развитии сахарного диабета, хотя по-прежнему не позволяют сделать окончательный вывод. По нашему мнению, можно предполагать существование реципрокных отношений между МТ и инсулином. Иными словами, не только МТ модулирует эндокринную функцию поджелудочной железы, но сама патология и уровень инсулина в плазме отражаются на секреции эпифизарного МТ.
Стрептозотоциновый диабет у грызунов по своим метаболическим параметрам ближе всего к сахарному диабету 1-го типа у человека и характеризуется снижением содержания инсулина в крови. Одновременно усиливается синтез МТ в эпифизе, а также индуцируются часовые гены (PerI и BmaII) [39, 40]. Обратная ситуация показана у крыс Goto-Kakizaki, состояние которых приравнивается к диабету 2-го типа. У них наблюдается гиперинсулинемия, сочетающаяся с падением уровня МТ в крови, снижением активности N-ацетилтрансферазы и плотности адренорецепторов в эпифизарной ткани и усилением экспрессии мРНК МР1 в панкреатических островках [41—44]. Таким образом, существуют тесные отношения между МТ и инсулином; в патологических условиях эти отношения приобретают реципрокный характер. Отсюда протективный эффект МТ при диабете в значительной мере зависит от исходной патологии.
Антидиабетическая функция МТ на клеточном и системном уровнях может определяться несколькими основными причинами. Важной стороной клеточного эффекта МТ является его влияние на процессы перекисного окисления липидов и уровень свободных радикалов, возрастающих при сахарном диабете. МТ признается одним из самых эффективных естественных антиоксидантов, который выступает в роли «ловушки» свободных радикалов и служит индуктором антиоксидантных ферментов [22, 45]. Кроме того, диабету сопутствует усиление местных воспалительных процессов аутоиммунного характера, а МТ обладает выраженными иммуномодуляторными свойствами [46—48].
На системном уровне МТ синхронизирует биологические ритмы и формирует четкий циркадианный и сезонный периодизм [2, 49]. Поскольку сахарный диабет, как и любая форма патологии, сопровождается дизритмией, то определенную терапевтическую ценность может иметь недавно показанная способность МТ сдвигать фазу суточной секреции инсулина через модуляцию экспрессии так называемых часовых генов, обнаруженных в поджелудочной железе [22, 50, 51]. Нельзя игнорировать и организацию МТ и сезонных периодических процессов [22, 50, 51]. Другой стороной системного эффекта следует признать регуляторное влияние МТ на активность различных эндокринных желез. Особое значение может иметь модуляторное воздействие эпифиза на функцию коры надпочечников [52].
Мелатонин и осложнения сахарного диабета
Согласно современным данным, МТ участвует не только в патогенезе сахарного диабета, но и в ограничении его осложнений. Имеются данные, что МТ ослабляет сердечно-сосудистые нарушения, возникающие у животных при моделировании данной патологии. В изолированной сердечной мышце крыс с алиментарным ожирением, у которых возрастает содержание инсулина и триглицеридов в плазме, при ишемии-реперфузии наблюдались грубые морфологические изменения. Если же животным предварительно регулярно вводили МТ, то подобные сдвиги были выражены гораздо слабее [53]. У крыс со стрептозотоциновым диабетом МТ нормализовал активность печеночной глюкозо-6-фосфатдегидрогеназы, снижал повышенную концентрацию окиси азота в плазме и уменьшал повреждение стенок аорты [12]. У мышей с алиментарным диабетом, длительное время (8 нед) перорально получавших МТ, наряду с восстановлением эндокринного статуса отмечалось усиление инсулиновой вазодилятации в скелетных мышцах и облегчение транспорта углеводов [54].
Защитная роль МТ показана и при диабетических поражениях головного мозга. В частности, если интравентрикулярные инъекции крысам стрептозотоцина провоцировали расстройства памяти, то на фоне предварительного введения МТ (20 мг/кг) наблюдалось ослабление амнезии с параллельным усилением экспрессии инсулиновых рецепторов и фосфорилирования Akt в полях СА1 и СА3 гиппокампа [55]. Хроническое использование более низких (а потому, естественно, и менее эффективных) дозировок МТ у животных со стрептозотоциновым диабетом существенно не отражалось на выраженности нейродегенеративных изменений в неокортексе и гиппокампальной ткани [56].
Подобно антихолинэстеразному ноотропному средству донепезилу, МТ в дозе 20 мг/кг снижал активность холинэстеразы в различных мозговых структурах мышей при одновременном ограничении скополаминовой амнезии [57]. Усиливая экспрессию инсулиноподобного фактора роста в перивентрикулярном белом веществе головного мозга крыс, МТ заметно ослабляли его гипоксическое повреждение [58].
Защитное действие МТ продемонстрировано и в иных ситуациях. Добавление МТ к культуре макрофагов, выделенных из селезенки крыс с аллоксановым диабетом, повышало антиоксидантный статус иммунотропных клеток за счет ограничения свободнорадикальных процессов [59]. Если беременным самкам крыс с экспериментальным диабетом профилактически длительное время вводили МТ, то в таких условиях существенно возрастала способность инсулина предупреждать летальность плодов и развитие врожденных уродств [60].
Заключение
Современные данные со всей очевидностью свидетельствуют об участии МТ в регуляции деятельности поджелудочной железы, поддержании энергетического гомеостаза организма в целом, а потому и в генезе сахарного диабета. Реализация эффектов МТ центрального и периферического происхождения зависит от его взаимодействия со специфическими рецепторами двух основных типов, представленных, в частности, на мембранах β- и α-клеток панкреатических островков. На различных моделях экспериментального диабета, как in vivo, так и in vitro показаны антидиабетические свойства МТ. Они базируются на отношениях с инсулином. Разные типы МР связаны с теми или иными клеточными элементами поджелудочной железы, формой сахарного диабета и особенностями суточного и сезонного образа жизни животных. В основе противодиабетического действия МТ может лежать несколько механизмов. На клеточном уровне основную роль играет, по-видимому, антиоксидантная активность МТ, а на системном — его ритморганизующая активность.
Имеющиеся данные, к сожалению, пока получены преимущественно в экспериментах на животных. Для их экстраполяции на человека необходимы масштабные многоцентровые исследования на больных сахарным диабетом. Правомерность таких исследований определяется естественным происхождением самого МТ с его универсальными адаптогенными свойствами и сравнительной безопасностью, убедительно доказанной опытом его использования при ряде нервных и соматических заболеваний.
Для успешного применения МТ в качестве лечебного средства чрезвычайно важен подбор адекватных доз. В отношении МТ они уже априори не могут быть стандартными и должны зависеть от времени суток и исходного эндокринного статуса.