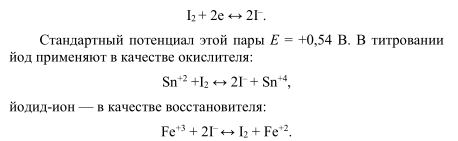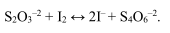ПЕРМАНГАНАТОМЕТРИЯ
ПЕРМАНГАНАТОМЕТРИЯ – метод объемного (титриметрического) химического анализа, основанный на применении стандартного (имеющего строго определенную концентрацию) раствора перманганата калия KMnO4. При действии восстановителей перманганат-ион в кислотной среде переходит в бесцветный катион марганца(2+):
Окончание титрования устанавливается по отсутствию розовой окраски перманганат-иона или с помощью индикатора (например, дифениламина).
Применение перманганатометрии несколько осложняется реакцией, которая может идти в конце титрования в случае недостаточной кислотности раствора и приводит к ошибкам аналитического определения восстановителей:
Эта реакция ускоряется в присутствии диоксида марганца. Для подкисления раствора при перманганатометрии обычно используют серную кислоту, так как соляная кислота (хлорид-ионы) и азотная (примеси оксидов азота) могут окисляться перманганатом калия и тем самым искажать результаты титрования.
При хранении раствора KMnO4 идет его постепенное разложение с выделением кислорода и образованием MnO2, что ведет к изменению концентрации исходного раствора.
Для приготовления стандартного раствора перманганата калия рекомендуется использовать дважды перегнанную дистиллированную воду (при вторичной перегонке к воде добавляют немного KMnO4). Если нет возможности использовать бидистиллят, приготовленный раствор KMnO4 кипятят, охлаждают и отделяют выпавший осадок MnO2 фильтрованием через стеклянный фильтр. Концентрацию (нормальность) раствора KMnO4 устанавливают титрованием точной навески щавелевой кислоты или оксалата натрия.
Перманганатометрически определяют железо(2+), хром(3+), таллий(1+), вольфрам(V), ванадий(IV), сурьму(III), пероксид водорода, гидразин, органические вещества. Перманганатометрическое титрование применяется для определения очень сильных восстановителей, реагирующих с катионами железа(3+), переводя их в катионы железа(2+), которые оттитровывают перманганатом калия. Метод используется также для косвенных определений, например в феррометрии, суть которого заключается в восстановлении окислителей катионами железа(2+), избыток которого реагирует с перманганатом калия.
Обратным перманганатометрическим титрованием определяют восстановители, медленно реагирующие с KMnO4 – такие как иодиды, цианиды, тиоцианаты и т.п.
Крешков А.П. Основы аналитической химии. Качественный и количественный анализ, т. 2. М., Химия, 1965
Бабко А.К., Пятницкий И.В. Количественный анализ. М., Высшая школа, 1968
Харитонов Ю.Я. Аналитическая химия: Аналитика, с 2-х кн. Кн. 2: Количественный анализ. Физико-химические (инструментальные) методы анализа. М., Высшая школа, 2005
2.3.4. Окислительно-восстановительного титрования
2.3.4.4. Перманганатометрия
При титровании в кислых растворах происходит реакция:
Окислительно-восстановительный потенциал данной системы в большей мере зависит от концентрации ионов водорода в растворе:
Окисление перманганатом в слабокислой, нейтральной или слабощелочной средах может проходить по уравнению
Прямое титрование в нейтральных или слабощелочных растворах затруднено тем, что в процессе титрования образуется двуокись марганца, которой надо дать осесть на дно сосуда, чтобы можно было увидеть, какого цвета жидкость над осадком. Тем не менее, такое титрование может дать хорошие результаты, например, при титровании марганца и хрома. В тех случаях, когда процесс окисления требует продолжительного времени, прибавляют KMnO4 в избытке и этот избыток оттитровывают обратно.
В первой стадии восстановления перманганата образуется манганат:
Реальный редокс-потенциал этой реакции в среде 1 моль/л раствора KOH составляет 0,61 В и практически не зависит от рН раствора.
Во второй стадии манганат восстанавливается до соединений Mn(IV):
Из этих двух реакций первая протекает со значительно более высокой скоростью, чем вторая, скорость которой возрастает с повышением [OH].
При этом зеленая окраска манганата меняется и наблюдается образование буро-черного осадка MnO2.
Относительно легко окисляются перманганатом в щелочной среде формиаты, йодиды, йодаты, цианиды, роданиды и все органические вещества, за исключением эфиров, предельных карбоновых кислот (за исключением щавелевой и пировиноградной) и третичных одноосновных спиртов. Интересно отметить, что в щелочной среде перманганат не окисляет оксалаты. Поэтому многие органические вещества окисляются в щелочной среде до оксалатов, а не до карбонатов, например:
Оксидиметрия. Перманганатометрия. Йодометрия. Хроматометрия
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Оксидиметрия
Основные понятия методов оксидиметрии
К методам окислительно-восстановительного титрования (оксидиметрия) относятся все титриметрические методы, в основе которых лежат окислительно-восстановительные реакции. Рабочим раствором является либо раствор окислителя, либо раствор восстановителя, а анализируемым раствором в первом случае — восстановитель, во втором — окислитель.
В зависимости от рабочего раствора в оксидиметрии применяют следующие основные методы:
Эквивалентная молярная масса Mэ окислителя и восстановителя зависит от числа принимаемых или отдаваемых электронов Mэ = Мм / n,
где Мм — молярная масса окислителя или восстановителя;
n — число электронов.
Проведение оксидиметрии возможно только в том случае, если:
1) скорость реакции достаточно велика;
2) можно определить точку эквивалентности.
В зависимости от условий реакции ЕО/В рассчитывается по уравнению Нернста:
В оксидиметрии существуют два типа индикаторов.
Второй тип индикаторов. Происходит изменение окрашивания раствора при изменении потенциала редокс-индикато. Дифениламин ↔ дифенилбензидин. При значении потенциала Е ≥ 0,79 В цвет раствора меняется с бесцветного на синий.
Перманганатометрия
Перманганатометрическим методом объемного анализа называют метод, основанный на окислении различных веществ перманганатом калия (KMnO 4 ). В зависимости от условий, в которых протекает реакция окисления-восстановления, ионы MnO 4 – могут принимать различное число электронов. В кислой среде:
То есть здесь более низкое значение потенциала. Но титрование в этой среде используют гораздо реже, чем в кислой среде. Изменение окрашивания малиновый — коричневый (трудно определить переход в окрашивании раствора). Перманганатометрию используют для определения:
Для метода применяют 0,02–0,05 н растворы перманганата калия (более концентрированные растворы окрашены более интенсивно, менее концентрированные — менее устойчивы при хранении). Необходимо устанавливать титр раствора перманганата через 10 ч после приготовления раствора. Титр устанавливают по оксалату натрия Na2C2O4. Раствор хранят в темных склянках в темном месте.
Молярная масса эквивалента нитрита равна половине его молярной массы. Ход анализа отработан десятилетиями и выполняется по методике, которая учитывает все нюансы.
Йодометрия
Йодометрия — титриметрический (объемный) метод определения веществ, основанный на окислительно-восстановительных реакциях с участием йода иили йодида калия. В основе всех йодометрических реакций лежит реакция:
Проводят йодометрию с индикатором крахмалом, который добавляют перед началом титрования (интенсивное синее окрашивание). Если используют йодид, то титрование проводят непрямым методом. К анализируемому раствору добавляют избыток йодида, затем образующийся йод титруют раствором тиосульфата натрия с образованием тиотионат-иона:
Хроматометрия
Хроматометрией называется метод объемного анализа, основанный на использовании раствора бихромата калия в качестве стандартного. Бихромат калия способен окислять многие неорганические и органичские вещества сульфиты, дитионаты, гексацианоферрат (II), арсениты, иодиды, спирты, гидрохинон, глицерин, аскорбиновую кислоту, тиомочевину и др. В качестве примера ниже приведена используемая в объемном анализе реакция окисления — восстановления, протекающяя с участием бихромата и гексацианоферрата (II)
Методическое пособие для выполнения лабораторно-практических работ по теме «Титриметрический метод анализа. Метод перманганатометрии»
Методическое пособие по выполнению лабораторно-практических работ по теме
«Титриметрический метод анализа. Метод перманганатометрии »
в слабокислой, нейтральной и щелочной средах:
Методом перманганатометрии можно определять и восстановители и окислители. Восстановители титруют непосредственно раствором перманганата, а количество окислителя определяют методом обратного титрования. При обратном титровании к отменному количеству окислителя прибавляют определенный объем восстановителя, взятый в избытке. Избыток восстановителя оттитровывают раствором перманганата калия. Концентрацию добавляемого раствора восстановителя определяют отдельным титрованием его тем же раствором перманганата.
Приготовление рабочего раствора перманганата калия.
Освоить особенность приготовления раствора перманганата калия.
Приготовить рабочий раствор перманганата калия заданной концентрации.
Очень трудно получить перманганат калия в чистом виде. Обычно он загрязнен следами оксида марганца. Кроме того, дистиллированная вода обычно содержит следы веществ, которые восстанавливают перманганат калия с образованием оксида марганца. Раствор, приготовленный обвешиванием определенного количества химически чистой соли, растворением ее и разбавлением в мерной колбе, нельзя считать титрованным. Титр его можно установить не ранее чем через 7 – 12 дней после приготовления раствора. Чтобы раствор был достаточно устойчив и титр его не изменялся, надо удалить из него оксид марганца, для чего необходимо пропустить раствор перед его употреблением через фильтр.
Надо иметь в виду, что перманганат калия окисляет резину, корковые пробки, фильтровальную бумагу, поэтому нельзя фильтровать перманганат калия через бумажный фильтр, а использовать для этих целей стеклянные фильтры.
При титровании перманганатом калия применяют бюретки со стеклянным краном. Бюретки и другую стеклянную посуду нельзя оставлять на продолжительное время с раствором перманганата калия, так как на стекле образуется налет оксида марганца коричнево-бурого цвета. Отмывают налет на стекле концентрированной соляной кислотой или смесью 2н. серной кислоты с раствором соли Мора или щавелевой кислоты.
Методом перманганатометрии можно определить
КЛАССИФИКАЦИЯ МЕТОДОВ. ИНДИКАТОРЫ. ПЕРМАНГАНАТОМЕТРИЯ. БИХРОМАТОМЕТРИЯ
Методы окислительно-восстановительного титрования основаны на использовании реакций, связанных с переносом электронов, то есть окислительно-восстановительных процессов.
Реакции окисления-восстановления – это реакции, в которых реагирующие вещества присоединяют или отдают электроны. Окислителем называется частица (ион, молекула, элемент), которая присоединяет электроны и переходит при этом из более высокой степени окисления в более низкую, т.е. восстанавливается. Восстановитель – это частица, которая отдает электроны и переходит при этом из более низкой степени окисления в более высокую, т.е. окисляется.
Методы окислительно-восстановительного титрования пригодны для определения многих органических соединений, в том числе фармацевтических препаратов, подавляющее большинство которых являются потенциальными восстановителями.
В зависимости от свойств используемого титранта различают оксидиметрию и редуктометрию.
Направление реакций окисления-восстановления зависит от соотношения энергии сродства высших степеней окисления реагирующих частиц к электронам.
В настоящее время не существует методов, позволяющих экспериментально определить абсолютное значение энергии сродства электрона к находящимся в растворе частицам и сопоставить эти значения между собой. Для сравнения служит водородный электрод, в котором энергия сродства электрона к ионам водорода принята равной нулю. Водородный электрод – это платиновая пластинка, покрытая платиновой чернью, которая насыщена газообразным водородом.
Значение стандартного потенциала определяется не только природой данной пары, но и активностью частиц. Зависимость потенциала Е от активности выражается уравнением Нернста:
Подставим в уравнение численные значения констант и преобразуем натуральный логарифм в десятичный. Тогда
Если реакция окисления-восстановления проходит с участием катионов водорода, то скорость ее увеличивается с увеличением их концентрации согласно закону действующих масс. В этом случае увеличивается и реальный редокс-потенциал системы. Например, для системы:
Реальная величина редокс-потенциала существенно зависит от концентрации кислоты; в присутствии концентрированной H2SO4 ее значение увеличивается от + 1,51 до + 1,9 В для реакции (2).
Определение конечной точки титрования в редокс-методах осуществляют безындикаторным методом или с помощью специ-фических и редокс-индикаторов.
Одним из наиболее широко известных редокс-индикаторов является дифениламин:
Под действием окислителей дифениламин по необратимой реакции сначала образует дифенилбензидин:

Далее бесцветный дифенилбензидин обратимо окисляется до окрашенного в интенсивный сине-фиолетовый цвет дифенилбен-зидина фиолетового:

ПЕРМАНГАНАТОМЕТРИЯ
Продукты восстановления перманганат-ионов могут быть различ-ными в зависимости от рН среды:
Ø в сильнокислой среде
Ø слабокислой или нейтральной среде
Ø слабощелочной среде
Титрованный раствор калия перманганата по точной навеске кристаллического препарата приготовить невозможно, так как в нем всегда содержатся некоторое количество МnО2 и другие продукты разложения. Перед установлением точной концентрации раствор КМnО4 выдерживают в темной склянке в течение 7-10 дней. За это время происходит окисление восстановителей, присутствие которых в дистиллированной воде полностью исключить не удается (пыль, следы органических соединений и т. п.). Для ускорения этих процессов раствор калия перманганата иногда кипятят. Необходимо учитывать, что вода обладает окислительно-восстановительными свойствами и может восстанав-ливать перманганат. Эта реакция идет медленно, но МnО2 и прямой солнечный свет катализируют процесс разложения КМnО4, поэтому через 7-10 дней осадок МnО2 необходимо удалить. Раствор КМnО4 обычно осторожно сливают с осадка или фильтруют через стеклянный фильтр. Приготовленный таким образом раствор КМnО4 не слишком низкой концентрации (0,05 моль/дм 3 и выше) и не изменяет титр продолжительное время. Титр раствора калия перманганата чаще всего устанавливают по безводному натрия оксалату Na2C2O4 или щавелевой кислоте Н2С2О4 ∙ 2Н2О:
Первые капли перманганата даже в горячем растворе обесцве-чиваются очень медленно. В ходе титрования концентрация ионов Мn 2+ возрастает, и скорость реакции увеличивается. Титр перманга-ната калия можно установить также по мышьяка (ІІ) оксиду или металлическому железу. Использование для установления титра металлического железа особенно целесообразно, если в дальнейшем предполагается перманганатометрическое опреде-ление этого элемента.
Этот процесс ускоряется на свету, поэтому растворы окса-латов рекомендуется хранить в темных склянках. Подкисленные растворы оксалатов более устойчивы, чем нейтральные или щелочные.
В перманганатометрии часто обходятся без применения специального индикатора, так как сам перманганат имеет интенсивную окраску, а его избыточная капля вызывает появление неисчезающей в течение 30 с розовой окраски pacтвора. При титровании разбавленными растворами применяют редокс-индикаторы, такие как дифениламинсульфокислота или ферроин (координационное соединение Fe (ІІ) с 1,10-фенантролином). Определение конечной точки титрования выполняют также потенциометрическим или амперометрическим методами.
Перманганатометрическим методом можно определить:
Например, при анализе свинца диоксид пробу растворяют в сернокислом растворе щавелевой кислоты:
и избыток щавелевой кислоты оттитровывают калия перманганатом.
Перманганатометрически можно определить ионы, не обладающие окислительно-восстановительными свойствами (титрование заместителя). Этим методом могут быть определены, например, катионы кальция, стронция, бария, свинца, цинка и другие, которые образуют малорастворимые оксалаты.
Этим методом можно определить также муравьиную, винную, лимонную, салициловую и другие кислоты, глицерин, фенол, формальдегид и другие органические соединения.
Перманганатометрия является фармакопейным методом анализа.
Титрантом метода является раствор 0,1 моль/дм 3 К2Сr2О7.
Поскольку К2Сr2О7 является стандартным веществом, из него готовят титрант первичной стандартизации.
Определение конечной точки титрования в этом методе проводят следующим образом:
— е + Fe 2+ ↔ Fe 3+ 6 Е 0 = 0,771 В;
В качестве индикатора используют натрия фениламиносульфонат, при этом окраска раствора в момент эквивалентности изменяется от зеленой до фиолетовой.
Растворы калия дихромата следует хранить в закрытой посуде в темном месте. В этих условиях титр раствора остается стабильным в течение продолжительного времени.
ЦЕРИМЕТРИЯ
Таким образом, ионы церия (IV) по окислительным свойствам близки к перманганату. Анализ цериметрическим методом проводят в кислой среде. При этом следует иметь в виду, что потенциал редокс-пары Се 4+ / Се 3+ в значительной мере зависит от природы используемой кислоты, анионы которой входят в состав комплексов с катионами.
Обычно готовят титрованные растворы церия (IV) сульфата. При их приготовлении прибавляют определенное количество серной кислоты, чтобы растворы имели рН ≤ 1. Это препятствует гидро-лизу с образованием малорастворимых основных солей церия и приводит к их устойчивости в течение длительного времени. Растворы, подкисленные соляной или азотной кислотой, менее устойчивы в результате разложения воды.
Конечную точку титрования определяют следующим образом:
Ø с помощью кислотно-основных индикаторов метилового оранжевого, метилового красного (в момент эквивалентности происходит необратимое окисление индикатора титрантом и соответственно происходит изменение окраски);
Метод используют для определения восстановителей:соединений олова (П), мышьяка (III), сурьмы (IП), железа (П), Н2О2, йодидов, нитритов и др. Определяют также органические вещества: фенолы, углеводы, щавелевую кислоту, аскорбиновую кислоту.



При определении Fe 2+ протекает следующая реакция:
— е + Fe 2+ ↔ Fe 3+ 1 Е 0 = 0,77 В;
+ е + Се 4+ → Се 3+ 1 Е 0 = 0,45 В
Fe 2+ + Се 4+ → Fe 3+ + Се 3+
БРОМАТОМЕТРИЯ
Метод основан на окислительных свойствах КвrО3:
Например, окисление арсенитов в кислой среде броматом протекает по уравнению:
Например, при определении стрептоцида протекает реакция:
К анализируемому раствору, содержащему стрептоцид, добавляют H2SО4, раствор КВг, индикатор метиловый оранжевый и титруют стандартным раствором КВгО3 до исчезновения розовой окраски. Титрантом метода является раствор 0,1 моль/дм З калия бромата КВгО3. Так как КвгО3 является стандартным веществом, из него готовят титрант первичной стандартизации.
Конечную точку титрования в броматометрии определяют с помощью индикаторов метилового оранжевого или метилового красного, которые обесцвечиваются избыточной каплей титранта в результате их необратимого окисления бромом в конечной точке титрования.
Методом броматометрии определяют следующие органические соединения: фенол, резорцин, салициловую кислоту, стрептоцид и др.