Лекарственная терапия
С помощью лекарств сегодня лечат большинство опухолей. Это самый универсальный и самый распространенный метод лечения рака в силу его особенностей:
Виды лекарственной терапии
С развитием нанотехнологий, молекулярной медицины и генной инженерии в портфеле онкологов появились множество новых противоопухолевых препаратов, лекарства стали более избирательными к злокачественным клеткам и менее токсичными для здоровых тканей и организма в целом. Появились прицельные лекарства, так называемые таргетированные, молекулы которых воздействуют более избирательно на клетки рака.
Все лекарства против рака по механизму действия делят на цитостатические и цитотоксические. Первые, цитостатические, тормозят размножение злокачественных клеток и вызывают их апоптоз, или программу самоуничтожения, клеточный распад. Вторые, цитотоксические, препараты вызывают гибель клеток вследствие их интоксикации, разрушения оболочки и ядра клетки, других структур, и в конечном итоге некроз опухоли.
Учитывая разные механизмы действия, в большинстве случаев онкологи подбирают комбинацию из двух-трех препаратов разных фармакологических групп.
К лекарственному лечению онкологических заболеваний относят:
Лекарственное лечение обычно проводится курсами. Курс включает время введения препарата (от 1 до 5 дней для внутривенных препаратов, может быть дольше для таблетированных препаратов) и время перерыва для восстановления организма и снижения риска побочных эффектов лечения. Перед началом каждого нового курса обычно производится контроль анализов крови и консультация врача онколога для решения вопроса о необходимости корректировки доз препаратов и/или увеличения интервала до следующего введения препарата.
Для длительного лекарственного лечения есть понятие «линий» лечения. «Линия» лечения – последовательное назначение одинаковых курсов химио- (или других видов) терапии. «Линия» лечения проводится до достижения необходимого эффекта или до момента потери чувствительности со стороны болезни. Если опухоль продолжила расти на фоне одной схемы химиотерапии – производится смена лекарств. Продолжение лечения с использованием новой схемы химиотерапии называется «Второй (третьей, четвёртой и т.д.) линией» лечения.
Химиотерапия
Химиотерапия – наиболее распространённый вид лекарственной терапии. Химиотерапия бывает:
1. Лечебной – когда химиотерапия является основным методом лечения заболевания. Например, для многих пациентов с лейкозами, лимфомами, герминогенными опухолями яичка химиотерапия может быть основным методом лечения, который часто приводит к выздоровлению. Для большинства пациентов с распространёнными формами рака, с метастазами в различные органы, химиотерапия является основным методом лечения, дающим максимальную возможность длительно сдерживать болезнь.
2. Неоадъювантной – когда химиотерапия предшествует основному методу лечения. Чаще всего такая химиотерапия назначается перед некоторыми видами операций, с целью уменьшения опухоли и снижения активности её клеток.
3. Адъювантной – её ещё называют «профилактической». Она назначается после основного метода лечения, чаще всего после операции, с целью снижения риска возврата болезни.
Гормональная терапия
Показана только для гормоночувствительных видов рака. Будет ли опухоль реагировать на лечение гормонами или нет, определят с помощью специальных анализов и лабораторных исследований клеточного материала, взятого из опухоли.
Опухоли, реагирующие на гормоны, часто обнаруживают в репродуктивной системе и железах внутренней секреции, например, это:
На поздних неоперабельных стадиях опухолей, чувствительных к данному лечению, гормональная терапия может использоваться в качестве основного лечения. Как паллиативное лечение некоторых видов рака она достаточно эффективна и может продлить жизнь пациента на 3-5 лет.
Иммунотерапия
Иммунитет играет важную роль в профилактике и борьбе с раком. В норме иммунные тельца распознают атипичную клетку и убивают ее, защищая организм от развития опухоли. Но когда иммунитет нарушается в силу разных причин, и раковых клеток становится много, тогда опухоль начинает расти.
Иммунотерапия при раке помогает организму справится с заболеванием за счет активизации защитных ресурсов и не допустить развития повторных опухолей и метастазов. В онкологии используют интерфероны, вакцины от рака, интерлейкины, колониестимулирующие факторы и другие иммунные препараты.
Лечение подбирает иммунолог на основе лабораторных данных о состоянии иммунной системы онкопациента совместно с лечащим врачом-онкологом и другими специалистами, участвующими в лечении конкретного пациента.
Основные механизмы иммунотерапии:
Таргетная терапия
Таргетные лекарства очень специфичны и разрабатываются под конкретный мутировавший ген раковой клетки данного вида опухоли. Поэтому до таргетного лечения обязательно проводят генетическое исследование материала, взятого на биопсию.
Например, разработаны эффективные таргетные препараты для лечения различных генетических форм рака молочной железы, множественной миеломы, лимфомы, рака предстательной железы, меланомы.
В силу своей специфики и целевого попадания на раковую клетку-мишень таргетные препараты более эффективны для лечения опухолей, чем например, классические противоопухолевые. И менее вредны для нормальных клеток, не обладающими характеристиками опухолевых. Многие таргетные методы относят к иммунотерапии, так как по сути они формируют нужный иммунный ответ.
Фотодинамическая терапия
Осуществляется препаратами, воздействуя световым потоком определённой длины волны на раковые клетки и разрушая их.
Побочные эффекты лекарственного лечения рака
Выраженные осложнения наблюдаются далеко не у всех пациентов, но риск их возрастает с увеличением продолжительности лечения.
Часто встречаются следующие побочные эффекты после проведения лекарственной терапии:
Большинство осложнений поддаётся корректировке, при правильном проведении лечения многие из них можно предотвратить или остановить при первом проявлении. Тяжёлые осложнения могут быть причиной увеличения интервалов между курсами химиотерапии.
Эффективность
Чем раньше обнаружен рак и точнее диагностирован тип опухолевых клеток, тем успешнее лечение рака и благоприятнее прогноз выздоровления. Поэтому следует постоянно следить за состоянием своего здоровья, проходить диагностические исследования согласно возрасту, не закрывать глаза на недомогание или периодический дискомфорт в теле. Также лучше не тратить время на попытки вылечиться самостоятельно или при помощи нетрадиционной медицины, не имеющей никаких убедительных данных об эффективности, игнорируя современные методы медицинского лечения. Так можно только запустить онкологический процесс, усугубить стадию заболевания и затруднить последующее лечение. Не теряйте драгоценное время, обследуйтесь в специализированных центрах на современном оборудовании у высококвалифицированных врачей.
Мхт химиотерапия что это
Клинический научно-практический центр специализированных видов медицинской помощи (онкологический), Санкт-Петербург, Россия
Введение
На сегодняшний день перспективным методом лекарственного лечения злокачественных новообразований являются стратегии, основанные на поиске и подавлении «триггерных» мишеней с учетом биологии роста опухоли [1]. К ним относятся следующие ингибиторы:
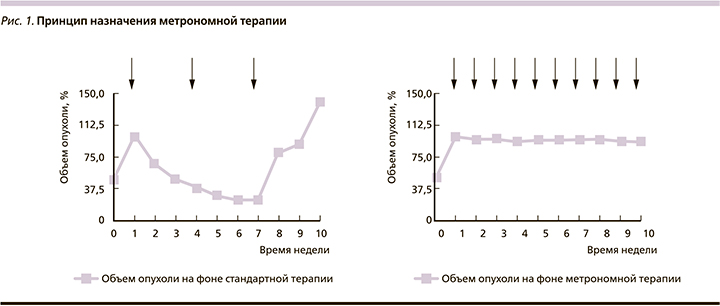
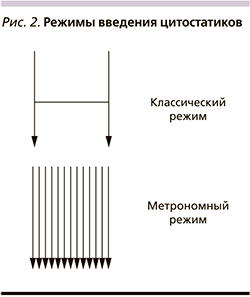
В итоге в арсенале клинического онколога принципиально имеются следующие возможности воздействия на злокачественные клетки: цитостатики, таргетная терапия, иммунотерапия и экспериментальные направления, целью которых служат регуляция метаболизма опухоли и эпигенетическая терапия. В результате подобные методы, безусловно, приводят к увеличению продолжительности жизни. Например, лекарственная терапия современными препаратами увеличивает медиану общей выживаемости больных раком молочной железы (РМЖ) с 32 до 50 месяцев [2],толстой кишки с 5–6 до 30 [3], желудка с 3–5 до 16 [4], легкого с 3,9 до 36 месяцев [5]. С другой стороны, иммунотерапевтические принципы лечения позволяют обсуждать 20%-ную возможность излечения. К сожалению, подобные успехи в большинстве своем характерны для определенной группы больных с учетом специфических предиктивных факторов [6]. В общей популяции подобная тенденция не столь выражена. Это обусловлено многими факторами, к которым относятся особенности кинетики роста, гетерогенность опухолевой популяции, опухолевая эволюция, репопуляция клеток, лекарственная резистентность, микроокружение или опухолевый матрикс, эпигенетические нарушения, тканевая иммуносупрессия, константы гомеостаза (pH, гликемия), стволовые клетки [7]. С целью возможности преодоления подобной резистентности опухолевых клеток разрабатываются новые стратегии терапии. К ним относится метрономная терапия (МТ) злокачественных опухолей. Это один из вариантов dose-dense терапии, в котором химиопрепараты назначаются через определенные короткие промежутки времени (часы, дни, недели) в низких (10–40% от терапевтической) дозах с целью увеличения продолжительности жизни больных неизлечимыми диссеминированными солидными опухолями [8]. Концепция применения метрономной терапии заключается в торможении роста злокачественных клеток, что теоретически снизит вероятность достижения «летального» объема опухоли и тем самым может повлиять на показатели выживаемости (рис. 1).
Метрономная терапия: от истоков к современности
История МТ началась с работ J. Folkman, который предположил возможность терапевтического воздействия на опухолевый ангиогенез [9]. В 1991 г. в лаборатории R. Kerbel было показано влияние цитостатиков на сосудистое русло в опухоли. В дальнейшем исследования Klement и Browder продемонстрировали возможность достижения значительного торможения роста опухоли низкими дозами химиопрепаратов на различных преклинических моделях. В то же время Hanahan предложил термин «метрономная терапия» [10].
Механизм действия МТ заключается в снижении пролиферации и ангиогенного потенциала эндотелиоцитов в опухоли, повышении экспрессии тромбоспондина-1, подавлении функции циркулирующих эндотелиальных клеток, блокаде мобилизации клеток-предшественниц эндотелиоцитов из костного мозга, а также в нормализации структуры сосудистой сети и в повышении перфузии опухолевой ткани.
Кроме того, обсуждается значительное влияние низких доз цитостатиков на регуляцию иммунной системы организма в виде повышения иммуногенности и возможности презентации антигенов, на мобилизацию антиген-презентирующих клеток, подавление функции Т-регуляторов и на повышение активности цитотоксических лимфоцитов. Несомнен факт их прямого воздействия на опухолевые клетки [11].
В качестве примера изучено антиангиогенное действие препаратов, связывающих микротрубочки. Оно заключается в повышении динамической нестабильности микротрубочек, нарушении переориентации центра организации микротрубочек, ослаблении сигнала от рецептора сосудистого эндотелиального фактора роста 2-го типа, пониженнии активации интегрина, ингибировании сигнала FAK/паксиллин/AKT, потере Hsp90, ингибировании активации eNOS, нарушении образования фокальных контактов, пониженной пролиферации и поляризации клеток, подавлении миграции клеток, разрушении связи микротрубочка+белок TIP, реорганизации актина в стресс-волокна, ингибировании сигнала Ras/Erk/Net (Elk3), повышении фосфорилирования MLC и сократимости актиномизина, изменении сигнала Rho-GTP-аза, разрушении VE-кадгерина, ингибировании сигнала VE-кадгерин/β-катенин/AKT, ингибировании образования трубочек, повышении проницаемости клеток, в регрессии капиллярных трубочек [12].
Эффективность МТ продемонстрирована во многих клинических исследованиях. Объективный ответ опухоли на лечение в среднем составлял 19–34% [15]. Мета-анализ 22 исследований метрономного режима при РМЖ, в который были включены 1360 больных, показал клиническую эффективность в 55% случаев, время до прогрессирования 6 месяцев — 56% больных и 2-летнюю общую выживаемость — 40% [15]. Среди особенностей подобных работ можно выделить следующие: в основном исследования I—II фаз, гетерогенность включенных пациентов, эмпирический выбор цитостатиков и режима, использование в качестве оценки эффективности лечения объективного ответа, а не общей выживаемости. В целом для МТ при РМЖ предпочтение отдавалось препаратам с высокой биодоступностью при применении внутрь и возможности частого внутривенного введения цитостатиков. В качестве примера назначение пожилым больным винорелбина внутрь в метрономном режиме приводило к увеличению времени до прогресирования болезни до 9,2 месяца [16].
Эффективность комбинации метрономного режима применения цитостатиков была продемонстрирована в исследовании VICTOR-2. В нем приняли участие 80 больных, из которых у 28 был диагностирован тройной негативный фенотип РМЖ. Капецитабин и винорелбин назначались в 1-й (35 больных) и 2-й линиях (45 больных) лечения. Частота объективного ответа составила 35,5 и 25,6% соответственно. Время до прогрессирования, превысившее 1 год, регистрировалось более чем у 20% больных. При этом клинически значимой токсичности практически не наблюдалось: фебрильная нейтропения была зарегистрирована у 0,4%, а слабость у 0,7% больных [17]. Низкая токсичность при применении метрономного режима применения цитостатиков послужила основанием исследования тройной комбинации препаратов в низких дозах при РМЖ. В исследовании VEX время до прогрессирования на фоне метрономного применения циклофосфамида, капецитабина и винорелбина в первой линии лечения составило 25,1 месяца [18]. Несмотря на активное изучение новых метрономных доз винорелбина, в клинические рекомендации лечения РМЖ в Российской Федерации входят следующие эффективные режимы его применения: 60 мг/м2 внутрь в 1-й, 8-й и 15-й дни; с 22-го дня — 80 мг/м2 1 раз в неделю.
По сравнению со стандартным режимом введения метрономный винорелбин демонстрирует схожую эффективность при более низкой токсичности. В исследовании XeNa объективный ответ опухоли составил 21,4 и 20,8%, клиническая эффективность — 37 и 41%, общая выживаемость — 660 и 701 день соответственно [19].
Заключение
Таким образом, МТ представляет собой новую парадигму лекарственного лечения в связи с интегрирующим воздействием как на опухолевые клетки, так и на их микроокружение. Данный подход демонстрирует клиническую эффективность определенной группы больных, резистентных к стандартной терапии. При этом длительная стабилизация процесса (более 6 месяцев), вероятно, может быть суррогатным маркером увеличения продолжительности жизни. С учетом механизма действия низких доз цитостатиков перспективным считается комбинация препаратов с различными терапевтическими опциями (иммунотерапия, антиангиогенная терапия).
На сегодняшний день подобная стратегия терапии требует изучения предиктивных маркеров. А с целью получения доказательной базы, безусловно, необходимо проведение масштабных рандомизированных исследований.
Литература
1. Hanahan D., Weinberg R.A. Hallmarks of cancer: the next generation. Cell. 2011;144(5):646–74. Doi: 10.1016/j.cell.2011.02.013.
2. Engel, J., Schubert-Fritschle G., Emeny R., Hölzel D.Breast cancer: are long-term and intermittent endocrine therapies equally effective? J Cancer Res Clin Oncol. 2020 May 29. Doi: 10.1007/s00432-020-03264-0.
3. Aggarwal H., Sheffield K.M., Li L., et al. Primary tumor location and survival in colorectal cancer: A retrospective cohort study. World J Gastrointest Oncol. 2020;12(4):405–23. Doi: 10.4251/wjgo.v12.i4.405.
4. Yarema R., Оhorchak М., Hyrya P., et al. Gastric cancer with peritoneal metastases: Efficiency of standard treatment methods. World J Gastrointest Oncol. 2020;12(5):569–81. Doi: 10.4251/wjgo.v12.i5.569.
5. Xu E., David E.A., Ding L., et al. Sequence of biologic therapies and surgery affects survival in non-small cell lung cancer. J Surg Oncol. 2020. May 20. Doi: 10.1002/jso.25937.
6. Cristescu R., Mogg R., Ayers M., et al. Pan-tumor genomic biomarkers for PD-1 checkpoint blockade-based immunotherapy. Science. 2018;362(6411):eaar3593. Doi: 10.1126/science.aar3593.
7. Murciano-Goroff Y.R., Warner A.B., Wolchok J.D.The future of cancer immunotherapy: microenvironment-targeting combinations. Cell Res. 2020. Doi: 10.1038/s41422-020-0337-2.
8. Hanahan D., Bergers G., Bergsland E. Less is more, regularly: metronomic dosing of cytotoxic drugs can target tumor angiogenesis in mice. J Clin Invest. 2000;105(8):1045–47. Doi: 10.1172/JCI9872.
9. Abdollahi A., Hlatky L., Huber P.E. Endostatin: the logic of antiangiogenic therapy. Drug Resist Updat. 2005;8(1–2):59–74. Doi: 10.1016/j.drup.2005.03.001.
10. Bocci G., Kerbel R.S. Pharmacokinetics of metronomic chemotherapy: a neglected but crucial aspect. Nat Rev Clin Oncol. 2016;13(11):659–73. Doi: 10.1038/nrclinonc.2016.64.
11. André N., et al. Metronomics: towards personalized chemotherapy? Nat Rev Clin Oncol. 2014. Doi: 10.1038/nrclinonc.2014.89.
12. Schwartz E.L. Antivascular actions of microtubule-binding drugs. Clin Cancer Res 2009;15(8):2594–601. Doi: 10.1158/1078-0432.CCR-08-2710.
13. Shaked Y., Pham E., Hariharan S. Evidence Implicating Immunological Host Effects in the Efficacy of Metronomic Low-Dose Chemotherapy. Cancer Res. 2016;76(20):5983–993. Doi: 10.1158/0008-5472.CAN-16-0136.
14. Briasoulis E., Aravantinos G., Kouvatseas G. Dose selection trial of metronomic oral vinorelbine monotherapy in patients with metastatic cancer: a hellenic cooperative oncology group clinical translational study. BMC Cancer. 2013;13(1):263. Doi: 10.1186/1471-2407-13-263.
15. Cazzaniga M.E., Munzone E., Bocci G. Pan-European Expert Meeting on the Use of Metronomic Chemotherapy in Advanced Breast Cancer Patients: The PENELOPE Project. Adv Ther. 2019;36(2):381–406. Doi: 10.1007/s12325-018-0844-4.
16. De Iuliis F., Salerno G., Taglieri L., et al. On and off metronomic oral vinorelbine in elderly women with advanced breast cancer. Tumori. 2015;101(1):30–5. Doi:10.5301/tj.5000207.
Химиотерапия: что это и как ее делают при онкологии
Лекарственная противоопухолевая терапия, в том числе и химиотерапия, – один из основных методов лечения рака. При химиотерапии в человеческий организм вводятся различные токсические вещества, которые губительно воздействуют на клетки злокачественных опухолей. Важно при этом, чтобы яды и токсины оказывали наименьшее отрицательное воздействие на весь организм больного.
Схемы химиотерапевтического лечения регламентируются международными методиками и правилами, и рассчитываются индивидуально. Врач-химиотерапевт подбирает пациенту лечение, руководствуясь различными критериями, среди которых:
Виды химиотерапии
Сложные комбинации из нескольких химиопрепаратов на сегодняшний день используются чаще, так как они более эффективные.
Химиотерапия нередко применяется как часть комбинированного лечения рака:
Дозы и режимы применения противоопухолевых препаратов
Противоопухолевые лекарственные препараты и их дозировка подбираются строго индивидуально.
У каждого препарата имеются свои характеристики и особенности. При проведении химиотерапии важными являются следующие параметры:
Дозу препарата рассчитывают исходя из схемы химиотерапии, роста, веса, возраста, состояния больного, а в некоторых случаях, на основании лабораторных показателей пациента.
Режимы
Если необходимо повысить интенсивность химиотерапии, то увеличивают дозу препарата, это так называемая высокодозная терапия, либо сокращают интервал между курсами ХТ, то есть вводят уплотненные режимы.
Также существуют метрономные режимы применения цитостатических препаратов, когда вводятся малые дозы препаратов, но постоянно в течение длительного времени.
После каждого курса химитерапевтического лечения обязательно делается определенный перерыв для восстановления организма. Как правило, повторные курсы ХТ проводят через каждые три-четыре недели, это период, в течение которого восстанавливаются показатели лейкоцитов, тромбоцитов и пр.
При использовании некоторых химиопрепаратов, к примеру, нитрозопроизводных, этот интервал увеличивается до 6 недель.
Продолжительность лечения и количество курсов химиотерапии зависит от вида опухоли, от особенностей течения болезни от того, как организм реагирует на лечение. Иногда возникает необходимость прекратить или изменить лечение, и это решение принимает лечащий врач.
Способы применения химиопрепаратов
Правила введения противоопухолевых препаратов
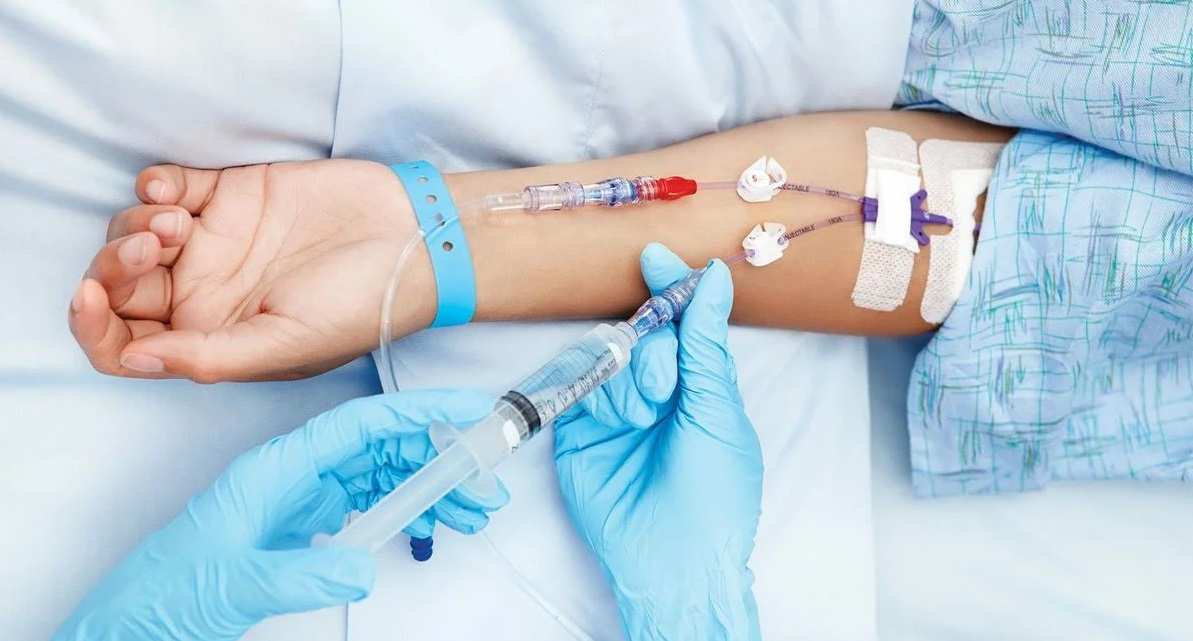
Наиболее широко используется внутривенное введение противоопухолевых средств. При этом врач обязательно учитывает индивидуальные особенности вен пациентов.
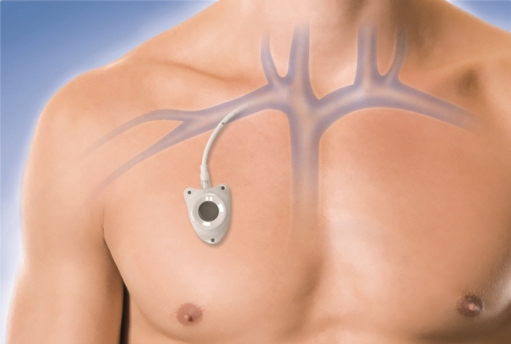
Имплантируемые порт-системы
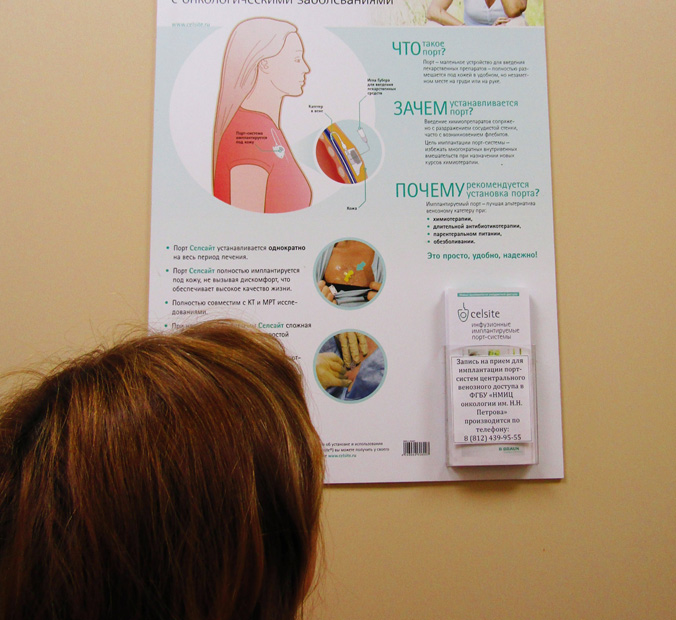
Имплантируемая порт-система — это катетер, установленный в сосуд или полость и соединенный с ним резервуар-камера. Система «порт — катетер» широко используется в медицине уже более чем 30 лет.
Порт-системы помогают проходить лечение более эффективно, безопасно и качественно. Особенно актуальна их установка в качестве устройства сосудистого доступа пациентам, которым назначено длительное лечение, при осложнениях на фоне химиотерапии, которые привели к затруднению венозного доступа.
При этом терапию пациент может получать как в условиях стационара, так и амбулаторно.
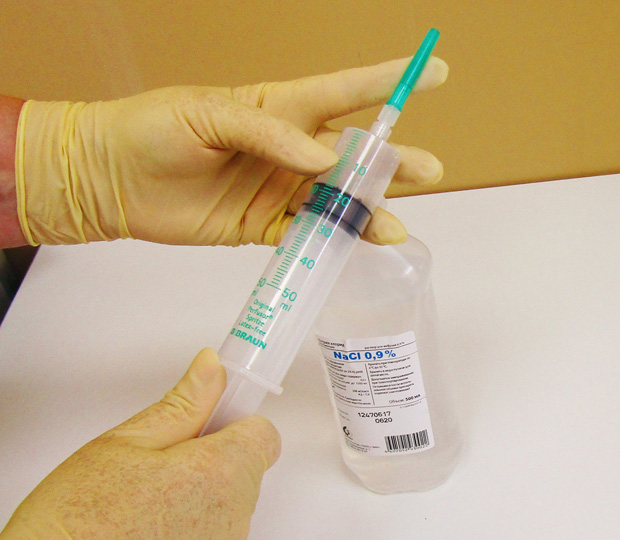
Инфузия лекарственных препаратов производится с помощью специальных игл типа Губера, которые, пунктируя силиконовую мембрану порта, позволяют вводить инфузионный раствор в резервуар, не повреждая силиконовую мембрану. Далее препарат попадает через катетер в кровоток или полость, в зависимости от вида порт-системы и места расположения катетера.
Порт- система полностью скрыта под кожей. Поэтому она подходит для длительного использования, не обременяет пациента и не мешает проведению гигиенических процедур. Необходимо помнить, что при отсутствии использования порт-систему необходимо промывать как минимум 1 раз в 2 месяца.
Подготовка к химиотерапии
Чтобы не было проблем с поиском вен и установкой катетера за день до химиотерапии желательно выпить 1,5-2 литра жидкости.
Для тренировки вен рекомендуется периодически сжимать кистевой эспандер по 10 мин 3 раза в день или до усталости. При этом рука должна быть свешена ниже уровня сердца.
В день проведения ХТ нужно держать руки в тепле, возможно применение теплых обертываний на места инъекций. Можно периодически обрабатывать руки теплыми полотенцами.
Во время прохождения химиотерапии
В день химиотерапии, с утра необходимо позавтракать.
Далее необходимо соблюдать несколько несложных правил:
Об осложнениях после химиотерапии читайте здесь.
Возможно ли повысить эффективность химиотерапии?
Поиск основных направлений повышения эффективности терапии опухолей осуществляется в разных направлениях:
Лекарственная противоопухолевая терапия: химиотерапия
Мы не советуем обсуждать лечение с другими пациентами в коридорах и кабинетах, искать ответы на вопросы в интернете, на форумах в переписке с «бывалыми». Помните о вашей индивидуальности! Вы получаете персонализированное лечение по поводу именно вашего заболевания, с учетом индивидуальных особенностей и согласно только вашему плану лечения. Все возникшие вопросы обсуждайте с лечащим врачом. Рекомендации, полученные в непроверенных источниках, могут быть ошибочными и представлять опасность для здоровья.
Что такое химиотерапия?
Химиотерапия (ХТ) – это один из нескольких видов противоопухолевого лекарственного лечения. Это системное лечение, которое проникает практически во все органы и ткани. Ограничено поступление ХТ в головной мозг и яички у мужчин. Препараты, которые используются при химиотерапии, называют цитостатиками. Они действуют в первую очередь на активно делящиеся клетки, к которым относятся опухолевые клетки. Однако кроме них активно обновляются и делятся также и нормальные клетки: кожи, кроветворения и слизистой желудочно-кишечного тракта. Поэтому на фоне химиотерапии возможны различные осложнения: изменения кожи, выпадение волос, анемия, тромбоцитопения, лейкопения, стоматиты, рвота и диарея.
Обязательна ли для меня химиотерапия и эффективна ли она при моем заболевании?
Химиотерапия является обязательным этапом комбинированного или комплексного лечения большинства опухолей. Чувствительность опухолей к химиотерапии варьируется от возможного полного излечения (например, хориокарцинома матки, герминогенные опухоли, острый лимфобластный лейкоз у детей, лимфома Ходжкина, опухоль Беркитта) до малочувствительности к ХТ (например, рак печени) или отсутствия чувствительности к ХТ (например, почечноклеточный рак). Во время первого приема в отделении химиотерапии вас консультирует врач-онколог, обладающий большим опытом лекарственного лечения онкологических заболеваний. Решение о назначении того или иного вида лечения принимается консилиумом врачей с учетом данных гистологического, иммуногистохимического, молекулярно-генетического обследований, а также данных лабораторного, инструментального, лучевых методов обследования. При неоднозначности в назначении лекарственной терапии врач всегда обсудит с вами плюсы и минусы ее назначения и учтет ваше мнение при принятии решения.
Зачем проводится химиотерапия и существуют ли другие методы лечения?
При онкологических заболеваниях чаще всего используется комбинированное лечение. Это означает, что химиотерапия применяется как один из этапов лечения, наряду с хирургическим лечением и/или лучевой терапией. Однако, в некоторых случаях лекарственное лечение является единственным методом, который может быть применен. Выбор тактики полностью зависит от целей лечения. Соответственно, лекарственная терапия может проводиться для:
Как долго будет проводиться лечение и с какой частотой вводятся препараты?
Длительность лечения зависит от стадии и агрессивности заболевания, задач лечения, чувствительности опухоли к химиотерапии, а также режима и схемы ХТ. Получать цитостатики пациент может ежедневно, еженедельно или ежемесячно. Сама по себе химиотерапия – это курсовое лечение. Обычно курс включает 6-8 циклов химиотерапии, однако данный показатель определяется индивидуально. Наиболее часто используемая схема лечения – «цикл каждый 21 день». B цикл входит период непосредственного использования препаратов с самого первого дня и перерыв между их применением. Например, для введения противоопухолевых препаратов в течение первых 3 дней «каждого 21-дневного цикла» подразумеваются 3 дня непосредственного лечения и 18 дней «отдыха». Далее начинается очередной цикл. Перерыв между введениями цитостатиков, который продолжается в среднем 3 недели, позволяет организму построить новые здоровые клетки, восстановить силы и подготовиться к очередному циклу лечения.
Как вводятся лекарственные препараты, которые я буду получать?
Противоопухолевые препараты могут вводиться внутривенно, внутримышечно или приниматься внутрь через рот. Эффективность проводимого лечения никак не связана со способом введения лекарств. Однако большинство противоопухолевых препаратов вводятся в кровоток, т.е. внутривенно. Длительность введения препаратов разнится. Некоторые вводятся струйно, другие могут вводиться от 10 минут до нескольких часов или даже дней. При частых или многочасовых инфузиях устанавливается периферический венозный катетер. Срок использования такого устройства не превышает нескольких дней.
При тонкости вен или их хрупкости, a также при планируемом длительном лечении, предполагающем использование препаратов с многочасовым или многосуточным введением, стоит посоветоваться с вашим врачом об установке подключичной порт-системы.
Данное устройство полностью имплантируется под кожу передней грудной стенки на длительное время, вплоть до многих лет, и обеспечивает постоянный доступ к необходимому сосуду. Противопоказаниями для имплантации порт-систем являются: неконтролируемые нарушения свертывающей системы крови; воспалительные процессы в зоне предполагаемой имплантации; наличие лихорадки неясного генеза; абсолютная нейтропения (отсутствие нейтрофилов в клиническом анализе крови) на фоне ХТ. Порт необходимо промывать 10-20 мл физ. раствора: до и после каждого использования; после введения каждого нового препарата; каждые 4-6 недель (если порт не используется). При этом в период использования порт-системы само устройство практически не ощущается, что позволяет вести привычный образ жизни, не отказывая себе, в том числе и в занятиях спортом.
Болезненно ли проведение химиотерапии?
Наверняка в течение жизни вам вводились лекарственные препараты внутривенно. При данной манипуляции небольшое чувство дискомфорта всегда присутствует. Тем не менее при возникновении каких-либо необычных ощущений во время введения препарата, необходимо немедленно сообщить об этом медицинской сестре или врачу. Прием таблетированных цитостатических препаратов по ощущениям ничем не отличается от приема любых других таблетированных средств.
Можно ли принимать другие лекарства по поводу сопутствующих заболеваний во время проведения химиотерапии?
Да, другие лекарства для лечения сопутствующих заболеваний принимать можно, и в корректировке их приема чаще всего нет необходимости. Однако перед проведением химиотерапии обязательно сообщите лечащему врачу, какое дополнительное лечение вы получаете. Так противорвотные препараты (апрепитант, фосапрепитант), цитостатики (доксорубицин, винкристин, циклофосфамид, винбластин, ифосфамид и т.д.), таргетные препараты (афатиниб, дабрафениб, сунитиниб, кризотиниб, лапатиниб, пазопамид, регорафениб, палбоциклиб, рибоциклиб, иксабепилон, олапариб), гормонотерапия (тамоксифен, торемифен) влияют на фермент CYP, посредством которого метаболизируются антиаритмические препараты (амиодарон, квинидин), антикоагулянты (варфарин), опиоидные анальгетики (альфентанил, фентанил, суфентанил); блокаторы кальциевых каналов: дилтиазем, фелодипин, никардипин, нифедипин, нимодипин, нисолдипин, верапамил и т.д. Лучше всего составить список препаратов, их дозы и частоту приема, a также указать, какой врач прописал вам препараты и по какой причине.
Как будет оцениваться эффективность и безопасность лечения?
Оценка эффективности лекарственной противоопухолевой терапии зависит от цели проводимого лечения. При послеоперационной, т.е. адъювантной химиотерапии (см. вопрос «Зачем проводится химиотерапия») непосредственная оценка эффективности лечения с помощью инструментальных методов не проводится. Основная задача данного вида лечения – воздействие на возможные микроскопические скопления опухолевых клеток, которые невозможно выявить при стандартных методах обследования: ультразвуковых исследованиях (УЗИ), компьютерной томографии (KТ), магнитно-резонансной томографии (МРТ) и т.д. Применение адъювантной химиотерапии при ее назначении именно в вашей клинической ситуации является обоснованным статистически – ее эффективность изучена и подтверждена в крупных клинических исследованиях.
Для оценки эффективности неоадъювантной (предоперационной) или паллиативной лекарственной терапии вам с определенной частотой будут назначаться контрольные инструментальные или лабораторные исследования. Это могут быть анализы крови, УЗИ, эндоскопическое исследование (бронхоскопия, ФГДС, колоноскопия), KT, MPT и т.д. Частота и кратность назначения исследований зависит от клинической ситуации. Чаще всего контрольное обследование проводится перед началом лечения и после каждых 2-4 циклов химиотерапии. Важно помнить, что для оценки эффективности лечения необходимо использовать одни и те же методы обследования, предпочтительнее КТ и/или МРТ (с учетом показаний).
Определение безопасности проводимого лечения основывается на оценке жалоб пациента и его состояния, а также показателей клинического и биохимического анализов крови, которые отображают функционирование органов и систем организма.
Что мы будем делать, если проведенная лекарственная терапия окажется неэффективной?
Каждый раз после проведенного контрольного обследования врач решает вопрос о дальнейшей тактике лечения. При отсутствии данных о прогрессировании заболевания лечение продолжается по запланированной ранее схеме. Однако не всегда лекарства, которые назначены, могут контролировать заболевание. Опухолевая клетка имеет свойство «привыкать» к получаемым препаратам, a в отдельных случаях оказывается к ним и вовсе невосприимчивой. В случае прогрессирования заболевания, т.е. при увеличении имеющихся очагов болезни или появлении новых, будет сделан выбор в пользу другой схемы лечения с использованием препаратов с иным механизмом действия. При этом принимаются во внимание общее состояние пациента, распространенность заболевания, переносимость предыдущего лечения и, несомненно, научные данные об эффективности назначаемых препаратов.
Что будет, если я пропущу один или несколько приемов препарата? Что будет, если я пропущу один или несколько циклов?
Пропуск лечения нежелателен. Лекарственная противоопухолевая терапия – это цикловое лечение, и перерывы между курсами дают возможность восстановиться здоровым клеткам. Но если пропустить очередное введение препарата, могут восстановиться не только здоровые клетки, но и злокачественные. Это определяет интервал между курсами. Если пропустить несколько циклов, опухолевые клетки могут выработать устойчивость к противоопухолевым препаратам, которые вводились до этого. В некоторых случаях очередное введение препаратов может быть отложено на несколько дней. Данное решение принимается лечащим врачом, если он считает, что организм недостаточно восстановился после предыдущего курса химиотерапии и риск осложнений при продолжении лечения превышает предполагаемую пользу. Чаще данное решение основывается на результатах анализов крови (см. далее «химиотерапия и анализы крови»).
Важно помнить, что если вы пропустили утренний прием пероральных цитостатиков, то не стоит увеличивать дозу вечернего приема, и наоборот. Любые изменения в схеме лечения возможны только после согласования с лечащим врачом.
Стоит ли избегать контактов c людьми при прохождении лечения? Заразен ли я?
Нет, вы не заразны. Вы не должны избегать контактов с окружающими вас людьми. Но нужно помнить, что большинство химиопрепаратов ослабляют действие иммунной системы, поэтому стоит избегать контактов с людьми, больными инфекционными заболеваниями, так как риск заразиться повышен. Чаще мойте руки, особенно при посещении общественных мест, перед приготовлением пищи и перед прикосновением к лицу, носу, рту и глазам.
Могу ли я работать во время лечения?
В зависимости от общего состояния вы можете продолжать работать. Многие пациенты продолжают работать, если чувствуют себя во время лечения удовлетворительно. Более того, выход на работу позволяет отвлечься от проводимой терапии, помогает вернуться к привычному образу жизни, почувствовать себя нужным.
Как правильно питаться во время прохождения химиотерапии?
Одним из главных условий для назначения и проведения лекарственной противоопухолевой терапии является хорошее общее состояние пациента, которое, несомненно, зависит от правильного питания. Конечно, в силу перегруженности информацией после посещения онколога, не все пациенты готовы обращать внимание на диетическое питание и изменение образа жизни во время лечения. Однако необходимо понимать, что соблюдение сбалансированной, рациональной диеты помогает легче противостоять побочным явлениям от проводимого лечения.
При отсутствии заболеваний желудочно-кишечного тракта (в том числе диареи или запоров, обусловленных противоопухолевой терапией) рекомендуется придерживаться средиземноморской диеты, которая, как показывают данные крупных эпидемиологических исследований, положительно влияет на риск развития и течение онкологических заболеваний. В рамках данной диеты следует употреблять продукты с низким содержанием жиров животного происхождения, продукты с высоким содержанием клетчатки, фрукты, овощи, оливковое масло, рыбу, нежирное мясо, мясо птиц, цельные зерна, бобы и чечевицу.
Дополнительная питательная поддержка (нутритивная поддержка) необходима не только для поддержания метаболических резервов организма, но и для повышения его устойчивости к лечению (лекарственному, хирургическому, лучевой терапии). В настоящее время нет доказательств стимулирующего действия длительного искусственного питания на опухолевый рост. Питательная поддержка должна начинаться одновременно с началом противоопухолевого лечения и соответствовать состоянию пациента на каждом из этапов лечения и реабилитации.
Возможно ли применение биологически активных добавок для усиления противоопухолевого эффекта или коррекции осложнений?
Практически в любом нетрадиционном лекарственном препарате, если его применение не связано с «лечением» пустышками, присутствуют биологически активные вещества. B современной традиционной медицине, основанной на принципе доказательности, любой лекарственный препарат в ходе исследования подлежит тщательной проверке на предмет эффективности и безопасности, в том числе на предмет взаимодействия с другими лекарственными препаратами. Нетрадиционные лекарственные препараты такую проверку не проходят, поэтому однозначно сказать о безопасности их применения, a также о взаимодействии с используемыми в лечении онкологических заболеваний противоопухолевыми лекарствами не представляется возможным. Поэтому в ходе прохождения химиотерапии самостоятельно использовать дополнительные препараты, обладающие возможным противоопухолевым или защитным действием, не рекомендуется.
Мультивитаминные комплексы не относятся к биологически активным добавкам и рекомендованы к применению на регулярной основе по согласованию с лечащим врачом.
Можно ли получать фитотерапию (препараты растительного происхождения)?
Доказательств в пользу применения лекарственных трав поддерживающей терапии при лечении рака недостаточно, а некоторые растительные средства могут взаимодействовать с химиотерапевтическими препаратами, при этом вызывать повышение функциональной активности ферментов печени, снижать функцию почек, поэтому их следует избегать пациентам, получающим большинство противоопухолевых препаратов.
Пациенты с онкологическими заболеваниями часто задают вопросы своим врачам о лекарственных травах, которые традиционно используются для укрепления иммунной системы, помогают бороться с инфекцией, со слабостью или усталостью. Примером является эхинацея, астрагал и женьшень и др. Но проведенные исследования данных средств не доказали их эффективность в отношении контроля опухолевого роста или влияния на качество жизни, например, в виде уменьшения общей слабости.
Существует растущий интерес к растительным противовоспалительным средствам. Изучается возможность употребления совместно с основными продуктами питания куркумы, зеленого чая, красного винограда и черники.
Использовать малоизученные растительные препараты непосредственно во время лечения не рекомендуется, так как их многосоставность и сложность делает эти вещества трудно предсказуемыми в отношении развития побочных эффектов или нежелательного взаимодействия с традиционными препаратами. Несмотря на признанный в нетрадиционной медицине потенциал некоторых растительных препаратов именно в качестве основных лекарственных противоопухолевых средств, убедительно просим отказаться от их применения на период проведения химиотерапии и обязательно поставить в известность своего врача в случае их использования.
Следует отметить, что в арсенал онкологов входят разнообразные противоопухолевые препараты, в том числе, растительного происхождения, доказавшие свою эффективность и безопасность. Напоминаем, что вам назначено наиболее эффективное современное лечение, выбор которого основан на индивидуальных особенностях вашего организма и опухолевого процесса.
Есть ли необходимость увеличивать физическую активность или не стоит нагружать организм?
Существуют доказательства пользы от физических упражнений во время и после лечения онкологических заболеваний. Например, в отношении рака молочной железы наибольшая польза была выявлена у женщин, которые выполняли нагрузки, эквивалентные быстрой ходьбе, в среднем по 4-5 часов в неделю.
Во время лечения можно совершать упражнения на сопротивление (силовые тренажеры). Выполнение силовых тренировок два-три раза в неделю является безопасным и хорошо переносится, приводит к увеличению мышечной массы и снижению количества жировой ткани. Исследования дают положительную оценку использованию упражнений на сопротивление во время лечения рака в виде снижения побочных эффектов противоопухолевого лечения.
Можно ли вести интимную жизнь во время прохождения химиотерапии?
Когда пациенту поставили диагноз – «злокачественная опухоль» и ему предстоит пройти противоопухолевую терапию, он как никогда нуждается в близости и поддержке любимого человека. Однако лечение отнимает много сил, поэтому возможностей для интимной жизни часто не остается. На фоне химиотерапии может снижаться либидо, возникает сухость слизистых, включая слизистые влагалища. В данном случае можно обратиться к андрологам (для мужчин) либо гинекологам, занимающимся нарушениями сексуальной функции или влечения.
При этом крайне важным является осознание того, что все цитостатические противоопухолевые препараты обладают повреждающим действием на плод в первом треместре беременности. Если вы способны к деторождению, избегайте беременности или зачатия на всем протяжении цитостатической противоопухолевой терапии, используйте контрацептивные средства. В качестве приемлемых методов контрацепции рассматриваются негормональная внутриматочная спираль, презерватив с антивагинальным спермицидом, шеечные колпачки со спермицидом или диафрагмы со спермицидом. Длительность контрацепции после окончания химиотерапии зависит от нескольких факторов – характера опухоли, степени ее распространения, проведенного лечения, дальнейших перспектив и т.д. и требует согласования с лечащим врачом.
Как после завершения лекарственного противоопухолевого лечения может измениться способность иметь детей (фертильность)?
Фертильность – это способность мужчины или женщины воспроизводить потомство. Многие виды противоопухолевого лечения могут нарушать будущую фертильность. У большинства мужчин, излеченных от опухолей, наблюдаются нарушения репродуктивной функции, снижение или исчезновение активности и жизнеспособности сперматозоидов, часто ведущие к бесплодию. У женщин лекарственная противоопухолевая терапия нарушает функцию яичников, в результате y 30-70% женщин репродуктивного возраста наступает бесплодие. Выраженность и длительность нарушения функции зависит от вида и дозы используемых противоопухолевых лекарств. Если вы находитесь в возрасте, предполагающем возможность иметь детей, обязательно уточните y своего врача о возможном влиянии лечения на фертильность до его начала на этапе планирования противоопухолевой терапии. В настоящее время существуют методики с высокой вероятностью сохранения фертильности даже y пациентов, прошедших интенсивную противоопухолевую терапию. У мужчин используется метод криоконсервации (замораживания) спермы. Длительное хранение замороженной спермы не влияет на оплодотворяющую способность сперматозоидов, поэтому криоконсервация спермы позволяет мужчине после лечения иметь своего ребенка. У женщин применяется криоконсервации ткани яичника, яйцеклетки или эмбриона. Подробную информацию можно также получить у врача-репродуктолога, специализирующегося на сохранении фертильности y онкологических пациентов.
Какова роль психологической помощи и есть ли у меня возможность ее получения?
Психологический компонент является важной частью процесса лечения. Основные цели психологической коррекции – это не только улучшение эмоционального фона, уменьшение уровня стресса, психологическая подготовка к предстоящему процессу лечения, но и обучение навыкам самостоятельной регуляции. Чтобы получить консультацию психолога, обратитесь к лечащему врачу.
Каковы побочные явления и что делать, если они возникли?
При применении любого лекарственного препарата (например, парацетамол, но-шпа и т.п.) существует вероятность развития побочных эффектов, причем, в инструкциях к данным лекарствам список побочных эффектов достаточно длинен. Тем не менее в течение жизни мы зачастую с легкостью принимаем решения о приеме данных препаратов и чаще всего избегаем развития осложнений, получая необходимый терапевтический эффект. Тот же принцип действует в отношении противоопухолевых препаратов. У каждого из них существует длинный теоретический список осложнений и реакций, которые могут произойти. Такие списки формируются в ходе клинических исследований данных препаратов на сотнях и тысячах пациентов. Но это совершенно не означает, что перечисленные побочные эффекты обязательно возникнут. Тем не менее частота возникновения побочных эффектов при цитостатической химиотерапии выше, чем при приеме, например, парацетамола. Интенсивность и выраженность побочных эффектов зависит от получаемого цитостатического препарата, индивидуальной реакции организма, психоэмоционального статуса и других факторов. Перечисленные ниже побочные эффекты являются наиболее распространенными при проведении химиотерапии, но это совершенно не означает, что они обязательно возникнут y вас.
Слабость
Слабость является одним из самых распространенных побочных эффектов противоопухолевой лекарственной терапии. Слабость иногда путают с усталостью. Усталость обычно возникает после определенных видов деятельности к концу дня, а хороший сон помогает решить эту проблему. Слабость, обусловленную общей интоксикацией организма при лекарственной противоопухолевой терапии, сон скорректировать не может. Она может длиться недолго, но может занимать и несколько дней или недель.
В борьбе со слабостью могут помочь следующие меры:
Тошнота, рвота
Наряду со слабостью, тошнота и рвота также являются одними из самых распространенных побочных эффектов химиотерапии.
При возникновении данного побочного эффекта улучшение самочувствия обычно наступает в течение 1-2 дней. В некоторых случаях тошнота может сохраняться в течение 3-4 дней после проведенного лечения. Для того чтобы снизить риск возникновения тошноты, врач обязательно по умолчанию назначает противорвотную терапию до введения противоопухолевых препаратов. Вам будет назначен один или несколько препаратов, обладающих противорвотным эффектом в зависимости от типа проводимой терапии и переносимости ранее проведенного лечения. При возникновении тошноты или рвоты в домашних условиях обязательно сообщите об этом своему лечащему врачу. С современными возможностями сопроводительной терапии чаще удается скорректировать или предупредить тошноту и рвоту – современный пациент не должен испытывать данный побочный эффект. В последние годы выпущены крайне эффективные противорвотные препараты, и в лекарственном арсенале нашего центра они имеются.
Для борьбы с тошнотой рекомендуется:
Обязательно свяжитесь с врачом, если ваш организм перестал воспринимать твердую пищу или жидкости, a так же если вас вырвало назначенным противорвотным препаратом.
Выпадение волос
Потеря волос (алопеция) не представляет собой угрозу для организма и приводит больше к психологической травме у женщин, которые, в отличие от мужчин, более восприимчивы к существенным изменениям внешности. Интенсивность выпадения волос непосредственно связана с тем, какие именно противоопухолевые препараты применяются. Практически всегда к алопеции приводит использование доксорубицина, эпирубицина, этопозида, таксананов, препаратов платины. Как правило, уже через 2-3 недели после начала лечения возникает некоторый дискомфорт в области кожи головы, после чего начинают выпадать волосы, равномерно или сразу целыми клочьями. Иногда полная потеря волос может произойти в течение недели. Выпадение волос происходит на всех участках тела, но они вновь вырастают после окончания курса химиотерапии. Полное восстановление волос происходит через 2-4 месяца после окончания лечения. B некоторых случаях они могут стать волнистыми и даже изменить цвет.
Мы рекомендуем короткую стрижку или бритье до того, как на голове будет потеряна значимая часть волос. Заранее обратитесь в специализированные магазины для подбора парика под цвет и длину имеющихся волос или изготовьте парик из собственных волос.
Для того чтобы уменьшить выпадение волос, лучше всего пользоваться мягкими шампунями на основе растительного сырья с нормальным показателем рН. Используйте атласные наволочки для обеспечения максимального комфорта во время сна и снижения трения волос о ткань. Вместо расчески лучше пользоваться щеткой с мягким ворсом. Не рекомендуется пользоваться феном, красить волосы, делать завивку, а также использовать лак и иные химические реагенты.
Повреждение кожного и слизистого покровов
Во время проведения лекарственной терапии могут возникнуть проблемы с кожей, например, сыпь, зуд, шелушение, покраснение. Поддержание чистоты и уход за кожным покровом обязательны. Не стоит принимать ванну, лучше пользоваться душем. Рекомендуется принимать душ ежедневно. Не стоит пользоваться спиртовыми лосьонами, больше подойдут кремы и лосьоны для сухой кожи.
Солнечные лучи усиливают токсическое действие некоторых лекарственных препаратов на кожный покров, поэтому не рекомендуется загорать. При нахождении на солнце используйте солнцезащитные кремы. Носите одежду с длинными рукавами, лучше из хлопковой ткани. При работе по дому или в саду используйте перчатки для защиты ногтей и кожи рук.
Для профилактики повреждения слизистой после каждого приема пищи рекомендовано полоскать рот водой или отваром ромашки.
Обязательной является процедура чистки зубов, для чего рекомендуется использовать зубные щетки с мягкой щетиной. При возникновении стоматита или снижении уровня тромбоцитов менее 20 тысяч клеток (по данным клинического анализа крови) используются специальные поролоновые щетки или частые полоскания. При снижении количества лейкоцитов менее 1,5 тысяч клеток рекомендовано полоскать полость рта раствором фурацилина в дневное время каждые 2 часа, a также дважды в день обрабатывать слизистую полости рта мирамистином или гексоралом.
Диарея (понос)
Диарея может стать грозным осложнением химиотерапии, в тяжелых случаях быть причиной обезвоживания и электролитных нарушений, поэтому при первых признаках следует связаться с лечащим врачом.
Если диарея возникла на фоне проведения химиотерапии, введение цитостатиков следует прекратить. Для купирования приступов диареи рекомендовано принимать капсулы препарата лоперамид в дозировке первоначально 2 капсулы (4 мг), затем – по 1 капсуле (2 мг) после каждого акта дефекации в случае жидкого стула. Максимальная суточная доза 16 мг (2 капсулы). Если диарея не купируется лоперамидом, поставьте в известность лечащего врача.
Помимо приема антидиарейных лекарственных средств рекомендуется:
Возобновление химиотерапии после окончания диареи возможно только по назначению лечащего врача.
Запор
Оформленный стул должен быть ежедневно. При отсутствии стула более трех дней на фоне применения слабительных препаратов следует сделать клизму.
Для того чтобы нормализовать стул, помимо приема слабительных средств, рекомендуется:
Зачем мне рекомендуют так часто сдавать кровь? Что такое гематологическая токсичность?
Перед тем, как провести очередной цикл ХТ, необходимо сдать кровь для проведения клинического и биохимического анализов, что поможет врачу понять работоспособность костного мозга и основных систем организма. B большинстве случаев химиотерапевтические препараты снижают активность костного мозга, нарушая способность вырабатывать форменные элементы крови: эритроциты, лейкоциты, тромбоциты, это гематологическая токсичность.
Эритроциты – это красные кровяные тельца, в которых содержится гемоглобин, выполняющий функцию переноса кислорода. При низком содержании гемоглобина вы можете ощущать слабость и головокружение. Отмечается бледность кожного покрова. Больше отдыхайте, избегайте тяжелых физических нагрузок. Также поможет и пребывание на свежем воздухе: прогулки, сон при открытых окнах.
Лейкоциты – это белые кровяные тельца – «охранники», стоящие на страже нашего организма и выполняющие защитную функцию. При низком содержании лейкоцитов увеличивается вероятность развития инфекции. Источником инфекционных заболеваний могут быть бактерии и вирусы, которые находятся как внутри организма, так и в окружающей среде.
Тромбоциты – играют важную роль в остановке кровотечения. При повреждении сосудов они скапливаются в месте травмы, образуя сгусток крови, который препятствует кровотечению. Главная опасность, которая может возникнуть при снижении тромбоцитов – это кровотечение. Следует обращать внимание на появление неожиданных синяков, кровотечение из носа или десен. При появлении черного стула, a так же спонтанно возникших синяков и кровотечений срочно обращайтесь к врачу.
Для предупреждения возникновения кровотечений при сниженном уровне тромбоцитов:
Для раннего выявления гематологических осложнений и своевременной помощи всем пациентам, получающим химиотерапию, еженедельно следует сдавать клинический анализ крови и при отклонениях сообщать лечащему врачу.
При повышении температуры выше 37,6 С и изменениях показателей клинического анализа крови (нейтропения) только после консультации с лечащим врачом назначается эмпирическая антибактериальная терапия – Ципрофлоксацин 500 мг 2 раза в день (или его аналоги) и Амоксиклав 1000 мг 2 раза в день 5-7 дней.
В случаях высокой степени токсичности и присоединении других нежелательных явлений требуется проведение интенсивной терапии, наблюдение за пациентом в условиях госпитализации. Начало очередного цикла химиотерапии возможно только после нормализации показателей крови при удовлетворительном состоянии пациента.
При каких побочных явлениях я должен немедленно обратиться к врачу?
Некоторые побочные эффекты могут быть незначительными, a другие оказаться достаточно серьезными, поэтому срочно обратитесь к врачу, если у вас:
Список литературы: