Флемоксин Солютаб, 20 шт., 500 мг, таблетки диспергируемые
Сдайте клинический анализ крови с лейкоцитарной формулой и анализ на С-реактивный белок
Вам также могут быть
 Скидки и бонусы по программе «Моё Здоровье»
Скидки и бонусы по программе «Моё Здоровье»
Флемоксин Солютаб: инструкция по применению
Состав
| Таблетки растворимые | 1 табл. |
| амоксициллин (в виде амоксициллина тригидрата) | 125 мг |
| 250 мг | |
| 500 мг | |
| 1000 мг | |
| вспомогательные вещества: диспергируемая целлюлоза; МКЦ; кросповидон; ванилин; ароматизатор мандариновый; ароматизатор лимонный; сахарин; магния стеарат |
в блистере 5 шт.; в коробке 4 блистера (125, 250, 500, 1000 мг) или в блистере 7 шт.; в коробке 2 блистера (125 мг).
Описание лекарственной формы
Таблетки диспергируемые от белого до светло-желтого цвета, овальной формы с логотипом фирмы и цифровым обозначением на одной стороне и риской, разделяющей таблетку пополам, на другой стороне. Цифровое обозначение: Флемоксин Солютаб ® (125 мг) — «231»; Флемоксин Солютаб ® (250 мг) — «232»; Флемоксин Солютаб ® (500 мг) — «234»; Флемоксин Солютаб ® (1000 мг) — «236».
Фармакодинамика
Активен в отношении таких грамположительных и грамотрицательных микроорганизмов, как Streptococcus pyogenes, Streptococcus pneumonia, Clostridium tetani, C.welchii, Neisseria gonorrhoeae, Neisseria meningitidis, Staphylococcus aureus (не вырабатывающих бета-лактамазы), Bacillus anthracis, Listeria monocytogenes, Helicobacter pylori. Менее активен в отношении Enterococcus faecalis, Escherichia coli, Proteus mirabilis, Salmonella typhi, Shigella sonnei, Vibrio cholerae. Не активен в отношении микроорганизмов, продуцирующих бета-лактамазы, Pseudomonas spp., индолположительных Proteus spp., Serratia spp., Enterobacter spp.
Фармакокинетика
После приема внутрь всасывается быстро и практически полностью (около 93%), кислотоустойчив. После приема внутрь в дозе 500 мг Cmax активного вещества в плазме составляет 5 мкг/мл и отмечается в плазме крови через 2 ч. При увеличении или уменьшении дозы препарата в 2 раза Cmax в плазме крови также изменяется в 2 раза. Прием пищи практически не влияет на абсорбцию препарата.
Связывание с белками плазмы около 20%. Амоксициллин хорошо проникает в слизистые оболочки, костную ткань, внутриглазную жидкость и мокроту в терапевтически эффективных концентрациях. Концентрация амоксициллина в желчи превышает его концентрацию в плазме крови в 2–4 раза. В амниотической жидкости и пуповинных сосудах концентрация амоксициллина составляет 25–30% от его уровня в плазме крови беременной женщины.
Плохо проникает через ГЭБ, но при воспалении мозговых оболочек концентрация в спинно-мозговой жидкости составляет около 20% от концентрации в плазме крови.
Частично метаболизируется, большинство его метаболитов неактивны в отношении микроорганизмов.
Элиминируется преимущественно почками, около 80% путем канальцевой экскреции, 20% — посредством клубочковой фильтрации. При отсутствии нарушения функции почек T1/2 составляет 1–1,5 ч. У недоношенных, новорожденных и детей младше 6 мес — 3–4 ч.
Фармакокинетика в особых клинических случаях.
T1/2 амоксициллина не изменяется при нарушении функции печени.
При нарушении функции почек (Cl креатинина ≤15 мл/мин), T1/2 амоксициллина может увеличиваться и достигает при анурии 8,5 ч.
Показания
Инфекционно-воспалительные заболевания, вызванные чувствительными к препарату микроорганизмами:
инфекции органов дыхания;
органов мочеполовой системы;
кожи и мягких тканей.
Противопоказания
Повышенная чувствительность к препарату и другим бета-лактамным антибиотикам.
поливалентная гиперчувствительность к ксенобиотикам;
заболевания ЖКТ в анамнезе (особенно колит, связанный с применением антибиотиков);
Применение при беременности и кормлении грудью
Возможно назначение препарата в период беременности и лактации в том случае, если ожидаемый положительный результат от применения препарата превышает риск развития побочных эффектов. В небольших количествах амоксициллин выделяется с грудным молоком, что может привести к развитию явлений сенсибилизации у ребенка.
Способ применения и дозы
Внутрь, до, во время или после приема пищи. Таблетку можно проглотить целиком, разделить на части или разжевать, запив стаканом воды или развести в воде с образованием сиропа (в 20 мл) или суспензии (в 100 мл).
Взрослым и детям старше 10 лет (при инфекциях легкой и средней тяжести) — по 500–750 мг 2 раза в сутки или по 375–500 мг 3 раза в сутки.
Детям от 3 до 10 лет — по 375 мг 2 раза в сутки или по 250 мг 3 раза в сутки; от 1 года до 3 лет — по 250 мг 2 раза в сутки или по 125 мг 3 раза в сутки. Суточная доза для детей (включая детей до 1 года) — 30–60 мг/кг/сут, разделенная на 2–3 приема.
При лечении тяжелых инфекций, а также при инфекциях с труднодоступными очагами (например острый средний отит) предпочтителен трехкратный прием препарата.
При хронических заболеваниях, рецидивах, тяжелых инфекциях: взрослым — по 0,75–1 г 3 раза в сутки, детям — до 60 мг/кг/сут в 3 приема.
При острой неосложненной гонорее — 3 г, однократно, в сочетании с 1 г пробенецида.
При инфекциях легкой и средней тяжести течения лечение проводят в течение 5–7 дней, при инфекциях, вызванных Streptococcus pyogenes, — не менее 10 дней.
При лечении хронических заболеваний, инфекций тяжелого течения дозы препарата должны определяться клинической картиной заболевания. Прием препарата продолжают в течение 48 ч после исчезновения симптомов заболевания.
Пациентам с Cl креатинина ниже 10 мл/мин дозу уменьшают на 15–50%.
Побочные действия
Со стороны органов ЖКТ: редко — изменение вкуса, тошнота, рвота, диарея; в отдельных случаях — умеренное повышение активности печеночных трансаминаз; крайне редко — псевдомембранозный и геморрагический колиты.
Со стороны мочевыводящей системы: крайне редко — развитие интерстициального нефрита.
Со стороны системы кроветворения: возможны агранулоцитоз, нейтропения, тромбоцитопения, гемолитическая анемия, но наблюдаются они также крайне редко.
Побочные действия со стороны нервной системы при использовании амоксициллина в лекарственной форме таблетки диспергируемые не зарегистрированы.
Аллергические реакции: кожные реакции, главным образом в виде специфической макулопапулезной сыпи; редко — мультиформная экссудативная эритема (синдром Стивенса-Джонсона); в отдельных случаях — анафилактический шок, ангионевротический отек.
Передозировка
Симптомы: тошнота, рвота, диарея, нарушение водно-электролитного баланса.
Лечение: промывание желудка, назначение активированного угля, солевых слабительных, проведение коррекции водно-электролитного баланса.
Взаимодействие
Пробенецид, фенилбутазон, оксифенбутазон, в меньшей степени ацетилсалициловая кислота и сульфинпиразон, тормозят канальцевую секрецию пенициллинов, что приводит к увеличению периода полувыведения и повышению концентрации амоксициллина в плазме крови. Бактерицидные антибиотики (в т.ч. аминогликозиды, цефалоспорины, ванкомицин, рифампицин) при одновременном приеме оказывают синергидное действие; возможен антагонизм при приеме с некоторыми бактериостатическими препаратами (например хлорамфеникол, сульфаниламиды). Одновременный прием с эстрогенсодержащими оральными контрацептивами может приводить к снижению их эффективности и повышению риска развития прорывных кровотечений). Одновременное назначение с аллопуринолом не увеличивает частоту кожных реакций в отличие от сочетания аллопуринола с ампициллином.
Особые указания
Возможна перекрестная устойчивость с препаратами пенициллинового ряда и цефалоспоринами.
Как и при применении других препаратов пенициллинового ряда, возможно развитие суперинфекции.
Появление тяжелой диареи, характерной для псевдомембранозного колита, является показанием для отмены препарата.
Назначать препарат больным с инфекционным мононуклеозом и лимфолейкозом нужно с осторожностью, т.к. высока вероятность появления экзантемы неаллергического генеза.
Характеристика
Бактерицидный кислотоустойчивый антибиотик широкого спектра действия из группы полусинтетических пенициллинов.
Гайморит: симптомы, особенности лечения и правила профилактики
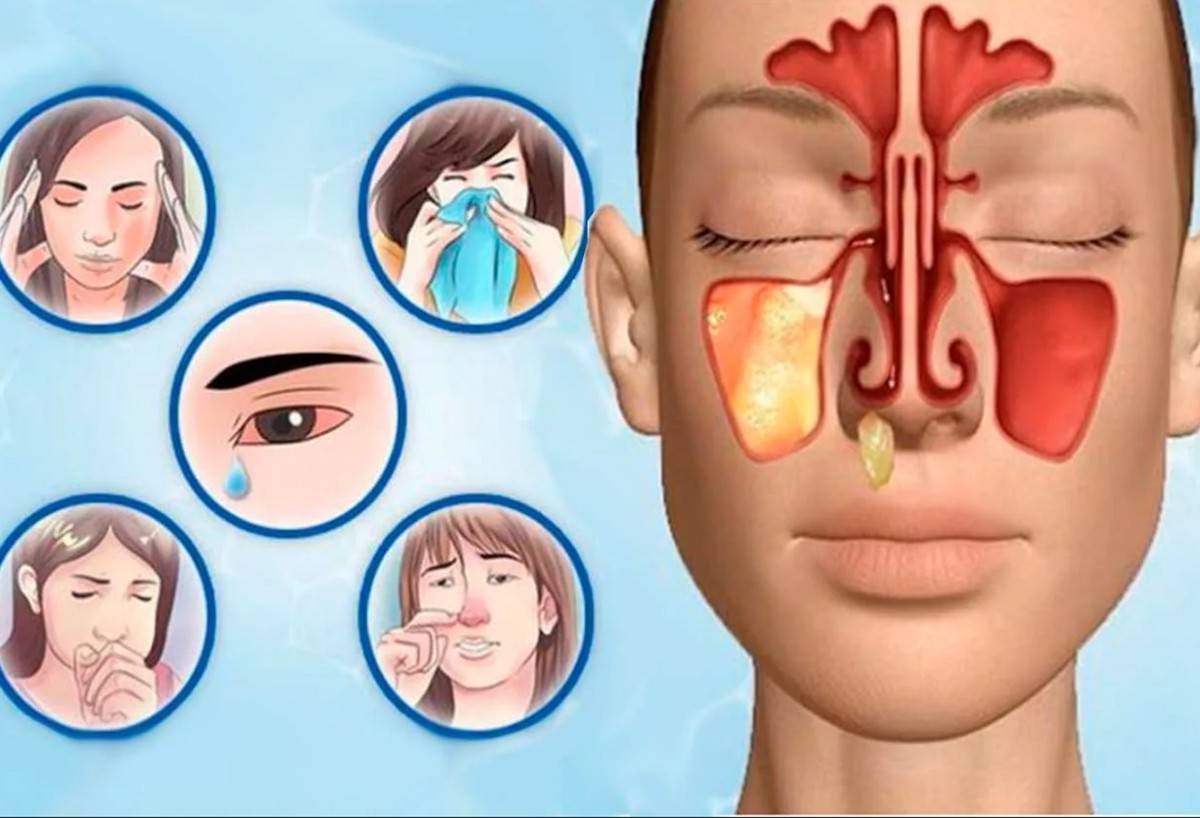
Гайморит – это воспалительный процесс в области гайморовой пазухи, расположенной в толще черепной кости над верхней челюстью, слева и справа. Этот процесс является одной из разновидностей синуситов (это общее название для воспалительных процессов в области придаточных пазух – лобной, гайморовой, решетчатой или клиновидной). Обычно воспалительный процесс затрагивает слизистые оболочки, выстилающие пазухи изнутри, реже затрагиваются более глубокие слои тканей, вплоть до костных структур. Обычно процесс возникает как осложнение вирусных или бактериальных инфекций в области носоглотки и верхних дыхательных путей.
Исходя из причины развития, механизмов формирования и симптомов, гайморит бывает нескольких типов. Выделение каждого из них важно для определения тактики лечения, прогноза и разработки мер профилактики.
Острый – развивается быстро, как осложнение ОРВИ, насморков, простудных заболеваний, воспаления в области корней зубов на верхней челюсти. Возбудители проникают через каналы, соединяющие пазухи с полостью носа с гайморовыми пазухами, размножаются в полости. Тело начинает активно вырабатывать иммунные клетки и слизь, чтобы обезвредить патогенные организмы. Если слизь закупорит проток пазухи, возникает давление на стенки, усиление воспалительного процесса. По мере очищения пазухи от содержимого воспалительный процесс постепенно затухает.
Хронический – воспалительный процесс, который длится более 4 недель, имеет вялое или волнообразное течение, с периодами обострений. Обычно возникает из-за не долеченной острой формы, наличия аденоидов, тонзиллитов, отитов.
Гнойный – обычно становится осложнением острой формы либо обострения хронического процесса, если процесс не лечится, предпринимаются попытки самолечения или пациент переносит инфекцию на ногах. Патогенные бактерии накапливаются в пазухах, в смеси с лейкоцитами образуют гнойное содержимое. Самое опасное осложнение при этой форме – прорыв гноя в полость черепа, поражение костных тканей, мозга.
Двусторонний – одна из тяжелых форм, поражение локализовано сразу в обеих пазухах – левой и правой. Нередко возникает как осложнение инфекций в полости рта и носоглотки, обычно грибковой или бактериальной. Обычно имеет острое течение, редко переходит в хроническую форму.
Аллергическое поражение возникает у пациентов, страдающих от чрезмерно активной реакции иммунной системы на различные вещества. Особенно часто эта форма синусита бывает при поллинозе, круглогодичном рините, реакции на плесень, пылевых клещей.
Катаральный – преимущественно бывает у детей. Он развивается при проникновении в полость пазух патогенных организмов, что формирует отек и раздражение слизистых. Считается самой легкой формой болезни, проходящей при активном лечении без осложнений и последствий.
Полипозная форма формируется при образовании полипозных разрастаний слизистых из-за чрезмерно быстрого деления клеток. Рост полипов могут провоцировать инфекции, травмы, велика роль наследственности.
Одонтогенный – формируется как результат серьезных проблем зубов, особенно 4-6 зуба на верхней челюсти, корни которых расположены в непосредственной близости от пазухи. Если возникают проблемы в области корней этих зубов, воспаление и нагноение может переходить на пазуху, она заполняется секретом и воспаляется.
Причины
Придаточные пазухи, включая гайморовы, созданы как естественный барьер на пути инфекций, фильтр для различных опасных веществ в воздухе. Они помогают согревать воздух, увлажнять его и очищать от примесей перед попаданием в гортань, и ниже по респираторному тракту. Основная причина воспаления и появления признаков гайморита – это проникновение бактерий, грибков или вирусов, аллергенов. Реже инфекция попадает с током крови из других, отдаленных очагов.
Нарушать работу пазух могут патологии иммунной системы, частые ОРВИ, респираторная форма аллергии, носительство патогенных бактерий в носоглотке (стафило-, стрепто- или менингококк).
Среди ключевых причин, которые могут привести к развитию гайморита, можно выделить:
Осложнения
Не все люди знают, как начинается гайморит, поэтому многие принимают симптомы за тяжелую простуду и лечатся самостоятельно. Это может привести к определенным осложнениям, отдаленным последствиям. Среди ключевых осложнений можно выделить поражения бронхов и распространение инфекции на легкие, развитие отитов (поражение среднего уха), переход болезни в хроническую форму.
Тяжелый и запущенный, своевременно не вылеченный гайморит может привести к воспалению внутренних органов – сердца, глаз, почек, поражению суставов и мозга, его оболочек. Если образуются гнойные полости в гайморовых пазухах, возможен прорыв гноя в кровь (возникает сепсис), проникновение его в соседние пазухи с развитием пансинусита, воспаление мозговых оболочек с явлениями менингита. Всех этих осложнений можно избежать при полноценном лечении гайморита под руководством лор-врача.
Симптомы и диагностика
Конечно, при развитии гайморита нужно немедленно обращаться к врачу, но как понять, что гайморит начался? Начальные признаки неспецифичные – это повышение температуры от незначительной до высокой, сильная слабость, заложенность носа или обильные густые выделения, болезненность в проекции пазух или в области лица.
Боль при гайморите может быть различной – от тупой, давящей до сильной, мучительной. Она локализуется в подглазничной области, может отдавать в область переносицы, лобную зону или верхние зубы. При надавливании на область пазух или наклонах головы вперед она усиливается, распространяясь по подглазничной области. Могут краснеть и отекать веки.
Врачи отмечают некоторые особенности того, как проявляется болезнь в определенных возрастных группах. Так, у взрослых самым ключевым признаком могут быть болевые ощущения, головная боль, нарушение восприятия запахов. Может меняться голос, он становится гнусавым, нос сильно заложен, выделяется полупрозрачная или желто-зеленая слизь. Высокая лихорадка типична для острой формы, при хроническом или аллергическом гайморите болезнь может протекать без температуры.
На фоне поражения пазух возможно слезотечение, неприятный привкус во рту, слабость, постоянное утомление, нарушения аппетита, расстройства сна, ознобы и приступы кашля.
Заразен ли гайморит? Само по себе воспаление – это результат влияния патогенных факторов, и это не заразно. Бактерии или вирусы, которые спровоцировали заболевание, могут передаваться от человека к человеку, но не обязательно вызовут поражение пазух.
Диагноз гайморита ставит лор-врач после проведения ряда тестов и осмотра пациента. Важно подробно рассказать, как началось заболевание, какие жалобы были ранее и имеются в данный момент. Врач осмотрит полость носа и глотку, прощупает проекцию пазух, определяя болезненность.
Дополнительно могут понадобиться КТ или МРТ придаточных пазух, рентгенограмма, УЗИ исследование, эндоскопия носоглотки, при необходимости – биопсия полипозных образований. Назначаются анализы крови, посевы отделяемой из носа слизи для определения флоры, чтобы подобрать необходимые препараты.
Как лечить у взрослого
Терапия болезни должна быть комплексной. Она направлена на борьбу с инфекцией, устранение воспаления, налаживание оттока слизи из пазух и улучшение носового дыхания. В неосложненных случаях возможно лечение гайморита дома под постоянным контролем оториноларинголога. В тяжелых случаях и при необходимости хирургического лечения пациент госпитализируется в стационар.
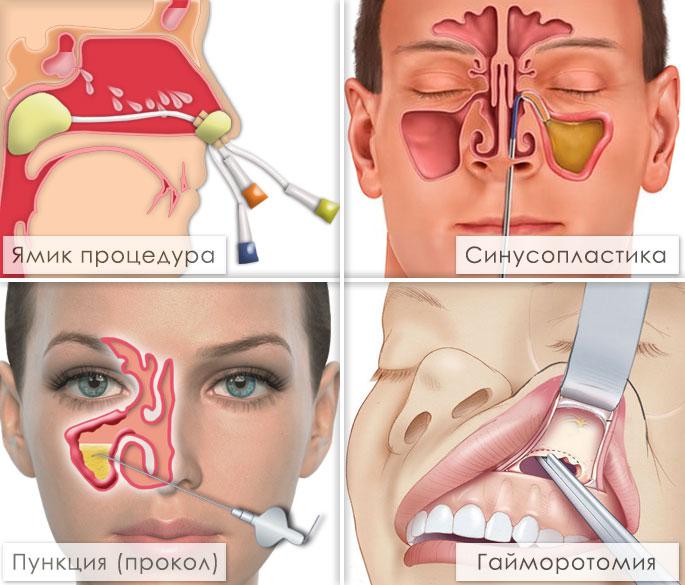
Возможно консервативное лечение с назначением антибактериальных препаратов, противовоспалительных средств, антигистаминных препаратов и различных капель, спреев для носа. Также применяют пункционное лечение или хирургические вмешательства. Выбор зависит от возраста пациента, вида патологии, тяжести состояния и возможных осложнений.
Многим пациентам назначают пункции (с местным обезболиванием) – они помогают удалить гнойное содержимое, помочь в оценке характера воспаления, плюс приносят существенное облегчение. После удаления содержимого пазухи промывают физраствором или фурациллином, вводят растворы антибиотиков и противовоспалительные препараты. Минус подобной тактики – не всегда достаточно одного прокола, поэтому требуется курс процедур в течение нескольких недель. Метод достаточно неприятный, имеет ряд противопоказаний и осложнений, процедура болезненна как во время прокола, так и после него.
Новое в рекомендациях по лечению хламидийной инфекции во время беременности
Хламидийная инфекция может существенно осложнить беременность. С ней может быть связан риск таких неблагоприятных исходов беременности, как послеродовой эндометрит, преждевременные роды, рождение детей с низкой массой тела (W. A. Andrews et al., 2000).
Хламидийная инфекция может существенно осложнить беременность. С ней может быть связан риск таких неблагоприятных исходов беременности, как послеродовой эндометрит, преждевременные роды, рождение детей с низкой массой тела (W. A. Andrews et al., 2000).
По данным Центра по контролю заболеваемости США (U.S. Centers for Disease Control and Prevention, CDC), распространенность хламидийной инфекции у беременных женщин составляет от 2 до 24%. У 25–50% детей, рожденных инфицированными женщинами, развивается хламидийная инфекция глаз, у 10–20% — хламидийная пневмония (J. Schachter, 1995). Риск передачи инфекции новорожденному составляет около 70%.
Необходимость терапии урогенитального хламидиоза у беременных, если ее по разным причинам не удалось провести до беременности, не вызывает сомнений у специалистов. Единственное условие, которое следует неукоснительно соблюдать при выборе адекватной терапии беременных, это четкое следование признанным, т. е. соответствующим принципам доказательной медицины, рекомендациям. На самом деле любые назначения в современной практике должны соответствовать таким принципам, но когда речь идет о лечении беременных, эти требования должны соблюдаться неукоснительно — во избежание тяжелых последствий.
При освещении вопросов терапии хламидийной инфекции у беременных мы ориентировались на современные подходы к решению этой проблемы, изложенные в последних редакциях трех руководств — российском («Рациональная фармакотерапия заболеваний кожи и инфекций, передаваемых половым путем», под редакцией А. А. Кубановой, 2005 г.), европейском («Европейское руководство по ИППП», 2001 г.) и американском («Руководство по лечению ИППП» CDC, 2006 г.).
Хорошо известно, что основными антибиотиками, рекомендованными всеми мировыми руководствами для лечения хламидийной инфекции, являются тетрациклины и макролиды. Из фторхинолонов — только офлоксацин. Также известно, что препараты тетрациклинового ряда и фторхинолоны противопоказаны при беременности из-за патологического влияния на формирование зубов и костной ткани у плода. Таким образом, из рекомендованных для лечения беременных антибиотиков, обладающих противохламидийной активностью, остаются только макролиды.
Первым из макролидов появился эритромицин. Огромное число наблюдений, накопившееся почти за 60 лет существования эритромицина, показало его безопасность для плода. Этот антибиотик — один из немногих, разрешенных к применению у беременных и новорожденных. В связи с этим для лечения хламидийной инфекции у беременных женщин в качестве препарата первого выбора во всех рекомендациях долгое время фигурировал эритромицин.
При приеме любых макролидов могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха), а также аллергические реакции.
Вопрос переносимости становится одним из основных при выборе препарата для лечения хламидийной инфекции у беременных.
Побочные эффекты, в основном со стороны желудочно-кишечного тракта, при приеме эритромицина развиваются у 15–100% больных, 12–33% больных из-за этого прекращают курс терапии (J. Kacmar, 2001). У беременных побочные эффекты после приема эритромицина наблюдаются особенно часто. Это заставляет искать новые методы терапии беременных препаратами, не уступающими по безопасности эритромицину. Проблема с назначением новых, даже относительно новых антибиотиков беременным объясняется тем, что специально клинические испытания на беременных никто по этическим соображениям не проводит. Даже если в экспериментах на животных препараты не обладали тератогенным или мутагенным действием, уходят многие годы на накопление данных о безопасности применения препаратов у беременных и кормящих женщин. Прогресс в этой области идет очень медленно, что тем не менее оправдано ввиду сложности проблемы и огромной ответственности, связанной с внесением коррекций в существующие рекомендации.
В последние 15 лет наиболее активным противохламидийным препаратом и основным средством для лечения различных форм урогенитальной хламидийной инфекции признан азитромицин. Именно этот антибиотик все упомянутые руководства относят к препаратам выбора при лечении хламидиоза. Этому способствуют уникальные фармакокинетические характеристики азитромицина: продолжительный период полувыведения, высокий уровень всасывания и устойчивость в кислой среде, способность этого антибиотика транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, а также возможность проникновения внутрь клетки. Благодаря тому, что высокая терапевтическая концентрация азитромицина в тканях достигается после однократного приема стандартной дозы антибиотика и сохраняется в местах воспаления не менее 7 сут, с появлением азитромицина впервые возникла возможность эффективного лечения больных хламидийной инфекцией путем однократного приема антибиотика внутрь. Излечение хламидийной инфекции после однократного приема азитромицина подтверждается самой высокой комплаентностью в сравнении со всеми другими антибиотиками, которые следует назначать не менее чем на 7 дней. Показано, что нарушение многодневных режимов лечения отмечают до 25% больных, а при развитии побочных эффектов этот показатель значительно возрастает. Таким образом, явным преимуществом азитромицина является возможность его назначения однократно, что особенно актуально у беременных.
Оригинальным и наиболее известным из препаратов азитромицина является сумамед, который используется в Российской Федерации с начала 90-х годов прошлого века. Именно в отношении этого препарата накоплен самый большой опыт по лечению самых разнообразных форм хламидийной инфекции.
Несмотря на общие требования, касающиеся использования в публикациях только международных названий препаратов, при описании эффективности применения лекарства, его переносимости представляется важным указывать, какой именно коммерческий препарат использовался в исследовании, потому что качество одних и тех же лекарств, выпускаемых различными производителями, может быть различным. Чтобы показать эффективность и переносимость именно своего продукта, многие фармацевтические компании, выпускающие дженерики, проводят сравнительные испытания своей продукции с оригинальным препаратом, каковым, как уже было отмечено выше, и является сумамед. С использованием сумамеда проведена основная масса фармакологических и клинических исследований азитромицина во всем мире, поскольку именно из субстанции, поставлявшейся той же компанией, которая производила сумамед, распространенный в странах Восточной Европы, в течение многих лет в США производили зитромакс, поставлявшийся в страны Западной Европы, Америки и Японию.
Согласно российскому руководству при хламидийной инфекции у беременных препаратами выбора служат:
Таким образом, из относительно новых макролидов в отечественных рекомендациях среди препаратов выбора присутствует азитромицин и джозамицин. Хотя в России нет пока национальных стандартов по лечению ИППП, наша страна стала одним из первых в мире государств, где азитромицин появился в официальных рекомендациях в качестве основного препарата для лечения хламидийной инфекции во время беременности.
В европейском руководстве среди основных препаратов фигурируют:
А в качестве альтернативных приводятся следующие схемы:
По мнению европейских коллег, несмотря на эффективность и безопасность азитромицина, наблюдения относительно безопасности его применения пока недостаточно длительны, чтобы рекомендовать его рутинное применение во время беременности. Правда, следует напомнить, что речь идет о Рекомендациях 2001 г., которые с тех пор не корректировались.
До недавнего времени и в американском руководстве азитромицин отсутствовал среди основных препаратов, рекомендуемых для лечения хламидийной инфекции у беременных. Еще в 2002 г. для лечения беременных, согласно Руководству по лечению ИППП — CDC, рекомендовали применять только эритромицин или амоксициллин. Но после российских специалистов и американцы пошли на изменение своих рекомендаций: новая редакция Руководства от 2006 г. уже рекомендует однократный прием азитромицина в качестве основной схемы лечения хламидийной инфекции у беременных. Эритромицин впервые был переведен в разряд альтернативных препаратов. Амоксициллин остался как препарат выбора наряду с азитромицином.
Можно ожидать, что скоро и Европа присоединится к российским и американским коллегам.
Хотелось бы прокомментировать некоторые процитированные выше рекомендации.
Итак, почему же азитромицин выходит на первое место при терапии хламидийной инфекции у беременных?
Все рекомендации, касающиеся лечения беременных, очень консервативны и не меняются десятилетиями, пока не накапливаются данные о безопасности нового лекарственного средства. Доклинические испытания на животных не показали какого-либо тератогенного эффекта азитромицина. Только этого недостаточно для разрешения его применения у беременных. Появление азитромицина как средства лечения хламидийной инфекции у беременных в некоторых признанных рекомендациях свидетельствует о том, что к настоящему времени по всему миру уже накопилось достаточное количество сведений о результатах применения азитромицина, как в ходе запланированных исследований, так и в результате случайного приема беременными, не знавшими, что они находятся в этом состоянии. Ни одного достоверного сообщения о негативном действии на плод азитромицина пока не получено. Все эти данные накапливались постепенно в разных странах, причем самый длительный опыт у исследователей из Хорватии, где и был впервые получен азитромицин.
По данным V. Simunic и соавторов, эффективность 1 г азитромицина при лечении хламидийной инфекции у беременных составила 92,1%, а семидневного курса эритромицина — 87,5%. При этом комплаентность и переносимость терапии азитромицином были гораздо лучше, а исходы беременности в группах достоверно не отличались. У женщин с отягощенным акушерско-гинекологическом анамнезом и наличием хламидийной инфекции после применения азитромицина в 10,5% случаях произошли преждевременные роды, в 7,9% — ранние выкидыши, в 2,6% — поздние выкидыши. В группе таких же беременных, получавших эритромицин, преждевременные роды, ранние выкидыши и поздние выкидыши наблюдали в 12,5, 8,4 и 4,1% случаев соответственно.
В другом исследовании (C. D. Adair et al., 1998) также был показан сравнимый терапевтический эффект азитромицина и эритромицина — 88,1 и 93,0%. Но переносимость курса лечения с применением азитромицина оказалась гораздо выше, чем при использовании эритромицина — желудочно-кишечные расстройства наблюдались у 11,9% пациенток, принимавших азитромицин (из них у 1 больной (2,4%) лечение пришлось отменить из-за развития рвоты через 4 ч после приема препарата), и у 58,1% больных, принимавших эритромицин (лечение были вынуждены прекратить 18,6% больных). Меньшая частота развития побочных эффектов при приеме азитромицина отчасти связана с однократным приемом этого препарата. Никаких патологических влияний проведенной терапии на новорожденных зафиксировано не было.
В исследовании M. R. Bush и соавторов (1994) побочные эффекты при приеме эритромицина отмечали у всех больных (15 пациентов), при назначении азитромицина — ни у одного из 15. Пятеро из 15 больных, принимавших эритромицин, не смогли полностью закончить лечение.
По данным Кохрановского обзора, показатель микробиологической излеченности у беременных женщин в результате применения всех указанных в руководствах антибиотиков колеблется в пределах 90%. В этом же обзоре, несмотря на небольшое количество данных, делается вывод, что беременные женщины лучше переносят азитромицин и поэтому лечение азитромицином может быть более эффективным. Проведенные исследования не позволили сделать вывод о том, что микробиологическая излеченность во время беременности гарантирует от последующего заболевания новорожденных или послеродовых проявлений хламидийной инфекции у женщин.
Амоксициллин относится к группе пенициллинов, в принципе не рекомендованных к применению при хламидиозе, но, по данным Кохрановского обзора, имеются сообщения о его успешном использовании при наличии хламидийной инфекции у беременных, хотя этот факт вызывает удивление. Он реже, чем эритромицин или азитромицин, вызывает побочные эффекты, которые заставляют прекращать лечение. Так, в исследовании J. Kacmar и соавторов (2001) сообщается о развитии побочных эффектов у 40% больных, принимавших азитромицин, и 17% — принимавших амоксициллин. Однако около 16% больных, принимавших амоксициллин, нарушали режим лечения, пропускав прием лекарства. Эффективность лечения составила 80% при приеме амоксициллина и 94,7% при приеме азитромицина (различия не являются статистически достоверными). Отсутствие долгосрочных исследований влияния применения амоксициллина на риск развития неонатальных инфекций не позволяет с уверенностью рекомендовать этот препарат для рутинной клинической практики. Длительное наблюдение за группой новорожденных и их матерей, во время беременности лечившихся амоксициллином от хламидийной инфекции, позволило бы клиницистам более широко применять эту схему лечения. Амоксициллин, без сомнения, может использоваться как альтернативный препарат для терапии беременных при непереносимости макролидов.
Всем пациенткам, получившим лечение эритромицином, который пока еще чаще используют у беременных, рекомендуется проводить повторное лабораторное исследование через 3 нед после окончания терапии, поскольку побочные эффекты могут вынуждать пациентку нарушать схему его применения.
В заключение мы еще раз хотели вернуться к проблеме изменения традиционных рекомендаций по лечению хламидийной инфекции у беременных. Это очень ответственное решение, требующее многолетних наблюдений. За последние годы единственным серьезным изменением в этой области явилось появление азитромицина среди препаратов выбора в российских и основных мировых рекомендациях. Конечно, этому способствовали многие особенности этого антибиотика, такие как продолжительный период полувыведения, высокий уровень всасывания и устойчивость в кислой среде, способность транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, возможность проникновения внутрь клетки, хорошая переносимость. Но основным препаратом для лечения урогенитальной хламидийной инфекции у беременных женщин азитромицин стал прежде всего благодаря низкой токсичности и безопасности для плода.
А. М. Соловьев, кандидат медицинских наук, доцент
М. А. Гомберг, доктор медицинских наук
МГМСУ, Москва