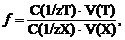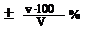Техника выполнения титриметрического анализа



Измерительная посуда.Мерные цилиндры применяют для приближенного, с точностью до 1-2 мл, измерения жидкостей.
Мерные колбы используют для приготовления растворов с точно известной концентрацией. Обычно навеску вещества количественно переносят в мерную колбу, растворяют и разбавляют водой до определенного объема (например, 100 мл), ограниченного круговой меткой (чертой) на горлышке (пока нижний край мениска жидкости не коснется черты).
Пипетки используют для отбора и переноса точного объема раствора из одного сосуда в другой. Перед употреблением пипетку моют, промывают дистиллированной водой и обязательно ополаскивают тем же раствором, который будут отмеривать. Иначе оставшаяся в пипетке вода разбавит отмериваемый для анализа раствор и концентрация его изменится. Правила работы с пипетками: Нижний конец пипетки погружают в раствор и засасывают раствор резиновой грушей через верхнее отверстие. Когда уровень жидкости поднимется выше черты, быстро закрывают верхнее отверстие указательным пальцем правой руки и вынимают пипетку из раствора. Затем лишний раствор осторожно выпускают, пока нижний край мениска не совпадет с чертой, нанесенной на пипетку. В тот момент, когда мениск коснется черты, палец плотно прижимают к верхнему отверстию пипетки и останавливают вытекание жидкости. Наполненную пипетку переносят в колбу для титрования. Для этого колбу держат в наклонном положении, пипетку приставляют нижним ее концом к стенке колбы, держа пипетку вертикально. Слегка отпустив указательный палец, дают раствору стечь, ждут еще примерно 15 секунд и удаляют последнюю каплю прикосновением кончика пипетки к стенке колбы. Не следует выдувать или вытряхивать последние капли жидкости из пипетки, так как при калибровке пипетки метку наносят с учетом того, что при свободном истечении жидкости немного ее остается на стенках.
Бюретки представляют собой цилиндрические градуированные сосуды с краном или резиновым затвором. Крупные деления нанесены через каждый миллилитр, а мелкие – через 0,1 мл. Бюретки используют для измерения объема раствора, израсходованного на титрование. Перед работой бюретку моют, затем ополаскивают раствором, которым будут титровать. Затем, поместив зажим на резиновую часть бюретки, наполняют ее раствором для титрования выше «0» деления, заполняют оттянутую трубку, следя за тем, чтобы в ней не оставалось воздуха. После этого устанавливают нижний мениск на «0» делении, выпуская лишний раствор из бюретки. Отсчеты по бюретке делают с точностью до 0,05 мл. Выполнение отсчета затрудняется тем, что жидкость в бюретке имеет вогнутый мениск. Поэтому глаз при отсчете следует держать точно на уровне жидкости. В противном случае отсчет будет сделан неправильно. Каждое титрование начинают с «0» деления, так как при этом лучше всего компенсируются погрешности калибрования бюретки. Выпускают раствор из бюретки не очень быстро (не быстрее 3-4 капель в секунду), иначе он не будет вовремя стекать со стенок и отсчет окажется неверным.
Приготовление стандартных растворов:
1. Составить уравнение реакции между стандартным веществом и веществом, концентрацию которого следует установить. По уравнению реакции рассчитать молярную массу эквивалента (Э) стандартного вещества. Далее рассчитать массу стандартного вещества, необходимую для приготовления заданного объема раствора заданной концентрации, используя формулу:
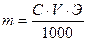
где С – молярная концентрация эквивалента (нормальность) раствора; V – необходимый объем раствора в мл.
2. На технохимических весах взвесить пустой бюкс.
3. Взвесить бюкс с навеской на технохимических весах.
4. Взвесить бюкс с навеской на аналитических весах.
5. Количественно без потерь перенести навеску из бюкса в мерную колбу через сухую воронку (после перенесения вещества воронку из колбы не вынимать!). Взвесить пустой бюкс на аналитических весах.
6. Приготовить раствор. Для этого вначале смыть остатки вещества с воронки в колбу, предварительно чуть приподнять воронку, чтобы был зазор между ней и стенками колбы. Добавить в колбу дистиллированной воды на 1/3 – 1/2 её объема и содержимое колбы вращательными движениями тщательно перемешать до полного растворения навески. Довести объем раствора до калибровочной метки (по нижнему мениску), закрыть колбу пробкой и, придерживая, её указательным пальцем, тщательно перемешать, переворачивая колбу горлышком вниз не менее 8 раз.

7. Рассчитать титр стандартного раствора, используя при этом точную массу навески, т.е. данные взвешиваний на аналитических весах (п. 4-5) по формуле (23) с точностью до пятого знака после запятой.
8. Рассчитать нормальность (молярную концентрацию эквивалента) стандартного раствора с точностью до четвертого знака после запятой по формуле:
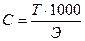
Отбор пробы и титрование:
1. Подготовить к работе бюретку. Для этого ополоснуть бюретку небольшим количеством раствора титранта, использованный раствор вылить. После этого заполнить бюретку раствором титранта почти доверху; затем, подставив под неё стакан и приоткрыв зажим, заполнить «носик» бюретки (оттянутую трубку бюретки) так, чтобы в ней не оставалось пузырьков воздуха. Установить уровень титранта на «0» деление по нижнему мениску раствора.
2. В колбу для титрования отобрать с помощью мерной пипетки отдельную порцию титруемого раствора (аликвоту), предварительно ополоснув пипетку отбираемым раствором, чтобы удалить из неё остаток воды. Добавить в колбу необходимые для титрования реагенты, индикатор.
3. Провести титрование. Для этого колбу с титруемым раствором помещают на штатив под бюретку таким образом, чтобы «носик» бюретки находился в колбе. Левой рукой держат зажим, правой рукой – колбу за её верхнюю часть, чтобы не закрывать раствор, находящийся в колбе. Сжимая зажим и круговыми движениями постоянно перемешивая содержимое колбы, осуществляют титрование. При этом титрант выпускают из бюретки не быстрее 3-4 капель в секунду, иначе он не будет вовремя стекать со стенок и отсчет окажется неверным. По достижении точки эквивалентности (внешне это проявляется в изменении окраски раствора) титрование прекращают. Снимают показания титрования по бюретке с точностью до 0,05 мл и записывают объем титранта в лабораторный журнал. Титрование осуществляют не менее трех раз. При этом результаты титрования должны быть сходящимися, т.е. расхождение не должно превышать 0,1мл. При получении трех сходящихся результатов, находят среднее значение и рассчитывают концентрацию анализируемого раствора. Если в результате трех титрований сходящиеся результаты не получены, проводят 4-е, 5-е титрование до получения трех сходящихся результатов.
Расчеты результатов титрования:
Расчет среднего объема титранта осуществляют по формуле:
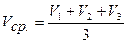
Расчет молярной концентрации эквивалента (нормальности) титранта по раствору стандартного вещества.По закону эквивалентов:
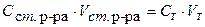
Из формулы (31) выразим молярную концентрацию эквивалента титранта:
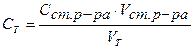
Расчет массы определяемого вещества в определенном объеме раствораосуществляют по формуле:
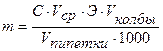
где С – нормальность титранта; Э – молярная масса эквивалента определяемого вещества; Vср – средний объем трех сходящихся результатов титрования.
Титриметрический анализ
Титриметрический (объемный) анализ объединяет группу методов количественного химического анализа, основанных на процессе титрования. Он заключается в измерении объема раствора реагента, израсходованного на эквивалентное взаимодействие с определяемым веществом. По концентрации и объему раствора реагента вычисляют содержание определяемого вещества. Титриметрический метод анализа применим для определения средних и больших содержаний веществ (свыше 1%).
Реакции, используемые в титриметрии, должны удовлетворять следующим основным требованиям:
– реакция должна протекать количественно, т. е. константа равновесия реакции должна быть достаточно велика;
– реакция должна проходить быстро;
– реакция не должна осложняться протеканием побочных реакций;
– должен существовать способ определения окончания реакции.
Если реакция не удовлетворяет хотя бы одному из этих требований, она не может быть использована в титриметрическом анализе.
В зависимости от типа реакции, которая лежит в основе определения, различают следующие методы титриметрического анализа: кислотно-основное, окислительно-восстановительное, осадительное и комплексиметрическое.
По способу индикации конечной точки различают визуальное, потенциометрическое, фотометрическое, кондуктометрическое, амперометрическое титрование и др.
В зависимости от способа проведения титрование бывает прямым, обратным, косвенным (по заместителю).
Титрование можно проводить из отдельных навесок и пипетированием. В первом случае титруют все количество определяемого вещества. При пипетировании исследуемый раствор (или навеску вещества) количественно переносят в мерную колбу, доводят водой до метки и тщательно перемешивают. Далее из мерной колбы отбирают пипеткой несколько проб раствора (аликвоты) для параллельных титрований.
Основные термины, применяемые в титриметрическом анализе
Титрование – процесс постепенного контролируемого приливания раствора с точно известной концентрацией к определенному объему другого раствора.
Титрант (титрованный, рабочий раствор) – раствор, который приливают, имеет точно известную концентрацию.
Титруемый раствор – раствор, к которому приливают титрант.
Титриметрическая система – смесь веществ, образовавшаяся при взаимодействии титранта и титруемого вещества.
Точка эквивалентности (т. э.) – момент титрования, когда число эквивалентов титранта равно числу эквивалентов определяемого вещества.
Индикатор – вещество или прибор, применяемые для установления конечной точки титрования, которая обычно мало отличается от точки эквивалентности.
Степень оттитрованности (f) – отношение количества эквивалентов титранта, пошедшего на титрование в любой момент титрования, к исходному количеству эквивалентов определяемого вещества:
где С(1/z T) и С(1/z Х) – молярные концентрации эквивалентов титранта и титруемого вещества, соответственно;
V(Х) – исходный объем титруемого вещества; V(Т) – добавленный объем титранта.
Стандарт (исходное вещество, установочное вещество) – химическое соединение, используемое для приготовления раствора с точно известной концентрацией (первичный стандарт), удовлетворяющее ряду требований:
– вещество должно быть химически чистым;
– состав вещества должен строго соответствовать формуле;
– вещество должно быть устойчивым при хранении в твердом виде и в растворе;
– должно иметь возможно большую молярную массу эквивалента.
Лишь немногие вещества удовлетворяют этим требованиям.
Стандартизация титранта – процесс определения точной концентрации титранта титрованием ранее стандартизированного раствора или установочного вещества.
Фиксанал – запаянная ампула, в которой находится определенное количество соответствующего вещества. Фиксаналы используют для приготовления растворов первичных стандартов. Ампулу разбивают над воронкой, помещенной в мерную колбу, вещество смывают дистиллированной водой и раствор доводят до метки.
Прямое титрование – один из способов титрования, когда определяемое вещество в процессе титрования непосредственно реагирует с веществом рабочего (стандартного) раствора. Например, титрование кислот основаниями и наоборот.
Обратное титрование – один из способов титрования, когда к анализируемому веществу добавляют известное количество другого вещества, а затем избыток этого вещества, не вступившего в реакцию, оттитровывают соответствующим стандартным раствором.
Титрование по заместителю – один из способов титрования, когда после реакции определяемого вещества с избытком вспомогательного реагента оттитровывают продукт реакции, количество эквивалентов которого в точности равно количеству эквивалентов определяемого вещества.
Работа с измерительной посудой
Точные объемы растворов в титриметрическом анализе отмеряют с помощью измерительной посуды – мерных колб, пипеток, бюреток.
Титрование проводят, приливая титрант из бюретки (градуированной стеклянной трубки) к раствору определяемого вещества.
Бюретка градуирована в см3 с делениями через одну или две десятых см3. По системе СИ рекомендуется выражать объемы в дм3 и см3, однако допускаются и старые единицы: литры и миллилитры. 1 литр занимает объем 1 дм3, 1 миллилитр – 1 см3. Обычные бюретки имеют емкость 10, 25 и 50 см3 (мл), а отсчет объема раствора в них дает три цифровых знака – десятки, единицы и десятые доли миллилитра. Сотые доли миллилитра определяют приближенно.
Мерные колбы обычно имеют емкость 25, 50, 100, 200, 250, 500 и 1000 см3 (мл). Пипетки обычно делают объемом 5, 10, 15, 20, 25, 50 см3 (мл).
Пользуясь мерной посудой, следует помнить, что ее емкость часто не точно соответствует обозначенной. Посуда 1 класса емкостью более 10 мл пригодна для работы с точностью 0,1%, для посуды 2 класса допускаемые отклонения вдвое больше.
Заполнение бюреток раствором
Чистую бюретку заполняют на 1/3 титрантом, убеждаются в исправности затвора и отсутствии в нем пузырька воздуха. Для этого кончик бюретки поднимают и слегка открывают зажим. Если жидкость идет ровной струей, без пузырьков воздуха, бюретка заполнена правильно. Наклоняя и поворачивая бюретку, смачивают стенки раствором, после чего сливают почти весь раствор через носик. Перед началом титрования бюретку устанавливают строго вертикально и заполняют титрантом до нуля. При этом уровень мениска жидкости вогнутой частью должен совпадать с нулевым делением шкалы (нулевое деление должно находиться на уровне глаз) для бесцветных растворов. Для окрашенных растворов нуль устанавливают по верхнему краю мениска.
Отмеривание растворов пипеткой
Чистую пипетку с помощью резиновой груши заполняют титруемым раствором до начала расширения. Закрыв верхний конец указательным пальцем, несколько раз поворачивают пипетку, стараясь смочить раствором всю внутреннюю поверхность немного выше метки. Сливают раствор.
Теперь заполняют пипетку с помощью резиновой груши немного выше метки. Снимают грушу, отверстие слегка закрывают пальцем, «держа» метку пипетки на уровне глаз, осторожно сливают избыток раствора так, чтобы мениск жидкости вогнутой частью совпадал с меткой. После этого отверстие пипетки зажимают и переносят ее в другой сосуд. Верхнюю часть пипетки открывают и дают жидкости спокойно вытечь. После того как жидкость из пипетки стечет, последние капли сливают, касаясь стенки сосуда, в который выливают жидкость. Затем пипетку вынимают, не обращая внимания на жидкость, которая в ней осталась. Выдувать жидкость из пипетки нельзя.
Правила титрования
Место, где проводится титрование, должно быть хорошо подготовлено и освещено. На основание штатива с бюреткой следует положить лист белой бумаги. Бюретку укрепляют параллельно стержню штатива.
Титруют малыми порциями – по каплям. Открывают зажим бюретки левой рукой, а колбу для титрования держат правой, постоянно перемешивая ее содержимое вращательными движениями. После вытекания раствора отсчет делений на бюретке производят через 20-30 с, чтобы дать возможность стечь жидкости, оставшейся на стенках бюретки.
Отсчет снимают по нижнему (бесцветные растворы) или по верхнему (окрашенные растворы) краю мениска. Мениск должен находиться на уровне глаз. Для получения достоверных результатов повторяют титрование не менее трех раз. Каждое повторное титрование начинают с нулевого отсчета бюретки.
Погрешности титрования
При титровании возможны случайные и систематические погрешности. Случайные погрешности связаны с измерением объема и массы навески, систематические (индикаторные) появляются при несоответствии точки конца титрования точке эквивалентности.
Погрешности измерения растворов возникают вследствие неточности отмеривания растворов вещества и титранта. Они складываются из объема одной капли (V
0,05 мл), которой обычно перетитровывают раствор, и погрешности калибровки измерителей (бюретки, пипетки, мерной колбы), у которых допускаются отклонения ± (0,01 – 0,02) мл. Относительная погрешность титрования зависит от объема затраченного титранта или титруемого раствора и равна:
0,05 мл) и отклонений в объеме
Можно ли титровать пипеткой
Правила работы с пипетками. Во время работы с пипеткой избегают прикосновения рукой к ее средней части. От тепла, сообщаемого рукой стеклу, емкость пипетки и, следовательно, объем вмещаемой ею жидкости увеличиваются.
При работе пипетку берут за верхнюю часть большим и средним пальцами правой руки и глубоко (почти до самого дна сосуда) погружают нижний конец пипетки в раствор. Придерживая левой рукой сосуд, из которого берут жидкость, всасывают ртом жидкость в пипетку так, чтобы уровень в ней поднялся на 2—3 см выше метки. Затем быстро закрывают верхнее отверстие пипетки указательным пальцем (рис. 25), чтобы жидкость не выливалась из пипетки. Избыток жидкости медленно сливают из пипетки, ослабив слегка нажим пальца.
Рис. 24. Пропаривание мерной колбы:
Когда нижняя полоса мениска коснется метки, отверстие пипетки плотно закрывают, усилив нажим пальца на верхнее отверстие, и переносят содержимое пипетки в колбу для титрования. При этом пипетку держат так, чтобы метка находилась на уровне глаза (рис. 26).
Выливать содержимое пипетки в другой сосуд необходимо медленно, давая всей жидкости равномерно стечь из отверстия пипетки. При быстром сливании раствора значительная часть его в силу законов истечения жидкости останется на стенках пипетки. Во время сливания жидкости пипетку держат в вертикальном положении.
К концу сливания, несмотря на все предпринятые меры, в пипетке все же остается некоторая часть жидкости. Поэтому по окончании сливания прикасаются на мгновение нижним концом пипетки к внутренней стенке сосуда, в который сливают раствор.
Можно пользоваться и другими способами наполнения пипетки и выливания из нее жидкости. Но существует одно обязательное правило: необходимо придерживаться во время работы одного и того же способа наполнения и выливания жидкости из пипетки.
Для наполнения пипетки легколетучими и ядовитыми жидкостями (хромовая смесь, растворы аммиака, органические растворители и т. п.) пользуются специальными приспособлениями (рис. 27). Засасывать такие жидкости ртом категорически запрещается.
Пипетки, промытые дистиллированной водой или соответствующим растворителем, хранят в специальных штативах (рис. 28).
Рис. 25. Положение пальцев при отборе пробы с помощью пипетки.
Рис. 26. Положение глаза при измерении объема с помощью пипетки.
Рис. 27. Прибор для заполнения пипетки летучими или ядовитыми жидкостями: 1 — резиновая груша; 2 — резиновые пробки; 3 — широкая стеклянная трубка; 4 — сосуд с раствором; 5 — пипетка.
Рис. 28. Штатив для хранения пипеток.
Во избежание попадания в пипетку пыли верхнее отверстие пипеток накрывают стеклянными или бумажными колпачками.
Очистка пипеток. Придерживаясь требуемых правил работы с пипеткой, все же можно допустить очень большие ошибки при выполнении объемно-аналитических определений. Это случается при работе с недостаточно очищенной или загрязненной в процессе употребления пипеткой.
Ошибки, обусловливаемые загрязнением пипетки, могут быть значительны, так как емкости пипеток сравнительно невелики, а искажения вследствие загрязнения пипеток могут быть относительно большими. Поэтому следует работать с абсолютно чистыми пипетками. Перед употреблением пипетки должны быть тщательно вымыты и пропарены.
Проверка емкости пипетки. Действительная емкость пипетки может значительно отличаться от номинальной емкости, обозначенной на пипетке. Поэтому перед употреблением пипетки следует проверить ее емкость.
Емкость пипетки проверяют путем взвешивания воды, вмещаемой пипеткой. Для этого предварительно взвешивают на технических весах пустую колбу емкостью 
Пример. Проверить емкость пипетки номинальной емкостью 

Техника работы с пипеткой



ЛАБОРАТОРНАЯ РАБОТА №4
«Основные приемы работы с химической посудой, используемой для приготовления растворов»
Цель работы: Научиться подготавливать оборудование для приготовления и титрования растворов.
Задачи:
1. Ознакомиться с хим. посудой, применяемой для приготовления растворов и требованиями к химреактивам, используя лекционный материал и видео-материалы.
2. Ответить на контрольные вопросы
1. Общие рекомендации
1.1. Лабораторную работу выполнять в тетради для лабораторных работ по УП.02.
1.2. Обязательно написать название, цель, задачи работы и краткие ответы на контрольные вопросы.
1.4 Сканы направить в л.с.
КОНТРОЛЬНЫЕ ЗАДАНИЯ
1. Правила заполнения бюретки
2. Как проверить носик бюретки на наличие воздуха.
3. Правила монтажа бюретки.
4. Как считывать показания с бюретки
5. Перечислить квалификации химических реактивов по чистоте.
6. Охарактеризовать реактивы квалификации “Ч” и “ЧДА”.
7. Охарактеризовать реактивы квалификации “ОСЧ” и “ЧДА”.
Информационный блок
«Основные приемы работы с химической посудой для приготовления точных растворов»
Приступая к выполнению работы, студент должен внимательно прочитать ее описание и в соответствии с ним подготовить необходимую посуду и реактивы, расположив их так, чтобы удобно было ими пользоваться. Все лишнее следует убрать на полки или в ящики стола.
Использованные растворы и реактивы, ставшие ненужными, выливают по указанию лаборанта, освобождают, моют посуду и убирают на место, где она должна храниться.
Приемы работы с химической мерной посудой
Мерные колбы предназначены для отмеривания точного объема на вливание. Они представляют собой круглые плоскодонные сосуды с узким длинным горлом (шейкой). На шейке есть кольцевая метка, до которой следует наполнить колбу. Термин «на вливание» означает, что если наполнить мерный сосуд жидкостью точно до метки, то объем жидкости при комнатной температуре будет соответствовать вместимости, указанной на стенке сосуда. Мерные колбы могут иметь вместимость от 10 мл до 2 л; вместимость указывается на колбе заводом-изготовителем.
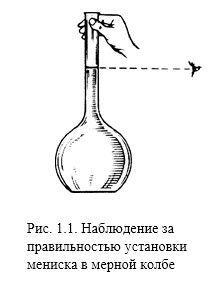
Мерные колбы применяют для приготовления стандартных растворов, а также для разбавления анализируемых проб перед взятием аликвоты (точно отмеренной кратной части общего объема) раствора для анализа. Раствор, находящийся в колбе, доводят до метки в несколько приемов. Сначала наливают растворитель до 1/3 или 1/2 вместимости колбы и, не закрывая пробкой, кругообразными движениями перемешивают содержимое колбы. Затем добавляют растворитель до горла колбы, после чего приливают его тонкой струйкой из промывалки, немного не доводя до метки. Последние порции растворителя приливают в колбу из капельницы или из промывалки до тех пор, пока вогнутый мениск своей нижней частью не сольется с линией метки (рис. 1.1).
При этом после добавления каждой капли колбу поднимают перед собой за верхнюю часть шейки (выше метки) так, чтобы метка находилась на уровне глаз. Нельзя держать мерную колбу за ее нижнюю часть, иначе может произойти искажение объема за счет тепла, сообщаемого рукой. Следует также помнить, что растворитель, как и раствор в колбе, должен иметь температуру рабочего помещения. После доведения уровня жидкости до метки колбу закрывают пробкой и хорошо перемешивают полученный раствор, переворачивая колбу вверх-вниз.

Пипетки предназначены для точного измерения объемов растворов на выливание. Это означает, что если заполнить пипетку до метки, а затем вылить жидкость, ее объем будет соответствовать вместимости, указанной на пипетке. Пипетки бывают двух типов: градуированные (дифференциальные) и простые (рис. 1.2).
Техника работы с пипеткой
1. В соответствии с правилами мытья посуды, хорошо промывают пипетку одной из моющих смесей, а затем водой. После этого дважды ополаскивают ее тем раствором, точный объем которого отбирают для анализа. Для этого берут пипетку правой рукой, держа верхний конец (выше метки) большим и средним пальцами, погружают нижний конец пипетки в раствор и засасывают его с помощью груши до тех пор, пока уровень жидкости не поднимется до расширенной части пипетки. Затем закрывают верхний конец указательным пальцем и вынимают пипетку из колбы. Держа ее над стаканом или над раковиной, придают ей горизонтальное положение и, вращая и чуть наклоняя пипетку (рис. 1.3, а), смачивают внутреннюю поверхность от нижнего конца до метки и немного выше. После этого жидкость сливают через нижний конец пипетки в раковину или стакан и повторяют ополаскивание. Нельзя сливать раствор через верхний конец пипетки, иначе он попадет в грушу.
2. Для отбора аликвоты раствора используют те же приемы, но всасывают жидкость до уровня, немного превышающего метку (рис. 1.3, б). Закрывают верхний конец пипетки указательным пальцем и вынимают пипетку с жидкостью из раствора. Левой рукой обтирают снаружи нижнюю часть пипетки полоской фильтровальной бумаги (рис. 1.3, в).
После того как стечет весь раствор, ждут еще 10-15 с. Небольшую часть раствора, которая остается в пипетке, нельзя выдувать или стряхивать: при строгом соблюдении правил работы с пипеткой эта оставшаяся часть всегда будет одной и той же. Ни в коем случае нельзя засасывать ртом летучие или ядовитые жидкости, а также концентрированные кислоты или щелочи. Для отбора такого рода жидкостей с помощью пипетки следует пользоваться резиновой грушей.
Значение объема отмечается по нижнему уровню мениска, если раствор в бюретке прозрачен; при этом глаз наблюдателя должен находиться на уровне мениска.
Повысить точность измерения объема по бюретке позволяет экран, сделанный из куска белого картона (примерно 5×5 см), нижняя половина которого окрашена черной тушью. Если раствор в бюретке непрозрачен (например, раствор КМп04), отсчет ведут по верхнему уровню жидкости.