Аденомы гипофиза. Выступление врача-нейрохирурга Лещинского А.В.
Опухоли гипофиза. Врач-нейрохирург Лещинский Андрей Владиславович.
Краткое содержание:
Здравствуйте, уважаемые слушатели!
Я сам врач-нейрохирург, оперирую опухоли гипофиза. Хиазмально-селлярная область — это место, где находится гипофиз и патологические процессы, которые исходят из него.
Гипофиз — это центральный орган эндокринной системы, который регулирует весь гормональный обмен в организме.
Когда я объясняю пациентам по поводу того, что это такое, я обычно говорю, что гипофиз — это как генерал, который контролирует все железы внутренней секреции, выделяя соответствующие гормоны.
Некоторые гормоны действуют на весь организм, некоторые только прицельно на какие-то органы-мишени.
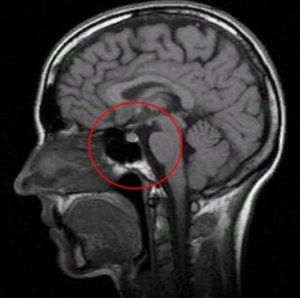
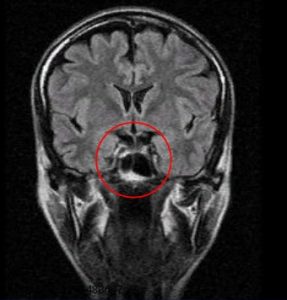
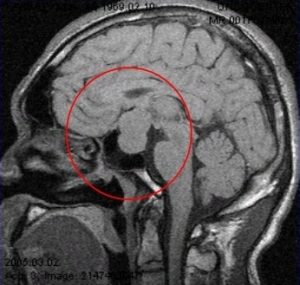
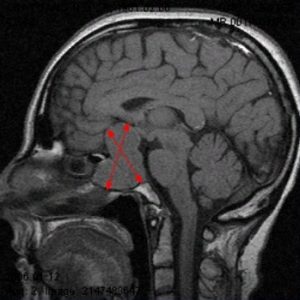
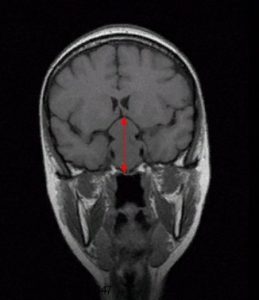
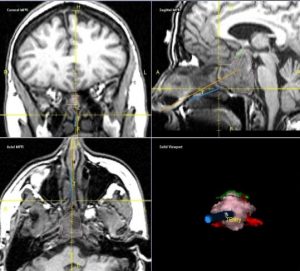
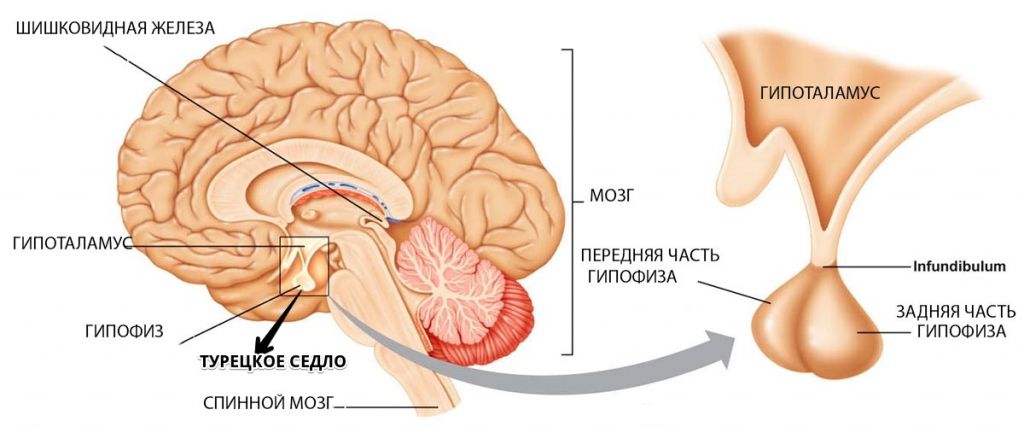
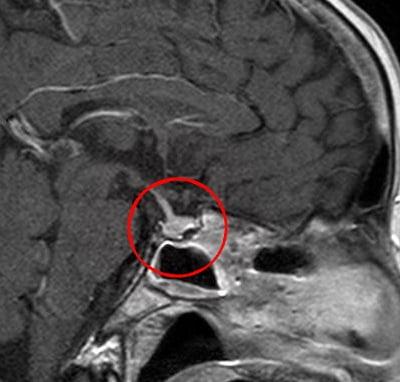
Рис.1 и 2. Нормальная анатомия хиазмально-селлярной области. МРТ
Вот это гипофиз, вот это хиазма, между ними ножка гипофиза или стебель гипофиза. Это нормальная анатомия.
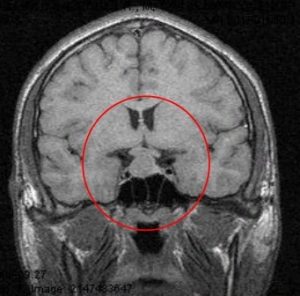
Рис. 3 и 4. Аденома гипофиза. МРТ
На рисунках 3 и 4 показана патологическая анатомия. Из этого маленького органа выросла вот такая большая аденома гипофиза.
Рост опухоли может быть кверху, он называется супраселлярный, может быть книзу, он называется инфраселлярный. Может быть кзади — ретроселлярный, кпереди — антеселлярный. Или вправо или влево — это называется латероселлярный рост в соответствующую сторону, вправо или влево.
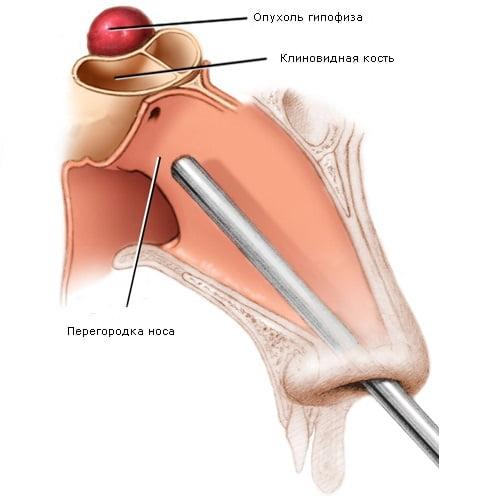
Доступ осуществляется через полость носа, если мы говорим про трансназальный подход. Далее хирург попадает в такую воздухоносную пазуху. Это полость в кости, которая называется основная кость. В ней внутри есть некоторые перегородки. Хирург их убирает и оказывается перед турецким седлом. Турецкое седло — это костный карман, в котором как раз находится гипофиз. То есть хирург делает как бы трепанацию вот здесь вот, убирает косточку, и вот здесь. И попадает в то место, где производится оперативное лечение.
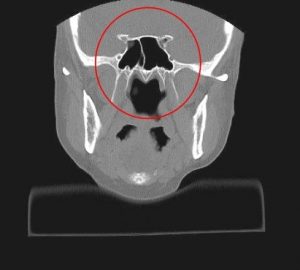
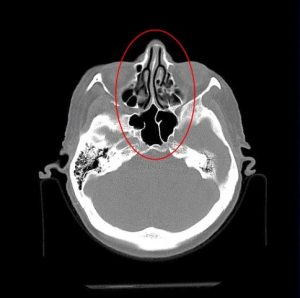
Рис. 5 и 6 Компьютерная томография головного мозга
До этого была магнитно-резонансная томография головного мозга. Это компьютерная томография головного мозга. Просто еще раз хочу показать. Доступ осуществляется через полость носа. Это передняя стенка пазухи. Черное — это воздух. Это задняя стенка пазухи. И хирург оказывается в области турецкого седла. Иногда внутри пазухи существуют дополнительные перегородки.
По размерам нам важно знать, что бывает:
Главное, чтобы размер был минимум в двух проекциях измерен.
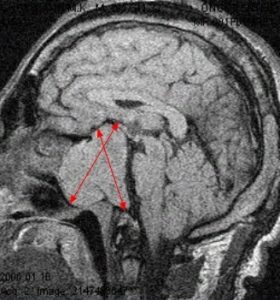
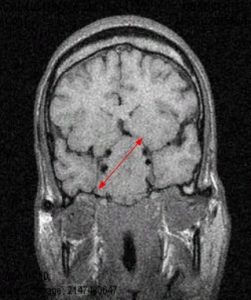
Рис.7 Примеры гигантских аденом гипофиза
Вот гигантская аденома гипофиза с супраселлярным ростом кверху, с инфраселлярным ростом книзу. Тут латероселлярный рост в одну из сторон (вправо). И также видите, какой огромный узел. Все это можно удалить.
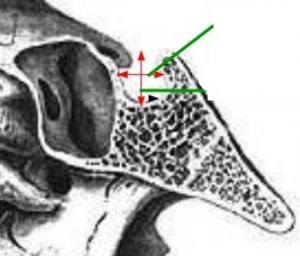
Рис. 8 Рентгенография черепа (оценка турецкого седла)
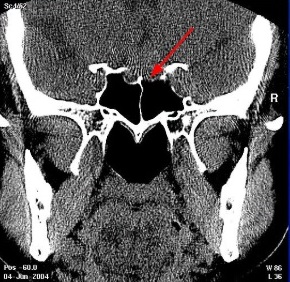
Рис. 9 Компьютерная томография
По компьютерной томографии : мы специально иногда ее назначаем, с той точки зрения, чтобы посмотреть, не разрушены ли костные структуры, потому что на КТ очень хорошо видны именно костные структуры.
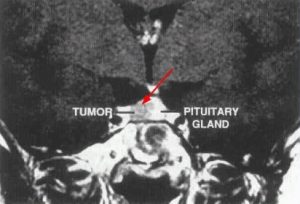
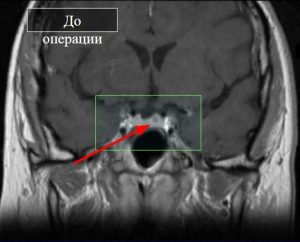
Рис. 10 МРТ с контрастным усилением
Но, тем не менее, золотой стандарт, как я уже сказал, — это МРТ, обязательно с контрастным усилением. На рисунке 10: серое — это опухоль, а эта часть — нормальный гипофиз. Показана стрелкой опухоль. Особенно это актуально для микроаденом гипофиза, которые находятся в толще нормального, неизменённого гипофиза, и которые иными способами выявить невозможно. Это характерно для гормонально активных опухолей, например.
При подозрении на опухоль хиазмально-селлярной области существует следующий алгоритм :
Бывают гормонально активные опухоли и гормонально неактивные.
Гормонально активные опухоли.
Клиническая картина гиперпролактинемии
| Женщины | Мужчины |
| Нарушение менструального цикла: аменорея, олигоменорея, ановуляторные циклы, укорочение лютеиновой фазы | Снижение или отсутствие либидо и потенции |
| Бесплодие | Уменьшение выраженности вторичных половых признаков (особенно при начале заболевания в постпубертатном возрасте) |
| Лакторея | Бесплодие, вследствие олигоспермии |
| Снижение либидо, фригидность | Гинекомастия |
| Гиперандрогения: гирсутизм, акне | Лакторея |
| Метаболические нарушения: остеопороз, ожирение, гиперинсулинемия (вследствие снижения печёночной и периферической резистентности) | |
| Психоэмоциональные нарушения: повышенная утомляемость, слабость | |
Клиническая картина акромегалии:
Клиническая картина гиперкортицизма:
Исходя из того, что бывают опухоли гормонально активные, с уществуют частные показания к операции.
Соматотропиномы — это синдром акромегалии, в качестве первого этапа, иногда при отсутствии эффекта от медикаментозного лечения. Но хирургия все-таки является помощью первой линии.
Пролактинома — при отсутствии эффекта от медикаментозного лечения, при непереносимости препаратов, аллергической реакции, например, на них. Все-таки мы считаем, что первая линия лечения — это медикаментозное лечение. Иногда бывают случаи, когда очень поздно выявили пролактиному у пациента. Она большого или гигантского размера. Очень сильно сдавила окружающие структуры мозга, вызвала, например, нарушение зрения, называется хиазмальный синдром. В этом случае совместно с эндокринологом проводится консилиум и в определенных ситуациях мы отказываемся от медикаментозной терапии, по крайней мере дооперационной, и берем сразу на операцию.
Тиреотропиномы и гонадотропиномы — это редкий вариант опухоли. Их не будем пока обсуждать.
Клиническая картина гормонально неактивных аденом состоит из воздействия массы опухоли на окружающие структуры.
Так как опухоли не выделяют гормоны, пациенты начинают чувствовать, или почувствуют ее намного позже, чем гормонально активные опухоли.
Половые нарушения : аменорея, олигоопсоменорея, лакторея, бесплодие, эректильная дисфункция у мужчин.
Гипопитуитарные нарушения : вторичный гипокортицизм, вторичный гипотиреоз.
Абсолютное показание к операции — это:
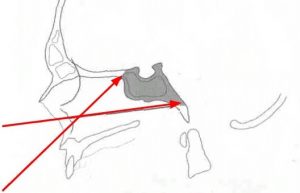
Рис. 11 Трансназальный доступ (угол хирургического действия)
Транскраниальные доступы нужны только в отдельно взятых случаях и это обсуждается отдельно с пациентами.
Как я уже говорил, доступ осуществляется через полость носа. Это основная пазуха, воздухоносоная, основная кость, в которой находится вот такая полость. Осуществляется трепанация передней стенки пазухи и задней стенки пазухи. И мы попадаем вот в этот костный кармашек, который называется турецкое седло, где лежит гипофиз, из которого могут развиваться большие опухоли. Стрелками показано, что даже через полость носа можно убирать большие опухоли, которые могут далеко выходить за полость турецкого седла. Это угол хирургического действия, который позволяет нам широко удалять большие опухоли с различными вариантами роста.
То есть существуют некоторые методики, которые позволяют нам удалять распространенные сложные опухоли, большие, например, или те, которые имеют какой-то интересный рост в сторону: вправо, влево, вверх, вниз, которые не видны обычным взглядом, например, через микроскоп.
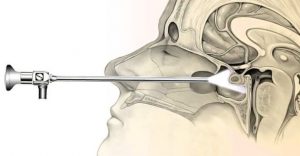
Рис. 11. Применение эндоскопической техники
В данном случае, если вы видите, то зелененькое сверху — это хиазма, то есть зрительные нервы, а красненькое — это сонные артерии. И на нижнем снимке видно, как хирург удаляет часть опухоли. И видно, что это происходит около сонной артерии и он тут должен быть внимательным, собранным, чтобы не повредить данный сосуд. И также это позволяет увидеть часть инструментов, которые могут быть зарегистрированы этой операционной системой, нейронавигацией. Хирург знает, где они расположены. Это очень важный момент.
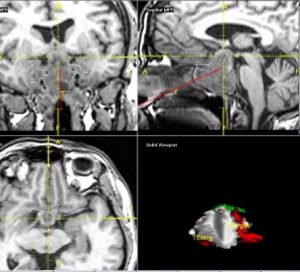
12 и 13 Использование операционной нейронавигации

Рис. 14. Использование операционной нейронавигации
Применение нейроэндоскопии, системы операционной нейронавигации позволяют:
— Свободно ориентироваться в условиях узкой и глубокой операционной раны (мы говорим про трансназальную хирургию).
— Эта система, все вместе — позволяет улучшить общее состояние пациента после операции и как можно быстрее пациент возвращается к обычной жизни и быстрее выписывается из стационара. Что, мне кажется, является очень важным для пациента.
Некоторые клинические случаи я вам покажу.
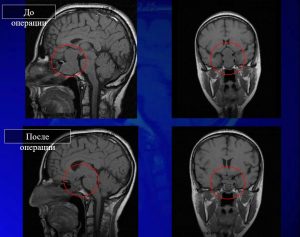
Рис. 15 Клинический случай, гигантская аденома гипофиза
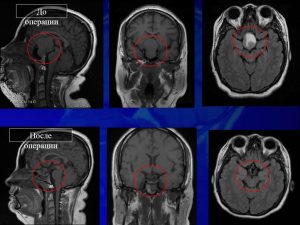
Рис. 16 Клинический случай, питуитарная апоплексия
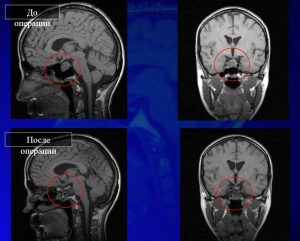
Рис. 17. Клинический случай, небольшие образования
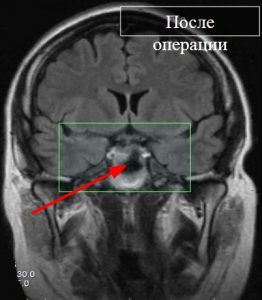
Рис. 18 Клинический случай, микроаденома (кортикотропинома)
Среднее пребывание в палате реанимации у пациентов в основном не более суток. Пациент прооперирован, на следующий день переводится в свою палату. На 3-6 сутки он может быть выписан.
Фотография сделана на третьи сутки после операции. Это типичные пациенты с акромегалией, у которых были удалены опухоли, выделяющие гормон роста, соматотропиномы.
Производится в это время:
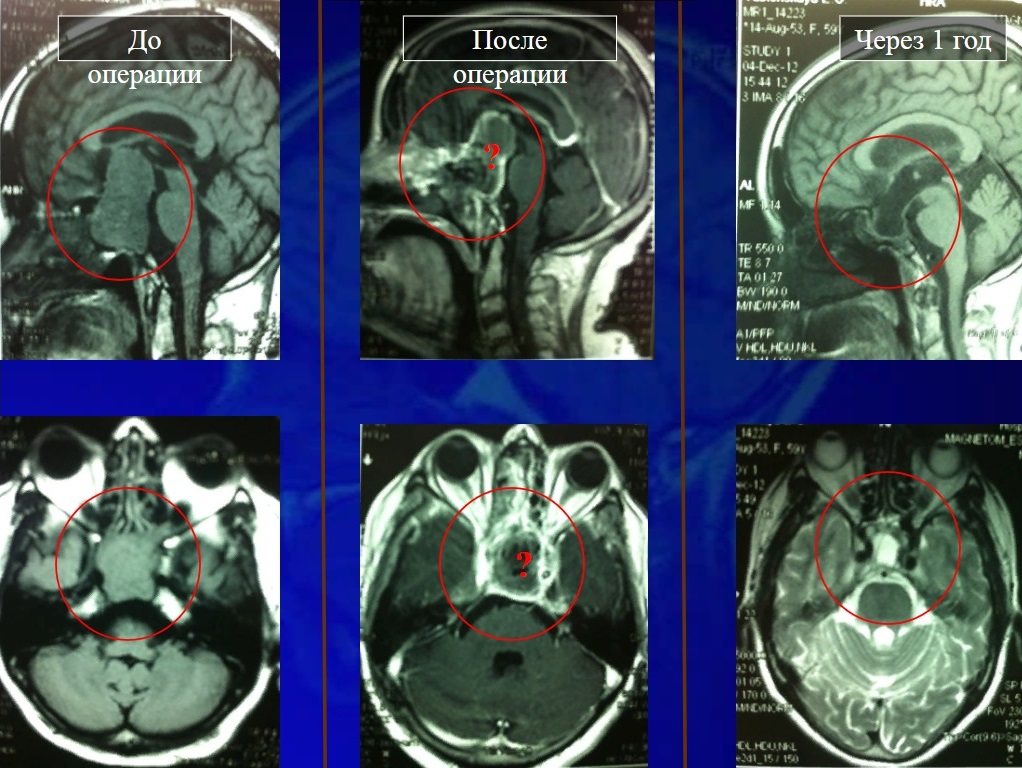
Рис. 19 Снимки МРТ до операции, сразу после и через год
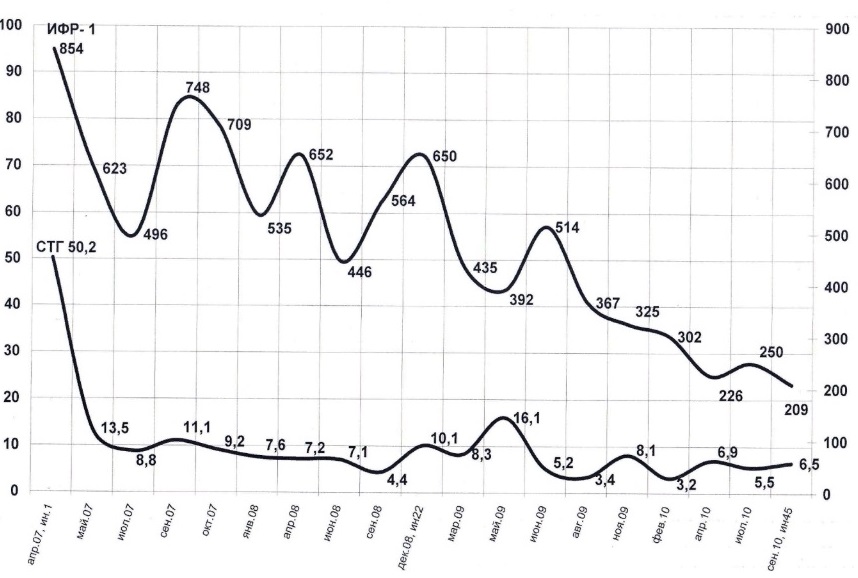
Рис. 20 Динамика СТГ, ИРФ-1 после операции
Конечно же, это командная работа : то есть это офтальмолог, невролог, эндокринолог, нейрохирург, рентгенолог, лор-врач, иногда радиотерапевт, если будет требоваться лучевая терапия.
Показания к радиохирургии:
Радиохирургических установок очень много, самая распространенная — это гамма-нож или кибер-нож. (Рисунок 21)

Рис. 21 Радиохирургические установки
Благодарю вас за внимание, если у вас будут какие-то вопросы — задавайте. Если есть какие-то личные вопросы, пожалуйста, тут моя почта, мой телефон.
Аденома гипофиза головного мозга: операция, симптомы, лечение и последствия
Аденома гипофиза головного мозга (АГГМ) представляет собой опухоль железистой ткани мозгового придатка. Гипофиз – это значимая в организме человека эндокринная железа, располагающаяся в нижней части мозга в гипофизарной ямке турецкого седла. Этот маленький орган эндокринной системы, у взрослого человека весом всего в 0,7 г, отвечает за собственную продукцию гормонов и контроль над синтезом гормонов щитовидной и паращитовидной железой, мочеполовыми органами. Гипофиз участвует в регуляции водно-жирового обмена, отвечает за рост и вес человека, развитие и работу внутренних органов, начало родовой деятельности и лактацию, становление репродуктивной системы и др. Не зря эту железу медики величают «виртуозным дирижером», управляющим звучанием большого оркестра, где оркестр – это весь наш организм.
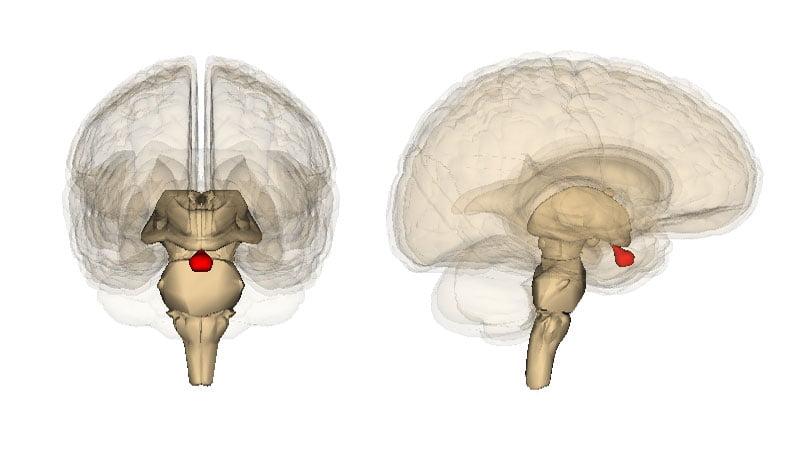
Схематичное изобрадение расположения опухоли.
Но, к сожалению, уникальный орган, без которого слаженный функциональный баланс в организме невозможен, не защищен от патологических образований, или болезней на почве гормонального и/или неврогенного расстройства. Одним из серьезных заболеваний является аденома, при которой железистый, гормонально активный эпителий гипофиза головного мозга патологически разрастается, что может стать причиной инвалидизации больного.
Аденомы могут быть активными (ААГ) и неактивными (НАГ). В первом случае страдает гормональный фон от переизбытка выделяемых гипофизарных гормонов. Во втором – массив опухоли раздражает, сдавливает близко расположенные ткани, чаще затрагивается зрительный нерв. Стоит отметить, что сильно увеличенные пропорции и активного патологического очага так же негативно воздействуют на внутричерепные ткани, находящиеся вблизи. О других особенностях патологии, включая специфику лечения, предлагаем узнать из статьи.
Эпидемиология: причины, частота заболеваемости
Фактор, который стимулирует развитие гипофизарной опухоли, до сих пор не выявлен, поэтому остается главным предметом исследований. Специалисты относительно вероятных причин озвучивают лишь версии:
Новообразование встречается не так уж и редко, в общей структуре опухолей головного мозга на его долю приходится 12,3%-20% случаев. По частоте встречаемости оно занимает 3 место среди нейроэктодермальных неоплазий, уступая лишь глиальным опухолям и менингиомам. Заболевание, как правило, доброкачественной природы. Однако в медицинской статистике зафиксированы данные о единичных случаях злокачественной трансформации аденомы с образованием вторичных очагов (метастазов) в головной мозг.
Патологический процесс чаще диагностируется у женщин (примерно в 2 раза больше), чем у мужчин. Далее приведем данные о распределении возрастов из расчета 100% пациентов с клинически подтвержденным диагнозом. Эпидемиологический пик приходится на возраст 35-40 лет (до 40%), в 30-35 лет заболевание определяется у 25% пациентов, в 40-50 лет – у 25%, 18-35 и старше 50 лет – по 5% на каждую возрастную категорию.
По статистике, около 40% пациентов имеют неактивную опухоль, которая не секретирует в избытке гормональные вещества и не отражается на эндокринном равновесии. Приблизительно у 60% пациентов определяют активное образование, отличающееся гиперсекрецией гормонов. Порядка 30% людей становятся инвалидами из-за последствий агрессивной гипофизарной аденомы.
Классификация аденом гипофиза головного мозга
Гипофизарный очаг формируется в передней доли железы (в аденогипофизе), которая составляет основную массу органа (70%). Развивается заболевание при мутации одной клетки, как результат, она выходит из-под иммунного надзора и выпадает из физиологического ритма. Впоследствии, путем многократного деления клетки-предшественника образуется аномальное разрастание, состоящее из группы идентичных (моноклональных) клеток. Это и есть аденома, такой механизм развития самый частый. Однако в редких случаях очаг может изначально происходить из одного клеточного клона, а после рецидива – из другого.
Патологические образования различают по активности, величине, гистологии, характеру распространения, виду секретируемых гормонов. Мы уже выяснили, какого вида активности бывают аденомы, – гормонально-активные и гормонально-неактивные. Рост дефектной ткани характеризует параметр агрессивности: опухоль может быть неагрессивной (небольшая и не склонная к увеличению) и агрессивной, когда она достигает больших размеров и оказывает инвазию на соседние структуры (артерии, вены, нервные ветви, пр.).
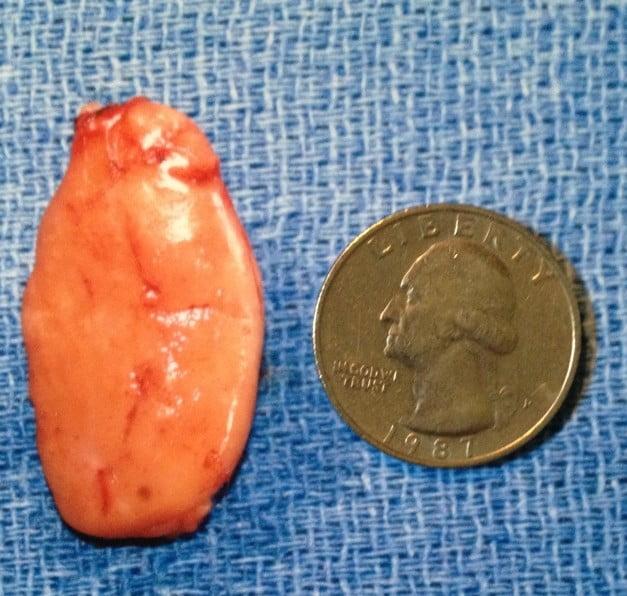
Крупная аденома после удаления.
По величине аденомы гипофиза ГМ бывают следующих видов:
АГГМ по распространению делятся на:
► супраселлярно – в полость черепа;
► латероселлярно – в пещеристый синус или под твердую мозговую оболочку;
► инфраселлярно – растут вниз в сторону клиновидной пазухи носа/носоглотки;
► антеселлярно – затрагивают решетчатый лабиринт и/или глазницу;
► ретроселлярно – в заднюю черепную ямку и/или под Блюменбахов скат.
По гистологическому признаку аденомам присвоены наименования:
Среди гормонально-активных аденом различают:
Клинические проявления опухоли
Многие симптомы пациентами, как они сами подчеркивают, поначалу не воспринимаются серьезно. Недомогания зачастую связывают с банальным переутомлением или, к примеру, стрессом. Действительно, проявления могут быть неспецифичными и завуалированными долгое время – 2-3 года или больше. Заметим, что характер и интенсивность симптомов зависят от степени агрессии, вида, локализации, объема и многих других характеристик аденомы. Клиника новообразования складывается из 3 симптоматических групп.
Примерно у 50% людей на фоне гипофизарной аденомы возникает симптоматический (вторичный) диабет. У 56% диагностируют утрату зрительных функций. В той или иной мере почти все испытывают классические для гипофизной гиперплазии головного мозга симптомы: головная боль (более чем у 80%), психоэмоциональные, метаболические, сердечно-сосудистые расстройства.
Методы диагностики патологии
Специалисты придерживаются единой схемы диагностики при подозрении у человека этого диагноза, которая предусматривает:
Отметим, что специфика забора и изучения биологического материала на гормоны состоит в том, что выводов не делают после первого же обследования. Для достоверности гормональной картины необходимо наблюдение в динамике, то есть потребуется неоднократно с определенными промежутками сдавать кровь для исследования.
Принципы лечения заболевания
Сразу оговоримся, при этом диагнозе пациент нуждается в высококвалифицированной медицинской помощи и постоянном наблюдении. Поэтому не нужно полагаться на случай, считая, что опухоль рассосется и все пройдет. Самоустраниться очаг не может! При отсутствии адекватной терапии слишком велика опасность стать инвалидом с необратимыми функциональными нарушениями, летальные случаи от последствий тоже бывают.
В зависимости от степени тяжести клинической картины больным рекомендуется решение проблемы оперативным путем или/и консервативными методами. К базовым процедурам терапии относят:
Трансназально оперируют 90% пациентов, 10% нуждаются в транскраниальной эктомии. Последняя тактика применяется при массивных опухолях (более 3 см), ассиметричном разрастании новообразованной ткани, выходе очага за пределы седла, опухолях с вторичными узлами.
Не использовать операцию, а рекомендовать наблюдение за человеком с диагнозом «аденома гипофиза», врач может при отсутствии очаговых неврологических и офтальмологических нарушений при гормонально-неактивном поведении опухоли. Ведение такого пациента осуществляет врач-нейрохирург в плотном сотрудничестве с эндокринологом и окулистом. Подопечного систематично обследуют (1-2 раз в год), направляя на МРТ/КТ, глазное и неврологическое обследование, измерение гормонов в крови. Параллельно с этим человек проходит курсами целенаправленную поддерживающую терапию.
Поскольку оперативное вмешательство является ведущим методом лечения аденомы гипофиза, вкратце осветим ход хирургического процесса эндоскопической операции.
Трансназальная операция по удалению аденомы гипофиза головного мозга
Это – миниинвазивная процедура, не требующая краниотомии и не оставляющая после себя никаких косметических дефектов. Выполняется чаще под местной анестезией, основным прибором хирурга будет эндоскоп. Нейрохирург через нос с помощью оптического устройства удаляет мозговую опухоль. Как же все это делается?
Пациента активизируют в раннем периоде – уже на первые сутки после малотравматичной нейрооперации. Примерно на 3-4 сутки оформляется выписка из стационара, дальше понадобится пройти специальный курс реабилитации (антибиотикотерапию, физиотерапию и пр.). Несмотря на перенесенную хирургию по иссечению аденомы гипофиза, некоторым больным будет предложено дополнительно придерживаться гормонозаместительной терапии.
Риски интра- и послеоперационных осложнений при эндоскопической процедуре сведены до минимума – 1%-2%. Для сравнения, негативные реакции разного характера после транскраниальной резекции АГГМ возникают примерно у 6-10 чел. из 100 прооперированных пациентов.
После трансназального сеанса у большинства людей некоторое время наблюдается затруднение носового дыхания, неприятные ощущения в носоглотке. Причина – необходимое интраоперационное разрушение отдельных структур носа, как следствие, болезненные признаки. Дискомфорт в носоглоточной области обычно не расценивается как осложнение, если не усиливается и длится недолго (до 1-1,5 мес.).
Окончательно оценить эффект от операции возможно только через 6 месяцев по снимкам МРТ и результатам гормональных анализов. В целом, при своевременном и правильном проведении диагностики и оперативного вмешательства, качественной реабилитации, прогнозы благоприятные.
Заключение
Центральный Военный Госпиталь г.Прага.
Обратите внимание, не менее успешной в области нейрохирургии головного мозга является Чехия. В Чешской Республике благополучно оперируют аденомы гипофиза, используя самые передовые технологии аденомэктомии, причем так же технически безупречно и с минимумом рисков. Разница между Чехией и Германией/Израилем в том, что услуги чешских клиник как минимум вдвое обходятся дешевле, а медицинская программа всегда включает полноценную реабилитацию.
Можно ли удалить гипофиз
ФГБВОУ ВПО «Военно-медицинская академия им.С.М. Кирова», Санкт-Петербург
ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Исследование качества жизни больных с аденомами гипофиза в до- и послеоперационном периодах
Журнал: Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2019;83(2): 11-16
Черебилло В. Ю., Курнухина М. Ю. Исследование качества жизни больных с аденомами гипофиза в до- и послеоперационном периодах. Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2019;83(2):11-16.
Cherebillo V Yu, Kurnukhina M Yu. Quality of life in patients with pituitary adenomas in the pre- and postoperative period. Zhurnal Voprosy Neirokhirurgii Imeni N.N. Burdenko. 2019;83(2):11-16.
https://doi.org/10.17116/neiro20198302111
ФГБВОУ ВПО «Военно-медицинская академия им.С.М. Кирова», Санкт-Петербург
Цель исследования — оценить изменения качества жизни у больных до и после удаления аденомы гипофиза. Материал и методы. Проведено клиническое исследование 42 больных с аденомами гипофиза. Установление диагноза основывалось на клинико-лабораторных данных и результатах лучевых и инструментальных методов исследования. Удаление аденомы гипофиза осуществлялось трансфеноидальным доступом. Анализ качества жизни проводился у больных в дооперационном и раннем послеоперационном периодах. Больные были в возрасте от 22 до 63 лет (медиана 45 лет). Для оценки качества жизни в до- и послеоперационном периодах нами был выбран специальный опросник — EORTC QLQ-C30, созданный группой оценки качества жизни Европейской организации исследования и лечения рака. Он используется во многих международных клинических исследованиях. Результаты. У исследованных больных отмечена положительная динамика в послеоперационном периоде по всем функциональным шкалам. По симптоматическим шкалам отмечено снижение утомляемости, выраженности болевого синдрома, проявлений тошноты и рвоты, одышки. После операции нормализировалась моторика кишечника, снизилась частота проявления диареи и запоров, стабилизировался сон. Исследуемые также отмечали улучшение показателя общего здоровья и уменьшение ожидаемых финансовых затруднений. Заметным показателем было снижение аппетита. Выводы. При исследовании различных показателей качества жизни до и после операции у пациентов с аденомами гипофиза выявлено, что оперативное вмешательство с использованием трансфеноидального доступа для тотального удаления аденомы гипофиза приводит к улучшению качества жизни больных.
ФГБВОУ ВПО «Военно-медицинская академия им.С.М. Кирова», Санкт-Петербург
ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Аденома гипофиза — это опухоль эндокринной системы, которая проявляется гипер- или гипосекрецией гормонов передней доли гипофиза, а также клиническими симптомами, вызванными влиянием новообразования на окружающие селлярную область анатомические структуры [1].
Согласно статистическим данным, ежегодно в России и странах СНГ выявляется около 3 тыс. вновь заболевших [2]. Среди интракраниальных опухолей аденомы гипофиза занимают 3-е место, составляя от 7,3 до 18% всех верифицированных опухолей мозга, и поражают преимущественно лиц работоспособного возраста, на который приходится около 75% всех случаев заболевания [3].
Цель любого из видов лечения опухолей гипофиза (хирургического вмешательства, лекарственной или лучевой терапии) — нормализовать секрецию гипофизарных гормонов, ликвидировать клинические проявления их гиперсекреции, уменьшить размеры крупной опухоли, сдавливающей жизненно важные структуры головного мозга, или полностью устранить ее, а также избежать отдаленных рецидивов, сохранив функцию передней доли гипофиза [4].
К настоящему времени накоплен большой опыт по удалению аденом гипофиза трансфеноидальным доступом [5—7]. Несомненным преимуществом в методике эндоскопического удаления опухолей хиазамально-селлярной области является возможность панорамного обзора структур этой зоны в условиях хорошей освещенности [8]. Это позволяет четко отдифференцировать основные анатомические структуры, избежать их повреждения, а также более радикально удалять опухоли. Применение увеличительной оптики, операционных микроскопов и эндоскопов, использование микрохирургической техники при удалении опухолей гипофиза существенно улучшило результаты оперативных вмешательств, уменьшило летальность, количество рецидивов заболевания и интраоперационных осложнений [4]. Использование оптического увеличения с разным углом зрения позволяет удалять опухоли «из-за угла» (в том числе и новообразования, расположенные латеральнее внутренней сонной артерии), под непосредственным визуальным контролем [9].
Важным направлением современной медицины является исследование качества жизни пациентов. В настоящее время часто в медицинской сфере используется термин «качество жизни, связанное со здоровьем» (health-related quality of life — HRQOL) [10, 11]. В конце XX века силами ВОЗ было осуществлено исследование по разработке основополагающих критериев HRQOL. В основу современных опросников по HRQOL были положены выстроенные связи вопросов и ответов, которые затем использовались для вычисления по методу суммирования рейтингов. Существуют общие опросники, которые направлены на оценку здоровья населения в целом, независимо от патологии, и специальные — для определенных заболеваний. Каждый опросник имеет свои критерии и шкалы оценки [12].
Цель настоящего исследования — анализ и оценка изменений качества жизни больных до и после удаления аденомы гипофиза.
Материал и методы
Проведено исследование 42 больных (25 женщин и 17 мужчин в возрасте от 22 до 63 лет) с гистологически подтвержденным диагнозом аденомы гипофиза. Средний возраст пациентов 43,95±11,3 года, медиана 45 лет. Установление диагноза у этих больных основывалось на клинико-лабораторных данных, результатах лучевых и инструментальных методов исследования. У всех пациентов использован трансфеноидальный доступ с применением эндоскопической ассистенции.
Для определения степени инвазии аденомы гипофиза в полость кавернозного синуса использовались МРТ-срезы на уровне турецкого седла и Knosp Scale [13]. В нашей серии наблюдений присутствовали разные степени заболевания: Grade 0 (нормальное расположение внутренней сонной артерии и венозных пространств) — у 14,3% больных, Grade I (опухоль проникает через медиальную касательную линию, но не распространяется за интракаротидную линию) — у 83,3%, Grade II (аденома распространяется за внутрисонную линию, но не переходит за латеральную) — у 2,4%.
Степень радикальности операции оценивалась через 3—6 мес после оперативного лечения. У исследуемых пациентов, по данным МРТ головного мозга, не было выявлено остатков опухоли, что подтверждало тотальность удаления образования.
Клинический анализ включал выяснение анамнеза заболевания исследуемых, оценку лабораторных, инструментальных данных, особенностей оперативного вмешательства, определение послеоперационных изменений качества жизни исследуемых.
Анализ изменений качества жизни проводился у больных в дооперационном и раннем послеоперационном периодах (первые 5—7 дней после оперативного лечения, до выписки из стационара).
В настоящее время существуют различные опросники для оценки качества жизни больных с аденомой гипофиза (Anterior Skull Base Questionnaire — ASBQ), Sino-nasal outcome test (SNOT-22), EORTC QLQ-C30). Опросник ASBQ включает 35 вопросов, объединенных в группы, которые характеризуют продуктивность, двигательную активность, выносливость, боль, эмоции, специфические симптомы [14]. Тест SNOT-22 включает 22 вопроса, посвященных характеру выделений из носа, наличию заложенности носа, болевого синдрома, головокружений, нарушению обоняния/вкуса, сна, описанию эмоционального состояния, снижению концентрации внимания [15].
Специальный опросник EORTC QLQ-C30 сходен с указанными предыдущими опросниками. Он был создан Группой оценки качества жизни Европейской организации исследования и лечения рака [16] и используется во многих международных клинических исследованиях. EORTC QLQ-C30 высокочувствителен и применим для оценки качества жизни у больных независимо от вида онкологического заболевания. Опросник состоит из 30 вопросов и различных шкал: общего состояния здоровья; 5 функциональных шкал — физической, ролевой, когнитивной, эмоциональной и социальной функций; шкал симптоматики. В симптоматическую шкалу входят такие симптомы, как усталость, тошнота/рвота и боль. Кроме того, в EORTC QLQ-C30 вошли 6 отдельных пунктов — бессонница, потеря аппетита, запор, диарея, диспноэ, финансовые трудности [17—19].
Для нашего исследования мы выбрали опросник EORTC QLQ-C30, так как он, в отличие от ASBQ и SNOT-22, включает оценку самим пациентом своего здоровья и качества жизни.
Ответы на вопросы каждой шкалы опросника EORTC QLQ-C30 подвергались переводу в числовой диапазон от 0 до 100. Таким образом, при более высоких значениях в функциональных, симптоматических шкалах предполагались высокий уровень функционирования и меньшая выраженность определенных симптомов, токсичности. И наоборот, чем ниже были показатели по шкалам общего статуса здоровья, тем выше была оценка пациентом общего состояния своего здоровья до и после оперативного лечения [19].
Полученные в процессе исследования данные обрабатывались c помощью лицензионной программы SPSS Statistics 22.0 в два этапа. На первом этапе оценивался вид распределения признаков в выборках, на втором — в зависимости от вида распределения рассчитывали среднее значение и его стандартное отклонение (М±SD) или медиану и интерквартильные интервалы (Me; 25/75). Для анализа качественных переменных использовали критерий χ 2 Пирсона.
Проверка закона распределения при необходимости анализа количественных переменных проводилась при помощи теста Колмогорова—Смирнова. Для определения силы связи в случае ненормального распределения переменных использовали двухсторонний ранговый корреляционный анализ Спирмена, в случае нормального распределения — двухсторонний корреляционный анализ (r) Пирсона. Оценивали также значимость различий между группами (p). Критический уровень достоверности нулевой статистической гипотезы (об отсутствии различий и влияний) принимали равным 0,05 [20, 21].
Результаты
У исследуемых пациентов для удаления аденомы гипофиза был выбран трансфеноидальный доступ. Радикальное удаление всех аденом гипофиза — тотальная резекция. Средняя длительность оперативного вмешательства составила 33,57±9,96 мин, средняя продолжительность анестезии — 63,69±17,22 мин. Длительность госпитализации исследуемых составила 7,74±3,07 дня. Нами была проведена оценка общего состояния больных (performance status) с использованием шкалы Карновского и ECOG-ВОЗ. Таким образом, выявлено, что все исследуемые больные в дооперационном периоде соответствовали 90% по шкале Карновского (пациент способен к нормальной деятельности, отмечаются незначительные симптомы или признаки заболевания), и 1 баллу по ECOG-ВОЗ (есть симптомы заболевания, но ближе к нормальному состоянию). В послеоперационном периоде 7,1% исследуемых отмечали улучшение — отсутствие жалоб (100% по шкале Карновского, 0 баллов по ECOG-ВОЗ) [22—24].
Проведен анализ жалоб больных при поступлении. Основные жалобы больных в дооперационном периоде: головная боль диффузной локализации (69%), ухудшение памяти (57,1%), зрительные расстройства (42,9%). Реже пациенты отмечали головокружение (9,5%), головную боль определенной локализации (4,8%), тошноту и боль в суставах (2,4%). У 31% больных отмечалась акромегалия, у 11,9% — гормональная дисфункция. Выявлена корреляционная связь между возрастом и жалобами на болевой синдром в дооперационном периоде: чем старше пациент, тем более выраженным был у него болевой синдром (r=0,523; p=0,001).
Зрительные расстройства были представлены у пациентов снижением остроты зрения. При этом выявлена корреляционная связь между снижением остроты зрения и возрастом пациентов (r=0,408; р=0,007), жалобы на снижение остроты зрения перед операцией чаще отмечались у лиц более старшего возраста. Кроме того, у пациентов наблюдалось также выпадение полей зрения — гемианопсия. У пациентов с гомонимной гемианопсией отмечалось выпадение височного поля зрения только с левой стороны (левосторонняя гемианопсия). Гомонимная гемианопсия в дооперационном периоде отмечена у 11,9% исследуемых, в послеоперационном периоде — лишь у 4,8%. Битемпоральная гемианопсия до операции была у 19% пациентов, в послеоперационном периоде она сохранилась у 11,9%.
Оценка качества жизни больных проводилась в до- и послеоперационном периодах. Произведен анализ показателей качества жизни по функциональным и симптоматическим шкалам.
У пациентов отмечена положительная динамика в послеоперационном периоде по всем функциональным шкалам. Так, после операции улучшилось физическое (с 89,7±11,7 до 94,7±8,9), ролевое (с 85±22 до 94,5±15,8), когнитивное (с 69,4±24,4 до 91,7±13,8), эмоциональное (с 69±24,7 до 92,9±18,8, p 
Показатели качества жизни у больных с аденомами гипофиза в динамике по функциональным шкалам (EORTC QLQ-C30).
По симптоматическим шкалам отмечено снижение утомляемости (c 62,9±25,9 до 77,1±19,8), выраженности болевого синдрома (с 71,4±30,4 до 84,9±22), проявлений тошноты и рвоты (с 95,6±12,3 до 96±9,6), одышки (с 86,6±24,5 до 90,5±22,4). У больных после операции нормализировалась моторика кишечника, снизилась частота проявления диареи (с 96,8±12,3 до 100) и запоров (с 90,5±18,4 до 95,3±13,9), стабилизировался сон с изменением показателя с 72,3±33,7 до 81,1±28,6. Кроме того, после оперативного вмешательства исследуемые отмечали уменьшение своих ожидавшихся финансовых затруднений (с 89,7±23,9 до 98,4±7,1). При опросе пациентов о причине уменьшения финансовых трудностей в послеоперационном периоде мы выявили, что после операции пациенты испытывали облегчение в связи с тотальностью удаления образования, улучшением общего состояния и готовы были приступить к своим служебным обязанностям вовремя, не нуждаясь в длительном периоде реабилитации.
После операции пациенты отмечали прогрессирование симптома «снижение аппетита» (с 91,3±19,5 до 89,8±20,1). Отмечено улучшение показателя общего здоровья (с 46,5±19 до 25,3±13).
Таким образом, мы выявили положительную динамику в 14 из 15 шкал качества жизни EORTC QLQ-C30. Получен достоверно положительный результат по 1 шкале — эмоциональное функционирование. Отрицательная динамика отмечена только по одной симптоматической шкале — снижение аппетита.
У исследуемых больных отсутствовали интра- и послеоперационные осложнения.
Установлена корреляционная связь между шкалой общего здоровья и функциональными, симптоматическими шкалами у исследуемых в послеоперационном периоде. Более высоко оценили свое состояние здоровья после операции те пациенты, которые были удовлетворены своим положением в обществе (социальным статусом) (r=0,350; p=0,023), и те, у которых улучшился аппетит (r=0,433; p=0,004).
На основании того, что по 14 из 15 шкал качества жизни в послеоперационном периоде у больных отмечена положительная динамика, мы пришли к заключению, что оперативное вмешательство с использованием трансфеноидального доступа для тотального удаления аденомы гипофиза приводит к улучшению качества жизни больных. Мы предполагаем, что такие значимые улучшения качества жизни больных в раннем послеоперационном периоде, возможно, вызваны повышенным эмоциональным фоном. На момент выписки исследуемые нами пациенты были счастливы от того, что самый важный этап в их лечении (оперативное лечение) уже позади, опухоль доброкачественная, удалена тотально и отсутствуют осложнения. А это значит, что вернуться к прежнему ритму жизни больные смогут быстрее, чем планировали до операции.
Была проанализирована литература по теме исследования. Ранее C. Andela и соавт. [25] изучили изменения качества жизни у больных с аденомой гипофиза. В их анализ было включено 102 работы. Авторами отмечено, что хирургические и фармакологические мероприятия по лечению аденом гипофиза улучшают, но не нормализуют качество жизни.
Заключение
Оперативное вмешательство с использованием трансфеноидального доступа для тотального удаления аденомы гипофиза приводит к улучшению качества жизни больных. После операции пациенты отмечали отрицательную динамику только по одному симптому — снижение аппетита. Более высокие оценки своего состояния здоровья после операции давали пациенты с более высоким социальным статусом (r=0,350; p=0,023) и те, у которых улучшился аппетит (r=0,433; p=0,004). Отмечены полное улучшение и отсутствие жалоб после операции у 7% исследуемых (100% по шкале Карновского, 0 баллов по ECOG-ВОЗ).
Авторы заявляют об отсутствии конфликта интересов.
Комментарий
При любой плановой нейрохирургической операции важно не только сохранить жизнь пациенту, минимизировать осложнения, но и обеспечить достойный уровень качества жизни в послеоперационном периоде, который у пациентов с аденомой гипофиза зависит от зрительных функций, гормонального фона и других факторов.
Сопоставив состояние больных до и после трансназальных аденомэктомий, авторы выявили лишь один отрицательный момент в серии из 42 пациентов — прогрессирование снижения аппетита в послеоперационном периоде. Наиболее вероятно, что это могло быть связано с усугублением вторичного гипокортицизма. Важно было бы провести корреляцию этого осложнения с точки зрения исходного и послеоперационного гормонального статуса.
Статья, безусловно, актуальна, ибо динамика качества жизни все шире применяется для оценки результатов в хирургии. Однако дефектом планирования работы можно считать, что послеоперационное состояние больных оценивалось только в раннем послеоперацинном периоде — до момента их выписки из стационара. Возможно, поэтому данные, полученные авторами, в основном говорят о повышенном эмоциональном фоне пациентов в раннем послеоперационном периоде, а не о реальном улучшении качества жизни. Сами авторы отмечают, что пациенты (и их близкие) счастливы от того, что перенесли операцию без серьезных осложнений, опухоль оказалась доброкачественной, она удалена тотально.
В то же время опыт Московского нейрохирургического центра им. Бурденко и данные других исследователей говорят о том, что в первые недели после трансназальной аденомэктомии качество жизни пациентов может заметно ухудшаться: отек слизистой после операции нарушает носовое дыхание днем и ночью, возникают временные нарушения обоняния, в течение длительного времени сохраняются кровяные выделения из носа и другие послеоперационные проявления. Кроме того, пациенты в первые недели после операции весьма ограничены физически, им противопоказаны физические нагрузки, наклоны, чиханье, натуживание, т.е. все то, что может привести к повышению внутричерепного давления (в целях профилактики послеоперационной ликвореи). В раннем послеоперационном периоде часто нарастают или появляются симптомы гипопитуитаризма и транзиторного несахарного диабета, гормональная перестройка организма требует в первые недели после операции приема гормональной заместительной терапии, что также не может заметно улучшить качество жизни.
Поэтому, по нашему мнению и по данным ряда авторов (E. McCoul. J Neurosurg. 2015;123:813-820), качество жизни после трансназальной операции возвращается на дооперационный уровень лишь через 6 нед. В связи с этим исследовать качество жизни целесообразно не только в раннем послеоперационном периоде, но и через 3, 6, 12 нед и т.д.
Тем не менее очевидная польза от этой публикации состоит в том, что она ориентирует широкий круг специалистов (нейрохирургов, эндокринологов и специалистов смежных специальностей) на возможность использования в практике различных современных оценочных критериев их работы.
П.Л. Калинин, А.Н. Шкарубо (Москва)