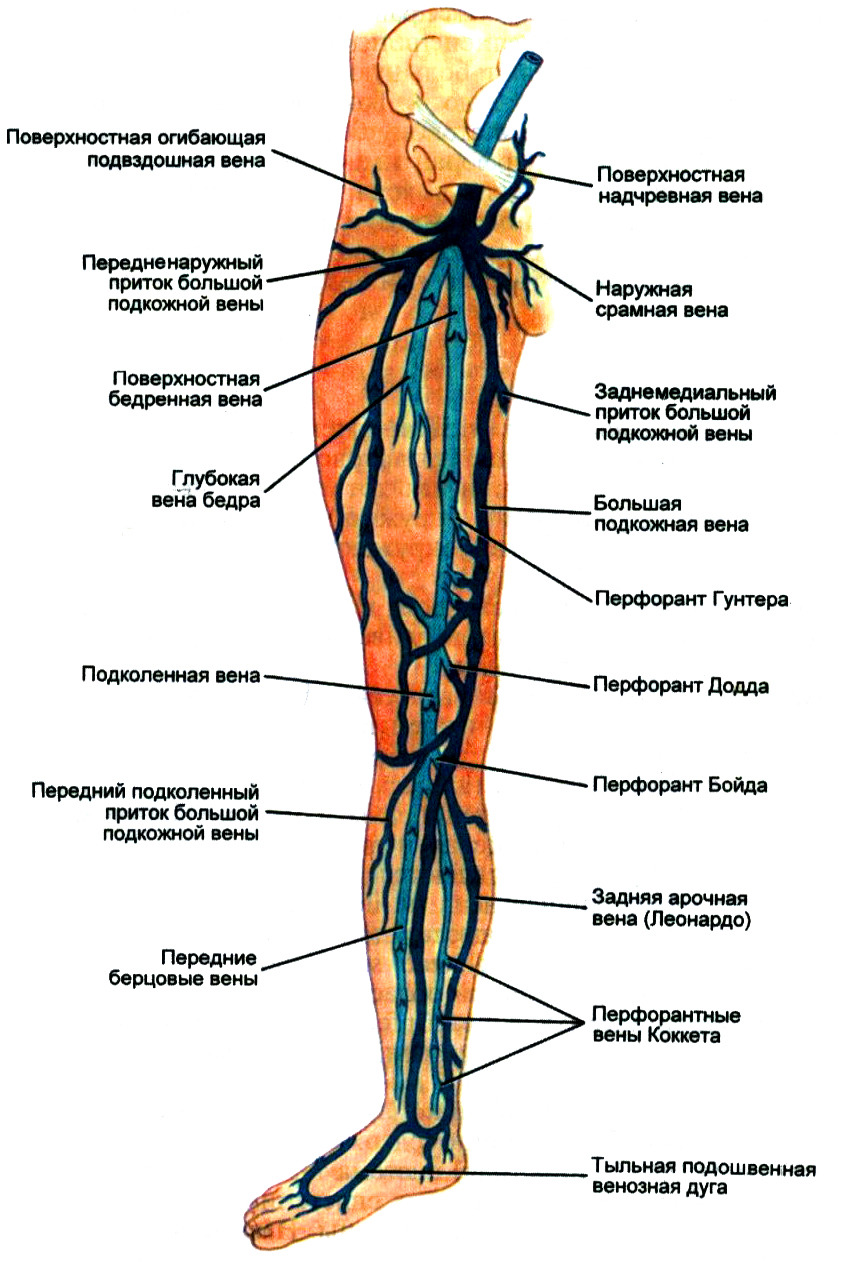
Основы венозной системы нижних конечностей
Своеобразное строение венозных сосудов и состав их стенок определяет их емкостные свойства. Вены отличаются от артерий тем, что являются трубками с тонкими стенками и просветами сравнительно большого диаметра. Так же как и стенки артерий, в состав венозных стенок входят гладкомышечные элементы, эластические и коллагеновые волокна, среди которых последних гораздо больше.
В венозной стенке выделяются структуры двух категорий:
— опорные структуры, к которым относятся ретикулиновые и коллагеновые волокна;
— упруго-сократительные структуры, к которым относятся эластические волокна и гладкомышечные клетки.
Коллагеновые волокна в обычных условиях поддерживают нормальную конфигурацию сосуда, а если на сосуд оказывается какое-либо экстремальное воздействие, то эти волокна сохраняют ее. В формировании тонуса внутри сосуда коллагеновые сосуды участия не принимают, а также они не оказывают влияние на сосудодвигательные реакции, так как за их регуляцию отвечают гладкомышечные волокна.
Вены состоят из трех слоев:
— адвентиция – наружный слой;
— медиу – средний слой;
— интиму – внутренний слой.
Между этими слоями находится эластические мембраны:
— внутренняя, которая выражена в большей степени;
— наружная, которая весьма слабо различается.
Среднюю оболочку вен в основном составляют гладкомышечные клетки, которые расположены по периметру сосуда в виде спирали. Развитие мышечного слоя зависит от ширины диаметра венозного сосуда. Чем больше диаметр вены, тем мышечный слой развит больше. Число гладкомышечных элементов становится больше сверху вниз. Мышечные клетки, составляющие среднюю оболочку, находятся в сети коллагеновых волокон, которые сильно извиты и в продольном, и в поперечном направлении. Эти волокна распрямляются только тогда, когда происходит сильное растяжение венозной стенки.
Поверхностные вены, которые располагаются в подкожной клетчатке, имеют весьма развитый гладкомышечный строй. Это объясняет тот факт, что поверхностные вены в отличие от расположенных на том же уровне имеющих такой же диаметр глубоких вен, отлично противостоят и гидростатическому, и гидродинамическому давлению за счет того, что их стенки имеют эластическое сопротивление. Венозная стенка имеет толщину, которая обратно пропорциональна величине окружающего сосуд мышечного слоя.
Наружный слой вены, или адвентицию, составляет плотная сеть коллагеновых волок, которые создают своеобразный каркас, а также небольшое количество мышечных клеток, которые имеют продольное расположение. Этот мышечный слой с возрастом развивается, наиболее отчетливо его можно наблюдать в венозных сосудах нижних конечностей. Роль дополнительной опоры играют венозные стволы более или менее крупного размера, окруженные плотной фасцией.
Строение стенки вены определяется ее механическими свойствами: в радиальном направлении венозная стенка имеют высокую степень растяжимости, а в продольном направлении – малую. Степень растяжимости сосуда зависит от двух элементов венозной стенки – гладкомышечных и коллагеновых волокон. Жесткость венозных стенок во время их сильной дилатации зависит от коллагеновых волокон, которые не дают венам очень сильно растягиваться исключительно в условиях значительного повышения давления внутри сосуда. Если же изменения внутрисосудистого давления имеют физиологических характер, то за упругость венозных стенок отвечают гладкомышечные элементы.
Венозные клапаны
Венозные сосуды имеют важную особенность – в них есть клапаны, с помощью которых возможен центростремительный ток крови в одном направлении. Количество клапанов, а также их расположение служит для обеспечения кровотока к сердцу. На нижней конечности самое большее число клапанов расположено в дистальных отделах, а именно немного ниже того места, где находится устье крупного притока. В каждой из магистралей поверхностных вен клапаны расположены на расстоянии 8-10 см друг от друга. У коммуникантных вен, за исключением бесклапанных перфорантов стопы, также есть клапанный аппарат. Часто перфоранты могут впадать в глубокие вены несколькими стволами, которые по внешнему виду напоминают канделябры, что препятствует ретроградному кровотока вместе с клапанами.
Клапаны вен обычно имеют двустворчатое строение, и на то, как они распределяются в том или ином сегменте сосуда, зависит от степени функциональной нагрузки.
Каркасом для основы створок венозных клапанов, которые состоят из соединительной ткани, служит отрог внутренней эластической мембраны. У створки клапаны есть две покрытые эндотелием поверхности: одна – со стороны синуса, вторая – со стороны просвета. Гладкомышечные волокна, расположенные у основания створок, направленные вдоль оси вены, в результате изменения своего направления на поперечное создают циркулярный сфинктер, пролабирующий в синус клапана в виде своеобразного ободка крепления. Строму клапана формируют гладкомышечные волокна, которые пучками в виде веера идут на створки клапана. С помощью электронного микроскопа можно обнаружить имеющие продолговатую форму утолщения – узелки, которые расположены на свободном крае створок клапанов крупных вен. По мнению ученых, это своеобразные рецепторы, которые фиксируют тот момент, когда створки смыкаются. Створки интактного клапана имеют длину, превышающую диаметр сосуда, поэтому если они закрыты, то на них наблюдаются продольные складки. Избыточной длиной створок клапана, в частности, обусловлен физиологический пролапс.
Венозный клапан – это структура, имеющую достаточную прочность, которая может выдерживать давление до 300 мм рт. ст. Однако в синусы клапанов крупных вен через впадающие в них тонкие притоки, не имеющие клапанов, сбрасывается часть крови, из-за чего давление над створками клапана снижается. Помимо этого, ретроградная волна крови рассеивается об ободок крепления, что приводит к снижению ее кинетической энергии.
С помощью при жизни проведенной фиброфлебоскопии можно представить себе, как работает венозный клапан. После попадания ретроградной волны крови в синусы клапана, его створки приходят в движение и смыкаются. Узелки передают сигнал о том, что они соприкоснулись, мышечному сфинктеру. Сфинктер начинает расширятся до тех пор, пока не достигнет того диаметра, при котором створки клапана вновь раскроются и надежно перекроют ретроградной волны крови путь. Когда в синусе давление становится выше порогового уровня, то происходит раскрытие устья дренирующих вен, что приводит к снижению венозной гипертензии до безопасного уровня.
Анатомическое строение венозного бассейна нижних конечностей
Вены нижних конечностей делятся не поверхностные и глубокие.
К поверхностным венам относятся кожные вены стопы, расположенные на подошвенной и тыльной поверхности, большие, малые подкожные вены и их многочисленные притоки.
Подкожными венами в области стопы формируются две сети: кожная венозная подошвенная сеть и кожная венозная сеть тыла стопы. Общими тыльными пальцевыми венами, которые входят в кожную венозную сеть тыла стопы, в результате того, что они анастомозируют между собой, образуется кожная тыльная дуга стопы. Концы дуги имеют продолжение в проксимальном направлении и образуют два ствола, идущих в продольном направлении – медиальную краевую вену (v. marginalis medialis) и краевую латеральную вену (v. marginalis lateralis). На голени эти вены имеют продолжение в виде большой и малой подкожной вены соотвественно. На подошвенной поверхности стопы выделяется подкожная венозная подошвенная дуга, которая широко анастомозируя с краевыми венами, отправляет межголовчатые вены в каждый из межпальцевых промежутков. Межголовчатые вены, в свою очередь, анастомозируют с теми венами, которые образуют тыльную дугу.
Продолжением медиальной краевой вены (v. marginalis medialis) является большая подкожная вена нижней конечности (v. saphena magna), которая по переднему краю внутренней стороны лодыжки переходит на голень, а затем, проходя по медиальному краю большеберцовой кости, огибает медиальный мыщелок, выходит на внутреннюю поверхность бедра с задней стороны коленного сустава. В области голени БПВ находится около подкожного нерва, с помощью которого происходит иннервация кожного покрова на стопе и голени. Эта особенность анатомического строения должна учитываться при флебэктомии, так как из-за повреждения подкожного нерва могут появиться долговременные, а иногда и пожизненные нарушения иннервации кожного покрова в области голени, а также привести к парестезиям и каузалгиям.
В области бедра большая подкожная вена может иметь от одного до трех стволов. В области имеющей овальную форму ямки (hiatus saphenus) находится устье БПВ (сафенофеморальный анастомоз). В этом месте ее терминальный отдел делает перегиб через сероповидный отросток широкой фасции бедра и, в результате прободения решётчатой пластинки (lamina cribrosa), впадает в бедренную вену. Местоположение сафенофеморального анастомоза может располагаться на 2-6 м ниже того места, где находится пупартовая связка.
К большой подкожной вене по всей ее длине присоединяется много притоков, которые несут кровь не только с области нижних конечностей, из наружных половых органов, с области передней брюшной стенки, а также с кожи и подкожной клетчатки, находящихся в ягодичной области. В нормальном состоянии большая подкожная вена имеет ширину просвета 0,3 – 0,5 см и имеет от пяти до десяти пар клапанов.
Постоянные венозные стволы, которые впадают в терминальный отдел большой подкожной вены:
Малая подкожная вена, проходя по месту соединения средней и верхней третей голени, проникает в зону глубокой фасции, располагаясь между ее листками. Доходя до подколенной ямки, МПВ проходит сквозь глубокий листок фасции и чаще всего соединяется с подколенной веной. Однако в некоторых случаях малая подкожная вена проходит над подколенной ямкой и соединяется либо с бедренной веной, либо с притоками глубокой вены бедра. В редких случаях МПВ впадает в один из притоков большой подкожной вены. В зоне верхней трети голени между малой подкожной веной и системой большой подкожной вены образуется множество анастомозов.
Самым крупным постоянным приустьевым притоком малой подкожной вены, имеющим эпифасциальное расположение, является бедренно-подколенная вена (v. Femoropoplitea), или вена Джиакомини. Эта вена связывает МПВ большой подкожной веной, расположенной на бедре. Если по вене Джиакомини из бассейна БПВ возникает рефлюкс, то из-за этого может начаться варикозное расширение малой подкожной вены. Однако может сработать и обратный механизм. Если возникает клапанная недостаточность МПВ, то варикозную трансформацию можно наблюдать на бедренно-подколенной вене. Кроме того, в данный процесс будет вовлечена и большая подкожная вена. Это нужно учитывать во время хирургического вмешательства, так как в случае сохранения бедренно-подколенная вена может быть причиной возврата варикоза у пациента.
Глубокая венозная система
К глубоким венам относятся вены, расположенные с тыльной стороны стопы и подошвы, на голени, а также в зоне колена и бедра.
На голени венозная система состоит из трех пар глубоких вен – передней и задней большеберцовой веной и малоберцовой веной. Основная нагрузка по оттоку крови с периферии возложена на задние большеберцовые вены, в которые, в свою очередь, дренируются малоберцовые вены.
Система суральных вен состоит из парных икроножных мышц (vv. Gastrocnemius), дренирующих в подколенную вену синус икроножной мышцы, и непарной камбаловидной мышцы (v. Soleus), отвечающей за дренаж в подколенную вену синуса камбаловидной мышцы.
На уровне суставной щели в подколенную вену общим устьем или раздельно, выходя из головок икроножной мышцы (m. Gastrocnemius), впадает медиальная и латеральная икроножная вена.
Рядом с камбаловидной мышцей (v. Soleus) постоянно проходит одноименная артерия, которая в свою очередь является ветвью подколенной артерией (а. poplitea). Камбаловидная вена самостоятельно впадает в подколенную вену или же проксимальнее того места, где находится устье икроножных вен, или же впадает в него.
Бедренная вена (v. femoralis) большинством специалистов подразделяется на две части: поверхностная бедренная вена (v. femoralis superfacialis) расположена дальше от места впадения глубокой вены бедра, общая бедренная вена (v. femoralis communis) расположена ближе к тому месту, где в нее впадает глубокая вена бедра. Данное подразделение важно как в анатомическом отношении, так и в функциональном.
Кроме большое подкожной вены, в общую бедренную вену также впадает медиальная латеральная вены, которые идут вокруг бедра. Медиальная вена находится проксимальнее, чем латеральная. Место ее впадения может располагаться либо на одном уровне с устьем большой подкожной вены, либо немного выше его.
Перфорантные вены

Прямые и непрямые перфорантные вены
Прямые перфорантные вены – это сосуды, с помощью которых глубокая и поверхнастная вены соединяются между собой. В качестве самого типичного примера прямой перфорантной вены можно привести сафеноподколенное соустье. Количество прямых перфорантных вен в организме человека не так много. Они являются более крупными и в большинстве случаев располагаются в дистальных областях конечностей. Например, на голени в сухожильной части расположены перфорантные вены Коккета.
Основной задачей непрямых перфорантных вен является соединение подкожной вены с мышечной, которая имеет прямое или опосредованное сообщение с глубокой веной. Количество непрямых перфорантных вен достаточно большое. Это чаще всего очень мелкие вены, которые в большей части находятся там, где расположены мышечные массивы.
Анатомия
Значительная вариабельность строения поверхностной венозной сети нижних конечностей усугубляется разночтением в названиях вен и присутствием большого количества фамилий, особенно в наименованиях перфорантных вен. Для устранения таких разночтений и создания унифицированной терминологии вен нижних конечностей в 2001 году в Риме был создан Международный междисциплинарный консенсус по венозной анатомической номенклатуре. Согласно ему все вены нижних конечностей условно подразделяются на три системы:
1.Поверхностные вены
2.Глубокие вены
3.Перфорантные вены.
Поверхностные вены обеспечивают отток примерно 10% крови от нижних конечностей. Глубокие вены расположены в пространствах, располагаемых глубже этой мышечной фасции. Кроме этого, глубокие вены всегда сопровождают одноименные артерии, чего не бывает с поверхностными венами. Глубокие вены обеспечивают основной дренаж крови– 90% всей крови от нижних конечностей оттекает по ним. Перфорантные вены прободают глубокую фасцию, соединяя при этом поверхностные и глубокие вены.
| i — тип расположения БПВ на бедре | h — тип расположения БПВ на бедре | s — тип расположения БПВ на бедре | ||||||||
|
|
2. Наиболее постоянные притоки БПВ: 2.2 Задняя окружающая бедро вена (vena circumflexa femoris posterior), в англоязычной литературе — posterior thigh circumflex vein. Может иметь своим истоком МПВ, а также латеральную венозную систему. Поднимается из задней части бедра, обвивая его, и дренируется в БПВ. 2.3 Передняя окружающая бедро вена (vena circumflexa femoris anterior), в англоязычной литературе — anterior thigh circumflex vein. Может иметь своим истоком латеральную венозную систему. Поднимается по передней поверхности бедра, обвивая его, и дренируется в БПВ. 2.4 Задняя добавочная большая подкожная вена (vena saphena magna accessoria posterior), в англоязычной литературе — posterior accessory great saphenous vein (сегмент этой вены на голени называется задняя арочная вена или вена Леонардо). Так называется любой венозный сегмент на бедре и голени идущий параллельно и кзади от БПВ. 2.5 Передняя добавочная большая подкожная вена (vena saphena magna accessoria anterior), в англоязычной литературе — anterior accessory great saphenous vein. Так называется любой венозный сегмент на бедре и голени идущий параллельно и кпереди от БПВ. 2.6 Поверхностная добавочная большая подкожная вена (vena saphena magna accessoria superficialis), в англоязычной литературе — superficial accessory great saphenous vein. Так называется любой венозный сегмент на бедре и голени идущий параллельно от БПВ и поверхностнее относительно её фасциального футляра. 2.7 Паховое венозное сплетение (confluens venosus subinguinalis), в англоязычной литературе — confluence of superficial inguinal veins. Представляет собой терминальный отдел БПВ возле соустья с БВ. Сюда кроме перечисленных последних трех притоков, впадают три достаточно постоянных притока: 3. Малая подкожная вена
Поднимается по задней поверхности голени и впадает в подколенную вену чаще всего на уровне подколенной складки. Принимает следующие притоки: 3.1 Поверхностная добавочная малая подкожная вена (vena saphena parva accessoria superficialis), в англоязычной литературе — superficial accessory small saphenous vein. Идёт параллельно со стволом МПВ над поверхностным листком её фасциального футляра. Часто самостоятельно впадает в подколенную вену. 3.2 Краниальное продолжение малой подкожной вены (extensio cranialis venae saphenae parvae), в англоязычной литературе cranial extension of the small saphenous vein. Ранее называлась бедренно-подколенной веной (v. femoropoplitea). Является рудиментом эмбрионального межвенозного анастомоза. Когда имеется анастомоз между этой веной и задней окружающей бедро веной из системы БПВ, она носит название вена Джиакомини. 4. Латеральная венозная система Несомненно, что имеют собственные имена и перечислены только основные клинически значимые венозные коллекторы. Учитывая высокое разнообразие строения поверхностной венозной сети, прочие не вошедшие сюда поверхностные вены следует называть по их анатомической локализации.
1. Перфорантные вены стопы 1.1 дорсальные перфорантные вены стопы 1.2 медиальные перфорантные вены стопы 1.3 латеральные перфорантные вены стопы 1.4 плантарные перфорантные вены стопы 2. Перфорантные вены лодыжки 2.1 медиальные перфорантные вены лодыжки 2.2 передние перфорантные вены лодыжки 2.3 латеральные перфорантные вены лодыжки 3. Перфорантные вены голени 3.1 медиальные перфорантные вены голени 3.1.1 паратибиальные перфорантные вены 3.1.2 заднебольшеберцовые перфорантные вены 3.2 передние перфорантные вены голени 3.3 латеральные перфорантные вены голени 3.4 задние перфорантные вены голени 3.4.1 медиальные икроножные перфорантные вены 3.4.2 латеральные икроножные перфорантные вены 3.4.3 межглавые перфорантные вены 3.4.4 параахиллярные перфорантные вены 4. Перфорантные вены области коленного сустава 4.1 медиальные перфорантные вены области коленного сустава 4.2 наднадколенниковые перфорантные вены 4.3 перфорантные вены латеральной поверхности коленного сустава 4.4 поднадколенниковые перфорантные вены 4.5 перфорантные вены подколенной ямки 5. Перфорантные вены бедра
5.1 Медиальные перфорантные вены бедра 5.1.1 Перфорантные вены приводящего канала 5.1.2 Перфорантные вены паховой области 5.2 Перфорантные вены передней поверхности бедра 5.3 Перфорантные вены латеральной поверхности бедра 5.4 Перфорантные вены задней поверхности бедра 5.4.1 Перфорантные вены заднее-медиальной поверхности бедра 5.4.2 Седалищные перфорантные вены 5.4.3 Перфорантные вены заднее-латеральной поверхности бедра 5.5 Срамные перфорантные вены 6. Перфорантные вены ягодиц Хирургические методы лечения основных форм хронических заболеваний вен нижних конечностейХирургическое лечение варикозной болезни Основным методом лечения варикозной болезни (ВБ) остается хирургическое вмешательство. Целью операции является устранение симптомов заболевания (в том числе и косметического дефекта), предотвращение прогрессирования варикозной трансформации подкожных вен. На сегодняшний день ни один из существующих хирургических методов сам по себе не отвечает всем патогенетическим принципам лечения, в результате становится очевидной необходимость их сочетания. Различные комбинации тех или иных операций в первую очередь зависят от выраженности патологических изменений в венозной системе нижних конечностей. Показанием к операции служит наличие рефлюкса крови из глубоких вен в поверхностные у больных с классами С2-С6. Комбинированная операция может включать следующие этапы: Этот объем операции выработан десятилетиями научного и практического поиска. Кроссэктомия большой подкожной вены. Оптимальным для лигирования БПВ является доступ по паховой складке. Надпаховый доступ имеет некоторые преимущества только у пациентов с рецидивом заболевания из-за оставленной патологической культи БПВ и высоким расположением послеоперационного рубца. БПВ должна быть лигирована строго пристеночно к бедренной вене, все приустьевые притоки, включая верхний (поверхностная надчревная вена) следует обязательно лигировать. Необходимости в ушивании овального окна или подкожной клетчатки после кроссэктомии БПВ нет. В связи с этим основой вмешательства в бассейне БПВ должен быть короткий стриппинг. Удаление ствола на всем протяжении допустимо только при его достоверно подтвержденной несостоятельности и значительном расширении (более 6 мм в горизонтальном положении). Выбирая способ сафенэктомии, предпочтение следует отдавать инвагинационным методикам (в том числе PIN-стриппингу) или криофлебэктомии. Хотя детальное изучение этих способов еще идет, их преимущества (меньшая травматичность) в сравнении с классической Бэбкокковской методикой несомненны. Тем не менее, способ Бэбкокка эффективен и может использоваться в клинической практике, при этом желательно применять оливы малого диаметра. Выбирая направление удаления вены, предпочтение следует отдавать тракции сверху вниз, т. е. ретроградно, за исключением криофлебэктомии, методика которой подразумевает антеградное удаление вены. Кроссэктомия малой подкожной вены. Строение терминального отдела малой подкожной вены очень вариабельно. Как правило, МПВ сливается с подколенной веной на несколько сантиметров выше линии коленного сгиба. В связи с этим доступ для кроссэктомии МПВ необходимо смещать проксимально с учетом локализации сафено-поплитеального соустья (перед операцией следует уточнить локализацию соустья с помощью ультразвукового сканирования). Удаление ствола малой подкожной вены. Как и в случае с БПВ, вену следует удалять только в тех пределах, в которых определено наличие рефлюкса. В нижней трети голени рефлюкс по МПВ встречается очень редко. Следует также использовать инвагинационные способы. Криофлебэктомия МПВ не имеет преимуществ перед этими методиками. Комментарий. Вмешательство на малой подкожной вене (кроссэктомия и удаление ствола) следует проводить в положении больного на животе. Термооблитерация магистральных подкожных вен. Современные эндовазальные методики – лазерная и радиочастотная – позволяют устранить стволовой рефлюкс и поэтому по своему функциональному эффекту могут быть названы альтернативой кроссэктомии и стриппингу. Травматичность термооблитерации значительно ниже, нежели стволовой флебэктомии, а косметический результат – существенно выше. Лазерную и радиочастотную облитерацию проводят без приустьевого лигирования (БПВ и МПВ). Одновременное выполнение кроссэктомии практически нивелирует преимущества термооблитерации, а стоимость затрат на лечение при этом вырастает. Эндовазальная лазерная и радиочастотная облитерация имеют ограничения по применению, сопровождаются специфичными осложнениями, значительно дороже, требуют обязательного интраоперационного ультразвукового контроля. Воспроизводимость методики невысока, поэтому она должна выполняться только опытными специалистами. Отдаленные результаты применения в широкой клинической практике пока неизвестны. В связи с этим методы термооблитерации требуют дальнейшего изучения и пока не могут полностью заменить традиционные хирургические вмешательства при варикозной болезни. Удаление варикозно измененных притоков. При элиминации варикозных притоков поверхностных стволов предпочтение следует отдавать их удалению с помощью инструментов для минифлебэктомии через проколы кожи. Все другие хирургические способы более травматичны и приводят к худшим косметически результатам. По согласованию с пациентом возможно оставление некоторых варикозно измененных вен, которые в последующем ликвидируют с помощью склеротерапии. Диссекция перфорантных вен. Основным дискутабельным вопросом данного подраздела является определение показаний к вмешательству, поскольку роли перфорантов в развитии ХЗВ и их осложнений требует уточнения. Противоречивость многочисленных исследований в этой области связана с отсутствием четких критериев определения несостоятельности перфорантных вен. Ряд авторов вообще ставит под сомнение тот факт, что несостоятельные перфорантные вены могут иметь самостоятельное значение в развитии ХЗВ и являться источником патологического рефлюкса из глубокой венозной системы в поверхностную. Основную роль при варикозной болезни отводят вертикальному сбросу по подкожным венам, а несостоятельность перфорантов связывают с возрастающей на них нагрузкой по дренированию рефлюксной крови из поверхностной венозной системы в глубокую. В результате они увеличиваются в диаметре и имеют двунаправленный ток крови (преимущественно в глубокие вены), что в первую очередь определяется выраженностью вертикального рефлюкса. Необходимо отметить, что двунаправленный ток крови по перфорантам наблюдается и у здоровых людей без признаков ХЗВ. Количество несостоятельных перфорантных вен находится в прямой зависимости от клинического класса по СЕАР. Эти данные отчасти подтверждаются исследованиями, в которых после вмешательств на поверхностной венозной системе и ликвидации рефлюкса значительная часть перфорантов становится состоятельной. Тем не менее, у больных с трофическими расстройствами от 25, 5% до 40% перфорантов остается несостоятельными и их дальнейшее влияние на течение заболевания не ясно. По всей видимости, при варикозной болезни классов С4-С6 после ликвидации вертикального рефлюкса возможности восстановления нормальной гемодинамики по перфорантным венам ограничены. В результате длительного воздействия на них патологического рефлюкса из подкожных и/или глубоких вен происходят необратимые изменения у определенной части из этих сосудов, и обратный ток крови по ним приобретает уже патологическое значение. Таким образом, на сегодняшний день можно говорить об обязательном тщательном лигировании несостоятельных перфорантных вен только у больных варикозной болезнью с трофическими расстройствами (классы С4-С6). При клинических классах С2-С3 решение о лигированиии перфорантов хирург должен принимать индивидуально в зависимости от клинической картины и данных инструментального обследования. При этом диссекция должна проводиться только при их достоверно подтвержденной несостоятельности. Если локализация трофических расстройств исключает возможность прямого чрескожного доступа к несостоятельной перфорантной вене, операцией выбора является эндоскопическая субфасциальная диссекция перфорантных вен (ЭСДПВ). Многочисленные исследования свидетельствуют о ее неоспоримых преимуществах по сравнению с широкой использовавшейся ранее операцией открытой субтотальной субфасциальной перевязкой перфорантов (операция Линтона). Частота раневых осложнений при ЭСДПВ составляет 6-7%, в то время как при открытом вмешательстве достигает 53%. При этом время заживления трофических язв, показатели венозной гемодинамики и частота рецидивов сопоставимы. Комментарий. Многочисленные исследования указывают, что ЭСДПВ может положительно повлиять на течение ХЗВ, особенно если речь идет о трофических расстройствах. Однако неясно, какие из наблюдаемых эффектов обусловлены диссекцией, а какие одновременно проводимым большинству пациентов хирургическим вмешательством на подкожных венах. Тем не менее, отсутствие отдаленных результатов у пациентов с С4-С6, которым не проводились вмешательства на перфорантных венах, а выполнялась только флебэктомия, пока не позволяет делать окончательные выводы относительно применения тех или иных методов хирургического лечения. Несмотря на имеющиеся противоречия, большинство исследователей все же считает необходимым сочетать традиционные вмешательства на поверхностных венах с ЭСДПВ у пациентов с трофическими расстройствами и открытыми трофическими язвами на фоне варикозной болезни. Частота рецидивов язв после комбинированной флебэктомии с ЭСДПВ составляет от 4% до 18% (сроки наблюдения 5-9 лет). При этом полное заживление происходит примерно у 90% пациентов в течение первых 10 месяцев. При использовании других малоинвазивных методик по устранению перфорантных вен, таких, как микропенная склерооблитерация, эндовазальная лазерная облитерация, также были получены хорошие результаты. Тем не менее, вероятность успеха при их применении прямо зависит от квалификации и опыта врача, поэтому пока они не могут быть рекомендованы для широкого применения. У больных с клиническими классами С2-С3 ЭСДПВ использоваться не должна, поскольку устранение перфорантного рефлюкса можно успешно провести из небольших (до 1 см) разрезов и даже из проколов кожи при помощи инструментов для минифлебэктомии. Коррекция клапанов глубоких вен. В настоящее время в данном разделе хирургической флебологии имеется больше вопросов, чем ответов. Это связано с имеющимися противоречиями, касающимися таких аспектов как значимость рефлюкса по глубоким венам и его влияние на течение ХВН, определение показаний к коррекции, оценка эффективности лечения. Несостоятельность различных сегментов глубокой венозной системы нижних конечностей приводит к разным гемодинамическим нарушениям, что важно учитывать при выборе способа лечения. Ряд исследований свидетельствует, что рефлюкс по бедренной вене не играет какой-либо существенной роли. В то же время, поражение глубоких вен голени может приводить к непоправимым изменениям в работе мышечно-венозной помпы и тяжелым формам ХВН. Оценить положительные эффекты непосредственно самой коррекции венозного рефлюкса в глубоких венах затруднительно, так как эти вмешательства в большинстве случаев выполняют в сочетании с операциями на поверхностных и перфорантных венах. Изолированное устранение рефлюкса по бедренной вене либо вообще не влияет на показатели венозной гемодинамики, либо приводит к незначительным временным изменениям лишь некоторых параметров. С другой стороны, только ликвидация рефлюкса по БПВ при варикозной болезни в сочетании с несостоятельностью бедренной вены приводит к восстановлению клапанной функции в данном венозном сегменте. Хирургические методы лечения первичного рефлюкса по глубоким венам можно разделить на две группы. Первая подразумевает проведение флеботомии и включает в себя внутреннюю вальвулопластику, транспозицию, аутотрансплантацию, создание новых клапанов и применение криоконсервированных аллотрансплантатов. Вторая группа не требует флеботомии и включает экстравазальные вмешательства, наружную вальвулопластику (трансмуральную или транскоммиссуральную), ангиоскопически ассистированную экстравазальную вальвулопластику, чрескожную установку корригирующих устройств. Вопрос о проведении коррекции клапанов глубоких вен следует поднимать только у больных с рецидивирующими или незаживающими трофическими язвами (класс С6), в первую очередь при рецидивирующих трофических язвах и рефлюксе по глубоким венам 3-4 степени (до уровня коленного сустава) по классификации Kistner. При неэффективности консервативного лечения у молодых лиц, не желающих пожизненного назначения компрессионного трикотажа, возможно проведение операции при выраженных отеках и С4b. Решение об операции должно приниматься на основании клинического статуса, но не на данных специальных исследований, поскольку симптомы могут не коррелировать с лабораторными показателями. Операции по коррекции клапанов глубоких вен должны выполняться только в специализированных центрах, имеющих опыт подобных вмешательств. Хирургическое лечение посттромботической болезни Результаты хирургического лечения больных ПТБ значительно хуже, нежели пациентов с варикозной болезнью. Так, после ЭСДПВ частота рецидивов трофических язв достигает 60% в течение первых 3 лет. Обоснованность вмешательств на перфорантных венах у данной категории пациентов не получила подтверждения во многих исследованиях. Пациенты должны быть проинформированы, что хирургическое лечение ПТБ сопряжено с высоким риском неудачных результатов. Вмешательства на подкожной венозной системе Подкожные вены при ПТБ у многих пациентов выполняют коллатеральную функцию и их удаление может привести к ухудшению течения заболевания. В связи с этим при ПТБ флебэктомия (а также лазерная или радиочастотная облитерация) не может использоваться в качестве рутинной процедуры. Решение о необходимости и возможности удаления подкожные вен в том или ином объеме должно приниматься на основании тщательного анализа клинических и анамнестических сведений, результатов инструментальных диагностических тестов (ультразвукового, радионуклидного). Коррекция клапанов глубоких вен. Посттромботическое поражение клапанного аппарата в большинстве случаев не поддается прямой хирургической коррекции. Несколько десятков вариантов операций по формированию клапанов в глубоких венах при ПТБ не вышли за рамки клинических экспериментов. Шунтирующие вмешательства. Во второй половине прошлого века при окклюзиях глубоких вен были предложены два шунтирующих вмешательства, одно из которых преследовало цель отведения крови из подколенной вены в БПВ при окклюзии бедренной (метод Уоррена-Тайра), другое – из бедренной вены в другую (здоровую) конечность при окклюзии подвздошных вен (метод Пальма-Эсперона). Клиническую эффективность продемонстрировал только второй способ. Данный вид операций является не только эффективным, но и на сегодняшний день единственным способом по созданию дополнительного пути оттока венозной крови, который может быть рекомендован к широкому клиническому применению. Аутогенные бедренно-бедренные перекрестные венозные шунты отличаются меньшей тромбогенностью и лучшей проходимостью, чем искусcтвенные. Однако имеющиеся по данному вопросу исследования включают небольшое количество пациентов с неоднозначными сроками клинического и флебографического наблюдения. Показаниями к бедренно-бедренному шунтированию служит односторонняя окклюзия подвздошных вен. Обязательным условием является отсутствие препятствий венозному оттоку в противоположной конечности. Кроме того, функциональные показания к операции возникают только при неуклонном прогрессировании ХВН (до клинических классов С4-С6), несмотря на адекватное консервативное лечение в течение нескольких (3-5) лет. Трансплантация и транспозиция вен. Трансплантация сегментов вен, содержащих клапаны, демонстрирует хорошую эффективность в ближайшие месяцы после операции. Обычно используют поверхностные вены верхней конечности, которые пересаживают в позицию бедренной вены. Ограничение возможностей метода связано с разницей диаметров вен. Вмешательство патофизиологически малообосновано: гемодинамические условия в верхней и нижней конечности существенно различаются, в связи с чем трансплантированные сегменты вен расширяются с развитием рефлюкса. Кроме того, замещение 1-2-3 клапанов при протяженном поражении глубокой венозной системы не может компенсировать нарушения венозного оттока. Методы транспозиции реканализованных вен «под защиту» клапанов интактных сосудов, из которых наиболее возможной с технической точки зрения может быть транспозиция поверхностной бедренной вены в глубокую вену бедра, не могут быть рекомендованы в широкую клиническую практику в связи с их сложностью и казуистической редкостью оптимальных условий для их выполнения. Небольшое количество наблюдений и отсутствие отдаленных результатов не позволяют делать каких-либо выводов. Эндовазальные вмешательства при стенозах и окклюзиях глубоких вен Окклюзия или стеноз глубоких вен является главной причиной возникновения симптомов ХВН примерно у трети пациентов с ПТБ. В структуре трофических язв от 1% до 6% больных имеют данную патологию. В 17% случаев окклюзия сочетается с рефлюксом. Следует отметить, что такая комбинация сопровождается самым высоким уровнем венозной гипертензии и самыми тяжелыми проявлениями ХВН по сравнению с только рефлюксом или окклюзией. Проксимальная окклюзия, особенно подвздошных вен, с большей вероятностью приведет к ХВН, чем поражение дистальных сегментов. В результате илиофеморального тромбоза, только 20-30% подвздошных вен полностью реканализируются, в остальных случаях наблюдается резидуальная окклюзия и образование более или менее выраженных коллатералей. Главной целью вмешательства является снятие ликвидация окклюзии или обеспечение дополнительных путей венозного оттока. Показания. К сожалению, нет надежных критериев «критического стеноза» в венозной системе. Это является главным препятствием при определении показаний для лечения и интерпретации его результатов. Рентгеноконтрастная флебография служит стандартным методом визуализации венозного русла, позволяя определить участки окклюзии, стеноза и наличие коллатералей. Интраваскулярная ультразвуковая сонография (ИВУС) превосходит флебографию в вопросах оценки морфологических особенностей и протяженности стеноза подвздошной вены. Окклюзия илиокавального сегмента и связанные с ней аномалии могут быть диагностированы при МРТ и спиральной КТ венографии. Опубликованные исследования по венозному стентированию часто имеют те же недостатки, что и сообщения об открытых хирургических вмешательствах (небольшое число пациентов, отсутствие отдаленных результатов, нет распределения больных на группы в зависимости от этиологии окклюзии, острой или хронической патологии и т. д. ). Методика стентирования вен появилась сравнительно недавно, в связи с этим сроки наблюдения за пациентами ограничены. Поскольку отдаленные результаты процедуры пока неизвестны, для оценки ее эффективности и безопасности необходимо продолжить мониторинг в течение еще нескольких лет. Хирургическое лечение флебодисплазий Эффективных методов радикальной коррекции гемодинамики у пациентов с флебодисплазиями не существует. Необходимость в хирургическом лечении возникает при опасности кровотечений из расширенных и истонченных подкожных вен, трофических язвах. В этих ситуациях проводят иссечение конгломератов вен с целью уменьшения локального венозного застоя. Операции по поводу ХЗВ могут выполнять в отделениях сосудистой или общей хирургии специалисты, прошедшие подготовку по флебологии. Некоторые виды вмешательств (реконструктивные: вальвулопластика, шунтирование, транспозиция, трансплантация) должны проводиться только в специализированных центрах по строгим показаниям. |