Что необходимо знать о мРНК-вакцинах: 5 позиций
В результате беспрецедентной скорости в разработке новых вакцин, миру были представлены первые клинически одобренные мРНК-вакцины
В результате беспрецедентной скорости в разработке новых вакцин, миру были представлены первые клинически одобренные мРНК-вакцины для борьбы с пандемией Covid-19 – одна из них произведена Pfizer и BioNTech, другая – компанией Moderna. Испытания показали эффективность этих вакцин на уровне не менее чем 94%.
1. Технология мРНК вакцин не так молода, как кажется
Классический механизм работы вакцин (например, против полиомиелита и гриппа) заключается в презентации иммунной системе инактивированных частиц вируса. Другие вакцины (например, против гепатита B) используют отдельно взятый белок, являющийся частью инфекционного агента, чтобы вызвать схожий иммунный ответ.
мРНК-вакцины работают по другому принципу, «обманывая» иммунную систему таким образом, что РНК (в основном матричная мРНК) кодирует белок, который продуцируется в клетке путем трансляции и представляется иммунной системе; он действует как антиген. Иммунная система учится избирательно бороться с клетками, экспрессирующими такие антигены, такими как клетки-хозяева, инфицированные вирусами, или опухолевые клетки.
Хотя вакцины от Pfizer/BioNTech и Moderna – первые препараты, одобренные в клинической практике, сама технология мРНК-вакцин существует относительно давно. Первые испытания в онкологии с использованием схожих технологий берут свое начало еще в 2011 году.
2. мРНК-вакцины не изменяют ДНК
Существуют абсолютно необоснованные опасения, что мРНК-вакцины способны изменять ДНК. На самом же деле мРНК не входит в ядро клетки, а после своего введения биодеградирует в течение нескольких дней. Именно поэтому для формирования полноценного иммунного ответа необходимо 2 инъекции препарата.
3. мРНК-вакцины имеют высокую специфичность
Вирус SARS-CoV-2 имеет достаточно сложную структуру и его различные части стимулируют иммунную систему на образование нейтрализующих антител, которые не всегда способны эффективно элиминировать инфекцию. мРНК-вакцины стимулируют иммунный ответ к спайк-белку вируса, являющегося только частью вирусной мембраны.
4. Разработчики и эксперты не «срезали углы» во время клинических испытаний
Испытания вакцин начались с доклинической фазы, проводимой на животных, а затем постепенно переходили на 1-ую, 2-ую и 3-ю фазы. Например, 3-я фаза вакцины от Pfizer/BioNTech включает более 40 000 человек, исследования эффективности и безопасности будут продлжаться следующие 2 года.
Основные проблемы, связанные с использованием вакцины, обычно возникают в первые 2 месяца. Тем не менее, не исключены редкие побочные эффекты на больших выборках в миллионы людей, поэтому за вакцинированными необходимо пристальное наблюдение, особенно с учетом инновационной природы технологии.
5. Вакцина запускает воспалительные реакции
Частично вакцина работает путем индуцирования локальных иммунных реакций, поэтому воспалительные признаки в месте инъекции и небольшой дискомфорт в первые дни – вполне нормальное явление.
Что такое ДНК и РНК человека простыми словами
Что такое ДНК и РНК человека простыми словами: Pixabay
В клетках всех живых организмов содержится структура, название которой не выговорить с первого раза. Дезоксирибонуклеиновая кислота содержит генетический код и информацию о РНК и белки. Можно ли назвать ДНК главной структурой в организме и зачем ей сопровождение в виде РНК?
Что такое ДНК человека?
Аббревиатуру ДНК используют для обозначения молекулы под названием дезоксирибонуклеиновая кислота. Она состоит из повторяющихся блоков, называемых нуклеотидами (органические соединения), поэтому на картинке выглядит как спираль с поперечными полосками.
В этих частичках содержится генетический код, который определяет характеристики человека — телосложение, рост, цвет глаз, волос. У каждого человека уникальная ДНК. Она идентична только у однояйцевых близнецов. Своя ДНК есть у животных и растений.
Какая структура ДНК человека? Молекула дезоксирибонуклеиновой кислоты состоит из четырех видов нуклеотидов:
Эти блоки склеиваются между собой по определенным правилам: аденин может связываться только с тимином, а цитозин — только с гуанином. Притяжение между нуклеотидами связывает две нити, входящие в состав ДНК. Таким образом, по одной части цепи молекулы всегда можно восстановить вторую: напротив аденина находится тимин, напротив гуанина — цитозин. Такое взаимосоответствие называется комплементарностью.
Что такое ДНК человека: Pixabay
Именно так кодируется информация обо всех признаках организма. От комбинации нуклеотидов зависит, как будет выглядеть человек. Совокупность генетического материала называется геномом человека. Хранение, реализация и передача наследственной информации — задача хромосомы (структура в клеточном ядре).
ДНК как химическое вещество было открыто Фридрихом Мишеров в 1869 году, как указано в статье Петтера Портина. Ученые научились расшифровывать генетическую информацию только в конце ХХ века. Затем ученые сумели извлечь из хромосомы ДНК, разрезать ее на части и сшить произвольным образом, используя ферменты.
Так зародилась генная инженерия, началось производство новых организмов со встроенными чужими генами — ГМО (генетически модифицированный организм). Что касается безопасности продуктов с ГМО, то мнения ученых расходятся, как объясняет Брунильда Назарио из WebMD.
Что такое РНК человека?
РНК — рибонуклеиновая кислота, одна из трех молекул, содержащихся в клеточном ядре. Она участвует в кодировании и выражении генов. Состоит она из длинной цепи, звенья которой называются нуклеотидами. Каждый нуклеотид состоит из рибозы, азотистого основания и фосфатной группы. Генетическая информация зашифрована в последовательности нуклеотидов.
Что такое РНК человека: Pixabay
РНК синтезируется в клетках всех живых организмов. Они выполняют функцию трансляции генетической информации в белки, а также дополнительные задачи — транспортировка аминокислот в рибосомы, синтез белка и другие. Поддержку стабильности генома в процессе передачи и синтеза обеспечивают РНК-связывающие белки.
Что общего у ДНК и РНК человека? Обе структуры — это большие молекулы, состоящие из нуклеотидов. В них содержится генетическая информация. Их функции взаимосвязаны. ДНК передает генетическую информацию в цитоплазму (внутреннюю среду) клетки, где при участии РНК происходит синтез белка.
Между ДНК и РНК есть несколько отличий:
ДНК и РНК — нуклеиновые кислоты, сходные по составу, но различные по функциям. Первая структура отвечает за хранение наследственной информации, вторая — за кодирование информации и передачу информации к месту синтеза белка.
Внимание! Материал носит лишь ознакомительный характер. Не следует прибегать к описанным в нем методам лечения без предварительной консультации с врачом.
Уникальная подборка новостей от нашего шеф-редактора
Микрочипы в вакцинах? Анализ крови даёт удивительные результаты
Дискуссии о вакцинах и вакцинации от COVID-19 не затухают, а, наоборот, становятся всё более горячими. Даже серьёзные медики сомневаются, что у них есть полное представление о составе тех препаратов, которыми делаются прививки. Что же там находится на самом деле?
От чего умирают люди?
Скепсис российских медиков лишь усилился после недавнего заявления академика А. Гинцбурга (Институт Гамалеи, разработчик линейки «Спутников»). Он упомянул какие-то «маркеры» в препарате «Спутник V», которые позволяют определить, кто вакцинацию проходил, а кто лишь купил справку о вакцинации. Об этих «маркерах» в официальной информации о «Спутнике V» ничего не говорится.
Масла в огонь споров и сомнений по вопросу о составе прививочных препаратов добавила конференция учёных-патологоанатомов, которая прошла 20 сентября этого года в Германии в Институте патологии в Ройтлингене (Pathologischen Institut in Reutlingen). В мероприятии, как отмечают СМИ, участвовало от 30 до 40 специалистов, в том числе из Австрии. Ключевыми фигурами были:
Скриншот страницы pathologie-konferenz.de/en/
В центре внимания участников конференции были результаты вскрытий восьми умерших после вакцинации от COVID-19, которые проводились в этом году под руководством профессора Арне Буркхардта. Результаты упомянутых вскрытий удивительным образом подтверждают выводы коллеги Арне Буркхардта профессора, доктора Питера Ширмахера (Prof. Dr. Peter Schirmacher). Последний сделал вскрытия более 40 умерших, имевших инфицирование вирусом ковида. Питер Ширмахер уверенно заявил, что около трети из них умерли не от ковида, а от вакцинации против ковида.
Эти заявления были сделаны летом, власти и подконтрольные им СМИ пытались замолчать или опровергать выводы профессора. И вот подоспела конференция патологов в Ройтлингене, которая вновь вскрыла смертельную опасность вакцинаций против ковида.
Они уже в нас
Конференция транслировалась по видеосвязи. На ней были представлены многочисленные фотографии и рисунки, наглядно дополнявшие картину, которую описывали выступавшие патологи.
Анализ тонких тканей умерших проводился с помощью специального, так называемого «темнопольного» микроскопа. Он позволил выявить содержание в тканях посторонних микрочастиц, которые по форме представляют собой явно неживые структуры достаточно правильной геометрической формы. Внешне они выглядят… как микросхемы!
Скриншот кадра видео Cause of death after COVID-19 vaccination & Undeclared components of the COVID-19 vaccines / odysee.com
Версий появления таких инородных объектов две. Либо они были введены в кровоток готовыми, либо сформировались в организме человека из наночастиц, содержащихся в вакцине. Случайное попадание посторонних частиц в тело человека исключается, поскольку одни и те же инородные объекты выявлены у всех умерших после вакцинации.
Упомянутый выше профессор, доктор Вернер Берггольц как специалист по микрочипам высказал своё мнение по поводу «открытия» патологов. Он не исключает возможности использования выявленных в тканях умерших частиц в качестве тех самых «маркеров» и «идентификаторов», о присутствии которых в вакцинах высказывали подозрения сторонники так называемой «теории заговора».
Pfizer с дополнениями
Это размышление профессора вполне корреспондирует с мнением тех специалистов, которые пытались и пытаются выявить «маркеры» вакцин без вскрытия, путём углублённого химического и физического изучения самих препаратов. Есть ряд исследований, в которых говорится об обнаружении в составе по крайней мере двух препаратов – Pfizer и Moderna (мРНК-вакцины) – графена (также оксид графена), который никакой медицинской роли не выполняет, но вполне годится на роль «маркера», «идентификатора». Масла в огонь добавило заявление Карен Кингстон (Karen Kingston), бывшей сотрудницы компании Pfizer. Кингстон утверждает, что хотя и в патентах на вакцину Pfizer оксид графена не упоминается, он фигурирует в ряде сопроводительных документов.
Скриншот кадра видео Stew Peters show «Former Pfizer Employee Confirms Poison in COVID ‘Vaccine’»/ redvoicemedia.com
Ещё одно направление изучения «пытливыми скептиками» необъявленных производителями вакцин компонентов и свойств препаратов – попытки идентифицировать получивших вакцины людей с помощью специальных технических средств. Та яростная энергия, с которой «Силиконовая мафия» (ведущие IT-корпорации, контролирующие интернет и социальные сети) удаляет публикации подобного рода, также наводят на мысль, что нет дыма без огня.
Трудно поверить, что сказанное на конференции в Ройтлингене по поводу инородных частиц в прививочных препаратах – лишь «дым», который быстро рассеется. Дыма без огня не бывает. Просто этот огонь тщательно скрывают. До того момента, когда начнется вселенский пожар, который уже не остановишь.
Участники конференции приняли резолюцию с призывом к властям Германии, Австрии и других стран начать проводить массовые патологоанатомические исследования умерших после вакцинаций от ковида, обращаться с соответствующими запросами к производителям препаратов и, конечно же, немедленно остановить дальнейший процесс прививок от COVID-19 до полного прояснения вопроса.
Казалось бы, при чём тут Гейтс?
Идея вживления микрочипа в тело человека через прививочный укол вынашивалась мировой элитой давно. В «Prevent Disease.Com» (электронном издании США, специализирующемся на разоблачении планов американской и международной «медицинской мафии») ещё в 2009 году появилась статья «Are Populations Being Primed For Nano-Microchips Inside Vaccines?». Название статьи на русском: «Подталкивается ли население к принятию наночипов, упрятанных в вакцины?». Как отмечалось в указанной статье, ещё в последние годы ХХ века удалось разработать микрочипы нового поколения, основанные на использовании нанотехнологий. Сверхкомпактные (не больше пылинки, радиус порядка 5 микромиллиметра, что примерно в 10 раз меньше радиуса волоса) и недорогие. Вот что, в частности, говорилось в указанной выше статье: «Запущенный Всемирной организацией здравоохранения сценарий с пандемией свиного гриппа как нельзя лучше подходит для пропаганды и принуждения населения добровольно согласиться на введение микрочипов через нановакцины. Всё это будет сделано под лозунгом «высшего блага» для человечества».
Пять лет тому назад была запущена частно-государственная инициатива под кодовым названием «ID2020». Её инициатором был Билл Гейтс, основатель и руководитель IT-корпорации Microsoft, одновременно основатель и руководитель крупнейшего в США благотворительного фонда. Инициатива была поддержана ООН. Суть её проста – провести глобальную цифровую идентификацию населения для того, чтобы мировая элита могла его держать под своим контролем. В первых выступлениях Билла Гейтса как главного энтузиаста тотальной цифровой идентификации он не скрывал, что идентификация через чипизацию является самым простым и надёжным способом решения поставленной задачи.
Но встретив непонимание и даже гневные протесты со стороны ряда политиков и общественных деятелей, Гейтс больше эту идею не озвучивал. И, как считают некоторые эксперты, продолжал её двигать, давая деньги на разработки наночипов, которые станут «бесплатной добавкой» к прививочным препаратам. Решением задачи «наночип и вакцина в одном флаконе» занимались совместно, в тесной кооперации две структуры, находящиеся под контролем Билла Гейтса: упомянутое выше частно-государственное партнёрство «ID2020» и Альянс по вакцинациям GAVI (также частно-государственное партнёрство). Уже в 2018 году все упоминания о наночипах в составе вакцин были удалены с сайтов «ID2020» и GAVI.
Что с того?
Хотя с конференции в Ройтлингене прошло почти два месяца, вы наверняка ничего про неё не слышали – и это яркий пример контроля, установленного «Силиконовой мафией» над каналами распространения информации.
Видео и другие материалы конференции блокируют всеми возможными способами, а там, где нельзя заблокировать, выступают с плакатными «разоблачениями» прозвучавших там «фейков».
Чего только не сделаешь ради воспитания в людях доверия к «спасительным» вакцинам!
Подавление экспрессии мутантного гена TTR, вызывающего семейную амилоидную полинейропатию: РНК-индуцируемый комплекс выключения гена (RISC) совместно с интерферирующей РНК (siRNA) бесстрашно летит навстречу злобной патогенной мРНК-мишени, предвкушая расправу.
иллюстрация авторов статьи
Авторы
Редакторы
Статья на конкурс «био/мол/текст»: Патисиран — первый препарат на основе РНК-интерференции, одобренный FDA, — не только спасает жизни людей, страдающих амилоидной полинейропатией. Он начинает писать новую страницу в терапии, о которой мечтали с момента открытия этого механизма подавления экспрессии генов, то есть уже более 20 лет. С какими сложностями сталкивались ученые и как их преодолели? Об этом вы можете узнать в нашей статье.
Конкурс «био/мол/текст»-2018
Эта работа опубликована в номинации «Биофармацевтика» конкурса «био/мол/текст»-2018.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
Амилоиды в первую очередь ассоциируются с болезнью Альцгеймера. Однако амилоидозы — это целая группа заболеваний, связанная с неправильным сворачиванием белка, приводящим к накоплению в тканях нерастворимых фибрилл. Подробнее об этом написано в статье «На руинах памяти: настоящее и будущее болезни Альцгеймера» [1].
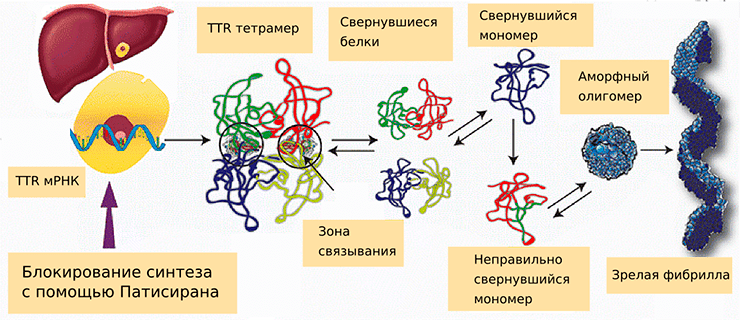
Семейная амилоидная полинейропатия (FAP), или наследственный транстиретиновый амилоидоз (hATTR), связана с различными точечными мутациями в гене, кодирующем транстиретин (TTR). В норме он вырабатывается гепатоцитами и осуществляет транспорт витамина А вместе с тиреоидными гормонами к периферическим тканям. Определенные мутации способствуют тому, что мономеры этого белка неправильно сворачиваются и образуют аморфные олигомеры, которые сливаются в фибриллы (рис. 1). По некоторым данным, именно небольшие олигомеры обладают наибольшей токсичностью в клетках [2].
Рисунок 1. Синтез мутантного варианта транстиретина и влияние на этот процесс патисирана. Без лечения мРНК TTR транслируется в белок, который в норме состоит из четырех субъединиц. Мутантные мономеры белка сворачиваются неправильным образом и образуют аморфные олигомеры, кластеры нефиксированного размера, сливающиеся в фибриллы. Образование фибрилл может привести к развитию нейродегенеративных заболеваний и проблемам с сердечно-сосудистой системой.
Рисунок 2. Связь генотипа с клиническими проявлениями при транстиретиновом амилоидозе (hATTR). До появления патисирана спасением для таких пациентов являлась трансплантация печени. В Европе также используют препарат тафамидис, который стабилизирует транстиретин. Он связывается с тетрамером и не дает ему диссоциировать на мономеры. Однако в США он так и не смог получить одобрение [5].
Человечество стремится познать природу, которая порой нашептывает удивительные решения многих наших задач. Приоткрывая завесу тайны жизни организмов, мы видим изумительные механизмы, созданные эволюцией. Так, например, система CRISPR/Cas, обеспечивающая адаптивный иммунитет прокариот, уже не один год вдохновляет ученых на создание генной терапии с ее помощью. О системе можно почитать в статьях «Просто о сложном: CRISPR/ Cas» [6] и «Когда ослепшие прозреют?» [7].
А вот один из молекулярных механизмов эукариот уже подарил нам первое лекарство и надежду на лечение огромного спектра заболеваний. Попробуем разобраться в тернистом двадцатилетнем пути с момента открытия РНК-интерференции до первого официально одобренного FDA (Food and Drug Administration, Управление США по контролю за лекарствами и пищевыми продуктами) препарата.
Итак, как же эукариоты «выключают» гены и зачем?
Воздействовать на белок мы можем принципиально тремя способами. Можно придумать молекулу, которая будет связываться с уже синтезированным белком, препятствуя его работе, или, напротив, побуждая его к действию. Так работает большинство лекарств, например, известный анальгетик и жаропонижающее средство ибупрофен ингибирует фермент циклооксигеназу (ЦОГ), уменьшая выработку простагландинов — веществ, ответственных за воспаление [20].
Но ученые мечтают о новых возможностях: о выключении таргетного гена, вызывающего генетическое заболевание, на уровне ДНК (нокаут) и о выключении без затрагивания самой последовательности ДНК на уровне РНК (нокдаун).
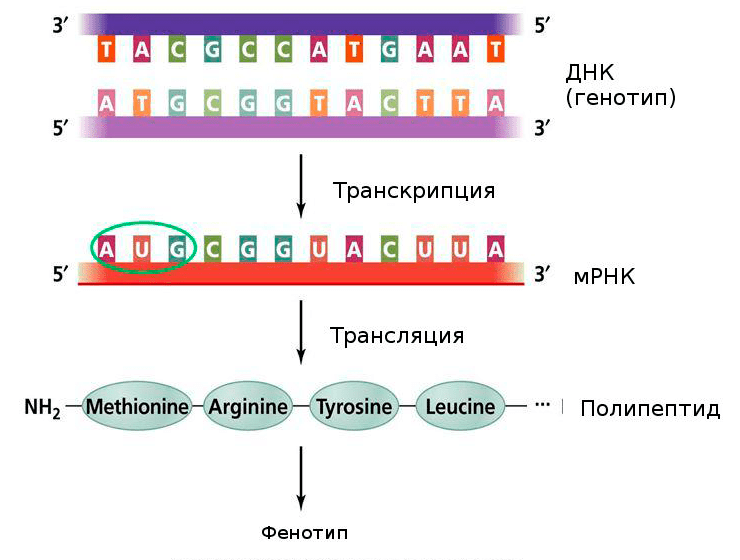
Рисунок 3. Центральная догма молекулярной биологии. Генетическая информация, закодированная в ДНК, переходит в мРНК, и уже с нее синтезируется полипептидная последовательность. Нуклеотиды одной цепочки нуклеиновой кислоты могут быть соединены с нуклеотидами другой по правилу комплементарности. В процессе транскрипции синтезируется смысловая цепь мРНК, и, зная ее последовательность, мы можем синтезировать комплементарную ей цепочку, или антисмысловую цепь.
Pearson Education, Inc., publishing as Benjamin Cummings
В своей работе 1996 года Эндрю Файр (Andrew Fire) и Крейг Мело (Craig Mello) на модельном объекте Caenorhabditis elegans (нематоде) показали, что при внесении двухцепочечной РНК можно полностью «выключить» ген. Как оказалось, происходит это от того, что антисмысловая цепь РНК, комплементарная гену-мишени, вместо ожидаемого повышения экспрессии гена (ведь мы вносим матрицу для трансляции белка) блокирует его синтез. Немногим позже, в 2006 году, за первое применение РНК-интерференции (RNAi) ученые получили Нобелевскую премию [8].
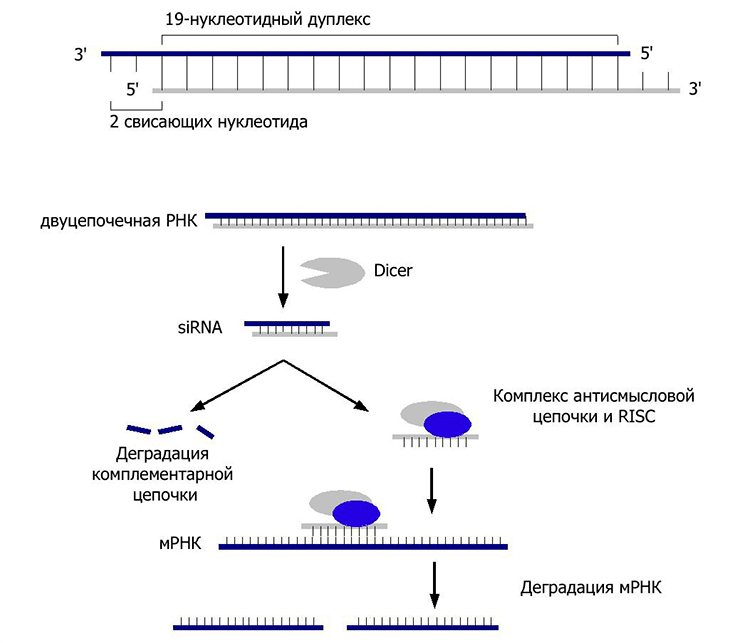
Процесс начинается с того, что поступившая в клетку экзогенная двухцепочечная РНК связывается с рибонуклеазой Dicer (да-да, как та самая овощерезка), которая нарезает ее на небольшие фрагменты длиной 20–25 пар нуклеотидов, с двумя неспаренными основаниями на каждом конце. Такая длина, видимо, оказалась оптимальной для специфического связывания с мишенью. Эти фрагменты взаимодействуют с белковым комплексом RISC, который отщепляет одну из цепей РНК, оставляя вторую на съедение нуклеазам (ферментам, расщепляющим нуклеиновые кислоты), и путешествует с ней по клетке в поисках таргетной мРНК. Обнаружив ее, белок Аргонавт из комплекса RISC разрезает свою мишень (рис. 1 и 4).
Рисунок 4. РНК-интерференция. Сверху представлена схема строения малой интерферирующей РНК (siRNA). Экзогенная двухцепочечная РНК разрезается ферментом Dicer и встраивается, расплетаясь, в белковый комплекс RISC. Готовый к работе, совместно с siRNA, он путешествует по клетке. При встрече с комплементарной мРНК комплекс индуцирует ее деградацию. Таким образом, клетка уничтожает потенциально вирусную РНК, препятствуя синтезу вирусных белков, а также борется с транспозонами.
Этот механизм выполняет защитную функцию против вирусов, которые стремятся заполучить контроль над клеткой, предоставляя ее белковой машинерии инструкции по производству вирусных агентов. Также интерферирующие РНК могут быть полезны клетке в борьбе с мобильными генетическими элементами, которые активируются при делении клетки и нарушают нормальную работу ее генетического аппарата.
Также стоит отметить, что РНК-интерференция является не единственным механизмом регуляции экспрессии генов. Для трансляции необходимо, чтобы мРНК была одноцепочечной, поэтому при попадании одноцепочечной антисмысловой РНК в клетку блокируется процесс синтеза белка, а также активируется РНКаза H, разрушающая транскрипт.
В каких случаях мы можем использовать этот изящный механизм?
Нокаут генов активно применяется в лабораторной практике, в биоинженерии и биотехнологии. Геном можно редактировать с помощью рестриктаз с последующим сшиванием лигазами, воздействовать ретровирусами, несущими правильную копию поврежденного гена, а также использовать уже упоминавшийся метод геномного редактирования с помощью CRISPR-Cas9 — системы белков и РНК. Смотрите подробнее в статьях «12 методов в картинках: генная инженерия. Часть II: инструменты и техники» [11] и «Человек генномодифицированный / Homo genere mutatio» [12].
Проблема с применением большинства таких методов для лечения человека заключается в низкой селективности редактирования, что может вносить дополнительные мутации в геном. Клетки могут перерождаться в раковые, уходить в апоптоз. Данные побочные действия затрудняют применение описанных подходов для лечения генетических заболеваний человека.
Всего этого можно избежать, выключая гены с помощью РНК-интерференции. Очень перспективна разработка антивирусных лекарств, препятствующих связыванию вирусных белков с таргетной клеткой, а также противоопухолевых препаратов.
Так что же останавливало ученых в реализации этой простой идеи?
Все, кто работал в лаборатории с РНК, знают ее коварство: она быстро деградирует под действием РНКаз, находящихся на поверхности кожи, в слюне, и в большом количестве в кровяном русле. Получается, что препарат просто не успевает добраться до нужных клеток, гены которых необходимо выключить с помощью RNAi.
После долгих и дорогостоящих попыток фармкомпании практически потеряли надежду на терапевтическое применение этого механизма. Однако решение было найдено [13]. Сегодня у одной только компании Alnylam известно семь препаратов на основе РНК-интерференции, находящихся на разных стадиях клинических испытаний (табл. 1).
Мишенями таких лекарств являются не только заболевания, связанные с образованием амилоидных бляшек, но и широкий спектр системных дисфункций. Примеры лекарств, разрабатываемых для лечения таких заболеваний, можно найти в статье «Есть ли смысл в антисенсах?» [10].
| Лекарство | Заболевание | Стадия клинических испытаний |
|---|---|---|
| Patisiran | Наследственный АТТР амилоидоз | Одобрен |
| Givosiran | Острые печеночные порфирии | Поздняя стадия (фаза 2–3) |
| Fitusiran | Гемофилия и редкие кровотечения | Поздняя стадия (фаза 2–3) |
| Inclisiran | Гиперхолестеринемия | Поздняя стадия (фаза 2–3) |
| ALNTTRsc02 | АТТR амилоидоз | Ранняя стадия (фаза 1–2) |
| Lumasiran | Первичная гипероксалурия типа 1 | Ранняя стадия (фаза 1–2) |
| Cemdisiran | Болезни, связанные с системой комплемента | Ранняя стадия (фаза 1–2) |
| * Интересно, что некоторые препараты несут в себе название siRNA, например, Givosiran, Inclisiran; а некоторые препараты, являющиеся антисмысловыми цепочками РНК — Alicaforsen, Inotersen. | ||
Патисиран — первый олигонуклеотидный препарат на основе РНК-интерференции
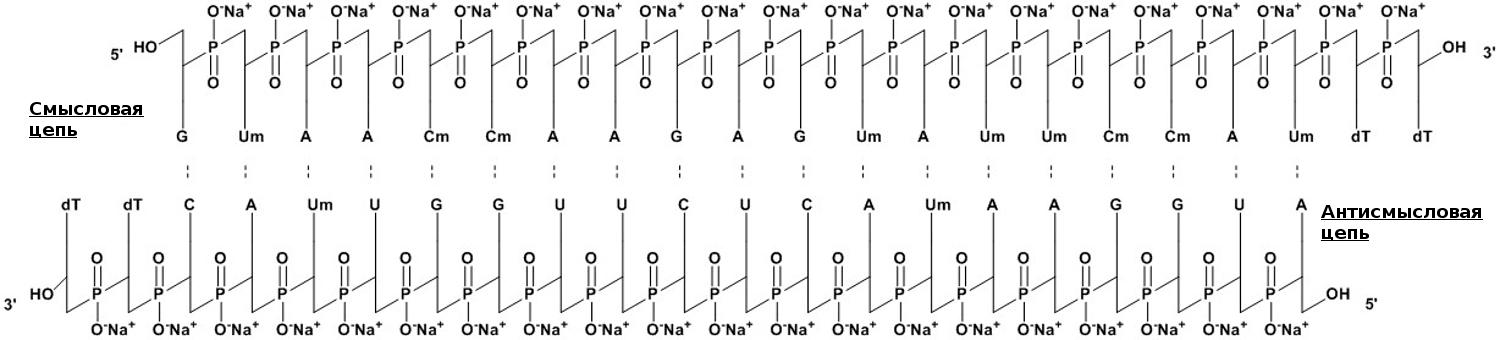
Лекарственная форма патисирана (коммерческое название — Onpattro, «Онпаттро») состоит из РНК, завернутой в липидные наночастицы (LNPs). При создании действующего вещества разработчики использовали короткие, по 21 паре нуклеотидов, двухцепочечные РНК, которые предварительно модифицировали метильной группой, присоединяемой к атомам кислорода (О-метилировали) [15], и защищали с 3′ конца для увеличения стабильности молекулы (рис. 5).
Как вообще можно увеличить стабильность РНК?
Этого можно добиться разными способами. Например, на практике используют комбинации метилирования, блокирования конца или «слабых» мест молекулы с помощью специальных белков и реагентов, а также формирование вокруг лекарственной молекулы защитной оболочки.
Рисунок 5. Нуклеотидная составляющая патисирана представляет собой короткую 21-буквенную двуцепочечную РНК из смысловой и антисмысловой цепей, которая комплементарна таргетному гену транстиретина (TTR). Для бóльшей устойчивости, некоторые из нуклеотидов О-метилированы (Um, Cm), а на 3′ концах пришиты два тимидина (dT). Молекулярная формула лекарства — C412H480N148Na40O290P40. Молекулярный вес составляет 14 304 Да.
Впервые система доставки малых двухцепочных РНК была предложена в 2010 году и после развивалась вплоть до первого успешного клинического испытания в 2016, которое показало возможность применения РНК-интерференции для лечения генетических заболеваний человека [13].
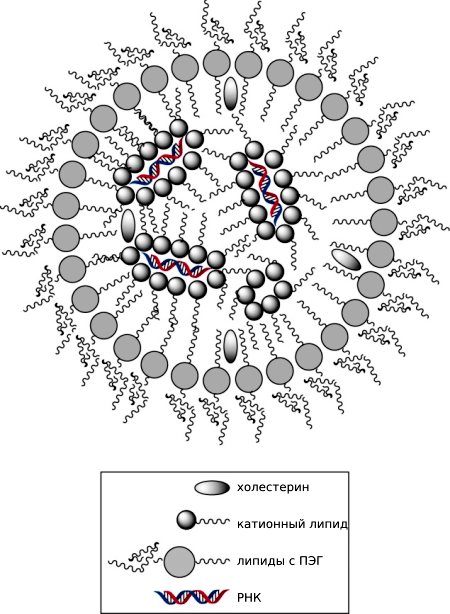
Липидные наночастицы, защищающие РНК, состоят из внешнего слоя, образованного липидами с полиэтиленгликолем и холестерином, и внутренней полости, заполненной буфером, в которой находятся окруженные катионными частицами интерферирующие агенты (рис. 6).
Рисунок 6. Строение липидных наночастиц. Для создания липидных наночастиц эмпирически был разработан специальный протокол, сочетающий различные буферы и типы липидов: смешиваются ионизированные катионные липиды с siRNA в буфере с низкой ионной силой, за счет чего РНК сближаются с липидами и собираются в наночастицы (разноименные заряды катионных липидов и РНК притягиваются). Далее собранные структуры покрываются вспомогательными липидами, холестерином и липидами с полиэтиленгликолем (ПЭГ).
Таким образом, препарат таргетно доставляется в гепатоциты — клетки, продуцирующие амилоидный транстиретин.
Клинические испытания
Любое лекарство проходит через несколько так называемых фаз клинических испытаний перед тем, как будет допущено к продаже и широкому клиническому применению. Узнать больше можно из статей спецпроекта «Клинические испытания».
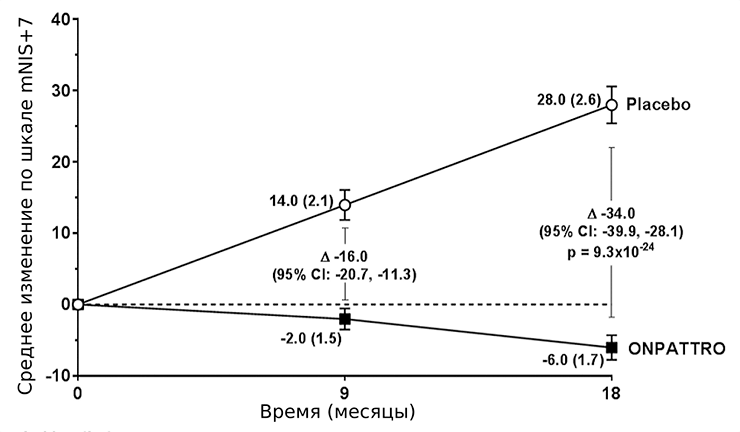
Для патисирана все клинические испытания прошли успешно. В последней, третьей фазе участвовало 225 пациентов с наследственным транстиретиновым амилоидозом (hATTR), из которых 77 получали плацебо. Ключевым показателем оценки состояния пациентов являлась модифицированная шкала ухудшения нейропатии (mNIS+7). Также использовали тест на ходьбу на расстояние 10 м, оценку индекса массы тела и опрос о качестве жизни. Наблюдение продолжалось в течение 18 месяцев. mNIS+7 ранжируется от 0 до 304 баллов: чем больше, тем хуже состояние пациента (рис. 7). По всем показателям выявили значимое улучшение состояния пациентов по сравнению с группой, принимавшей плацебо [16].
Рисунок 7. Динамика изменений средних значений модифицированной шкалы ухудшения нейропатии (mNIS+7). Разница между группами составляет 34,0 пунктов при p
Во время клинических испытаний возникли побочные эффекты: у 10% пациентов, принимавших лекарство, и 3%, принимавших плацебо, выявили инфекции верхних дыхательных путей. У всех пациентов наблюдали падение концентрации витамина А в крови (вспомним функции транстиретина).
FDA одобрило лекарство для всех стадий заболевания 10 августа 2018 года — так, патисиран стал не только первым одобренным препаратом для лечения наследственного транстиретинового амилоидоза, но и первым одобренным средством, в механизме работы которого лежит РНК-интерференция [17].
Комитет по лекарственным средствам для человека (CHMP), входящий в Европейское агентство лекарственных средств (EMA), рекомендовал предоставить разрешение на применение патисирана для лечения наследственного транстиретин-опосредованного амилоидоза у взрослых пациентов с полинейропатией 1 или 2 стадий. Значимого улучшения состояния пациентов с 3 стадией заболевания, по результатам клинических тестов и судя по комментариям представителя компании, достичь не удалось.
Лекарство будет доступно в виде раствора для внутривенного введения с концентрацией активного компонента 2 мг/мл. Примечательна периодичность инъекций: один раз в три недели.
Компания Alnylam предоставляет несколько типов финансовых тарифов для пациентов разных категорий. Рассмотрим два из них:
Нам удалось узнать подробнее о планах компании Alnylam на расширение рынка препарата. На данный момент патисиран доступен на территории США, о продаже на территории России речи пока не идет. Авторы надеются, что с течением времени терапия станет ближе для бóльшего числа больных.
Кто нас ждет теперь?
Как мы смогли убедиться, создание RNAi-препаратов сопряжено с огромными трудностями, связанными с доставкой хрупких РНК к клеткам. Сегодня остается еще много вопросов касательно дизайна и применения липидных наночастиц.
Это перспективное направление открывает, в первую очередь, невероятные возможности для лечения генетических заболеваний человека. Доказанная эффективность патисирана способствует дальнейшему исследованию РНК-интерферирующих агентов, их применению в клинической практике и еще большему накоплению багажа знаний. Возможно, когда-нибудь, мы увидим в аптеках волшебные лекарства против всего, а, может быть, приблизимся к «Дивному новому миру» Олдоса Хаксли. Время покажет.