Рецептор витамина D (VDR c.IVS7 +283 G>А)
Описание
Рецептор витамина D (VDR c.IVS7+283 G>А) — исследование мутаций гена VDR для выявления генетической предрасположенности к развитию остеопороза и рахита.
Важную роль в прогрессировании остеопороза играют нарушения в метаболизме и снижении чувствительности к витамину D. Вместе с COL1A1, VDR принадлежит ключевая роль в остеогенезе и минеральном обмене. В ряде исследований показана ассоциация полиморфизма VDR с возникновением переломов. Была выявлена ассоциация между увеличением частоты аллеля гена у женщин с впервые зарегистрированными переломами. Аллельный вариант ассоциирован с риском развития остеопороза, возникновением переломов.
Ген VDR
Ген VDR кодирует рецептор, который связывает витамин D3 (кальцитриол) и регулирует активность генов минерального обмена и секрецию паращитовидного гормона, контролируя, таким образом, гомеостаз кальция и фосфора. Этот рецептор также функционирует в качестве рецепторов для вторичной желчной кислоты — литохолевой кислоты. Рецептор принадлежит к семейству транс-активных регуляторных факторов транскрипции и имеет сходство между последовательностями с рецепторами стероидных и тиреоидных гормонов. Последующие мишени этого ядерного гормонального рецептора главным образом участвуют в минеральном обмене, хотя рецептор регулирует целый ряд других метаболических путей, например, тех, которые участвуют в иммунном ответе и раке. Мутации в этом гене связаны со II типом витамин D-резистентного рахита. Однонуклеотидный полиморфизм в старт-кодоне приводит к смещению иниациаторного кодона на три кодона от начала. В результате альтернативного сплайсинга образуются несколько вариантов транскриптов, кодирующих различные белки.
Витамин D-рецепторы экспрессируются в кишечнике, щитовидной железе и почках и играют жизненно важную функцию в гомеостазе кальция. Наследственные мутации в гене VDR приводят к рахиту, который характеризуется мышечной слабостью, отставанием в росте, деформацией костей и вторичным гиперпаратиреозом. Человеческий ген, кодирующий рецептор витамина D локализован на хромосоме 12q12-q14.
При аллеле B, уровень продукции рецептора повышен, что приводит к снижению уровня паращитовидного гормона в крови и повышению риска переломов независимо от плотности костной ткани. Данный полиморфизм также определяет эффективность терапии остеопороза.
Рацион и приём лекарственных препаратов не влияет на результат исследования.
Интерпретация результатов
Для интерпретации результатов генетического тестирования требуется консультация врача-генетика.
Мутации vdr что это
На протяжении последних десятилетий активно изучается роль гена, кодирующего рецептор витамина D (VDR). VDR является медиатором действия 1,25(OH)2D3 путем модуляции транскрипции генов-мишеней и был позиционирован как один из генов-кандидатов генетического контроля поддержания достаточной костной массы [33]. Исследования показали, что 1,25(OH)2D3 является стероидным гормоном, и его конечная точка приложения непосредственно связана с генетически детерминированными свойствами рецептора витамина D. Рецептор витамина D обнаружен во многих тканях и органах, включая желудочно-кишечный тракт, мочеполовую систему, органы эндокринной системы, а также в культуре клеточных линий скелетно-мышечной системы. Это явилось главным доказательством того, что биологическое действие 1,25(OH)2D3 выходит за рамки гомеостаза кальция и фосфора и играет ключевую роль в клеточной пролиферации и дифференцировке.
Рецептор витамина D (VDR) является членом надсемейства ядерных рецепторов транскрипционных регуляторов и посредником разнообразных биологических эффектов не только кальцитриола (1,25 (ОН)2D3), но и его аналогов. VDR предположительно возник путем дупликации анцестрального гена вместе с прегнан Х рецептором (PXR – оба члены подсемейства NR1I) [32].
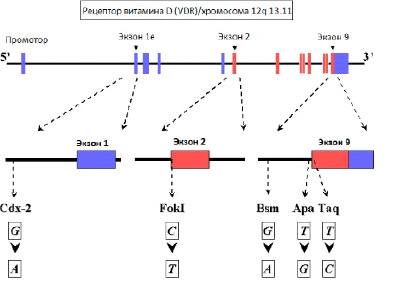
Ген VDR расположен на коротком плече 12 хромосомы имеет размер 75 Кб и содержит 11 экзонов. В гене выделяют некодирующую и кодирующую области. Некодирующая область находится на 5-конце гена и включает экзоны 1А, 1В и 1С. Последующие 8 экзонов кодируют структурную часть белкового продукта гена VDR. В гене VDR описано значительное количество аллельных вариантов, однако наиболее функционально значимыми являются 4 полиморфных сайта в позиции соответствующих точкам узнавания эндонуклеаз: BsmL, TaqI, FokI (рисунок).
Структура гена VDR: Сdx-2, FokI, Bsm, Apa, Taq – сайты для узнавания соотвествующих рестриктаз; G – гуанин; A – аденин;C – цитозин; T – тимин
Сохранение в VDR 18 из 22 лиганд-связывающих остатков было показано на видах позвоночных, от миноги до человека [20]. Разнообразная роль витамина D в развитии иммунитета, пролиферации и дифференцировке клеток [34], адсорбции фосфата и гомеостазе кальция [5] является, скорее всего, причиной избытка VDR во всех видах [9].
Лиганд-связанный VDR в комплексе с X рецепторами ретиноидов действует как перспективный фактор транскрипции [11]. Он трансактивирует или подавляет многочисленные гены-мишени путем связывания с положительным или отрицательным витамин-респонсивными элементами витамина D (VDREs и nVDREs, соответственно), присутствующими в промоторах, энхансерах или супрессорах этих генов [38]. В этом качестве VDR регулирует экспрессию генов, участвующих в разнообразных биологических функциях, включая развитие органов, контроль клеточного цикла, гомеостаз кальция и фосфата в метаболизме костей и детоксификацию ксенобиотиков [11]. VDR также играет роль в обеих врожденной и адаптивной ветвях иммунной системы, влияя таким образом на диапазон заболеваний. Неинфекционные заболевания, связанные с витамином D и VDR включают рак, а также аутоиммунные заболевания, такие как систематическая красная волчанка, болезнь Крона, диабет I типа, рассеянный склероз и ревматоидный артрит [16]. Инфекционные заболевания, связанные с VDR включают в первую очередь ВИЧ, туберкулез (ТБ) и проказу [36].
Известно, что VDR участвует в пролиферации и дифференциации клеток. VDR экспрессируется в нескольких белых кровяных клетках, включая моноциты и активированные Т- и B-клетки. Витамин D увеличивает экспрессию гена тирозингидроксилазы в медуллярных клетках надпочечников. Он также принимает участие в биосинтезе нейротрофических факторов, синтезе синтетазы оксида азота и повышении уровня глутатиона. Помимо активации VDR, известны различные механизмы альтернативного действия. Важным из них является его роль как природного ингибитора передачи сигнала с помощью белка хеджехог (гормона, участвующего в морфогенезе). [35]
Анализ онтологии генов (ГО) предполагаемых 11031 генов-мишеней VDR обнаруживает, что эти гены-мишени были вовлечены в ряд различных функции, а именно, метаболизм клеток (43 %), и морфология тканей (19 %), слияние клеток и адгезия (10 %), дифференцировка и развитие (10 %), ангиогенез (9 %), и транзиция эпителиальной ткани в мезенхимальную (5 %) [6]. Участие VDR в таком большом количестве разнообразных болезней и физиологические функции делает его сильным координатором для изучения основных механизмов заболеваний и их возможной профилактики [1,37]. Следовательно, важность функции VDR, и развитие экспрессии VDR, гарантирует понимание основных механизмов регуляции гена VDR.
Регулирование VDR в основных условиях и при индукции многогранно; оно формируется под воздействием окружающей среды, генетики и эпигенетики. Изучение взаимодействия и комбинированной роли этих трех аспектов регуляции генов будет способствовать более общему пониманию предрасположенности и прогрессирования заболеваний, связанных с VDR, таких как рак и туберкулез. Этот подход к изучению регуляции генов по отношению к болезни был выдвинут Бьорнссоном и др в качестве гипотезы генетики и эпигенетики распространенных заболеваний (CDGE) (2004).
Разнообразные факторы окружающей среды регулируют VDR, среди которых диета [22], солнце [17], возраст [10], загрязнение окружающей среды [2] и инфекции [23]. Большинство из этих факторов оказывают свое воздействие на VDR регулирование путем изменения уровней витамина D. Витамин D является коллективным названием для холекальциферола (D3) и эргокальциферола (D2), которые являются предшественниками активного VDR лиганда – 1?,25 (ОН)2D. Витамин D связывающий белок (DBP) транслоцирует витамин D из кожи [18] или кишечника в кровеносную систему, где он остается связанным с ним во время циркуляции в крови. DBP поставляет витамин D в печень для активации [9], где 25-гидроксивитамин D (25(OH)D) синтезируются из витамина D и снова доставляется с помощью DBP в кровеносную систему. Затем многофункциональный эндоцитотический клиренс рецептор мегалин способствует поглощению DBP-25(OH)D комплекса в проксимальные канальцы почки посредством эндоцитоза [30]. Этому процесс способствует ассоциированный с мембранами корецептор кубулин, который локализуется с мегалином [31]. Синтез активного 1?,25(OH)2D происходит в почках или другой ткани-мишени, которая катализируется CYP27B1, экспрессирующегося в большинстве тканей, включая клетки иммунной системы [42]. Последний поддерживает паракринную и аутокринную функцию в процессах, связанных с иммуннитетом.
При связи с VDR, активный витамин D (1?,25(OH)2D) регулирует экспрессию VDR посредством VDREs находящегося в его собственных энхансерах [43], таким образом, витамин D саморегулирует VDR. Хотя точный механизм регуляции гена VDR пока не известен, этот тип регулирования часто достигается путем модификации хроматина ядра посредством модификации гистонов и метилирования ДНК или деметилирования, происходящим в связи с корепрессорами и коактиваторами [7, 20, 25]. Приобретение предшественника витамина D, а также производство и биодоступность активного лиганда является важным для регулирования и активности VDR. Стабилизация белка VDR посредством его лиганда, увеличение его полужизни, является еще одним механизмом, с помощью которого экологически приобретенный витамин D может модулировать уровни VDR [38].
Исследования Трампа и других показывают, что витамин D (1,25 дигидроксихолекальциферол или кальцитриол) имеет значительную противораковую активность in vitro и in vivo в различных моделях рака человека, мышей и крыс (карцинома, рак простаты, легких, поджелудочной железы и миелома) [12-26, 39-40]. Кальцитриол индуцирует арест клеточного цикла, индуцирует и модулирует маркеры апоптоза и снижает сигналы выживаемости 27 in vitro и in vivo в большинстве из этих модельных систем. Глюкокортикоиды усиливают кальцитриол-опосредованную активность в преклинике (in vitro и in vivo) и клинике. Исследования показали, что дексометазон (dex) значительно усиливает противораковый эффект кальцитриола и уменьшает гиперкальцемию, вызванную кальцитриолом. Dex увеличивает присоединение лиганда рецептора витамина D (VDR) в раковых клетках in vitro и in vivo, в то время как в слизистой кишечника [41], где происходит абсорбция кальция [19], он его снижает.
VDR обнаружен не только в классических органах-мишенях (слизистая кишечника, почки, кости) и во многих других эпителиальных и мезенхимальных клетках, но также и в лейкемических и других злокачественных клетках. Кальцитриол ингибирует рост клеток in vitro и in vivo в моделях рака толстой кишки и рака молочной железы. Кальцитриол может индуцировать дифференциацию, арест клеточного цикла и апоптоз в лейкемических и раковых клетках. Прогрессия посредством клеточного деления регулируется при помощи циклинов и ассоциированных с ними циклин-зависимых киназ. Ингибиторами циклин-зависимых киназ p21Waf1/Cip1 и p27Kip участвуют в аресте G1-фазы. В клетках HL-60 кальцитриол блокирует деление клетки в G1-фазе; этот эффект достигается посредством увеличения p27. Кальцитриол-опосредованный арест в фазах G0/G1 также наблюдается в линиях клеток рака молочной железы. В линиях миеломоноцитарных клеток человека U937 функциональный VDRE был идентифицирован в регионе промотора p21, а также было обнаружено, что транскрипционная активация p21 с помощью VDR способствовала дифференцировке в этой линии клеток. [4].
Таким образом, нами были рассмотрены функции рецептора витамина D в организме человека, также выявлено что низкий уровень экспрессии VDR приводит к развитию многих распространенных заболевании, к числу которых относится и лейкоз.
Рецептор витамина D VDR: b/B (BsmI Polymorphism; IVS10+283G>A) в Москве
Приём и исследование биоматериала
Когда нужно сдавать анализ Рецептор витамина D VDR: b/B (BsmI Polymorphism; IVS10+283G>A)?
Подробное описание исследования
Название гена: VDR (Рецептор витамина D / vitamin D (1,25- dihydroxyvitamin D3) receptor)
Исследуемый полиморфизм: b/B (BsmI Polymorphism; IVS10+283G>A)
Международный код полиморфизма: rs1544410
Функция гена:
Важную роль в прогрессировании остеопороза играют нарушения в метаболизме и снижении чувствительности к витамину D. Вместе с COL1A1 VDR принадлежит ключевая роль в остеогенезе и минеральном обмене. В ряде исследований показана ассоциация полиморфизма VDR с возникновением переломов. Была выявлена ассоциация между увеличением частоты аллеля гена у женщин с впервые зарегистрированными переломами. Аллельный вариант ассоциирован с риском развития остеопороза, возникновением переломов.
Витамин D-рецепторы экспрессируются в кишечнике, щитовидной железе и почках и играют жизненно важную функцию в гомеостазе кальция. Наследственные мутации в гене VDR приводят к рахиту, который характеризуется мышечной слабостью, отставанием в росте, деформацией костей и вторичным гиперпаратиреозом. Человеческий ген, кодирующий рецептор витамина D локализован на хромосоме 12q12-q14.
Характерные проявления мутации:
Наличие аллеля B увеличивает риск переломов вертебральной и невертебральной локализации. При двух копиях аллеля b вследствие повышенного уровня паращитовидного гормона у женщин может развиваться спорадический первичный гиперпаратироидизм.
В настоящее время доказана роль рецептора витамина D (VDR) в патогенезе и особенностях течения артериальной гипертензии.
Тип наследования мутации:
аутосомно-доминантный (встречается у мужчин и женщин с одинаковой частотой, для развития заболевания достаточно унаследовать 1 мутантный вариант гена от одного из родителей, вероятность возникновения болезни у детей составляет 50 %).
Подготовка к исследованию
Специальной подготовки к исследованию не требуется. Необходимо следовать общим правилам подготовки к исследованиям.
ОБЩИЕ ПРАВИЛА ПОДГОТОВКИ К ИССЛЕДОВАНИЯМ:
Если Вы принимаете лекарства, обязательно предупредите об этом лечащего врача.
Генетические особенности чувствительности к витамину D и распространенность дефицита витамина D среди пациентов поликлиники
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Цель исследования: изучить распространенность дефицита витамина D среди пациентов, обратившихся за амбулаторной медицинской помощью, в том числе и у беременных, и зависимость его концентрации от полиморфизмов генов GC (DBP), CYP2R1, DHCR7.
Материал и методы: выполнялся ретроспективный анализ медицинской документации 565 пациентов, 449 из которых был сделан генетический тест на полиморфизм генов GC (DBP), CYP2R1, DHCR7 и анализ трех однонуклеотидных полиморфизмов (rs2282679 для гена GC; rs7944926 для гена DHCR7 и rs10741657 для гена CYP2R1).
Результаты и обсуждение: у 62% пациентов выявлены недостаток и дефицит витамина D, у беременных пациенток (62,5%) — недостаточность и дефицит витамина D. Любая концентрация 25 (OH) D ниже целевых уровней ассоциировалась с повышением уровня липопротеинов низкой плотности выше референсных значений. Концентрация витамина D имеет обратную зависимость от индекса массы тела, что связано с депонированием метаболита витамина D в подкожно-жировой клетчатке. Мутации в полиморфизмах генов, связанных с концентрацией 25 (OH) D, не так часты (30 из 449 человек); даже если мутация присутствует, это не всегда влечет недостаток и дефицит витамина D. Концентрации сывороточного 25 (OH) D зависят как от полиморфизмов генов, так и от внешних факторов, поэтому их следует рассматривать сообща. Лицам с генетическими факторами риска (предрасположенностью к значительному снижению концентрации 25 (OH) D) необходим прием более высоких доз препаратов витамина D.
Заключение: роль витамина D в нашем организме чрезвычайно многообразна: участие в фосфорно-кальциевом обмене, профилактика сахарного диабета 2-го типа, ожирения, сердечно-сосудистых, нейродегенеративных, онкологических и иммуноопосредованных заболеваний. Распространенность дефицита и недостатка витамина D у беременных соответствует распространенности в популяции, однако с учетом повышенного риска преждевременных родов, гестационного диабета, преэклампсии, кесарева сечения, ассоциированных с нехваткой витамина D, это состояние во время беременности требует незамедлительной коррекции.
Ключевые слова: витамин D, дефицит витамина D, генетический тест, полиморфизм генов, GC (DBP), CYP2R1, DHCR7, 25 (OH) D, беременность, чувствительность к витамину D.
Для цитирования: Полуэктова А.Ю., Мартынова Е.Ю., Фатхутдинов И.Р. и др. Генетические особенности чувствительности к витамину D и распространенность дефицита витамина D среди пациентов поликлиники. РМЖ. Мать и дитя. 2018;1(1):11-17. DOI: 10.32364/2618-8430-2018-1-1-11-17.
1 Pirogov Russian National Research Medical University, Moscow, Russian Federation
2 Sechenov University, Moscow, Russian Federation
3 Medical Center “Atlas”, Moscow, Russian Federation
Aim: to study prevalence of vitamin D deficiency among patients seeking outpatient care, including pregnant women, and dependence of its concentration on genes GC (DBP), CYP2R1, DHCR7 polymorphisms.
Patients and Methods: a retrospective analysis of medical records of 565 patients was performed, 449 of which were made a genetic test for the genes GC (DBP), CYP2R1, DHCR7 polymorphisms and analysis of three single nucleotide polymorphisms (rs2282679 for the GC gene; rs7944926 for the DHCR7 gene, and rs10741657 for the CYP2R1 gene).
Results and Discussion: 62% of the patients had moderate and severe vitamin D deficiency. In pregnant women, 62.5% had moderate and severe vitamin D deficiency. Any 25 (OH) D concentration below the target levels was associated with an increase in low-density lipoproteins above the reference values. The concentration of vitamin D has an inverse relationship to body mass index, which is associated with deposition of vitamin D metabolite in subcutaneous fat. Mutations in genes polymorphisms associated with 25 (OH) D concentration were not so frequent (30 of 449 people); even if the mutation is present, this does not always entail moderate and severe vitamin D deficiency. Serum 25 (OH) D concentrations depend both on gene polymorphisms and on external factors, so they should be considered together. Persons with genetic risk factors (a predisposition to a significant decrease in the concentration of 25 (OH) D) need to take higher doses of vitamin D medications.
Conclusion: the role of vitamin D in our body is extremely diverse: participation in phosphorus-calcium metabolism, prevention of type 2 diabetes, obesity, cardiovascular and neurodegenerative diseases, prevention of oncological and immuno-mediated diseases. The prevalence of moderate and severe vitamin D deficiency in pregnant women is consistent with the prevalence in population, but given the increased risk of preterm delivery, gestational diabetes, preeclampsia, and cesarean delivery, which are associated with vitamin D deficiency, this condition requires immediate correction during pregnancy.
Key words: vitamin D, vitamin D deficiency, genetic test, gene polymorphism, GC (DBP), CYP2R1, DHCR7, 25 (OH) D, pregnancy, vitamin D sensitivity.
For citation: Poluektova A.Yu., Martynova E.Yu., Fatkhutdinov I.R. et al. Genetic features of sensitivity to vitamin D and prevalence of vitamin D deficiency among outpatients. Russian journal of Woman and Child Health. 2018;1(1):11–17.
В статье описаны генетические особенности чувствительности к витамину D и распространенность дефицита витамина D среди пациентов поликлиники. Показано, что распространенность дефицита и недостатка витамина D у беременных соответствует распространенности в популяции. Это состояние во время беременности требует незамедлительной коррекции.
Введение
Материал и методы
Был проведен ретроспективный анализ 6034 медицинских карт, из них отобраны карты тех пациентов, кому проводился анализ крови на 25 (OH) D (метаболит витамина D). В исследование были включены 565 пациентов (373 женщины, из них 72 беременные, 192 мужчины). Средний возраст женщин — 40,8±13,9 года, мужчин — 41,5±12,5 года. Помимо 25 (OH) D собирались данные об уровне общего кальция (Ca), креатинина, липопротеинов низкой плотности (ЛПНП), аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), гликированного гемоглобина (HbA1c), паратиреоидного гормона (ПТГ), тиреотропного гормона (ТТГ); индексе массы тела (ИМТ), выполнялся анализ мочи на белок.
Заведомо были исключены пациенты, у которых уровни ПТГ и ТТГ выходили за пределы референсных значений.
На основании результатов экспериментальных исследований выявлено несколько генов-кандидатов, мутации в которых влияют на концентрацию 25 (OH) D: GC, CYP24A1, CYP2R1, CYP27B1, VDR, NADSYN1/DHCR7. В генетическом тесте определялись гены, связанные с 25 (OH) D, которые участвуют в транспортировке, активации и синтезе витамина D соответственно: GC (хромосома 4q12-q13) (ген специфической группы), DHCR7 (хромосома 11q13.4) (7-дегидрохолестеринредуктаза), CYP2R1 (хромосома 11p15.2) (цитохром P450, семейство 2, подсемейство R, полипептид 1) [13, 14]. GC кодирует связывающий белок витамина D (DBP), варианты которого отличаются сродством к 25 (OH) D [15]. Генетические полиморфизмы гена GC могут влиять на эффективность транспортировки, биодоступность при преобразовании в тканях организма 25 (OH) D в активную гормональную форму — 1,25 (OH) 2D [16]. Индуцированный ультрафиолетом синтез витамина D3 в коже из 7-дегидрохолестерина катализируется DHCR7 (НАДФ-зависимая 7-дегидрохолестеринредуктаза). В печени под влиянием фермента 25-гидроксилазы митохондрий (CYP27A1) и микросом (CYP2R1) происходит преобразование витамина D в его прогормональные формы 25 (OH) D3 (кальцидиол) и 25 (OH) D2 (эргокальцидиол). Последние являются основными циркулирующими формами витамина D, которые через кровоток поступают в почки [13, 17].
Установлена ассоциация показателей риска развития определенных заболеваний с наличием мутаций в генах, участвующих в метаболизме витамина D, и, соответственно, приводящих к снижению концентрации последнего [18]: GC (rs2282679): остеопороз, болезнь Грейвса; CYP2R1 (rs10741657): колоректальный рак, сахарный диабет 1-го типа [19]; CYP2R1 (rs10741657), GC (rs2282679): хронический гепатит С [20], рецидив рака толстой кишки [21]; GC (rs2282679), DHCR7 (rs7944926): рак яичников [22]. Концентрация 25 (OH) D ассоциируется с 18 однонуклеотидными полиморфизмами (SNP) в регионах вышеуказанных генов [23], в генетическом тесте проводился анализ 3 SNP (rs2282679 для гена GC (наиболее выраженная связь с показателем 25 (OH) D [14, 24]); rs7944926 для гена DHCR7 и rs10741657 для гена CYP2R1).
В генетическом тесте определялись гаплотипы (цис-положение двух или больше полиморфизмов, расположенных на одной хромосоме) и идентифицировались с концентрацией 25 (OH) D. Для гена GC (rs2282679) были характерны гаплотипы TGA, TT, TG, GG; для гена DHCR7SNP (rs7944926) — GG, AG, AA; для гена CYP2R1 (rs10741657) — AG, AA, GG.
Из 565 пациентов у 449 был проведен генетический тест на полиморфизм генов GC (DBP), CYP2R1, DHCR7 (методом секвенирования HiSeq2000 на ДНК чипах (Illumina)).
Расчет скорости клубочковой фильтрации (СКФ) выполнялся при помощи калькулятора CKD-EPI CREATININE EQ (2009) (mdrd.com). Деление на группы по уровню СКФ соответствовало «Национальным клиническим нефрологическим рекомендациям» (2016) [25, 26].
По уровню концентрации 25 (OH) D пациенты были поделены на группы: группа 0 — нормальный уровень витамина D ≥ 30 нг/мл (≥75 нмоль/л); группа 1 — недостаточность витамина D — 20–29 нг/мл (50–74 нмоль/л); группа 2 — дефицит витамина D 2 ); группа 2 — избыточная масса тела (25,0–29,9 кг/м 2 ); группа 3 — ожирение I степени (30,0–34,9 кг/м 2 ); группа 4 — ожирение II степени (35,0–39,9 кг/м 2 ); группа 5 — ожирение III степени (морбидное) (≥40 кг/м 2 ) [28].
Проводилась интерпретация генетического теста на особенности концентрации 25 (OH) D: группа 1 — с концентрацией без особенностей; группа 2 — с предрас-
положенностью к снижению концентрации 25 (OH) D;
группа 3 — с предрасположенностью к значительному снижению концентрации 25 (OH) D.
Статистический анализ данных проводился при помощи пакета прикладных программ Statistica 10.0.1011.0. Критический уровень достоверности нулевой гипотезы был принят равным 0,05.
Результаты и обсуждение
На основании проведенного исследования нами были сделаны следующие выводы:
Распространенность недостатка и дефицита витамина D среди пациентов клиники составляет 62%. Несмотря на то, что распространенность этих состояний у беременных соответствует распространенности в популяции, повышенный риск преждевременных родов, гестационного диабета, преэклампсии, кесарева сечения, ассоциированный с нехваткой витамина D, требует незамедлительной коррекции.
Связь витамина D с дислипидемией позволяет предположить, что поддержание целевых уровней витамина D может помочь в профилактике сердечно-сосудистой патологии.
Уровень общего кальция в крови в большей степени зависит от фильтрационных особенностей почек, чем от концентрации витамина D.
Существенное влияние на статус витамина D оказывают полиморфизмы в генах GC, CYP2R1 и DHCR7/NADSYN1.
Сведения об авторах: 1 Полуэктова Алена Юрьевна — студентка лечебного факультета; 2 Мартынова Евгения Юрьевна — аспирантка кафедры эндокринологии лечебного факультета; 3 Фатхутдинов Илдус Рифкатович — врач-педиатр, главный врач; 1 Демидова Татьяна Юльевна — д.м.н., профессор, заведующая кафедрой эндокринологии лечебного факультета; 1,3 Потешкин Юрий Евгеньевич — к.м.н., доцент кафедры эндокринологии, врач-эндокринолог. 1 ФГБОУ ВО Российский национальный исследовательский медицинский университет им. Н. И. Пирогова Минздрава России. 117997, Россия, г. Москва, ул. Островитянова, д. 1. 2 ФГАОУ ВО Первый Московский государственный медицинский университет им. И. М. Сеченова Минздрава России. 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2. 3 ООО «Медицинский центр «Атлас». 121170, Россия, г. Москва, пр-т Кутузовский, д. 34/14. Контактная информация: Полуэктова Алена Юрьевна, е-mail: alenapoluektova.068@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 21.07.2018.
About the authors: 1 Alena Y. Poluektova — a student of medical faculty; 2 Evgenia Y. Martynova — post-graduate student; 3 Ildus R. Fatkhutdinov — pediatrician, head physician; 1 Tatyana Y. Demidova — professor, Head of department; 1,3 Yury E. Poteshkin — Ph.D., associate professor of department. 1 Russian National Research Medical University. 1, Ostrovityanova str., Moscow, 117997, Russian Federation. 2 Sechenov University. 8–2, Trubezhkaya str., Moscow, 119991, Russian Federation. 3 Medical Center “Atlas”. 34/14, Kutuzovsky Ave., Moscow, 121170, Russian Federation. Contact information: Alena Y. Poluektova, e-mail: alenapoluektova.068@gmail.com. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 21.07.2018.
Только для зарегистрированных пользователей