Мутация g12d в гене kras что это
Как известно, КРР представляет собой гетерогенную группу опухолей, отличающихся как молекулярными изменениями, так и прогнозом течения болезни и особенностями терапии. В настоящее время для выбора тактики лечения необходимо учитывать не только клинические факторы, такие как распространение опухоли, функциональный статус пациента, но и молекулярный профиль заболевания. Изучению частоты мутаций гена KRAS и их связи с клинико-патологическими особенностями у пациентов с КРР были посвящены многочисленные исследования 4. В Республике Казахстан подобные исследования ранее не проводились.
Материал и методы исследования. В основу настоящей работы легли данные исследования 332 больных колоректальным раком, зарегистрированных в облонкодиспансерах РК, которым определялся статус гена KRAS по послеоперационному и/или биопсийному материалу за период с 2010 по 2014 г. методом ПЦР.
Молекулярно-генетические исследования по изучению статуса гена KRAS по послеоперационному и/или биопсийному материалу у пациентов с колоректальным раком проводились в лаборатории патоморфологии и молекулярной генетики Казахского НИИ онкологии и радиологии. После морфологической оценки качества исследуемого материала в зависимости от процентного содержания опухолевых клеток в образце, для экстракции ДНК проводили 3-5 макродиссекций и депарафинизацию. Во избежание получения ложноотрицательных результатов образцы, содержащие менее 20% опухолевых клеток, подвергали микродиссекции, по заранее отмеченной морфологом зоне слайдов. Экстракцию ДНК проводили, используя наборы (FFPE DNA extraction kit, Qiagen). Концентрацию экстрагированной ДНК определяли на спектрофотометре NanoDrop, а качество ДНК оценивали с помощью постановки контрольной ПЦР в режиме реального времени, сравнивая с контрольной ДНК (входит в состав коммерческого набора). KRAS-тест проводили, используя наборы BioLink для выявления мутаций в 12 и 13 кодонах экзон 2 аллель-специфичным ПЦР-методом.
Статистическая обработка материала производилась на персональном компьютере при помощи программы математической обработки данных с помощью пакета IBM SPSS Statistics 20 (trial-версия). Для выявления взаимосвязи между переменными использовался коэффициент линейной корреляции Пирсона (rp).
Результаты исследования и их обсуждение. Из 332 включенных в исследование больных с КРР мутации гена K-ras были выявлены у 149(44,9±4,0)%, а 183(55,1±3,6)% пациентов имели не мутированный, т.е. «дикий» тип. Из 149 мутаций 120(80,5%) обнаруживались в кодоне 12. В 29(19,5%) опухолевых образцах мутации выявились в 13 кодоне, таблица 1.
Распределение мутаций в 12-м и 13-м кодонах гена KRAS
Мутации генов семейства RAS
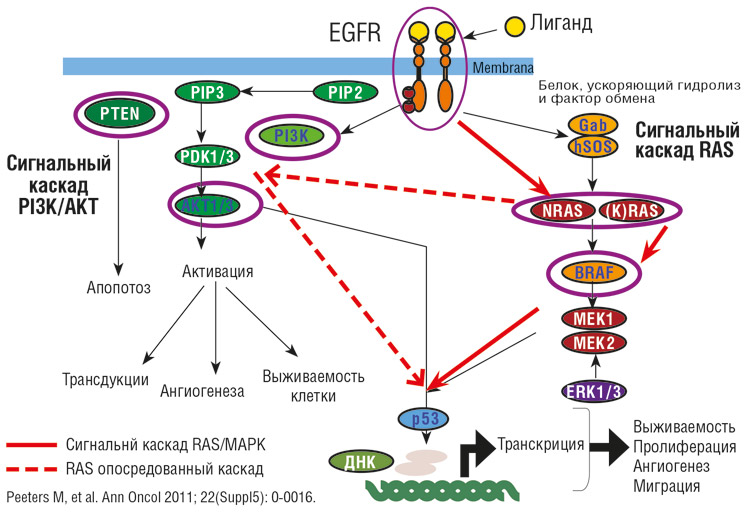
Сигнальный путь EGFR и мутации генов семейства RAS при колоректальном раке
Постоянная активация сигнального каскада рецептора эпидермального фактора роста (EGFR) является одной из ведущих причин опухолевой трансформации и прогрессии.
Причинами подобной активации могут быть:
Для колоректального рака характерны 1 и 3 пути активации.
Блокада сигнального каскада EGFR с помощью моноклональных антител, связывающихся с рецептором, показала высокую клиническую эффективность при целом ряде опухолей, в том числе при колоректальном раке. Однако использование этих препаратов в неселектированной группе больных приводило к ответу на лечение лишь у 25% пациентов.
Первоначальный молекулярный анализ образцов пациентов, участвовавших в исследованиях OPUS и CRYSTAL, показал, что существенную роль в резистентности опухоли к терапии моноклональными антителами играют мутации гена KRAS, одного из участников внутриклеточной части сигнального каскада EGFR.
Однако дальнейшие исследования показали, что не меньшее значение в определении полноты противоопухолевого ответа играют и другие участники сигнального пути, начинающегося с рецептора EGFR: гены RAS-RAF-MEK-ERK-МАРК.
Сигнальный путь RAS
В RAS-зависимом сигнальном пути ключевую роль играют белки семейства RAS. Фиксированные на внутренней стороне клеточной мембраны, белки RAS являются первыми членами каскада киназ, которые приводят к активации сигнальных путей и транскрипции генов, регулирующих дифференцировку и пролиферацию клетки.
Роль белка RAS в сигнальном пути EGFR
Семейство генов RAS (Retrovirus Associated DNA Sequences) включает 3 гена: KRAS, HRAS, NRAS. Первые два гена получили название от своих гомологов, выделенных из линий вирусов мышиной саркомы Kirsten и Harvey, последний был идентифицирован в клеточной линии нейробластомы. Три гена кодируют четыре варианта протеинов – два типа KRAS, А и В (наиболее часто распространенный), и по одному типу HRAS и NRAS.4 Все они относятся к белкам, связывающим энергетическую молекулу ГТФ. RAS-белки могут существовать в двух формах: неактивной, GDP- и активной, GTP-связанной. Благодаря собственной GTP-азной активности, а также под действием факторов обмена (Sos и др.), белок RAS циклически переходит из GTP-связанной активной формы в GDP-связанную неактивную и обратно.
Нормальный RAS находится преимущественно в неактивной, GDP-связанной форме. Активация RAS регулируется рецепторной тирозинкиназой EGFR. После связывания рецепторной внеклеточной части тирозинкиназы с фактором роста и ее димеризации происходит взаимное фосфорилирование ее внутриклеточных доменов. Фосфорилирование создает активную конформацию киназы. Образование активного комплекса RAS-GTP происходит в присутствии активирующего GTP-азу белка GAP, в сотни раз ускоряющего гидролиз. После гидролитического превращения GTP в GDP RAS снова инактивируется. Сигнал прерывается. Чтобы воспринять новый сигнал, если он еще существует вне клетки, цикл реактивации должен быть повторен.
Таким образом, каскадная последовательность реакций сигнального пути RAS действует как включатель, определяющий регуляцию генной экспрессии, требующуюся для реализации деления или дифференцировки клетки.
Нарушение систем передачи сигнала и канцерогенез
RAS-белки часто упоминают как протоонкогенные продукты: их постоянная активация ведет к злокачественному перерождению клеток. Характерный механизм перерождения RAS – точечные мутации в соответствующих генах. Наиболее частыми онкогенными мутациями генов всего семейства RAS являются мутации в 12 и 61 кодонах.
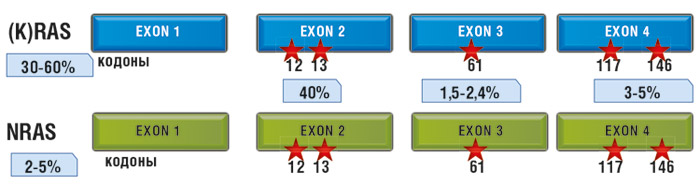
Мутации в гене KRAS в опухолях толстой кишки встречаются в 30-60% случаев. Наиболее часто мутации KRAS определяются в экзоне 2, кодонах 12 и 13. Однако описаны мутации в экзоне 3, кодоне 61, и в экзоне 4, кодонах 117 и 146. Мутации в гене NRAS (в идентичных экзонах и кодонах) при КРР составляют до 5%. Мутации в гене HRAS при аденокарциноме толстой кишки не описаны.
Мутации генов семейства RAS при злокачественных опухолях
(по базе данных COSMIC)
| Орган | Тип опухоли | Мутации (%) | ||
|---|---|---|---|---|
| HRAS | KRAS | NRAS | ||
| Колоректальный рак | Аденокарцинома | 0 | 42 | 5 |
| Желчные пути | Аденокарцинома | 0 | 35 | 2 |
| Мочевой пузырь | Уротелиальная карцинома | 12 | 4 | 2 |
| Печень | Гепатоцеллюлярный рак | 0 | 4 | 4 |
| Легкое | Крупноклеточный рак | 4 | 21 | 4 |
| Аденокарцинома | 0 | 16 | 1 | |
| Поджелудочная железа | Протоковая аденокарцинома | 0 | 69 | 1 |
| Эндокринные опухоли | 0 | 1 | 75 | |
| Кожа | Меланома | 1 | 2 | 20 |
Точечные мутации онкогенов RAS при мКРР
Значение различных мутаций RAS
Как уже говорилось выше, при колоректальном раке почти 90% всех нарушений представляют собой точечные замены одного нуклеотида на другой во втором экзоне генов KRAS и NRAS, в последовательностях, кодирующих 12 и 13 аминокислоты. В норме в обеих позициях располагается глицин, единственная аминокислота, не имеющая боковой цепи. Любое изменение этой последовательности приводит к замене глицина на разветвленные аминокислоты, что ведет к нарушению пространственной конформации протеина. В результате этого блокируется способность специальных белков инактивировать комплекс RAS с ГТФ путем гидролиза энергетической молекулы. Сигнал начинает передаваться от активированного RAS к другим участникам каскада независимо от статуса EGFR.
Около 10% мутаций этой гена в колоректальных опухолях происходят в 3 и 4 экзонах, с одинаковой частотой в 61 и 146 кодонах и крайне редко – в 117 кодоне. Мутации, затрагивающие 61 кодон, нарушают водородные связи между RAS и белками-инактиваторами, приводя к тому же эффекту, что и при нарушениях в 12 и 13 кодонах гена. Мутации 146 кодона не сопровождаются существенными изменениями активности протеина.
Тем не менее, эти мутации оказывают свое негативное воздействие в результате накопления дефектного белка на фоне аллельного дисбаланса – увеличения копийности мутантного гена или перехода его в гомозиготное состояние, что весьма характерно для опухолей с мутациями генов семейства RAS.
Возрастающая роль сигнального пути RAS в индивидуализированной терапии мКРР
Самым известным биомаркером в таргетной анти-EGFR терапии пациентов c мКРР является статус мутаций кодонов 12 и 13 гена KRAS. Доказано, что активация KRAS за счет мутации сводит на нет эффект ингибирования EGFR моноклональными антителами. Таким образом, наличие мутантных аллелей гена KRAS является независимым предсказательным маркером эффективности терапии ингибиторами EGFR. Поэтому панитумумаб и цетуксимаб назначают только больным мКРР с диким типом гена KRAS.
Влияние дополнительных мутаций гена KRAS и новых мутаций гена NRAS, а также мутаций гена BRAF на эффективность таргетной терапии ингибиторами EGFR изучалось в исследованиях с панитумумабом и цетуксимабом пациентов мКРР:
Все исследования показали, что, несмотря на то, что индивидуализация терапии антителами по статусу генов семейства RAS предусматривает сужение круга пациентов (примерно 50/50 вместо 60/40 при отборе только лишь по статусу 2 экзона гена KRAS), пациенты с диким типом генов KRAS и NRAS в опухоли получат максимальную пользу от терапии антителами в комбинации со стандартной химиотерапией, по сравнению с пациентами без мутаций гена KRAS во 2 экзоне. Пока нет достаточных доказательств негативного влияния мутаций генов BRAF, PI3K, PTEN и других участников сигнального пути RAS-RAF-MEK-ERK-МАРК по результатам крупных проспективных рандомизированных исследований, однако не исключено, что появление таких исследований вновь существенно изменит наши представления о группе пациентов, для которых применение анти-EGFR антител окажется наиболее выгодным.
В связи с этим целью программы является максимально широкое внедрение генетического тестирования при колоректальном раке в ежедневную практику онкологов, как одного из важнейших условий проведения современной эффективной терапии у целевой группы пациентов.
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.
Определение мутации в генах KRAS и NRAS при раке толстой кишки
Биологические функции генов семейства RAS
Одно из ключевых свойств любой опухоли — это нарушение баланса между клеточным делением, т.е. размножением клеток, и клеточной гибелью. Для того, чтобы процесс деления осуществлялся в норме, необходимо поступление верного сигнала в клеточное ядро. Подобным сигналом являются специальные белки – факторы роста. Они прикрепляются к определённым рецепторам на поверхности клеточной оболочки и запускают внутри клетки ряд последовательных биохимических реакций. Результатом становится производство и накопление внутри клетки белков, которые необходимы для дальнейшего деления.
Гены семейства RAS (KRAS, NRAS и HRAS) – это один из важнейших звеньев сигнальной цепочки внутри клетки. Они передают сигналы к делению от рецепторов к ядру клетки. В норме эта цепочка сигналов (или, по-другому, сигнальный каскад) запускается «по команде» факторов роста. Например, фактором роста может выступать белок EGF (Epidermal Growth Factor ‒ перевод «эпидермальный фактор роста»). EGF и другие белки способны стимулировать рост и деление различных клеток. В случае мутации в каком-либо из генов – KRAS, NRAS или HRAS – происходит самопроизвольная активация передачи импульса к делению, то есть клетки начинают размножаться без команды от фактора роста. Процесс выходит из-под контроля, и опухоль начинает активно расти.
Необходимо отметить, что активирующие мутации не только в этих генах, но и в других звеньях сигнальной цепочки могут приводить к постоянной стимуляции клеточного деления. К таким событиям относятся, например, мутации в генах EGFR, BRAF и др. Упомянутые генетические повреждения в разной степени свойственны опухолям различных органов. Например, мутации в генах семейства RAS (KRAS, NRAS, HRAS) встречаются при раке поджелудочной железы, толстой кишки, лёгкого, кожи и т.д. Мутации EGFR характерны для немелкоклеточного рака легкого, а повреждения BRAF с наибольшей частотой обнаруживаются при меланоме.
В каких случаях нужно сделать тест на мутацию в генах KRAS и NRAS?
Тестирование опухоли на наличие мутаций в генах KRAS и NRAS выполняется пациентам с опухолями толстой кишки. Тест позволяет лечащему онкологу решить вопрос о возможности использования в терапии антител к определенному фактору роста и деления клеток ‒ EGFR. Данные препараты – панитумумуаб или цетуксимаб ‒ блокируют расположенные на мембране клеток рецепторы эпидермального фактора роста (EGFR) и препятствуют росту опухоли.
Если в «нижележащих» генах-участниках сигнальной цепи (KRAS, NRAS или BRAF) присутствует мутация, то использование цетуксимаба и панитумумаба становится неэффективным. То есть препараты не будут препятствовать росту опухолевых клеток, поскольку воздействуют не на те звенья сигнальной цепочки, они не смогут предотвратить подачу сигнала к клетке.
Более того, существуют сведения о том, что ошибочное назначение анти-EGFR терапии пациентам, у которых мутация в перечисленных генах не выявлена, может ускорять рост опухоли. Частота мутаций в гене KRAS при опухолях толстой кишки достигает 50%. Ещё около 10-20% приходится на мутации в генах NRAS и BRAF. Таким образом, при правильном обследовании лечение антителами к EGFR должно назначаться не более 30-40% пациентов с раком толстой кишки, в остальных случаях используются другие схемы терапии.
Что делать, если в опухоли толстой кишки обнаружена мутация в гене KRAS или NRAS?
Обнаружение мутации в гене KRAS или NRAS является абсолютным противопоказанием к использованию цетуксимаба или панитумумаба, т.к. присутствие этих мутаций полностью препятствует противоопухолевому действию данных препаратов. Как упоминалось выше, при ошибочном назначении антител к EGFR пациентам с мутациями в генах RAS может наблюдаться ускорение роста опухоли – именно поэтому полноценное исследование данных генов является обязательным условием для подбора правильной терапии. В случае наличия мутаций в генах KRAS и NRAS в клетках опухоли успешно используются другие разновидности лечения.
Как сдать анализ на мутации в гене KRAS, NRAS, EGFR, BRAF?
Чтобы провести молекулярно-генетическое тестирование, специалистам необходимы опухолевые клетки. Они могут быть получены либо при биопсии, либо в ходе хирургической операции по удалению новообразования. При этом, материал для исследования должен быть подготовлен определенным образом. В противном случае тестирование будет невозможно.
В ходе первичного обследования онкологическому пациенту практически всегда выполняют биопсию, на основании которой происходит патоморфологическое подтверждение диагноза. Для этого полученные клетки пациента проходят многоэтапную химическую обработку. В результате из них создаётся специальный парафиновый блок. С одной стороны, он необходим для получения качественного тонкого среза (толщиной 5 мкм) с целью патоморфологической диагностики. С другой стороны, в правильно подготовленном парафиновом блоке молекулы ДНК надёжно сохраняются на протяжении десятилетий.
Аналогичные манипуляции патологи проводят в отношении опухолевых тканей, удалённых во время операции. Правильное выполнение процедуры фиксации тканей позволяет использовать образцы опухолей для молекулярно-генетического исследования ДНК спустя месяцы и годы после заливки образца в парафин.
Идеальным набором для молекулярно-генетического исследования является следующий комплект: парафиновый блок c тканью опухоли и одно стекло, окрашенное специальными красителями (гематоксилином и эозином). Всё перечисленное хранится в патологоанатомических архивах медицинских учреждений, а окраска гематоксилином и эозином – основная окраска, используемая в современной патоморфологической диагностике. Если медицинское учреждение по какой-либо причине не может предоставить блоки, то для молекулярно-генетического тестирования достаточно 5-10 неокрашенных срезов ткани опухоли на непокрытых стёклах толщиной 3-5 мкм и одно стекло, окрашенное гематоксилином и эозином.
Требования к упаковке материала перед транспортировкой
В настоящее время многие молекулярно-диагностические исследования выполняются за счет средств территориальных фондов ОМС регионов России (как Санкт-Петербурга, так и остальных субъектов РФ).
Авторская публикация:
Иванцов Александр Олегович
доктор медицинских наук, старший научный сотрудник научной лаборатории морфологии опухолей ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России
Что вам необходимо сделать
Публикации по теме:
1. Более того, существуют сведения о том, что ошибочное назначение анти-EGFR терапии пациентам, у которых мутация в перечисленных генах не выявлена, может ускорять рост опухоли.
2. Как упоминалось выше, при ошибочном назначении антител к EGFR пациентам с мутациями в генах RAS может наблюдаться ускорение роста опухоли.
Что из этого верно? Наверное, второе?
Мутация g12d в гене kras что это
KRAS, мутация KRAS, колоректальный рак, немелкоклеточный рак легкого, анти-EGFR антитела.
Синонимы английские
KRAS, KRAS mutation, colorectal cancer, non-small cell lung cancer, anti-EGFR antibodies.
Полимеразная цепная реакция.
Какой биоматериал можно использовать для исследования?
Образец ткани, образец ткани в парафиновом блоке.
Общая информация об исследовании
KRAS представляет собой протоонкоген из семейства белков RAS и кодирует G-белок, активно участвующий в регуляции и контроле клеточной пролиферации, дифференцировке и выживании. Белок Ras неактивен в нормальных непролиферирующих клетках, но вступает в работу при связывании с гуанозинтрифосфатом, что приводит к реактивации рецепторов факторов роста. Активированный комплекс Ras-ГТФ связывается и активирует ряд вторичных посредников передачи клеточного сигнала, такие как белки путей RAS/RAF/MEK/MAPK и PI3-K [PI3K/AKT/mTOR]. KRAS играет основную роль в контроле передачи сигнала от ряда основных рецепторов факторов роста, в том числе EGFR. Активирующие мутации в гене KRAS изменяют ГТФ-азную активность белка и блокируют возможность его деактивации, что ведет к гиперактивации ряда внутриклеточных путей передачи сигнала, контролирующих рост и пролиферацию клеток.
Примерно 40 % случаев колоректального рака характеризуется мутацией в гене KRAS. Около 90 % этих мутаций обнаруживается в кодонах 12 и 13 экзона 2 гена KRAS, а остальные мутации детектируются в кодонах 61 и 146 (примерно по 5 % на каждый кодон). Мутации KRAS приводят к EGFR-независимой конститутивной активации сигнального пути и служат предиктором отсутствия ответа на терапию моноклональными анти-EGFR-антителами, такими как цетуксимаб и панитумумаб.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Мутаций в экзонах 2, 3, 4 гена KRAS не обнаружено.
Обнаружена патогенная мутация в гене KRAS, ассоциированная с резистентностью к анти-EGFR-терапии при колоректальном раке, а также с резистентностью к ингибиторам EGFR при немелкоклеточном раке легкого.
Для получения заключения по результату обследования необходимо проконсультироваться у врача-онколога.
Мутация g12d в гене kras что это
Колоректальный рак (КРР) занимает одно из ведущих мест в структуре онкологической заболеваемости и смертности в развитых странах мира, выходя на третье место у мужчин и второе – у женщин [1, 6]. Рассматривая структуру заболеваемости раком среди мужского населения России, следует отметить, что злокачественные опухоли ободочной и прямой кишки занимают пятое и шестое место в общей статистике онкологических заболеваний. Суммарно, опухоли толстой и прямой кишки занимают второе место, уступая лишь раку легкого. Хирургия остается оптимальным методом лечения, поскольку диагностирование опухоли преимущественно на поздних стадиях заболевания требует оперативных и радикальных мер помощи пациенту в короткие сроки. Тем не менее, современные методы химиотерапии, направленные на уменьшение размеров опухоли, замедление опухолевого роста и предотвращение появления новых метастазов, не менее важны при лечении КРР.
Изучению частоты мутаций гена KRAS и их связь с клининико-патологическими особенностями у пациентов с колоректальным раком были посвящены многочисленные исследования [1]. На Юге России подобные исследования ранее не проводились. Вместе с тем, население данной территории имеет свои популяционные особенности, что требует подробного изучения.
Цель исследования заключалась в изучении популяционного полиморфизма 7 SNP-мутаций соматического происхождения в гене KRAS опухолевых биоптатов пациентов с диагнозом КРР Юга России для адекватного назначения таргетных препаратов (цетуксимаб, панитумумаб). Определялась взаимосвязь обнаруженных мутаций с клинико-патологическими особенностями пациентов, получавших стационарное лечение в ФГБУ «Ростовский научно-исследовательский онкологический институт» Министерства здравоохранения Российской Федерации.
В настоящее исследование было включено 168 пациентов (73 мужчины, 95 женщин) в возрасте от 28 до 89 лет с морфологически подтвержденным диагнозом аденокарциномы толстой или прямой кишки. Из фиксированных в 10%-м забуференном формалине и залитых в парафин образцов тканей опухолей получали срезы толщиной 8-10 мкм. Для молекулярно-генетического исследования использовали срезы, содержащие не менее 20% опухолевых клеток. Процедура экстракции ДНК включала в себя стандартную депарафинизацию срезов орто-ксилолом, отмывку 96-% этанолом, инкубирование при комнатной температуре в лизирующем буфере с протеиназой K в течение 12 часов и последующую инкубацию при температуре 900 в течение 1 часа. Затем образцы обрабатывали набором реагентов QIAamp® DNA FFPE Tissue Kit (QIAGENE, Германия) согласно протоколу производителя. Концентрацию выделенной из образцов ДНК измеряли на флюориметре Qubit 2.0® с использованием набора Quant-iT™ dsDNA High-Sensitivity (HS) Assay Kit (Invitrogen, США). Концентрация ДНК нормализовывалась до величины 1 нг/мкл. При помощи набора реагентов «Real-Time-PCR-KRAS-7M» («Биолинк», Россия) проводили определение 7 SNP-мутаций (Single Nucleotide Polymorphism) в 12 и 13 кодонах гена KRAS: G12C, G12S, G12R, G12V, G12D, G12A, G13D с использованием термоциклера Bio-Rad CFX96 (Bio-Rad, США).
Статистический анализ выполняли с использованием прикладных пакетов программ Microsoft Excel 2010 и STATISTICA 8.0. Определяли различия в группах, выделенных в соответствии с определенными признаками (пол, возраст, локализация первичной опухоли, степень дифференцировки опухолевых клеток, наличие метастазов в печень, регионарные и отдаленные лимфоузлы, стадия заболевания), у пациентов с мутантным и диким типом гена KRAS. Оценку различий проводили с использованием χ2-критерия, для уровня статистической значимости р 55лет