Мутация группы крови что это
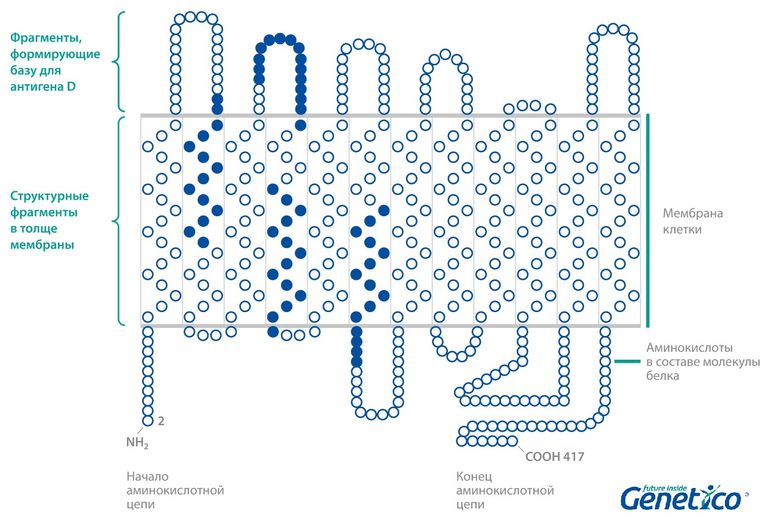
В этой статье мы расскажем о редких вариантах гена RHD и особенностях оценки риска возникновения резус-конфликта. Гены RHD и RhCE у человека работают вместе: они кодируют белки, которые формируют в мембране комплекс, образовывающий базу для антигенов D (резус-фактор), C, c, E, e. Эти белки представляют собой как бы нитки, прошивающие мембрану петлями: их небольшие фрагменты торчат из мембраны, а основная часть находится в ее толще. То есть какие-то аминокислоты белка выполняют строительную функцию – держат белок в мембране, а другие основную – формируют площадку для антигена.
Если гена RHD нет из-за делеции этого участка хромосомы, то и белка на мембране нет. В таком случается получается истинный Rh- фенотип. Однако в редких случаях ген RHD не полностью отсутствует, а несет в себе мутацию. Тогда структура соответствующего белка может нарушаться и приводить не к полному отсутствию антигена D, а к разным промежуточным состояниям. Например, мутации, приводящие к изменению в тех частях белка, которые находятся в толще мембраны, могут влиять на способность белка держаться на поверхности клетки: то есть и ген RHD на месте, и белок нормально синтезируется, однако он с трудом встраивается в мембрану и потому его может быть настолько мало на поверхностях клеток, что иммунная система человека будет их замечать, а вот биохимические методы анализ на резус-фактор – не будут. В случае такого рода мутаций в гене RDH генотип называется Weak D или DEL вместо Rh-. Также при мутациях, затрагивающих выступающие из мембраны участки, антиген D будет неполноценным, так как площадка для его формирования будет неполная или не совсем верная, что тоже может привести к ложным результатам при биохимическом анализе крови. Такой генотип носит название Partial D.
Почему все это важно? Дело в том, что чаще всего статус резус-фактора определяют биохимически по анализу крови. Это значит, что в лаборатории есть антитела к антигену D, эти антитела капают на специально подготовленный препарат крови и смотрят, насколько сильно будет светиться специфическая метка. Если она светится слабо или сигнала нет совсем – это означает, что антителам не с чем было связываться, то есть антигена D на поверхности клеток в анализируемой крови не было. Для обычной ситуации – присутствие или отсутствие гена RHD – этот способ прекрасно работает, но он не позволяет отличить Rh+ гомо- и гетерозигот, поэтому его используют как скрининговый – простой и недорогой метод для первичного обследования. Однако в случае частичной делеции RHD или различных мутаций он срабатывает неправильно. При проверке работы четырех разных наборов реагентов для биохимического анализа крови на резус на 500 образцах для 2% образцов были получены неоднозначные результаты. После генетического тестирования оказалось, что именно эти образцы имели генотип Partial D или Weak D.
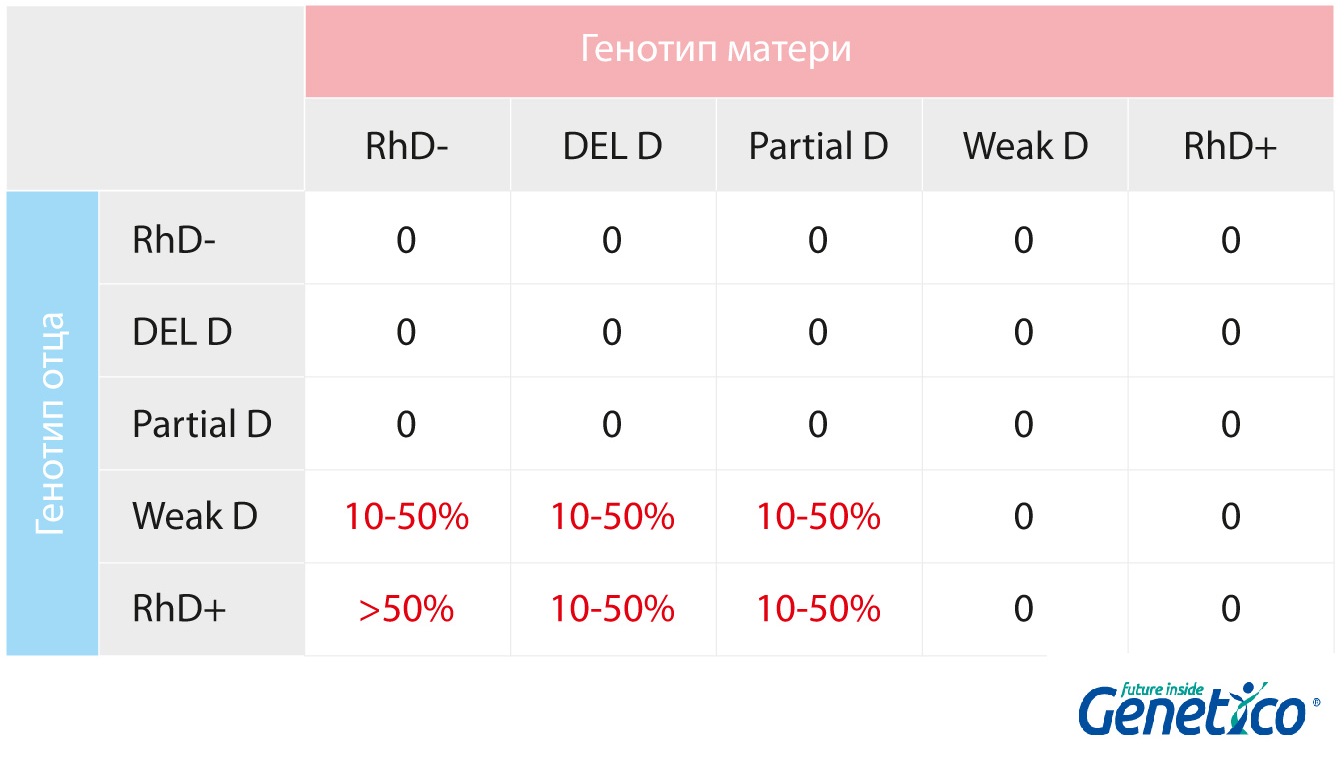
Примерные оценки вероятности развития резус-конфликта при разных сочетаниях генотипов родителей:
Опасность неправильного определения резус-статуса в сложных ситуациях заключается в том, что пара не будет подозревать о рисках, пока не возникнет опасная для жизни и здоровья малыша ситуация. Важно понимать, что главной проблемой при резус-конфликте является то, что организм матери не знаком с антигеном D как с нормальным, «своим», поэтому клетки, отмеченные этим антигеном, начинают отторгаться. При этом иммунная система может познакомиться с этим антигеном как со «своим» даже если этого антигена на поверхности клеток совсем немного, настолько немного, что биохимические методы ставят статус Rh-. В таком случае тревога о возможности развития резус-конфликта у женщины с таким неверным биохимическим анализом будет ложной. С другой стороны, если такой неверный результат будет выдан будущему отцу, то это может привести к развитию резус-конфликта, так как несмотря на биохимически отрицательный резус, ген RHD у отца присутствует и антиген D на поверхности клеток тоже есть. Таким образом, наиболее точный результат получается в результате генетического анализа гена RHD и гена RHCE, методом MLPA. Он позволит идентифицировать наличие/отсутствие гена RHD у будущих родителей, идентифицировать особые состояния этого гена, выявить гомо/гетерозиготность каждого партнера по этим показателям и более эффективно оценить не только вероятность развития резус-конфликта, но и целесообразность различных превентивных или терапевтических мер по устранению этого осложнения при беременности.
Важно помнить, что эти необычные ситуации все же редкость, и в большинстве случаев простой биохимический анализ крови дает верный результат. То есть после него резус-положительные женщины чаще всего спокойно беременеют вне зависимости от генотипа мужа по гену RHD, у резус-отрицательных женщин с резус-отрицательным партнером в большинстве случаев также нет проблем, а резус-отрицательные будущие мамы с резус-положительным отцом отправляются на дополнительные анализы для оценки рисков. Однако, к сожалению, вероятность несовпадения биохимического результата и истинного фенотипа, хоть и мала, но присутствует и может привести к катастрофическим для семьи результатам. Самое безопасное решение – узнать свой генотип по этим генам, который позволит совершенно точно узнать о том, есть ли повод для беспокойства.
Могут ли измениться группа крови и резус-фактор в течение жизни?
Чтобы разобраться, могут ли у человека измениться резус-фактор и группа крови, проясним сначала, что означают эти термины.
Группа крови определяется в зависимости от наличия на поверхности красных клеток крови (эритроцитов) двух видов молекул-антигенов, условно обозначаемых буквами А и В. Выделяют 4 группы крови в зависимости от того, есть оба антигена, есть какой-либо один из них или же нет обоих: О (I), А (II), В (III), АВ (IV).
Резус-фактор – качественная характеристика крови, которая определяется наличием D-антигена в организме человека. Если он есть – резус-фактор будет положительным, если нет, соответственно, отрицательным.
Казалось бы, все просто: антиген в организме или есть, или его нет. Обе характеристики врожденные. Но почему же меняются результаты анализов?
Дело в том, что анализы на определение группы крови проводят, наблюдая за склеиванием эритроцитов (агглютинацией). Капли крови капают в сыворотки, в которых содержатся антитела α, β, α + β, и наблюдают в микроскоп, в каких случаях эритроциты склеиваются.
Однако при некоторых инфекционных заболеваниях в кровь выделяется фермент, который отщепляет часть антигена А, и последний становится похож на антиген В. В этот момент анализ может показать неверный результат. То есть на самом деле не изменяется состав крови, а всего лишь искажается ее реакция на стандартные анализы. После выздоровления картина станет прежней.
Привести к похожим результатам могут и болезни, при которых усиливается выработка эритроцитов. В этом случае антигенов А и В в пробирке останется ничтожно мало, и реакция с их участием просто будет незаметна. При беременности в организме женщины тоже наблюдается интенсивный синтез эритроцитов, поэтому сделанные в этот период анализы также могут показать «смену» группы крови.
То же самое касается и резус-фактора: за него также отвечают белки, находящиеся на оболочке эритроцитов.
В случае «смены» резус-фактора возможно еще одно объяснение: наличие в крови белков, которые при ряде условий могут проявлять те же качества, что и положительный резус-фактор. Что опять-таки приводит к неверной интерпретации результатов анализов.
Другие возможные случаи «смены» группы крови и резус-фактора
Теоретически изменение группы крови возможно при трансплантации костного мозга. Причем собственный костный мозг реципиента в этом случае должен погибнуть полностью, а группа крови донора должна быть другой.
Однако на практике это маловероятно. Дело в том, что антигенные профили донора и реципиента должны быть близки. В противном случае пересадка приведет к тому, что лимфоциты донора будут проявлять агрессию к тканям организма реципиента (так называемая реакция «Трансплантант против хозяина»). А это может привести к смертельному исходу.
Встречаются также упоминания об исследованиях, зафиксировавших изменение резус-фактора при пересадке печени и селезенки. Однако серьезных доказательств в подтверждение этой теории пока что не существует.
Таким образом, мы можем сделать вывод, что все случаи «изменения» группы крови и резус-фактора в течение жизни – это на самом деле ошибочные результаты анализов. В реальности же эти показатели измениться у человека не могут.
 masterok
masterok
Мастерок.жж.рф
Хочу все знать
Кто же не знает, что у людей существуют четыре основные группы крови. Первая, вторая и третья встречаются довольно часто, четвёртая распространена не столь широко. Эта классификация основана на содержании в крови так называемых агглютиногенов — антигенов, ответственных за образование антител.
Группу крови чаще всего определяет наследственность, например если у родителей вторая и третья группы, у ребёнка может быть любая из четырёх, в случае, когда у отца и матери первая группа, у их детей также будет первая, а если, скажем, у родителей четвёртая и первая, у чада будет либо вторая, либо третья.
Однако, в некоторых случаях дети рождаются с группой крови, которой по правилам наследования у них быть не может — это явление называется бомбейский феномен, или бомбейская кровь.
В пределах систем групп крови ABO/Резус, которые используются для классификации большинства типов крови, существует несколько редких типов крови. Самый редкий – AB-, этот тип крови наблюдается менее чем у одного процента населения земли. Типы B- и O- также очень редкие, на каждый из них приходится менее 5% населения земли. Однако помимо этих двух основных есть более 30 общепризнанных систем определения группы крови, включающих множество редких типов, некоторые из которых наблюдаются совсем у небольшой группы людей.
Тип крови определяется по наличию в крови определенных антигенов. Антигены A и B очень распространены, что облегчает классификацию людей в зависимости от того какой антиген у них присутствует, тогда как у людей с типом крови O нет ни того ни другого антигена. Положительный или отрицательный знак после группы означает наличие или отсутствие резус-фактора. В то же время, помимо антигенов A и B возможно присутствие и других антигенов, и эти антигены могут вступать в реакцию с кровью определенных доноров. Например, у кого-то может быть группа крови A+, и при этом в крови отсутствует другой антиген, что говорит о вероятности неблагоприятной реакции с донорской кровью группы A+, содержащей этот антиген.
В бомбейской крови нет антигенов A и B, поэтому её часто путают с первой группой, однако нет в ней и антигена H, что может стать проблемой, например, при определении отцовства — ведь у ребёнка в крови не присутствуют ни одного антигена, которые есть у его из родителей.
Редкая группа крови не доставляет её обладателю никаких проблем, кроме одной — если ему вдруг понадобится переливание крови, то использовать можно только такую же бомбейскую, причём эту кровь можно переливать человеку с любой группой без каких-либо последствий.
Первые сведения об этом явлении появились в 1952 году, когда индийский врач Вхенд, проводя анализы крови в семье пациентов, получил неожиданный результат: у отца была 1 группа крови, у матери II, а у сына — III. Он описал этот случай в крупнейшем медицинском журнале «Ланцет». Впоследствии некоторые врачи сталкивались с подобными случаями, но объяснить их не могли. И только в конце XX столетия ответ был найден: оказалось, что в подобных случаях организм одною из родителей мимикрирует (подделывается) под 1 группу крови, в то время как на самом деле имеет другую, в формировании группы крови участвуют два гена: один определяет группу крови, второй кодирует выработку фермента, который позволяет реализоваться этой группе. У большинства людей эта схема работает, но в редких случаях второй ген отсутствует, стало быть, и фермента нет. Тогда наблюдается такая картина: человек имеет, например. III группу крови, но реализоваться она не может, и анализ выявляет II. Ребенку же такой родитель передает свои гены — отсюда и появляется у ребенка «необъяснимая» группа крови. Носителей такой мимикрии немного — менее 1% населения Земли.
Бомбейский феномен был открыт в Индии, где «особенной» кровью обладают, согласно статистике, 0,01% населения, в Европе бомбейская кровь встречается ещё реже — примерно у 0,0001% жителей.
А теперь еще немного подробнее :
Генов, отвечающих за группу крови, бывает три вида – А, В, и 0 (три аллеля).
Каждый человек имеет два гена группы крови – один, полученный от матери (А, В, или 0), и второй, полученный от отца (А, В, или 0).
Возможно 6 комбинаций:
| гены | группа |
| 00 | 1 |
| 0А | 2 |
| АА | |
| 0В | 3 |
| ВВ | |
| АВ | 4 |
Как это работает (с точки зрения биохимии клетки)
На поверхности наших эритроцитов имеются углеводы – «антигены Н», они же «антигены 0». (На поверхности эритроцитов имеются гликопротеины, обладающие антигенными свойствами. Они называются агглютиногены.)
Ген А кодирует фермент, который превращает часть антигенов Н в антигены А. (Ген А кодирует специфическую гликозилтрансферазу, которая присоединяет остаток N-ацетил-D-галактозамина к агглютиногену, при этом получается агглютиноген А).
Ген В кодирует фермент, который превращает часть антигенов Н в антигены В. (Ген В кодирует специфическую гликозилтрансферазу, которая присоединяет остаток D-галактозы к агглютиногену, при этом получается агглютиноген В).
Ген 0 не кодирует никакого фермента.
В зависимости от генотипа, углеводная растительность на поверхности эритроцитов будет выглядеть так:
| гены | специфические антигены на поверхности эритроцитов | группа крови | буквенное обозначение группы |
| 00 | — | 1 | 0 |
| А0 | А | 2 | А |
| АА | |||
| В0 | В | 3 | В |
| ВВ | |||
| АВ | А и В | 4 | АВ |
Скрестим для примера родителей с 1 и 4 группами и посмотрим, почему у них не может быть ребёнка с 1 группой.
(1 группа)
(Потому что ребенок с 1 группой (00) должен получить по 0 от каждого родителя, но у родителя с 4 группой крови (АВ) нет 0.)
Бомбейский феномен
Возникает в том случае, если у человека на эритроцитах не образуется «исходного» антигена Н. В таком случае человек не будет иметь ни антигенов А, ни антигенов В даже при наличии необходимых ферментов. Ну, придут великие и могучие ферменты превращать Н в А… опа! а превращать-то нечего, аша нету!
Исходный антиген Н кодируется геном, который немудрёно обозначается Н.
Н – ген, кодирующий антиген Н
h – рецессивный ген, антиген Н не образуется
Пример: человек с генотипом АА должен иметь 2 группу крови. Но если он будет ААhh, то группа крови у него будет первая, потому что антиген А не из чего сделать.
Впервые эта мутация была обнаружена в Бомбее, осюда и название. В Индии она встречается у одного человека из 10 000, на Тайване – у одного из 8 000. В Европе hh встречается очень редко – у одного человека из двухсот тысяч (0,0005%).
Пример работы бомбейского феномена №1: если один родитель имеет первую группу крови, а другой – вторую, то ребенок не может иметь четвёртую группу, потому что ни у одного из родителей нет необходимого для 4 группы гена В.
(1 группа)
(1 группа)
(2 группа)
А теперь бомбейский феномен:
(1 группа)
(2 группа)
Фокус в том, что первый родитель, несмотря на свои гены ВВ, не имеет антигенов В, потому что их не из чего делать. Поэтому, не смотря на генетическую третью группу, с точки зрения переливания крови группа у него первая.
Пример работы бомбейского феномена №2. Если оба родителя имеют 4 группу, то у них не может получиться ребенок 1 группы.
(4 группа)
А теперь бомбейский феномен
(4 группа)
(4 группа)
(1 группа)
(3 группа)
Как видим, при бомбейском феномене у родителей с 4 группой всё-таки может получиться ребенок с первой группой.
Цис-положение А и В
У человека с 4 группой крови во время кроссинговера может произойти ошибка (хромосомная мутация), когда в одной хромосоме окажутся оба гена – и А, и В, а в другой хромосоме не будет ничего. Соответственно, и гаметы у такого АВ получатся странные: в одной будет АВ, а в другой – ничего.
| Что могут предложить другие родители | Родитель-мутант | ||||||||||||||||||
| АВ | — | ||||||||||||||||||
| 0 | АВ0 Конечно же, хромосомы, содержащие АВ, и хромосомы, не содержащие совсем ничего, будут выбраковываться естественным отбором, т.к. они будут с трудом конъюгировать с нормальными, немутантными хромосомами. Кроме того, у детей ААВ и АВВ может наблюдаться генный дисбаланс (нарушение жизнеспособности, гибель зародыша). Вероятность встретить мутацию цис-АВ оценивается примерно в 0,001% (0,012% цис-АВ относительно всех АВ). Пример цис-АВ. Если один родитель имеет 4 группу, а другой первую, то у них не могут получиться дети ни 1, ни 4 группы.
| ||||||||||||||||||
 masterok
masterok 










