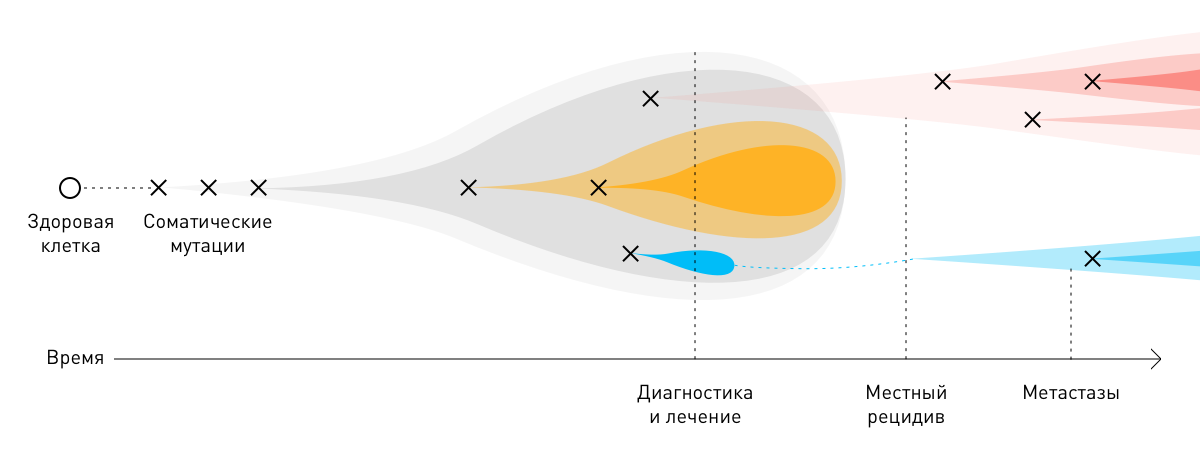
Соматические мутации в опухоли
Мутация — любое изменение в молекуле ДНК либо структуре хромосом. Изменения, которые происходят в гаметах — половых клетках, называют герминальными, в любых других клетках организма — соматическими. Герминальные мутации передаются от родителей по наследству в виде генетических заболеваний. Соматические изменения не наследуются, а возникают в результате внешних воздействий (курения, радиоактивного излучения и других).
Доказано, что злокачественные опухоли в 90–95 % случаев возникают в результате соматических мутаций (спорадический рак). Наследственный рак, развивающийся в результате герминальных изменений, составляет 5–10 % от всех случаев заболевания.
Клеточные механизмы возникновения рака: протоонкогены и онкосупрессоры
Соматические мутации увеличивают шанс превращения здоровых клеток в раковые за счет активации онкогенов — генов, стимулирующих образование злокачественных опухолей. Онкогены образуются из обычных генов — протоонкогенов.
Деление клеток опухоли и разрастание опухолевой ткани тормозят антионкогены — гены-супрессоры. Протоонкогены и гены-супрессоры образуют систему стимуляции и подавления злокачественного процесса.
В подавляющем большинстве случаев раковые опухоли возникают из одной клетки в результате двух последовательных мутаций: первичной (герминальной) и вторичной (соматической). Для развития новообразования достаточно 3–6 таких повреждений. Вызванные ими изменения постепенно накапливаются в ДНК, вызывают неконтролируемое размножение пораженных клеток и образование атипичных тканей.
Драйверные соматические мутации и их использование для лечения злокачественных опухолей
В этиологии опухолей изменения в клетках вызывают ошибки копирования ДНК при делении — соматические драйверные мутации. В одних органах и тканях стволовые клетки делятся чаще, чем в других. В них злокачественные новообразования образуются чаще, чем в других структурах организма. По данным международного агентства по исследованию рака IARC, риск заболеть раком, а также выживаемость раковых клеток на 70–80 % зависят от интенсивности деления стволовых клеток и увеличиваются с возрастом.
Генетические маркеры опухолей (изменения в структуре белков в результате соматических драйверных мутаций) можно использовать как мишень и прицельно блокировать с помощью фармакологических препаратов. На этом принципе основан один из наиболее результативных современных методов лечения рака — таргетная терапия. Она позволяет:
Выявление драйверных соматических мутаций для диагностики злокачественных опухолей
Чем больше генетических маркеров известно, тем более адекватно подбирается лечение. Для выявления соматических мутаций при диагностике злокачественных опухолей используют следующие методики:
Целесообразность использования того или иного метода в каждом конкретном случае определяет врач.
Соматические мутации опухолей: влияние на диагностику и лечение
В процессе роста злокачественные новообразования приспосабливаются к факторам онкологического лечения — лучевой, химио- и иммунотерапии. Молекулы онкологических клеток, выжившие после того или иного лечебного этапа, нередко мутируют. Соматические мутации опухолей способствуют прогрессированию болезни и её более агрессивному (рецидивирующему и метастатическому) течению. Из-за индивидуальных различий на молекулярном уровне общеклинические стратегии лечения того или иного вида рака могут быть неэффективны для отдельных пациентов.
Чтобы максимально снизить риск рецидивов, улучшить качество жизни больных и увеличить её продолжительность, соматические мутации в опухолях в ответ на фармако- и химиотерапию необходимо учитывать. Для их выявления разработан инновационный метод исследования — молекулярное профилирование. Результаты этого вида диагностики позволяют врачу назначать наиболее оптимальное персонализированное лечение.
Ваши гены сломаны: что нужно знать каждой о раке груди?
Как рак груди связан с мутациями в генах? Что делать, если эти мутации есть у вас или кого-то из близких родственников? Рассказал маммолог-онколог, профессор, экс-главный маммолог страны Леонид Путырский.
Почему возникает рак груди?
— Причин очень много. Но можно выделить 6 основных групп:
Мутации каких генов вызывают рак груди?
— Как правило, основных мутаций две – генов BRCA1 и BRCA2. Они продуцируют белки и восстанавливают ДНК в случае ее повреждения внешними факторами. Если у человека происходит нарушение в ДНК, из-за мутации оно не восстанавливается. «Поломки» накапливаются и могут появиться клетки, которые приведут к злокачественным образованиям в молочной железе, яичниках, а у мужчин в предстательной железе.
Можно ли снизить риск передачи этой мутации детям?
— Нет такого средства или способа, чтобы точно не передать эту «поломку». Как мы уже говорили, она передается в 50% случаев. Маме, которая знает, что у нее есть мутация в гене, нужно потом объяснить дочке, что нужно тщательно следить за своим здоровьем. Если эту мутацию у девочки обнаружили — не нужно паниковать. Нужно посоветоваться с грамотным специалистом-онкологом. Наличие мутации не всегда приводит к развитию рака.
Рак в генетическом коде человека будет всегда и у всех последующих поколений?
— Если ген с мутацией не передался по наследству детям, то на этом этапе передача мутации прекратится. Но онкологические заболевания могут возникнуть и без учета наследственных факторов — про это тоже не нужно забывать и учитывать факторы, которые на это влияют.
Насколько высока вероятность заболеть раком груди, если есть мутации в генах BRCA1 и BRCA2?
— В мире 5-10% всех случаев рака молочной железы и 20% рака яичников связаны именно с мутацией гена BRCA1.
Мужчины могут быть носителями мутаций в этих генах, но они реже проявляются клинически. На 100 заболевших раком молочной железы женщин приходится 1 заболевший мужчина.
Можно ли обнаружить эти мутации заранее?
— Чтобы исследовать мутации, берут анализ крови. Или делают биопсию опухолевой ткани, если она уже появилась. Сейчас есть лаборатории, в которых любой желающий может пройти платное исследование на мутации в генах BRCA1 и BRCA2. Но нужно ли это делать — вопрос спорный.
С другой стороны — обнаружение мутации в генах BRCA1 и BRCA2 позволяет правильно выбрать тактику лечения для пациентов, у которых опухоль уже появилась. Есть таргетные препараты, которые эффективно воздействуют на BRCA-ассоциированные опухоли. Также эта информация помогает планировать профилактику и наблюдение для людей, у которых симптомов заболевания еще нет. Таким пациентам нужно чаще проходить обследования, чтобы выявить опухоль на ранней стадии, если она возникнет.
Кому показано обследоваться на мутации?
— Обычно назначают обследования на мутации в генах тем, у кого:
Как часто нужно посещать маммолога?
— Сейчас рак молодеет. Нужно, чтобы молодые девушки уже с 20 лет делали самостоятельный осмотр груди не реже раза в месяц. И сразу при обнаружении каких-то уплотнений, выделений, деформаций неотложно приходили к специалисту.
До 40 лет рекомендуют посещать маммолога раз в год. Можно периодически делать УЗИ и МРТ молочных желез. После 40 приходить к маммологу желательно раз в полгода.
Мужчинам — носителям мутации рекомендуется с 35 лет проходить ежегодное обследование грудных желез.
С 40 лет можно делать обследование предстательной железы. Профилактика поможет не только диагностировать заболевание на ранней стадии, но и снизить вероятность неблагоприятных исходов.
Нужно ли для профилактики удалять молочные железы женщинам, у которых есть мутации в генах BRCA1 и BRCA2
и высок риск развития рака груди?
— Сейчас есть такая тенденция. Женщины, у которых есть мутация в генах, рожают детей, выкармливают их и профилактически удаляют молочные железы. Ведущие маммологи против такого способа, потому что удаление здорового органа – это неправильный путь. При мутациях в BRCA1 и BRCA2 рак может появиться и в яичниках, и в кишечнике, и в предстательной железе. По такой логике получается, что все это тоже нужно профилактически удалить?
Злокачественные опухоли и их метастазы не только растут, но и активно изменяются независимо друг от друга
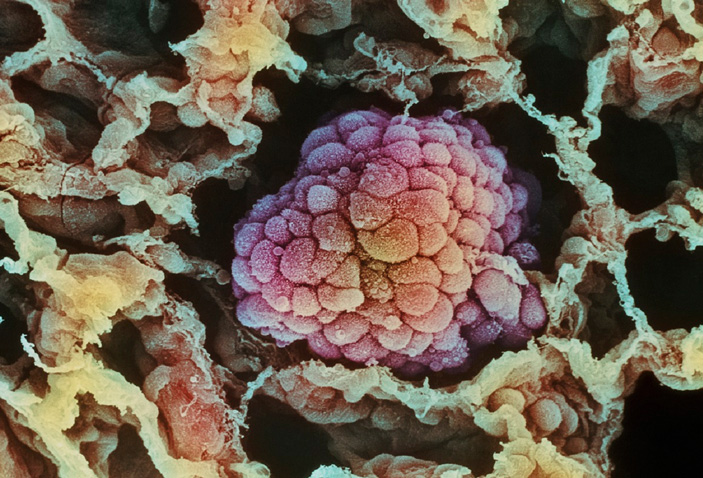
Рис. 1. Электронная микрофотография раковой опухоли легкого на ранней стадии роста. Изображение из журнала National Geographic
Одна из самых важных задач при лечении злокачественных опухолей — борьба с метастазами. Существование непролеченных метастаз может свести на нет все успехи в лечении онкологического заболевания. Особенно осложняет ситуацию то, что первичная опухоль и метастазы могут иметь разную чувствительность к тем или иным препаратам, в результате чего лекарства, которые хорошо справляются с первичной опухолью, могут оказаться бессильны против метастаз, и наоборот. Поэтому одной из важных областей онкологии является изучение процесса метастазирования, его молекулярных и генетических механизмов. В том числе, многое может дать поиск мутаций, общих для раковых опухолей и их метастазов. Тщательное исследование таких мутаций позволит найти эффективные методы диагностики и лечения рака.
Распространение клеток первичной опухоли в другие органы и ткани организма и их размножение там (метастазирование) является наиболее опасным процессом с точки зрения лечения злокачественных опухолей. Клетки первичной опухоли, возникшей в каком-либо органе, отделяются от опухоли и переносятся с током крови, лимфы, цереброспинальной жидкости (по каналу между головным и спинным мозгом) в другие органы и ткани и образуют там метастазы — вторичные опухоли. Метастазирование свойственно многим типам рака. Однако простым переносом и размножением клеток в местах новой дислокации процесс не ограничивается: клетки опухоли и метастазов продолжают активно изменяться. В частности, об этом свидетельствуют результаты двух недавно опубликованных работ.
В первой из них была исследована медуллобластома — наиболее часто встречающаяся у детей форма рака мозга. Большая группа исследователей (Wu et al.) из Канады, США и Европы провела детальное исследование медуллобластомы и ее метастазов на мышах и на аналогичном материале от больных. С помощью мутагена-транспозона «спящая красавица» (Sleeping Beauty, SB) авторы ввели случайные мутации в клетки-предшественники головного мозга мышей.
Транспозон — один из так называемых мобильных элементов генома, он может самопроизвольно покинуть занимаемое место в ДНК и случайным образом внедриться в другой участок генома. Если точка внедрения — это ген, кодирующий какой-либо белок, его структура или работа могут быть нарушены. В результате возникает мутация. Современные методы исследования позволяют определить локализацию возникших мутаций. Таким образом, появляется возможность связать изменения в развитии и метастазировании опухолей с теми или иными белками.
Полученную линию мышей скрестили с двумя другими линиями, уже предрасположенными к возникновению опухолей мозга. В итоговой линии резко возросла частота возникновения медуллобластом, сократился период их возникновения. В отличие от родительских линий, у которых опухоли обычно четко локализованы, у гибридов происходило распространение клеток опухоли через цереброспинальную жидкость, и метастазы образовывались в тех же участках оболочки головного и спинного мозга, что и у больных.
С помощью новых методов широкомасштабного секвенирования — определения последовательности нуклеотидов ДНК — авторы смогли проследить точки внедрения транспозона SB и идентифицировали много генов, которые могут быть вовлечены в образование опухоли. Удалось найти ряд новых генов, связанных с медуллобластомой.
Полученные модели позволили проследить мутации, имеющиеся как в первичных опухолях, так и в метастазах. К удивлению исследователей, оказалось, что, как правило, только немногие мутации были общими для первичных опухолей и метастазов каждой исследованной мыши. В то же время, набор мутаций в различных метастазах был очень сходным. Аналогичные результаты дали также анализ распределения метилированных динуклеотидов CpG (см. CpG site), с которым обычно связано подавление активности генов, и анализ потерь и увеличения количества копий различных участков генома. Эти же закономерности наблюдались и у пациентов, больных медуллобластомой: существенные генетические различия первичной опухоли и метастазов, гораздо большее сходство метастазов между собой, чем с первичной опухолью. Тем не менее, требуются дополнительные исследования с целью установить, насколько сходны биологические свойства и клинические характеристики медуллобластомы и ее метастазов у человека и мыши.
Авторы приходят к выводу, что образовывать метастазы способны лишь некоторые клетки опухоли на ранней стадии ее развития (ранняя опухоль). Затем и в первичной опухоли, и в метастазах независимо накапливаются новые мутации. Наиболее важный с практической точки зрения вопрос, возникающий по результатам этой работы, таков: в какой мере генетические различия первичной опухоли и метастазов приведут к различиям в чувствительности их к средствам противораковой терапии? Авторы приводят данные, свидетельствующие о том, что она может быть различна. Мутации некоторых генов, идентифицированные авторами, могут нарушать пути метаболизма и передачи сигналов, и эти пути могут служить мишенями для эффективной терапии. Таких мутаций оказалось довольно много, и еще предстоит определить, какие из них существенны для развития опухоли, насколько часто такие мутации возникают в опухолях человека, в какой мере они помогут определить возможные мишени для терапии. Разумеется, наиболее эффективными мишенями будут общие для первичной опухоли и метастазов.
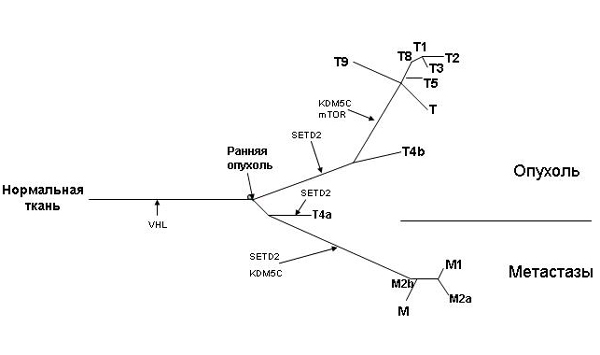
Другая группа исследователей (Gerlinger et al.) провела широкомасштабное секвенирование экзомов (см. exome sequencing) ДНК, выделенной из первичных опухолей метастазирующего рака почки человека и их метастазов. Экзом (см. exome) представляет собой набор фрагментов генома, кодирующих белки (эти фрагменты называются «экзоны») и другие функционально важные продукты (рибосомные РНК, транспортные РНК). Примерно 20 000 генов человека включают в себя
200 000 экзонов, занимающих
1,5% генома. Набор мутаций в различных участках опухолей оказался весьма различным, а в метастазах он отличался еще больше. Авторы построили филогенетическое дерево различных частей опухолей и метастазов.
Филогенетическое дерево дает графическое представление об эволюции: его «листья» соответствуют состоянию различных частей опухолей и метастазов в момент исследования, они «растут» из общего корня — первичной опухоли.
Метастазы «ответвлялись» от первичных опухолей довольно рано, а затем и опухоли, и метастазы эволюционировали независимо друг от друга, накапливая различные мутации. Только 30–37% мутаций оказались общими для всех секвенированных проб. Гетерогенность опухолей подтвердили также данные количественного анализа профилей мРНК, соответствующих большому количеству генов (этот параметр показывает, насколько сильно экспрессируется тот или иной ген), и данные по дисбалансу аллелей: пары хромосом из клеток разных частей опухолей содержали разное количество копий определенных участков ДНК. Неожиданной оказалась находка на разобщенных ветвях филогенетического дерева независимо возникших, но аналогичных друг другу мутаций. То есть, несмотря на генетическую дивергенцию в процессе прогресса опухоли, происходила также фенотипическая конвергенция — независимое появление сходных признаков.
Рис. 2. Филогенетическое дерево злокачественной опухоли почки и ее метастазов.Т — различные области опухоли, М — различные метастазы. Длина ветвей пропорциональна накоплению различающихся мутаций. Стрелками с названиями генов обозначены независимо возникшие «конвергентные» мутации в этих генах. Изображение из обсуждаемой статьи в The New England Journal of Medicine, с изменениями
Полученные результаты свидетельствуют, что анализ геномов из отдельных образцов опухоли может быть недостаточен для оценки всего набора мутаций. В то же время реконструкция филогенетического дерева опухоли позволит найти «стволовые» мутации — то есть те, которые возникли на ранних стадиях развития опухоли и были унаследованы всеми или многими частями зрелой опухоли и метастазами. Это позволит найти информативные маркеры для диагностики рака и определить наиболее эффективные пути терапии.
С практической точки зрения результаты обоих исследований означают, что для эффективной терапии рака следует тщательно и индивидуально анализировать опухоли и метастазы с помощью современных методов, подбирать средства, воздействующие на различные пути метаболизма и передачи сигналов. Это сложная и дорогостоящая работа.
Источники:
1) Xiaochong Wu, Paul A. Northcott, Adrian Dubuc, et al. Clonal selection drives genetic divergence of metastatic medulloblastoma // Nature. 2012. V. 482. P. 529–533.
2) Marco Gerlinger, Andrew J. Rowan, Stuart Horswell, et al. Intratumor heterogeneity and branched evolution revealed by multiregion sequencing // The New England Journal of Medicine. 2012. V. 366. P. 883–892.
Генная терапия против рака
иллюстрация автора статьи
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Благодаря стремительному развитию медицины создаются инновационные техники, лекарства, оборудование, направленные на лечение сложных заболеваний, таких как рак. В последнее время большое внимание уделяется генной терапии как перспективному методу лечения онкозаболеваний, который в будущем станет особо важным инструментом для предотвращения и снижения смертности от рака. В данной статье кратко рассматриваются пути развития болезни, а также применение инновационных техник генной терапии в онкологии.
Конкурс «био/мол/текст»-2014
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2014 в номинации «Лучший обзор».
Главный спонсор конкурса — дальновидная компания «Генотек».
Конкурс поддержан ОАО «РВК».
Спонсором номинации «Биоинформатика» является Институт биоинформатики.
Спонсором приза зрительских симпатий выступила фирма Helicon.
Свой приз также вручает Фонд поддержки передовых биотехнологий.
Смертельные клешни
Человечество столкнулось с этой загадочной болезнью еще до нашей эры. Ее пытались понять и лечить ученые мужи в самых различных уголках мира: в Древнем Египте — Еберс, в Индии — Сушрута, Греции — Гиппократ. Все они и многие другие медики вели борьбу с опасным и серьезным противником — раком. И хоть эта битва продолжается до сих пор, сложно определить, есть ли шансы на полную и окончательную победу. Ведь чем больше мы изучаем болезнь, тем чаще возникают вопросы — можно ли полностью излечить рак? Как избежать болезни? Можно ли сделать лечение быстрым, доступным и недорогим?
Благодаря Гиппократу и его наблюдательности (именно он увидел сходство опухоли и щупалец рака) в древних врачебных трактатах появился термин «карцинома» (грец. carcinos), или «рак» (лат. cancer). В медицинской практике по-разному классифицируют злокачественные новообразования: карциномы (из эпителиальных тканей), саркомы (из соединительной, мышечной тканей), лейкемия (в крови и костном мозге), лимфомы (в лимфатической системе) и другие (развиваются в других типах клеток, например, глиома — рак головного мозга). Но в быту более популярен термин «рак», который подразумевает любую злокачественную опухоль.
Мутации: погибнуть или жить вечно?
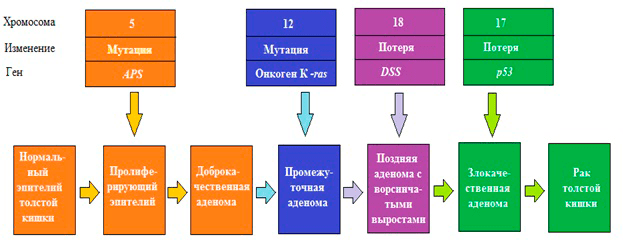
Многочисленные генетические исследования выявили, что возникновение раковых клеток — это результат генетических изменений. Ошибки в репликации (копировании) и репарации (исправлении ошибок) ДНК приводят к изменению генов, в том числе и контролирующих деление клетки. Основными факторами, которые способствуют повреждению генома, а в дальнейшем — приобретению мутаций, — являются эндогенные (атака свободных радикалов, образующихся в процессе обмена веществ, химическая нестабильность некоторых оснований ДНК) и экзогенные (ионизирующее и УФ-излучение, химические канцерогены). Когда мутации закрепляются в геноме, они способствуют трансформации нормальных клеток в раковые. Такие мутации в основном случаются в протоонкогенах, которые в норме стимулируют деление клетки. В результате может получиться постоянно «включенный» ген, и митоз (деление) не прекращается, что, фактически, означает злокачественное перерождение. Если же инактивирующие мутации происходят в генах, которые в норме ингибируют пролиферацию (гены-супрессоры опухолей), контроль над делением утрачивается, и клетка становится «бессмертной» (рис. 1).
Рисунок 1. Генетическая модель рака: рак толстой кишки. Первый шаг — потеря или инактивация двух аллелей гена АРS на пятой хромосоме. В случае семейного рака (familiar adenomatous polyposis, FAP) одна мутация гена АРС наследуется. Потеря обоих аллелей ведет к образованию доброкачественных аденом. Последующие мутации генов на 12, 17, 18 хромосомах доброкачественной аденомы могут привести к трансформации в злокачественную опухоль.
Очевидно, что развитие определенных видов рака включают в себя изменение большинства или даже всех этих генов и может проходить различными путями. Из этого следует, что каждую опухоль следует рассматривать как биологически уникальный объект. На сегодняшний день существуют специальные генетические информационные базы по раку, содержащих данные о 1,2 млн. мутаций из 8207 образцов тканей, относящихся к 20 видам опухолей: атлас Ракового Генома (Cancer Genome Atlas) и каталог соматических мутаций при раке (Catalogue of Somatic Mutations in Cancer, COSMIC) [2].
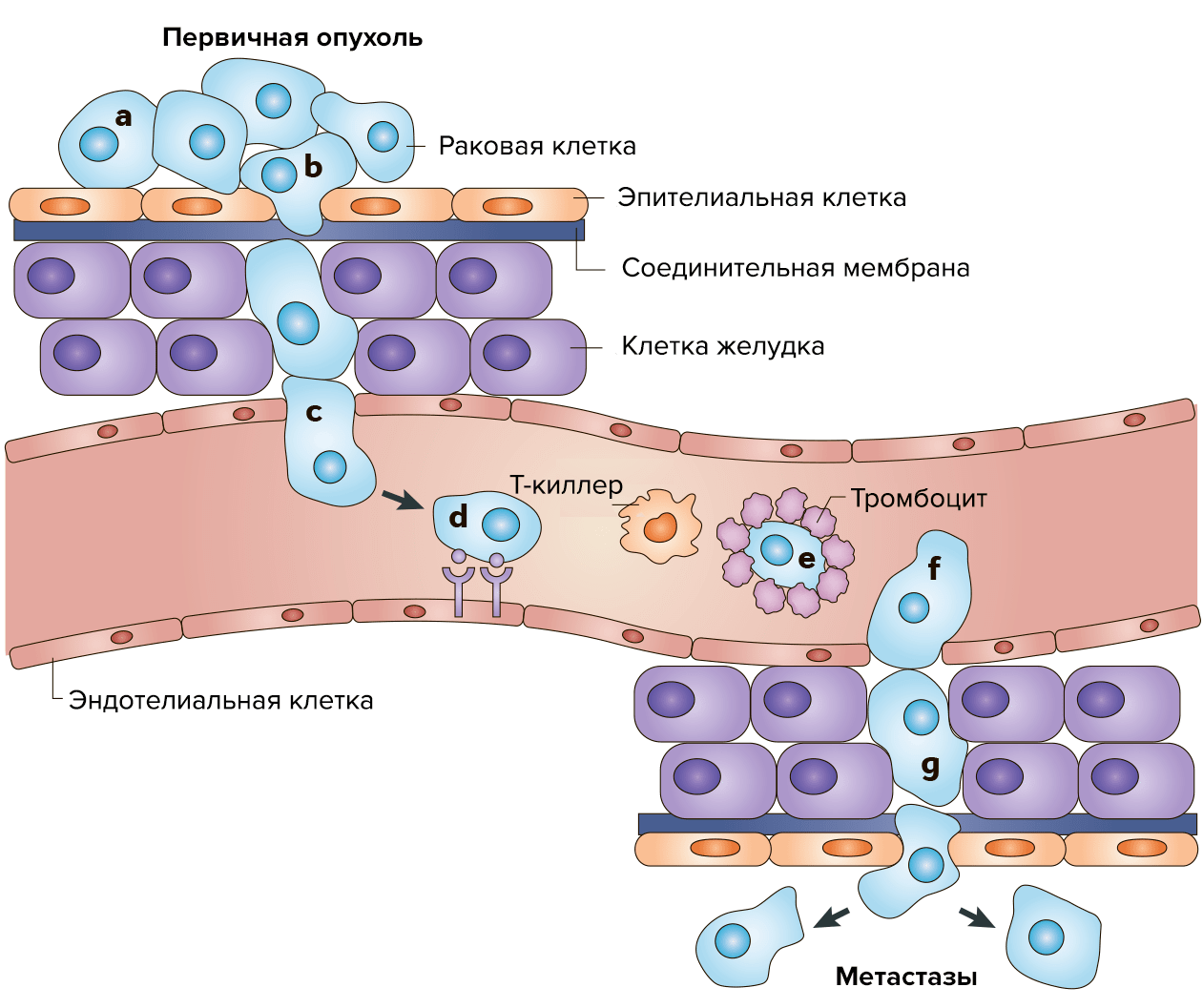
Результатом сбоя работы генов становится неконтролируемое деление клеток, а на последующих стадиях — метастазирование в различные органы и части тела по кровеносным и лимфатическим сосудам. Это достаточно сложный и активный процесс, который состоит из нескольких этапов. Отдельные раковые клетки отделяются от первичного очага и разносятся с кровью по организму. Затем с помощью специальных рецепторов они прикрепляются к эндотелиальным клеткам и экспрессируют протеиназы, которые расщепляют белки матрикса и образуют поры в базальной мембране. Разрушив внеклеточный матрикс, раковые клетки мигрируют вглубь здоровой ткани. За счет аутокринной стимуляции они делятся, образуя узел (1–2 мм в диаметре). При недостатке питания часть клеток в узле погибает, и такие «дремлющие» микрометастазы могут достаточно долго оставаться в тканях органа в латентном состоянии. В благоприятных условиях узел разрастается, в клетках активируются ген фактора роста эндотелия сосудов (VEGF) и фактора роста фибробластов (FGFb), а также инициируются ангиогенез (формирование кровеносных сосудов) (рис. 2).
Рисунок 2. Распространение метастазов
Однако клетки вооружены специальными механизмами, защищающими от развития опухолей:
Традиционные методы и их недостатки
Если системы защиты организма не справились, и опухоль все-таки начала развиваться, спасти может только вмешательство медиков. На протяжении длительного периода врачами используются три основные «классические» терапии:
Вышеописанные подходы не всегда могут избавить больного от рака. Часто при хирургическом лечении остаются единичные раковые клетки, и опухоль может дать рецидив, а при химиотерапии и лучевой терапии возникают побочные эффекты (снижение иммунитета, анемия, выпадение волос и др.), которые приводят к серьезным последствиям, а часто и к смерти пациента. Тем не менее, с каждым годом улучшаются традиционные и появляются новые методы лечения, которые могут победить рак, такие как биологическая терапия, гормональная терапия, использование стволовых клеток, трансплантация костного мозга, а также различные поддерживающие терапии. Наиболее перспективной считается генная терапия, так как она направлена на первопричину рака — компенсацию неправильной работы определенных генов.
Генная терапия как перспектива
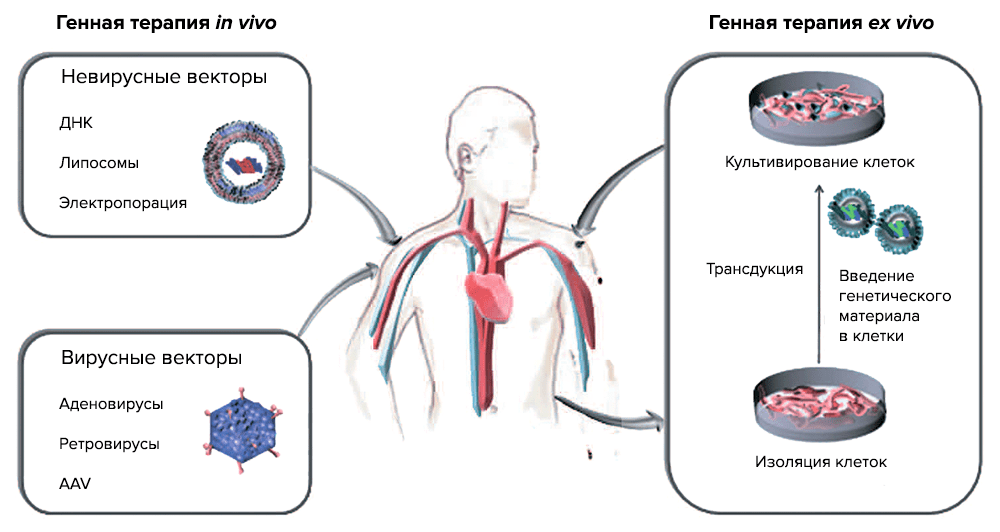
По данным PubMed, интерес к генной терапии (ГТ) раковых заболеваний стремительно растет, и на сегодняшний день ГТ объединяет ряд методик, которые оперируют с раковыми клетками и в организме (in vivo) и вне его (ex vivo) (рис. 3).
Рисунок 3. Две основные стратегии генной терапии. ex vivo — генетический материал с помощью векторов переносится в клетки, выращиваемые в культуре (трансдукция), а затем трансгенные клетки вводят реципиенту; in vivo — введение вектора с нужным геном в определенную ткань или орган.
Генная терапии іn vivo подразумевает перенос генов — введение генетических конструкций в раковые клетки или в ткани, которые окружают опухоль [9]. Генная терапия ex vivo состоит из выделения раковых клеток из пациента, встраивания терапевтического «здорового» гена в раковый геном и введения трансдуцированных клеток обратно в организм пациента. Для таких целей используются специальные векторы, созданные методами генной инженерии. Как правило, это вирусы, которые выявляют и уничтожают раковые клетки, при этом оставаясь безвредными для здоровых тканей организма, или невирусные векторы.
Вирусные векторы
В качестве вирусных векторов используют ретровирусы, аденовирусы, аденоассоциированные вирусы, лентивирусы, вирусы герпеса и другие. Эти вирусы отличаются по эффективности трансдукции, по взаимодействию с клетками (распознавание и заражение) и ДНК. Главным критерием является безопасность и отсутствие риска неконтролируемого распространения вирусной ДНК: если гены вставляются в неправильном месте генома человека, они могут создать вредные мутации и инициировать развитие опухоли. Также важно учитывать уровень экспрессии перенесенных генов, чтобы предотвратить воспалительные или иммунные реакции организма при гиперсинтезе целевых белков (табл. 1).
| Вектор | Краткое описание |
|---|---|
| Вирус кори (measles virus) | содержит отрицательную последовательность РНК, которая не вызывает защитного ответа в раковых клетках |
| Вирус простого герпеса (HSV-1) | может переносить длинные последовательности трансгенов |
| Лентивирус | производный от ВИЧ, может интегрировать гены в неделящиеся клетки |
| Ретровирус (RCR) | не способный к самостоятельной репликации, обеспечивает эффективное встраивание чужеродной ДНК в геном и постоянство генетических изменений |
| Обезьяний пенистый вирус (SFV) | новый РНК-вектор, который передает трансген в опухоль и стимулирует его экспрессию |
| Рекомбинантный аденовирус (rAdv) | обеспечивает эффективную трансфекцию, но возможна сильная иммунная реакция |
| Рекомбинантный аденоассоциированный вирус (rAAV) | способен к трансфекции многих типов клеток |
Невирусные векторы
Для переноса трансгенных ДНК также применяют невирусные векторы. Полимерные переносчики лекарственных средств — конструкции из наночастиц — используются для доставки препаратов с низкой молекулярной массой, например, олигонуклеотидов, пептидов, миРНК. Благодаря небольшим размерам, наночастицы поглощаются клетками и могут проникать в капилляры, что очень удобно для доставки «лечебных» молекул в самые труднодоступные места в организме. Данная техника часто используется для ингибирования ангиогенеза опухоли. Но существует риск накопления частиц в других органах, например, костном мозге, что может привести к непредсказуемым последствиям [11]. Самыми популярными невирусными методами доставки ДНК являются липосомы и электропорация.
Синтетические катионные липосомы в настоящее время признаны перспективным способом доставки функциональных генов. Положительный заряд на поверхности частиц обеспечивает слияние с отрицательно заряженными клеточными мембранами. Катионные липосомы нейтрализуют отрицательный заряд цепи ДНК, делают более компактной ее пространственную структуру и способствуют эффективной конденсации. Плазмидно-липосомный комплекс имеет ряд важных достоинств: могут вмещать генетические конструкции практически неограниченных размеров, отсутствует риск репликации или рекомбинации, практически не вызывает иммунного ответа в организме хозяина. Недостаток этой системы состоит в низкой продолжительности терапевтического эффекта, а при повторном введении могут появляться побочные эффекты [12].
Электропорация является популярным методом невирусной доставки ДНК, довольно простым и не вызывающим иммунного ответа. С помощью индуцированных электрических импульсов на поверхности клеток образуются поры, и плазмидные ДНК легко проникают во внутриклеточное пространство [13]. Генная терапия іn vivo с использованием электропорации доказала свою эффективность в ряде экспериментов на мышиных опухолях. При этом можно переносить любые гены, например, гены цитокинов (IL-12) и цитотоксические гены (TRAIL), что способствует развитию широкого спектра терапевтических стратегий. Кроме того, этот подход может быть эффективным для лечения и метастатических, и первичных опухолей [14].
Выбор техники
В зависимости от типа опухоли и ее прогрессии, для пациента подбирается наиболее эффективная методика лечения. На сегодняшний день разработаны новые перспективные техники генной терапии против рака, среди которых онколитическая вирусная ГТ, пролекарственная ГТ (prodrug therapy), иммунотерапия, ГТ с использованием стволовых клеток.
Онколитическая вирусная генная терапия
Для этой методики используются вирусы, которые с помощью специальных генетических манипуляций становятся онколитическими — перестают размножаться в здоровых клетках и воздействуют только на опухолевые. Хорошим примером такой терапии является ONYX-015 — модифицированный аденовирус, который не экспрессирует белок Е1В. При отсутствии этого белка вирус не может реплицироваться в клетках с нормальным геном p53 [15]. Два вектора, сконструированных на базе вируса простого герпеса (HSV-1) — G207 и NV1020 — также несут в себе мутации нескольких генов, чтобы реплицироваться только в раковых клетках [16]. Большим преимуществом техники является то, что при проведении внутривенных инъекций онколитические вирусы разносятся с кровью по всему организму и могут бороться с метастазами. Основные проблемы, которые возникают при работе с вирусами — это возможный риск возникновения иммунного ответа в организме реципиента, а также неконтролируемое встраивание генетических конструкций в геном здоровых клеток, и, как следствие, возникновение раковой опухоли.
Геноопосредованная ферментативная пролекарственная терапия
Базируется на введении в опухолевую ткань «суицидных» генов, в результате работы которых раковые клетки погибают. Данные трансгены кодируют ферменты, активирующие внутриклеточные цитостатики, ФНО-рецепторы и другие важные компоненты для активации апоптоза. Суицидная комбинация генов пролекарства в идеале должна соответствовать следующим требованиям [17]: контролируемая экспрессия гена; правильное превращение выбранного пролекарства в активное противораковое средство; полная активация пролекарства без дополнительных эндогенных ферментов.
Минус терапии состоит в том, что в опухолях присутствуют все защитные механизмы, свойственные здоровым клеткам, и они постепенно адаптируются к повреждающим факторам и пролекарству. Процессу адаптации способствует экспрессия цитокинов (аутокринная регуляция), факторов регуляции клеточного цикла (отбор самых стойких раковых клонов), MDR-гена (отвечает за восприимчивость к некоторым медикаментам).
Иммунотерапия
Благодаря генной терапии, в последнее время начала активно развиваться иммунотерапия — новый подход для лечения рака с помощью противоопухолевых вакцин. Основная стратегия метода — активная иммунизация организма против раковых антигенов (ТАА) с помощью технологии переноса генов [18].
Главным отличием рекомбинантных вакцин от других препаратов является то, что они помогают иммунной системе пациента распознавать раковые клетки и уничтожать их. На первом этапе раковые клетки получают из организма реципиента (аутологичные клетки) или из специальных клеточных линий (аллогенные клетки), а затем выращивают их в пробирке. Для того чтобы эти клетки могли узнаваться иммунной системой, вводят один или несколько генов, которые производят иммуностимулирующие молекулы (цитокины) или белки с повышенным количеством антигенов. После этих модификаций клетки продолжают культивировать, затем проводят лизис и получают готовую вакцину.
Широкое разнообразие вирусных и невирусных векторов для трансгенов позволяет экспериментировать над различными типами иммунных клеток (например, цитотоксическими Т-клетками и дендритными клетками) для ингибирования иммунного ответа и регрессии раковых клеток. В 1990-х годах было высказано предположение, что опухолевые инфильтрирующие лимфоциты (TIL) являются источником цитотоксических Т-лимфоцитов (CTL) и естественных киллеров (NK) для раковых клеток [19]. Так как TIL можно легко манипулировать ex vivo, они стали первыми генетически модифицированными иммунными клетками, которые были применены для противораковой иммунотерапии [20]. В Т-клетках, изъятых из крови онкобольного, изменяют гены, которые отвечают за экспрессию рецепторов для раковых антигенов. Также можно добавлять гены для большей выживаемости и эффективного проникновения модифицированных Т-клеток в опухоль. С помощью таких манипуляций создаются высокоактивные «убийцы» раковых клеток [21].
Когда было доказано, что большинство видов рака имеют специфические антигены и способны индуцировать свои защитные механизмы [22], была выдвинута гипотеза, что блокировка иммунной системы раковых клеток облегчит отторжение опухоли. Поэтому для производства большинства противоопухолевых вакцин в качестве источника антигенов используют опухолевые клетки пациента или специальные аллогенные клетки. Основные проблемы иммунотерапии опухолей — вероятность возникновения аутоиммунных реакций в организме больного, отсутствие противоопухолевого ответа, иммуностимуляция роста опухоли и другие.
Стволовые клетки
Мощным инструментом генной терапии является использование стволовых клеток в качестве векторов для передачи терапевтических агентов — иммуностимулирующих цитокинов, «суицидных» генов, наночастиц и антиангиогенных белков [23]. Стволовые клетки (СК), кроме способности к самообновлению и дифференцировке, имеют огромное преимущество по сравнению с другими транспортными системами (нанополимерами, вирусами): активация пролекарства происходит непосредственно в опухолевых тканях, что позволяет избежать системной токсичности (экспрессия трансгенов способствует разрушению только раковых клеток). Дополнительным позитивным качеством является «привилегированное» состояние аутологичных СК — использованные собственных клеток гарантирует 100%-совместимость и повышает уровень безопасности процедуры [24]. Но все же эффективность терапии зависит от правильной ex vivo передачи модифицированного гена в СК и последующего переноса трансдуцированных клеток в организм пациента. Кроме того, прежде чем применять терапию в широких масштабах, нужно детально изучить все возможные пути трансформации СК в раковые клетки и разработать меры безопасности для предупреждения канцерогенного преобразования СК.
Заключение
Если подвести итоги, можно с уверенностью говорить, что наступает эпоха персонализированной медицины, когда для лечения каждого онкобольного будет подбираться определенная эффективная терапия. Уже разрабатываются индивидуальные программы лечения, которые обеспечивают своевременный и правильный уход и приводят к значительному улучшению состояния пациентов. Эволюционные подходы для персонализированной онкологии, такие как геномный анализ, производство таргетных препаратов, генная терапия рака и молекулярная диагностика с использованием биомаркеров уже приносят свои плоды [17].
Особенно перспективным методом лечения онкозаболеваний является генная терапия. На данный момент активно проводятся клинические испытания, которые часто подтверждают эффективность ГТ в тех случаях, когда стандартное противораковое лечение — хирургия, лучевая терапия и химиотерапия — не помогает. Развитие инновационных методик ГТ (иммунотерапии, онколитической виротерапии, «суицидной» терапии и др.) сможет решить проблему высокой смертности от рака, и, возможно, в будущем диагноз «рак» не будет звучать приговором.
Видео. Рак: узнать, предупредить и устранить болезнь