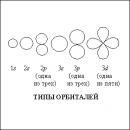
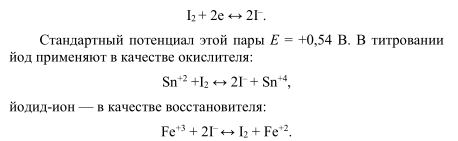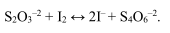ПЕРМАНГАНАТОМЕТРИЯ
ПЕРМАНГАНАТОМЕТРИЯ – метод объемного (титриметрического) химического анализа, основанный на применении стандартного (имеющего строго определенную концентрацию) раствора перманганата калия KMnO4. При действии восстановителей перманганат-ион в кислотной среде переходит в бесцветный катион марганца(2+):
Окончание титрования устанавливается по отсутствию розовой окраски перманганат-иона или с помощью индикатора (например, дифениламина).
Применение перманганатометрии несколько осложняется реакцией, которая может идти в конце титрования в случае недостаточной кислотности раствора и приводит к ошибкам аналитического определения восстановителей:
Эта реакция ускоряется в присутствии диоксида марганца. Для подкисления раствора при перманганатометрии обычно используют серную кислоту, так как соляная кислота (хлорид-ионы) и азотная (примеси оксидов азота) могут окисляться перманганатом калия и тем самым искажать результаты титрования.
При хранении раствора KMnO4 идет его постепенное разложение с выделением кислорода и образованием MnO2, что ведет к изменению концентрации исходного раствора.
Для приготовления стандартного раствора перманганата калия рекомендуется использовать дважды перегнанную дистиллированную воду (при вторичной перегонке к воде добавляют немного KMnO4). Если нет возможности использовать бидистиллят, приготовленный раствор KMnO4 кипятят, охлаждают и отделяют выпавший осадок MnO2 фильтрованием через стеклянный фильтр. Концентрацию (нормальность) раствора KMnO4 устанавливают титрованием точной навески щавелевой кислоты или оксалата натрия.
Перманганатометрически определяют железо(2+), хром(3+), таллий(1+), вольфрам(V), ванадий(IV), сурьму(III), пероксид водорода, гидразин, органические вещества. Перманганатометрическое титрование применяется для определения очень сильных восстановителей, реагирующих с катионами железа(3+), переводя их в катионы железа(2+), которые оттитровывают перманганатом калия. Метод используется также для косвенных определений, например в феррометрии, суть которого заключается в восстановлении окислителей катионами железа(2+), избыток которого реагирует с перманганатом калия.
Обратным перманганатометрическим титрованием определяют восстановители, медленно реагирующие с KMnO4 – такие как иодиды, цианиды, тиоцианаты и т.п.
Крешков А.П. Основы аналитической химии. Качественный и количественный анализ, т. 2. М., Химия, 1965
Бабко А.К., Пятницкий И.В. Количественный анализ. М., Высшая школа, 1968
Харитонов Ю.Я. Аналитическая химия: Аналитика, с 2-х кн. Кн. 2: Количественный анализ. Физико-химические (инструментальные) методы анализа. М., Высшая школа, 2005
На чем основан метод перманганатометрии
4.6. ОСНОВНЫЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ МЕТОДЫ АНАЛИЗА
Перманганатометрия – один из наиболее часто применяемых методов окислительно-восстановительного титрования. В качестве титранта используют раствор перманганата калия, окислительные свойства которого можно регулировать в зависимости от кислотности раствора.
Особенности и возможности метода
Перманганатометрически в щелочной среде, как правило, определяют органические соединения: формиаты, формальдегид, муравьиную, коричную, винную, лимонную кислоты, гидразин, ацетон и др.
Признаком окончания титрования служит бледно-розовая окраска избытка титранта КМ n О4 (одна капля 0,004 моль/л раствора титранта придает заметную окраску 100 мл раствора). Поэтому, если титруемый раствор бесцветен, о достижении точки эквивалентности можно судить по появлению бледно-розовой окраски избытка титранта КМ n О4 при титровании прямым способом или по исчезновению окраски при обратном титровании. При анализе окрашенных растворов рекомендуется использовать индикатор ферроин.
Перманганатометрию используют в следующих целях :
В случае замедленных реакций определение проводят способом обратного титрования избытка перманганата.
Так определяют муравьиную, поли- и оксикарбоновые кислоты, альдегиды и другие органические соединения, например:
Затем избыток перманганата оттитровывают щавелевой кислотой или оксалатами:
Cr2O7 2- + 6Fe 2+ + 14H + → 2Cr 3+ + 6Fe 3+ + 7H 2O
Титрование избытка ионов Fe 2+ проводят перманганатом (вспомогательным рабочим раствором):
3 Определение веществ, не обладающих окислительно-восстановительными свойствами, проводят косвенным способом, например титрованием по замещению. Для этого определяемый компонент переводят в форму соединения, обладающего восстановительными или окислительными свойствами, а затем проводят титрование. Например, ионы кальция, цинка, кадмия, кобальта осаждают в виде малорастворимых оксалатов
Осадок отделяют от раствора, промывают и растворяют в H 2 SO 4:
Приготовление и стандартизация раствора перманганата калия
Титр перманганата калия можно установить также по оксиду мышьяка ( III ) или металлическому железу. Использование для установки титра металлического железа особенно целесообразно, если в дальнейшем предполагается перманганатометрическое определение этого элемента.
В перманганатометрии применяют также растворы восстановителей – соли Fe ( II ), щавелевую кислоту и некоторые другие – для определения окислителей методом обратного титрования. Соединения Fe ( II ) на воздухе медленно окисляются, особенно в нейтральном растворе. Подкисление замедляет процесс окисления, однако обычно рекомендуется перед применением раствора F е( II ) в анализе проверить его титр. Оксалаты и щавелевая кислота в растворе медленно разлагаются:
Этот процесс ускоряется на свету, поэтому растворы оксалатов рекомендуется хранить в темных склянках. Подкисленные растворы оксалатов более устойчивы, чем нейтральные или щелочные.
Оксидиметрия. Перманганатометрия. Йодометрия. Хроматометрия
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Оксидиметрия
Основные понятия методов оксидиметрии
К методам окислительно-восстановительного титрования (оксидиметрия) относятся все титриметрические методы, в основе которых лежат окислительно-восстановительные реакции. Рабочим раствором является либо раствор окислителя, либо раствор восстановителя, а анализируемым раствором в первом случае — восстановитель, во втором — окислитель.
В зависимости от рабочего раствора в оксидиметрии применяют следующие основные методы:
Эквивалентная молярная масса Mэ окислителя и восстановителя зависит от числа принимаемых или отдаваемых электронов Mэ = Мм / n,
где Мм — молярная масса окислителя или восстановителя;
n — число электронов.
Проведение оксидиметрии возможно только в том случае, если:
1) скорость реакции достаточно велика;
2) можно определить точку эквивалентности.
В зависимости от условий реакции ЕО/В рассчитывается по уравнению Нернста:
В оксидиметрии существуют два типа индикаторов.
Второй тип индикаторов. Происходит изменение окрашивания раствора при изменении потенциала редокс-индикато. Дифениламин ↔ дифенилбензидин. При значении потенциала Е ≥ 0,79 В цвет раствора меняется с бесцветного на синий.
Перманганатометрия
Перманганатометрическим методом объемного анализа называют метод, основанный на окислении различных веществ перманганатом калия (KMnO 4 ). В зависимости от условий, в которых протекает реакция окисления-восстановления, ионы MnO 4 – могут принимать различное число электронов. В кислой среде:
То есть здесь более низкое значение потенциала. Но титрование в этой среде используют гораздо реже, чем в кислой среде. Изменение окрашивания малиновый — коричневый (трудно определить переход в окрашивании раствора). Перманганатометрию используют для определения:
Для метода применяют 0,02–0,05 н растворы перманганата калия (более концентрированные растворы окрашены более интенсивно, менее концентрированные — менее устойчивы при хранении). Необходимо устанавливать титр раствора перманганата через 10 ч после приготовления раствора. Титр устанавливают по оксалату натрия Na2C2O4. Раствор хранят в темных склянках в темном месте.
Молярная масса эквивалента нитрита равна половине его молярной массы. Ход анализа отработан десятилетиями и выполняется по методике, которая учитывает все нюансы.
Йодометрия
Йодометрия — титриметрический (объемный) метод определения веществ, основанный на окислительно-восстановительных реакциях с участием йода иили йодида калия. В основе всех йодометрических реакций лежит реакция:
Проводят йодометрию с индикатором крахмалом, который добавляют перед началом титрования (интенсивное синее окрашивание). Если используют йодид, то титрование проводят непрямым методом. К анализируемому раствору добавляют избыток йодида, затем образующийся йод титруют раствором тиосульфата натрия с образованием тиотионат-иона:
Хроматометрия
Хроматометрией называется метод объемного анализа, основанный на использовании раствора бихромата калия в качестве стандартного. Бихромат калия способен окислять многие неорганические и органичские вещества сульфиты, дитионаты, гексацианоферрат (II), арсениты, иодиды, спирты, гидрохинон, глицерин, аскорбиновую кислоту, тиомочевину и др. В качестве примера ниже приведена используемая в объемном анализе реакция окисления — восстановления, протекающяя с участием бихромата и гексацианоферрата (II)
Методическое пособие для выполнения лабораторно-практических работ по теме «Титриметрический метод анализа. Метод перманганатометрии»
Методическое пособие по выполнению лабораторно-практических работ по теме
«Титриметрический метод анализа. Метод перманганатометрии »
в слабокислой, нейтральной и щелочной средах:
Методом перманганатометрии можно определять и восстановители и окислители. Восстановители титруют непосредственно раствором перманганата, а количество окислителя определяют методом обратного титрования. При обратном титровании к отменному количеству окислителя прибавляют определенный объем восстановителя, взятый в избытке. Избыток восстановителя оттитровывают раствором перманганата калия. Концентрацию добавляемого раствора восстановителя определяют отдельным титрованием его тем же раствором перманганата.
Приготовление рабочего раствора перманганата калия.
Освоить особенность приготовления раствора перманганата калия.
Приготовить рабочий раствор перманганата калия заданной концентрации.
Очень трудно получить перманганат калия в чистом виде. Обычно он загрязнен следами оксида марганца. Кроме того, дистиллированная вода обычно содержит следы веществ, которые восстанавливают перманганат калия с образованием оксида марганца. Раствор, приготовленный обвешиванием определенного количества химически чистой соли, растворением ее и разбавлением в мерной колбе, нельзя считать титрованным. Титр его можно установить не ранее чем через 7 – 12 дней после приготовления раствора. Чтобы раствор был достаточно устойчив и титр его не изменялся, надо удалить из него оксид марганца, для чего необходимо пропустить раствор перед его употреблением через фильтр.
Надо иметь в виду, что перманганат калия окисляет резину, корковые пробки, фильтровальную бумагу, поэтому нельзя фильтровать перманганат калия через бумажный фильтр, а использовать для этих целей стеклянные фильтры.
При титровании перманганатом калия применяют бюретки со стеклянным краном. Бюретки и другую стеклянную посуду нельзя оставлять на продолжительное время с раствором перманганата калия, так как на стекле образуется налет оксида марганца коричнево-бурого цвета. Отмывают налет на стекле концентрированной соляной кислотой или смесью 2н. серной кислоты с раствором соли Мора или щавелевой кислоты.
Перманганатометрическое титрование



Перманганатометрическое титрование, или перманганатометрия, — метод количественного определения веществ (восстановителей, реже — окислителей и соединений, не обладающих окислительно-восстановительными свойствами) с применением титранта — раствора перманганата калия КМnO4.
Сущность метода. Перманганат калия — сильный окислитель, обладающий интенсивной фиолетово-малиновой окраской. В зависимости от кислотности титруемого раствора окислительные свойства перманганат-иона проявляются по-разному.
Стандартный ОВ потенциал редокс-пары МnО4‾, H + |Mn 2+ имеет довольно высокое значение и при комнатной температуре равен 1,51 В. Поэтому кислым раствором перманганата калия можно оттитровать целый ряд восстановителей, причем большинство таких ОВ реакций протекает с высокой скоростью. С ростом концентрации ионов водорода в растворе реальный потенциал рассматриваемой редокс-пары
| Е = Е o + | 0,059 | lg | [МnО4 ‾] [H + ] 5 |
| [Mn 2+ ] |
возрастает и эффективность перманганат-иона как окислителя повышается. Поскольку в ОВ полуреакции участвуют 5 электронов, то молярная масса эквивалента перманганата калия как окислителя в кислой среде равна
В нейтральной среде перманганат-ион восстанавливается до диоксида марганца МnО2.
Стандартный ОВ потенциал редокс-пары МnО4 ‾| МnО2 сравнительно невелик и при комнатной температуре равен E° = 0,60 В, поэтому в нейтральной среде эффективность перманганата калия как окислителя значительно ниже, чем в сильнокислых растворах. Кроме того, образующийся в результате ОВ реакции бурый осадок диоксида марганца затрудняет фиксацию КТТ, обладает развитой поверхностью и может адсорбировать определяемое вещество, что увеличивает ошибку анализа.
Поэтому как титрант-окислитель перманганат калия в нейтральной среде практически не применяется.
В сильнощелочных средах перманганат-ион восстанавливается до манганат-иона
Образующийся манганат-ион обладает зеленой окраской умеренной интенсивности, окрашивает раствор в зеленый цвет, что затрудняет обнаружение изменения окраски раствора и фиксацию КТТ. Манганат-ион вступает в реакцию с водой:
с образованием бурого осадка диоксида марганца и перманганат-иона, что искажает результаты анализа. Стандартный ОВ потенциал редокс-пары МnО4 ‾| МnО2 невелик и при комнатной температуре равен E° = 0,56 В, т.е. в щелочных средах перманганат калия как окислитель менее эффективен, чем в кислых растворах. Кроме того, щелочные растворы способны поглощать диоксид углерода из воздуха с образованием гидроксокарбонатных соединений, что также затрудняет проведение количественного анализа.
С учетом всех этих обстоятельств перманганат калия как титрант-окислитель в щелочных средах практически не применяется.
Таким образом, на основе вышеизложенного можно сделать вывод о том, что перманганатометрическое титрование целесообразно проводить в сильнокислых средах.
Условия проведения перманганатометрического титрования. При проведении перманганатометрического титрования необходимо соблюдать, по крайней мере, следующие основные условия:
1) Влияние рН среды. Перманганатометрическое титрование проводят в сильно кислой среде при концентрации ионов водорода [Н3O + ] = 1—2 моль/л. Кислая среда создается введением серной кислоты. Азотную кислоту применять нельзя, так как она сама является сильным окислителем и может окислять определяемое вещество.
Хлороводородную кислоту в перманганатометрии также не используют, так как хлорид-ионы окисляются перманганат-ионами до хлора по схеме:
10Сl‾ +2 МnО4 ‾ + 16Н + = 5Сl2 + 2 МnО 2 + 8Н2O
При этом часть титранта расходуется на окисление хлорид-ионов, что вызывает перерасход титранта и увеличивает ошибку анализа. В обычных условиях эта реакция идет медленно, однако ускоряется в присутствии соединений железа(II).
В сернокислой среде указанные побочные процессы отсутствуют, поэтому перманганатометрическое титрование ведут в сернокислой среде.
2) Влияние температуры. Чаще всего перманганатометрическое определение проводят при комнатной температуре. Исключением является реакция перманганат-иона с щавелевой кислотой и оксалатами, которую проводят при нагревании титруемого раствора.
3) Фиксация конечной точки титрования. При перманганатометрическом титровании обычно не применяют посторонний индикатор, так как сам титрант — раствор перманганата калия — обладает интенсивной малиново-фиолетовой окраской. Прибавление одной избыточной капли титранта в ТЭ приводит к окрашиванию титруемого раствора в розовый цвет. Так, чтобы придать отчетливую окраску 100 мл воды достаточно прибавить всего 0,2 мл раствора перманганата калия с молярной концентрацией эквивалента 0,1 моль/л.
Окраска раствора в КТТ неустойчива, раствор постепенно обесцвечивается. Это происходит вследствие того, что избыточные перманганат-ионы, придающие раствору розовую окраску, взаимодействуют с образовавшимися катионами марганца(II) Мn 2+ :
Хотя повышенная кислотность раствора способствует смещению равновесия влево, однако константа равновесия этой реакции велика и составляет
10 47 . Поэтому реакция протекает даже в кислой среде. Правда, скорость данной реакции в обычных условиях мала, поэтому окраска раствора в КТТ ослабляется медленно, в течение одной-двух минут. Тем не менее, указанное обстоятельство необходимо иметь в виду во избежание перетитровывания раствора.
В некоторых (редких) случаях перманганатометрическое титрование ведут очень разбавленным раствором титранта. В такой ситуации для более четкого фиксирования КТТ в титруемый раствор вводят редокс-индикатор, например ферроин или N-фенилантраниловую кислоту.
4) Ход титрования. Обычно в перманганатометрии к раствору определяемого вещества медленно, по каплям прибавляют раствор титранта, для того чтобы в растворе не было локального избытка окислителя — перманганат-иона и не протекали бы побочные процессы.
Для титрования применяют бюретки со стеклянными кранами; использование резиновых трубок исключается, так как резина взаимодействует с перманганатом калия.
Титрант метода. Титрантом метода, как уже говорилось выше, является водный раствор перманганата калия, чаще всего — с молярной концентрацией эквивалента 0,1 моль/л. Сам кристаллический перманганат калия обычно содержит примеси диоксида марганца. Водные растворы перманганата калия неустойчивы из-за склонности перманганат-ионов окислять воду по схеме
Хотя константа равновесия этой реакции довольно велика, однако в обычных условиях процесс протекает медленно, поэтому свежеприготовленный раствор перманганата калия можно использовать некоторое время в качестве титранта.
Разложение перманганат-ионов ускоряется на свету, при нагревании, под действием кислот и оснований, в присутствии катионов марганца(II) Мn 2+ диоксида марганца МnО2 который осаждается на стенках сосуда, образуя темный налет.
В силу указанных обстоятельств стандартный раствор перманганата калия нельзя приготовить по точной навеске. Для получения титранта вначале готовят раствор перманганата калия с приблизительной концентрацией, например, разбавляя водой более концентрированный раствор. Поскольку дистиллированная вода всегда содержит следы различных веществ, при окислении которых перманганатом калия образуется диоксид марганца, то приготовленный первоначальный раствор перманганата калия следует либо прокипятить, охладить и профильтровать через стеклянный фильтр, либо выдержать длительное время (до нескольких недель) в темном месте и затем также профильтровать через стеклянный фильтр. После этого раствор стандартизуют.
Стандартизацию раствора перманганата калия проводят по различным установочным веществам: H2C2O4• 2H2O, Na2C2O4, Аs2О3, KJ, (NH4)2Fe(SO4)2 • 6H2O, по металлическому железу и т.д. Часто стандартизацию проводят по стандартному раствору щавелевой кислоты на основе реакции
Разработаны две методики стандартизации раствора перманганата калия по стандартному раствору щавелевой кислоты:
При этом расход титранта занижен на
0,4% вследствие протекания побочного процесса — окисления небольшой части щавелевой кислоты кислородом воздуха.
2) К нагретому раствору щавелевой кислоты быстро прибавляют
95% требуемого объема раствора перманганата калия, нагревают смесь примерно до
60 o С и заканчивают титрование, уже медленно прибавляя оставшуюся часть стандартизуемого раствора перманганата калия до получения устойчивой розовой окраски титруемого раствора, исчезающей в течение одной-двух минут.
Данная методика позволяет получить результаты с меньшей ошибкой.
Стандартизованный раствор перманганата калия хранят в темной склянке в темном месте. Концентрацию раствора периодически проверяют, поскольку по причинам, описанным выше, она несколько изменяется при хранении раствора.
Применение перманганатометрии. Перманганатометрическое титрование применяют преимущественно для определения веществ, играющих по отношению к перманганат-иону роль восстановителей, таких, как H2O2, MgO2, NaNO2, металлическое железо и некоторые другие металлы, карбоновые кислоты, соединения с гидразогруппами R—NH—NH—R, для определения общей окисляемости воды и почвы (т.е. для определения суммы восстановителей, присутствующих в этих объектах).
Пероксид водорода определяют прямым титрованием в сернокислой среде на основе реакции
Титрование ведут при комнатной температуре до появления устойчивой розовой окраски раствора.
Поскольку растворы пероксида водорода неустойчивы, то иногда для их стабилизации перед титрованием в них вносится небольшое количество карбамида, который не мешает титрованию.
Молекула пероксида водорода в указанной реакции отдает два электрона:
поэтому ее фактор эквивалентности равен 1/2; молярная масса эквивалента составляет М( 1 /2H2O2) = М(Н2O2)/2 = 34,0147/2 = 17,0073.
Содержание металлического железа определяют следующим образом. Препарат, содержащий железо, обрабатывают разбавленной серной кислотой при нагревании на водяной бане. Металлическое железо растворяется и переходит в железо(II):
После растворения железа раствор быстро охлаждают и разбавляют водой. Отбирают аликвоту полученного раствора и определяют железо(II) перманганатометрически прямым титрованием в сернокислой среде на основе реакции:
5Fe 2+ + МnО4 ‾ + 8H + = 5Fe 3+ + Mn 2+ + 4H2O
Титрование ведут при комнатной температуре до появления устойчивой (в течение
1—2 минут) розовой окраски раствора.
Поскольку один катион Fe 2+ отдает один электрон, то молярная масса эквивалента железа(II) в этой реакции равна его молярной массе.
Аналогично прямым перманганатометрическим титрованием определяют железо(II) в растворах солей железа(II).
Если анализируемый объект содержит железо(III), то после его растворения железо(III) предварительно восстанавливают до железа(II) хлоридом олова(II) или металлическим цинком, либо другими восстановителями, после чего железо(II) оттитровывают раствором перманганата калия.
При наличии в растворе хлорид-ионов Сl‾ во избежание их окисления перманганат-ионами в сернокислый раствор до проведения титрования вводят смесь серной, ортофосфорной кислот и сульфата марганца (смесь Рейнгарда-Циммермана). В присутствии этой смеси затормаживается окисление хлорид-ионов (по сравнению с протеканием основной реакции), железо(III) связывается в бесцветные устойчивые фосфатные комплексы, что повышает полноту протекания основной реакции и устраняет желтую окраску аквакомплексов железа(III). В основе определения нитритов лежит реакция
Поскольку нитрит-ион неустойчив в кислой среде и разлагается по схеме:
то аликвоту стандартизованного сернокислого раствора перманганата калия титруют нейтральным растворо.м нитрита натрия NaNO2 до обесцвечивания титруемого раствора в соответствии с реакцией
В данном случае собственно титрантом является анализируемый раствор нитрита натрия, а не стандартизованный раствор перманганата калия. Нитрит-ион в этой реакции отдает два электрона:
поэтому фактор эквивалентности нитрит-иона здесь равен 1/2, а молярная масса эквивалента нитрита натрия равна
Нитрит натрия можно определять также методом обратного титрования, К аликвоте нейтрального раствора нитрита натрия прибавляют избыток (по сравнению со стехиометрическим количеством) раствора перманганата калия, серную кислоту и оставляют на некоторое время. Нитрит натрия окисляется до нитрата, а избыток перманганата калия, не вступивший.в реакцию с нитрит-ионами, определяют либо титрованием раствором соли Мора (содержащем железо(II)), либо методом заместительного иодометрического титрования. В последнем случае к раствору прибавляют избыток иодида калия. Иодид-ионы окисляются пермангана-том калия до иода:
Иод, образовавшийся в количестве, эквивалентном количеству избыточного перманганата калия, оттитровывают стандартным раствором тиосульфата натрия:
Пероксид магния MgO2 также определяют прямым перманганатометрическим титрованием на основе реакции:
Для проведения анализа навеску препарата, содержащего не менее 25% пероксида магния, растворяют в разбавленной серной кислоте и титруют раствором перманганата калия до появления розовой окраски титруемого раствора.
Перманганатометрию применяют для определения не только восстановителей, но и окислителей, используя обратное титрование.
Так, например, можно определять дихромат-ионы. Для этого к аликвоте анализируемого раствора дихромата калия K2Cr2O7 прибавляют известное количество раствора FeSO4 избыточное по сравнению со стехиометрическим количеством. При этом железо(II) окисляется до железа(III):
Cr2O7 2+ + 6Fe 2+ + 14H + = 6Fe 3+ + 2Cr 3+ + 7H2O
Избыток непрореагировавшего железа(Н) оттитровывают стандартным раствором перманганата калия по реакции, описанной выше.
Общая оценка перманганатометрического титрования. Перманганатометрия — один из самых распространенных методов ОВ титрования. Метод обладает рядом достоинств: титрование проводится без постороннего индикатора, в широком диапазоне изменения рН раствора; высокое значение стандартного ОВ потенциала редокс-пары МnО4‾, H + |Mn 2+ позволяет определять большое число веществ; перманганат калия доступен и сравнительно недорог.
К недостаткам перманганатометрии относятся: невозможность приготовления стандартного раствора титранта по точной навеске, его нестабильность при хранении, необходимость строгого соблюдения условий проведения титрования, регламентируемых соответствующей аналитической методикой.