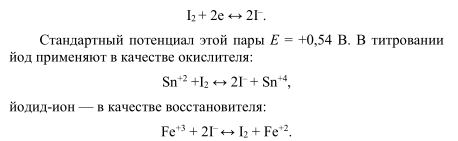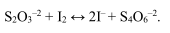Йодометрия: сущность метода, общая характеристика, область применения. Условия проведения йодометрических определений
I2 + 2е 
Т.к. стандартный окислительно-восстановительный потенциал пары невелик − E 0 (I2 /2I − ) = 0,54 В, йод является относительно слабым окислителем, а ионы I − – сравнительно сильным восстановителем.
С помощью метода йодометрии можно определять:
а) путем прямого титрования анализируемого раствора раствором йода:
б) путем обратного титрования, Используется, если скорость взаимодействия восстановителя с йодом невелика. В этом случае к раствору восстановителя добавляют избыток титрованного раствора I2, а спустя некоторое время не вступивший в реакцию йод титруют раствором тиосульфата натрия:
Проводить определение, титруя раствор окислителя йодидом калия KI нельзя, т.к. невозможно фиксировать конец титрования. Поэтому пользуются методом замещения: к анализируемому раствору окислителя добавляют избыток раствора KI:
2 MnO4 − + 10 I − + 16 H + = 5 I2 + 2 Mn 2+ + 8 Н2О. (2.11)
В результате реакции выделяется йод в количестве, эквивалентном количеству окислителя; йод титруют раствором тиосульфата натрия по уравнению (2.10).
К достоинствам метода йодометрии можно отнести следующие:
1. Большая точность по сравнению с другими методами окислительно-восстановительного титрования.
2. Растворы йода окрашены, и титрование можно проводить без индикатора. Желтая окраска ионов I3 − при отсутствии других окрашенных продуктов отчетливо видна при очень малой концентрации (5∙10 −5 н.).
3. Йод хорошо растворяется в органических растворителях, поэтому метод широко применяется для титрования в неводных средах.
Недостатки метода, вызывающие ошибки при выполнении йодометрических определений:
1. Потери йода из-за его летучести. Поэтому титрование проводят на холоду и по возможности быстро. При необходимости оставить раствор на некоторое время для завершения реакции, его хранят под притертой пробкой.
2. Окисление ионов йода кислородом воздуха в кислой среде.
3. Йодометрическое титрование нельзя проводить в щелочной среде вследствие диспропорционирования йода.
4. Относительно медленные скорости реакций с участием йода.
5. В процессе хранения стандартные растворы йода и тиосульфата изменяют свой титр. Чтобы избежать ошибок, необходимо периодически проверять титр йода по тиосульфату, а титр тиосульфата по дихромату калия.
Фиксируют конечную точку титрования в методе йодометрии с помощью специфического индикатора – крахмала, который образует с йодом комплексно-адсорбционное соединение синего цвета. Эта реакция очень чувствительна, она позволяет легко обнаруживать йод при концентрации 10 −5 н. Т.к. соединение йода с крахмалом очень прочное, крахмал следует добавлять в конце титрования, когда окраска раствора становится бледно-желтой. Если вводить крахмал раньше, то очень много йода будет связано с крахмалом. При титровании йод с трудом освобождается из соединения с крахмалом, и результат титрования окажется неточным.
При проведении йодометрических определений следует соблюдать следующие условия:
1. Т.к. стандартный окислительно-восстановительный потенциал пары I2/2I − невелик, многие йодометрические определения не доходят до конца. Поэтому для количественного протекания реакций необходимо создавать специальные условия (вводить комплексообразователи, осадители, буферные добавки и т.д.).
2. Йод – вещество летучее, поэтому титрование проводят на холоду. Кроме того, при увеличении температуры снижается чувствительность крахмала как индикатора (при 50 0 С индикатор в 10 раз менее чувствителен, чем при 25 0 С).
3. Растворимость йода в воде мала, поэтому определение окислителей необходимо проводить в присутствии большого избытка KI, который образует с йодом растворимое нестойкое комплексное соединение:
KI + I2 
4. Скорость реакции между окислителями и KI обычно невелика, поэтому к титрованию выделившегося йода обычно приступают спустя некоторое время.
5. Йодометрическое титрование нельзя проводить в щелочной среде, т.к. протекает побочная реакция:
I2 + 2 OH − = IO − + I − + Н2О (2.13)
Образующийся гипойодит является более сильным окислителем, чем йод, он окисляет тиосульфат до сульфата:
Поэтому во избежание побочных реакций титрование проводят при рН не более 9.
6. В кислых растворах йодиды постепенно окисляются кислородом воздуха:
Свет ускоряет эту реакцию, поэтому реакционную смесь хранят в темноте.
Рабочими растворами метода йодометрии являются растворы йода и тиосульфата натрия.
Титрованный раствор йода можно приготовить исходя из точной навески химически чистого кристаллического йода, который очищают от примесей путем возгонки.
Однако, очистка йода представляет собой очень трудоемкую операцию. Кроме того, титрованный раствор в процессе работы с ним и при длительном хранении меняет свой титр вследствие летучести йода, и периодически его нужно проверять. Поэтому обычно готовят раствор I2 приблизительно нужной концентрации (0,05–0,1 н.) растворением навески йода в растворе KI (40 г/л). Точную концентрацию полученного раствора устанавливают по раствору тиосульфата натрия (реакция 2.10).
Тиосульфат натрия Na2S2O3·5Н2О является неустойчивым веществом. Оно легко реагирует с углекислым газом и кислородом воздуха:
Поэтому готовят приблизительно 0,1 н. раствор тиосульфата, растворяя навеску соли в свежепрокипяченой воде (для удаления СO2). Хранить готовый раствор Na2S2O3 рекомендуется в темных бутылях, защищенных от двуокиси углерода трубкой с натронной известью. В дальнейшем титр раствора начинает медленно уменьшаться, поэтому его необходимо периодически проверять.
Для установки концентрации тиосульфата предложено много различных стандартных веществ, например твердый химически чистый йод, йодат калия KIO3, бромат калия KBrO3, дихромат калия и др. На практике чаще всего пользуются дихроматом калия K2Cr2O7.
В качестве стандартного в-ва используют K2Cr2O7, но т.к он с тиосульфатом взаимодействует не стехеометрично используют метод замещения. К подкисленному раствору KJ добавляют раствор дихромата и спустя 5-10 мин выделившийся йод титрую тиосульфатом по уравнению
Оксидиметрия. Перманганатометрия. Йодометрия. Хроматометрия
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Оксидиметрия
Основные понятия методов оксидиметрии
К методам окислительно-восстановительного титрования (оксидиметрия) относятся все титриметрические методы, в основе которых лежат окислительно-восстановительные реакции. Рабочим раствором является либо раствор окислителя, либо раствор восстановителя, а анализируемым раствором в первом случае — восстановитель, во втором — окислитель.
В зависимости от рабочего раствора в оксидиметрии применяют следующие основные методы:
Эквивалентная молярная масса Mэ окислителя и восстановителя зависит от числа принимаемых или отдаваемых электронов Mэ = Мм / n,
где Мм — молярная масса окислителя или восстановителя;
n — число электронов.
Проведение оксидиметрии возможно только в том случае, если:
1) скорость реакции достаточно велика;
2) можно определить точку эквивалентности.
В зависимости от условий реакции ЕО/В рассчитывается по уравнению Нернста:
В оксидиметрии существуют два типа индикаторов.
Второй тип индикаторов. Происходит изменение окрашивания раствора при изменении потенциала редокс-индикато. Дифениламин ↔ дифенилбензидин. При значении потенциала Е ≥ 0,79 В цвет раствора меняется с бесцветного на синий.
Перманганатометрия
Перманганатометрическим методом объемного анализа называют метод, основанный на окислении различных веществ перманганатом калия (KMnO 4 ). В зависимости от условий, в которых протекает реакция окисления-восстановления, ионы MnO 4 – могут принимать различное число электронов. В кислой среде:
То есть здесь более низкое значение потенциала. Но титрование в этой среде используют гораздо реже, чем в кислой среде. Изменение окрашивания малиновый — коричневый (трудно определить переход в окрашивании раствора). Перманганатометрию используют для определения:
Для метода применяют 0,02–0,05 н растворы перманганата калия (более концентрированные растворы окрашены более интенсивно, менее концентрированные — менее устойчивы при хранении). Необходимо устанавливать титр раствора перманганата через 10 ч после приготовления раствора. Титр устанавливают по оксалату натрия Na2C2O4. Раствор хранят в темных склянках в темном месте.
Молярная масса эквивалента нитрита равна половине его молярной массы. Ход анализа отработан десятилетиями и выполняется по методике, которая учитывает все нюансы.
Йодометрия
Йодометрия — титриметрический (объемный) метод определения веществ, основанный на окислительно-восстановительных реакциях с участием йода иили йодида калия. В основе всех йодометрических реакций лежит реакция:
Проводят йодометрию с индикатором крахмалом, который добавляют перед началом титрования (интенсивное синее окрашивание). Если используют йодид, то титрование проводят непрямым методом. К анализируемому раствору добавляют избыток йодида, затем образующийся йод титруют раствором тиосульфата натрия с образованием тиотионат-иона:
Хроматометрия
Хроматометрией называется метод объемного анализа, основанный на использовании раствора бихромата калия в качестве стандартного. Бихромат калия способен окислять многие неорганические и органичские вещества сульфиты, дитионаты, гексацианоферрат (II), арсениты, иодиды, спирты, гидрохинон, глицерин, аскорбиновую кислоту, тиомочевину и др. В качестве примера ниже приведена используемая в объемном анализе реакция окисления — восстановления, протекающяя с участием бихромата и гексацианоферрата (II)
На чем основан метод йодометрии
Иодометрические методы основаны на применении стандартного раствора тиосульфата натрия для титрования иода, выделившегося при взаимодействии определяемого окислителя с избытком иодида калия (при титровании по замещению) или оставшегося в избытке при медленном взаимодействии определяемого восстановителя с фиксированным объемом стандартного раствора иода (в случае обратного титрования).
Иодид-ион является восстановителем умеренной силы, его применяют для определения большого числа окислителей. Прямое титрование стандартным раствором KI не используют из-за трудностей индикации конечной точки титрования: прекращение образования свободного иода с помощью крахмала заметить нельзя. Поэтому для определения окислителей иодометрическим методом применяют способ титрования по замещению. Прямое титрование окислителей стандартным раствором тиосульфата натрия невозможно в связи с тем, что только I 2 в нейтральной среде окисляет ион S 2 O 3 2- быстро в соответствии со стехиометрией реакции
Другие окислители обладают способностью полностью или частично окислять тиосульфат до серы, сульфата или тетратионата, например
При титровании иода раствором тиосульфата наиболее благоприятна нейтральная либо слабокислая среда. Высокая кислотность раствора приводит к разложению тиосульфата:
H 2 SO 3 реагирует с I 2 в мольном соотношении 1:1
тогда как на 1 моль Na 2 S 2 O 3 расходуется ½ моль I 2. В щелочной среде иодометрическое определение также не следует проводить из-за реакции диспропорционирования иода:
Приготовление и стандартизация раствора тиосульфата натрия
Важнейшими факторами, определяющими устойчивость раствора тиосульфата, являются значение рН, присутствие микроорганизмов и примесей, концентрация раствора, присутствие атмосферного кислорода и воздействие прямого солнечного света. Для приготовления растворов тиосульфата следует применять дистиллированную воду, не содержащую примесей ионов тяжелых металлов – катализаторов окисления тиосульфата кислородом воздуха
Для приготовления растворов рекомендуется свежепрокипяченная вода, так как бактерии разлагают растворы тиосульфата. Активность бактерий при рН = 9–10 минимальна. Для подавления роста бактерий можно добавлять такие вещества, как хлороформ, бензоат натрия или Н gI 2. Кипячение воды для приготовления растворов тиосульфата также обеспечивает удаление растворенного СО2, под влиянием которого будут изменяться характеристики раствора, поскольку восстановителем вместо Na 2 S 2 O 3 будет выступать Na Н SO 3, образующийся в реакции:
Добавление небольших количеств (0,1г/л) Na 2СО3 способствует удалению СО2
Скорость разложения тиосульфата возрастает с уменьшением его концентрации в растворе. Если в растворе появляется муть, то такой раствор следует заменить. Наиболее часто Na 2 S 2 O 3 готовят в виде 0,05 н. растворов. Навеску рассчитывают, принимая f э( Na 2 S 2 O 3)=1/2.
В качестве первичного стандарта для растворов Na2S2O3 могут быть окислители КВ r О3, К IO 3, выделяющие при взаимодействии с избытком иодид-ионов эквивалентное количество иода, который титруют стандартизируемым раствором тиосульфата. Чаще используют бихромат калия К2С r 2О7, который можно легко получить в химически чистом состоянии перекристаллизацией; он негигроскопичен и не содержит кристаллизационной воды; растворы его устойчивы при продолжительном хранении. Способ стандартизации основан на реакциях
Методика приготовления раствора К2С r 2О7 аналогична методике приготовления первичного стандарта N а2С2О4. При расчете навески следует помнить, что f э(К2С r 2О7)=1/6.
В коническую колбу для титрования переносят пипеткой раствор установочного вещества К2С r 2О7, добавляют 10 мл 2н. раствора Н2 S О4 и 1 г кристаллического К I (или соответствующий объем его концентрированного раствора). Колбы закрывают стеклянными пробками или накрывают часовыми стеклами, содержимое перемешивают, дают постоять 5-10 мин в темном месте, пока не завершится реакция. Выделившийся I 2 титруют раствором Na 2 S 2 O 3 до тех пор, пока окраска не станет слабо-желтой, затем титруемый раствор разбавляют водой приблизительно в 2 раза, добавляют индикатор крахмал и заканчивают титрование в тот момент, когда синяя окраска раствора перейдет в светло-зеленую (ионы С r 3+ ).
Приготовление и стандартизация раствора иода (вторичный стандарт)
Трииодид-ион и молекулярный иод в окислительно-восстановительных реакциях выступают как реагенты практически равной окислительной способности (

Учитывая, что иод медленно растворяется в растворе иодида калия, навеску иода, взвешенную на технических весах в закрытом бюксе, следует полностью растворить в небольшом объеме концентрированного раствора иодида, а затем разбавить до нужного объема дистиллированной водой. Перед разбавлением весь иод должен перейти в раствор, в противном случае нормальность приготовленного титранта будет непрерывно увеличиваться за счет медленного перехода в раствор нерастворившегося иода.
Растворы иода неустойчивы вследствие летучести иода и способности растворенного атмосферного кислорода окислять иодид-ион до иода:
В коническую колбу для титрования переносят пипеткой раствор иода и титруют стандартным раствором тиосульфата натрия до тех пор, пока окраска раствора не станет соломенно-желтой. Затем добавляют 2-3 мл индикатора (крахмал) и продолжают титрование до полного обесцвечивания раствора. Используя средний объем титранта, затраченного на титрование, рассчитывают титриметрические характеристики раствора иода.
Растворами иода можно непосредственно титровать соединения As ( III ), Sb ( III ), Sn ( II ), сульфиты, сероводород и некоторые другие восстановители.
Иодометрическое титрование арсенита протекает по уравнению:
Иодометрическое определение олова проводят в солянокислой среде в атмосфере СО2 для предотвращения окисления кислородом воздуха
Перед титрованием олово восстанавливают металлическим свинцом или никелем.
Сульфиды цинка, кадмия и некоторых других элементов можно определить, растворяя их в соляной кислоте, содержащей титрованный раствор иода, который окисляет сероводород до свободной серы, и титруя избыточное количество иода тиосульфатом натрия.
Иодометрические методы широко применяют для определения многих органических веществ: формальдегида, сахаров, ацетона, спиртов, азот- и серосодержащих соединений (семикарбазид, тиомочевина и т.д.) и др. В большинстве методик окисление органического вещества проводят в щелочном растворе, после окончания реакции раствор подкисляют и избыток иода оттитровывают тиосульфатом. Так определяют, например, формальдегид
Ацетон в щелочном растворе под действием иода образует иодоформ
Тиомочевину можно титровать в кислом растворе, однако более хорошие результаты дает окисление в щелочной среде
Определение заканчивается обратным титрованием иода в кислом растворе.
Своеобразно иодометрическое определение воды в органических растворителях и других материалах с помощью реактива Фишера, состоящего из иода, диоксида серы и пиридина в метаноле. Анализируемую пробу помещают в метиловый спирт и определяют воду титрованием указанным реактивом. Реакция титрования проходит в две стадии. Упрощенно она может быть представлена уравнением
Окончание титрования можно заметить визуально по появлению коричневой окраски комплекса иода с пиридином.
Реактив Фишера применяют для определения воды в органических соединениях почти всех классов. Исключение составляют соединения, вступающие в реакцию с тем или иным компонентом реактива. Используют реактив Фишера также для определения воды в неорганических веществах, хотя мешающие соединения здесь встречаются чаще, чем при анализе органических веществ. Мешают определению сильные окислители и восстановители, которые реагируют с иодом или иодидом. Перхлораты вообще нельзя анализировать реактивом Фишера, так как при этом образуется взрывоопасная смесь.
Иодометрическое определение окислителей основано на окислении иодид-иона и тировании выделившегося иода тиосульфатом натрия. Одной из наиболее важных реакций этого типа является реакция иодида с дихроматом
Одним из практически важных применений реакции является использование ее для иодометрического определения катионов, образующих малорастворимые хроматы (барий, свинец и др.). В этом методе анализируемый катион осаждают в виде хромата, который затем растворяют в кислоте:
Дихромат в растворе определяют иодометрически по приведенной выше реакции. Можно также осадить хромат бария избытком титрованного раствора дихромата калия и иодометрически определить не вошедшее в реакцию количество дихромата.
Существенное значение для протекания указанной реакции имеет концентрация иодида, которая в 4-5 раз должна превышать требуемую по стехиометрии, и кислотность раствора, хотя концентрация иона водорода и не входит в явном виде в уравнение реакции. Необходимо создание слабокислой среды, так как в нейтральных растворах ионы С u 2+ гидролизуются, а продукты гидролиза реагируют с иодидом очень медленно, что удлиняет процесс титрования и затрудняет фиксирование точки эквивалентности. Установлено, что при иодометрическом определении меди pH в растворе должен быть меньше 4. В сильнокислых растворах ( [ H + ] > 0,3 моль/л) происходит индуцированное медью окисление иодида кислородом воздуха, что приводит к получению завышенных результатов.
Определение растворенного кислорода в воде. Классический метод Винклера определения растворенного кислорода в воде основан на окислении марганца ( II ) в щелочной среде растворенным кислородом и последующем окислении иодида гидроксидами марганца ( III ) и марганца ( IV ) при подкислении раствора. Практически поступают следующим образом. К пробе воды, содержащей растворенный кислород, добавляют сульфат марганца и щелочной раствор иодида калия. В щелочной среде ионы М n 2+ быстро окисляются растворенным кислородом:
При подкислении раствора гидроксиды марганца ( III ) и марганца ( IV ) окисляют иодид и растворяются:
Выделяющийся иод титруют тиосульфатом натрия и рассчитывают содержание кислорода в воде. Хотя в результате окисления марганца ( II ) кислородом получается смесь гидроксидов Mn ( OH )3 и MnO ( OH )2 с неизвестным соотношением компонентов, это не осложняет анализ, так как количество выделившегося иода остается эквивалентным количеству растворенного кислорода.
Определение пероксидов. Пероксид водорода, а также неорганические и органические пероксиды восстанавливают иодидом в кислой среде:
Пероксид водорода с иодидом реакирует медленно. Скорость реакции резко возрастает в присутствии катализаторов: соединений молибдена, вольфрама и некоторых других элементов, которые необходимо вводить в реакционную смесь для повышения скорости реакции. Для определения пероксидов в жирах и маслах в качестве растворителя используют ледяную уксусную кислоту или ее смесь с хлороформом или тетрахлоридом углерода. Титрование проводят в атмосфере инертного газа, чтобы не допустить окисления иодида кислородом воздуха.
Основой иодометрического определения кислот является реакция
Винную, лимонную и некоторые другие оксикислоты можно оттитровывать иодометрическим методом в присутствии ионов кальция, бария, магния или других катионов, образующих с оксикислотами устойчивые комплексные соединения. В таких условиях оксикислоты титруют так же, как обычные сильные кислоты.
Особенности и возможности метода
Источником погрешностей в иодометрии является недостаточная устойчивость раствора иода, связанная с его летучестью, малой растворимостью и склонностью иода окисляться кислородом воздуха. В связи с этим иодометрический метод имеет ограниченное применение.
Сильные восстановители определяют прямым титрованием стандартным раствором иода:
В иодометрии конечная точка титрования фиксируется по появлению или исчезновению окраски иода вблизи точки эквивалентности. Обычно для обнаружения конечной точки титрования раствором иода используют три различных приема.
Если иод – единственное окрашенное вещество в системе, появление или исчезновение желто-оранжевой окраски его является довольно чувствительным признаком для установления конечной точки титрования. Чтобы добиться более высокой чувствительности, к раствору добавляют несколько миллилитров не смешивающегося с водой органического растворителя, например, тетрахлорида углерода или хлороформа. При встряхивании основная масса иода переходит в органический слой и придает ему интенсивную фиолетовую окраску.
Широко используемым индикатором в иодометрии является водная суспензия крахмала, придающая раствору, содержащему следы иода, интенсивную синюю окраску за счет образования иод-крахмального комплекса.
Иодометрию применяют в аналитической практике для определения неорганических и органических соединений. Примеры таких определений представлены в таблице 4.3.