Свойства сернистой кислоты и её взаимодействие с другими веществами
Сернистая кислота — что она собой представляет
Сернистая кислота — это двухосновная кислородсодержащая кислота.
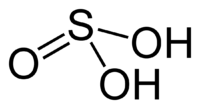
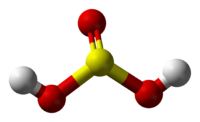
Сернистая кислота является неустойчивым веществом, распадающимся на диоксид серы S O 2 и воду. Валентность серы в сернистой кислоте равна IV, а степень окисления: +4. Структурная формула выглядит так:
Химические и физические свойства
Сернистый ангидрид S O 2 представляет собой бесцветный газ и обладает резким запахом.
Физические свойства сернистой кислоты:
Сернистая кислота в водном растворе является слабым электролитом. Диссоциация протекает обратимо по двум ступеням.
H 2 S O 3 ↔ H S O 3 – + H +
H S O 3 – ↔ S O 3 2 – + H +
В процессе самопроизвольного распада сернистой кислоты образуются диоксид серы и вода.
H 2 S O 3 ↔ S O 2 + H 2 O
Сернистая кислота вступает в химическую реакцию с сильными основаниями и их оксидами.
Взаимодействие сернистой кислоты с гидроксидами таких щелочных металлов, как натрий и калий, описывается уравнениями:
H 2 S O 3 + К О Н → K H S О 3 + H 2 O
H 2 S O 3 + 2 К О Н → К 2 S О 3 + 2 H 2 O
Среди всех химических свойств сернистой кислоты наиболее ярко выражены ее восстановительные свойства. Взаимодействуя с окислителями, сера повышают собственную степень окисления.
Обесцвечивание бромной воды с помощью сернистой кислоты:
H 2 S O 3 + B r 2 + H 2 O → H 2 S O 4 + 2 H B r
Процесс окисления сернистой кислоты азотной протекает достаточно легко по уравнению:
H 2 S O 3 + 2 H N O 3 → H 2 S O 4 + 2 N O 2 + H 2 O
Окисление сернистой кислоты с помощью озона:
H 2 S O 3 + O 3 → H 2 S O 4 + O 2
При контакте с сильными восстановителями могут проявляться окислительные свойства сернистой кислоты.
Взаимодействие сернистой кислоты и сероводорода сопровождается ее восстановлением до элементарной серы:
H 2 S O 3 + 2 Н 2 S → 3 S + 3 H 2 O
Качественная реакция на сернистую кислоту
Качественная реакция на сернистую кислоту представляет собой обесцвечивание раствора перманганата калия:
5 H 2 S O 3 + 2 K M n O 4 → 2 H 2 S O 4 + 2 M n S O 4 + K 2 S O 4 + 3 H 2 O
N a 2 S O 3 + 2 H C l → 2 N a C l + S O 2 ↑ + H 2 O
2 H + + S O 3 2 – → S O 2 ↑ + H 2 O
Способы получения и как применяется
Далее можно наблюдать реакцию, протекающую по уравнению:
C u ( м е д ь ) + 2 H 2 S O 4 ( с е р н а я к и с л о т а ) = C u S O 4 ( с у л ь ф а т с е р ы ) + S O 2 ( с е р н и с т ы й г а з ) + H 2 O ( в о д а )
Затем поток сернистого газа следует направить в пробирку с водой. При нахождении в ней газообразное вещество растворяется, частично протекает химическая реакция с водой. В итоге синтезируется сернистая кислота:
S O 2 ( с е р н и с т ы й г а з ) + H 2 O ( в о д а ) = H 2 S O 3
Таким образом с помощью пропускания сернистого газа через воду получают сернистую кислоту.
В процессе экспериментов с сернистым газом необходимо использовать индивидуальные средства защиты, так как вещество раздражает слизистую оболочку дыхательных путей. Подобное воздействие сопровождается воспалительным процессом и потерей аппетита. Длительное вдыхание сернистого газа приводит к потере сознания.
Сернистая кислота нашла применение в качестве восстановителя. Вещество используют для беления шерсти, шелка и других материалов, которые не способны выдержать отбеливание сильными окислителями в виде хлора. Сернистую кислоту используют в процессе консервирования плодов и овощей, а также для:
Сернистая кислота: строение и химические свойства
Сернистая кислота H2SO3 – это двухосновная кислородсодержащая кислота. При нормальных условиях — неустойчивое вещество, которое распадается на диоксид серы и воду.
Валентность серы в сернистой кислоте равна IV, а степень окисления +4.

Химические свойства
1. Сернистая кислота H2SO3 в водном растворе – двухосновная кислота средней силы. Частично диссоциирует по двум ступеням:
HSO3 – ↔ SO3 2– + H +
2. Сернистая кислота самопроизвольно распадается на диоксид серы и воду:
3. Сернистая кислота взаимодействует с сильными основаниями и их оксидами.
4. Наиболее ярко выражены восстановительные свойства сернистой кислоты. При взаимодействии с окислителями степень окисления серы повышается.
Азотная кислота очень легко окисляет сернистую:
Озон также окисляет сернистую кислоту:
Качественная реакция на сернистую кислоту – обесцвечивание раствора перманганата калия:
5. В присутствии сильных восстановителей сернистая кислота может проявлять окислительные свойства.
Оксид серы (IV)
Cпособы получения оксида серы (IV)
1. Сжигание серы на воздухе :
2. Горение сульфидов и сероводорода:
2CuS + 3O2 → 2SO2 + 2CuO
3. Взаимодействие сульфитов с более сильными кислотами:
4. Обработка концентрированной серной кислотой неактивных металлов.
Химические свойства оксида серы (IV)
SO2(изб) + NaOH → NaHSO3
Еще пример : оксид серы (IV) реагирует с основным оксидом натрия:
2. При взаимодействии с водой S O2 образует сернистую кислоту. Реакция обратимая, т.к. сернистая кислота в водном растворе в значительной степени распадается на оксид и воду.
3. Наиболее ярко выражены восстановительные свойства SO2. При взаимодействии с окислителями степень окисления серы повышается.
Сернистый ангидрид обесцвечивает бромную воду:
Азотная кислота очень легко окисляет сернистый газ:
Озон также окисляет оксид серы (IV):
Качественная реакция на сернистый газ и на сульфит-ион – обесцвечивание раствора перманганата калия:
Оксид свинца (IV) также окисляет сернистый газ:
4. В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства.
Оксид серы (IV) окисляет угарный газ и углерод:
SO2 + 2CO → 2СО2 + S
Сернистая кислота
| Сернистая кислота | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | сернистая кислота |
| Химическая формула | H2SO3 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Отн. молек. масса | 82.07 а. е. м. |
| Молярная масса | 82.07 г/моль |
| Плотность | 1,03 г/см³ |
| Термические свойства | |
| Химические свойства | |
| pKa | 1,81 |
| Растворимость в воде | 14.73 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7782-99-2 |
| Регистрационный номер EC | 231-973-1 |
| Безопасность | |
| Токсичность |  |
Серни́стая кислота — неустойчивая двухосновная неорганическая кислота средней силы. Химическая формула 
Химические свойства
Кислота средней силы:

Существует лишь в разбавленных водных растворах (в свободном состоянии не выделена):
Растворы H2SO3 всегда имеют резкий специфический запах (похожий на запах зажигающейся спички), обусловленный наличием химически не связанного водой SO2.
Двухосновная кислота, образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи):
и средние — сульфиты (в избытке щёлочи):
Как и сернистый газ, сернистая кислота и её соли являются сильными восстановителями:
При взаимодействии с ещё более сильными восстановителями может играть роль окислителя:
Качественная реакция на сульфит-ионы — обесцвечивание раствора перманганата калия:
слабая двухосновная кислота, отвечающая степени окисления серы +4
Применение
Сернистая кислота и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора). Сернистую кислоту применяют при консервировании плодов и овощей. Гидросульфит кальция (сульфитный щелок, Са(HSO3)2) используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнин — вещество, связывающее волокна целлюлозы, в результате чего волокна отделяются друг от друга; обработанную таким образом древесину используют для получения бумаги).
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Сернистая кислота» в других словарях:
СЕРНИСТАЯ КИСЛОТА — H2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в водных растворах. Соли сернистой кислоты сульфиты … Большой Энциклопедический словарь
СЕРНИСТАЯ КИСЛОТА — (H2SO3) слабая двухосновная кислота. Существует лишь в водных растворах. Соли С. к. сульфиты. Применяют в целлюлозно бумажной и пищевой промышленности. См. также Кислоты и ангидриды … Российская энциклопедия по охране труда
сернистая кислота — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN sulfurous acid … Справочник технического переводчика
сернистая кислота — Н2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в водных растворах. Соли серной кислоты сульфиты. * * * СЕРНИСТАЯ КИСЛОТА СЕРНИСТАЯ КИСЛОТА, H2SO3, слабая двухосновная кислота. В свободном виде не выделена,… … Энциклопедический словарь
сернистая кислота — sulfito rūgštis statusas T sritis chemija formulė H₂SO₃ atitikmenys: angl. sulfurous acid rus. сернистая кислота ryšiai: sinonimas – vandenilio trioksosulfatas (2–) … Chemijos terminų aiškinamasis žodynas
Сернистая кислота — H2SO3, слабая двухосновная кислота, отвечающая степени окисления серы +4. Известна только в разбавленных водных растворах. Константы диссоциации: K1 = 1,6 · 10 2, K2 = 1,0 · 10 7 (18°C). Даёт два ряда солей: нормальные Сульфиты и кислые… … Большая советская энциклопедия
СЕРНИСТАЯ КИСЛОТА — H2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в вод. р рах. Соли С. к. сульфиты … Естествознание. Энциклопедический словарь
Сернистая кислота — см. Сера … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
СЕРНИСТАЯ КИСЛОТА — см. Серы диоксид … Химическая энциклопедия
Сравнительная характеристика сернистой, селенистой и теллуристой кислот
Задача 843.
Дать сравнительную характеристику сернистой, селенистой и теллуристой кислот, указав изменения: а) устойчивости; б) кислотных свойств; в) окислительно-восстановительных свойств. Ответ иллюстрировать реакциями.
Решение:
а) В ряду H2SO3 — H2SeO3 — H2TeO3 устойчивость веществ закономерно уменьшается. Объясняется это тем, что при возрастании порядкового номера элемента возрастает его заряд и, соответственно, увеличивается радиус его атома, число электронных слоёв. При этом растёт удаление внешних электронов от ядра. С увеличением размеров внешних электронных облаков атомов степень их перекрывания уменьшается. Поэтому при переходе от H2SO3 к H2TeO3 уменьшается степень перекрывания электронных облаков атомов водорода и атома элемента главной подгруппы VI группы, а область перекрывания располагается на большем расстоянии от ядра атома элемента (S, Se, Te) и сильнее экранируется возросшим числом промежуточных электронных слоёв. Кроме того, в ряду S — Se — Te электроотрицательность атома элемента уменьшается. Поэтому в молекуле H2SO3 электронное облако атома водорода смещается в сторону атома кислорода в наибольшей степени, а в молекулах H2SeO3 — H2TeO3 – всё меньше и меньше. Это также приводит к уменьшению перекрывания взаимодействующих электронных облаков и, тем самым, к ослаблению связи между атомами. С уменьшением прочности связи в молекулах данных соединений элементов главной подгруппы VI группы падает устойчивость к нагреванию в ряду H2SO3 — H2SeO3 — H2TeO3. Сернистая кислота H2SO3 – очень непрочное соединение. Она известна только в водных растворах. При попытке выделить сернистую кислоту она распадается на SO2 и воду. Например, при действии концентрированной серной кислоты на раствор сульфита натрия вместо сернистой кислоты выделяется диоксид серы:
Теллуристая кислота H2TeO3 вообще не существует в природе.
в) Атомы элементов в H2SO3, H2SeO3 и H2TeO3 находятся в своей промежуточной степени окисления равной +4 и поэтому они могут проявлять как окислительные, так и восстановительные свойства. Сильные восстановители восстанавливают их до элементов. Сильные окислители окисляют до элемента в своей степени окисления +6, например:
Так как элементы S, Se и Те в H2SO3, H2SeO3 и H2TeO3 находятся в промежуточной степени окисления, то эти кислоты и их соли могут проявлять одновременно свойства и окислителя, и восстановителя, т. е. давать реакции самоокисления-восстановления, например сульфиты активных металлов при прокаливании разлагаются с образованием сульфидов и сульфатов:
Причём в ряду H2SO3 — H2SeO3 — H2TeO3 восстановительные свойства усиливаются, а окислительные уменьшаются. Объясняется это тем, что с ростом размеров атомов элементов уменьшается электростатическое взаимодействие внешних электронов и ядром, при этом атому легче отдать электрон, чем его принять.
Задача 844.
Какой из элементов VI группы образует шестиосновную кислоту? Написать ее формулу. Почему остальные элементы этой подгруппы не образуют подобных кислот?
Решение:
Из элементов VI группы теллур образует шестиосновную кислоту Н6ТеО6 (ортотеллуровая кислота). Образуется эта кислота при хранении очень слабой теллуровой кислоты, которая, в отличие от серной и селеновой кислоты, является очень слабой кислотой, поэтому она присоединяет молекулу Н2О и выпадает из раствора в виде кристаллов состава Н6ТеО6:
Н2SO4 и Н2ТеО4 – сильные электролиты, которые в водных растворах образуют ионы SO4 2- и SеО4 2- :
Теллуровая кислота с водой вступает во взаимодействие с образованием ортотеллуровой кислоты:
Триоксид теллура ТеО3, в отличие от триоксидов серы и селена, медленно взаимодействует с водой с образование слабой ортотеллуровой кислоты:
Задача 846.
Какие процессы последовательно протекают при постепенном добавлении щелочи к насыщенному раствору сероводорода? Написать уравнения реакций в ионно-молекулярной форме.
Решение:
Раствор сероводорода представляет собой слабый электролит. Сероводород – слабая двухосновная кислота. Она диссоциирует ступенчато и в основном по первой ступени:
Диссоциация по второй ступени протекает в ничтожно малой степени:
Поэтому при постоянном добавлении щёлочи к насыщенному раствору сероводорода сначала образуется кислая соль гидросульфид натрия:
затем образуется растворимая соль сульфид натрия:










