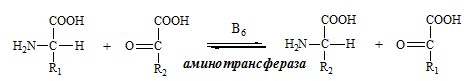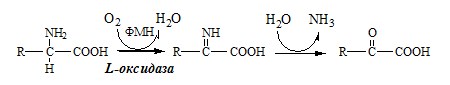Что такое аминокислоты и как их правильно принимать
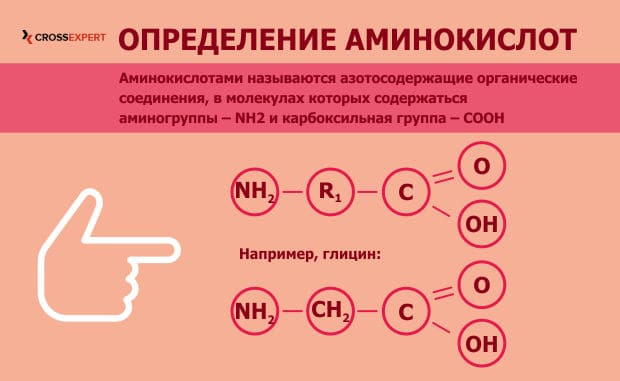
Аминокислоты – органические вещества, состоящие из углеводородного скелета и двух дополнительных групп: аминной и карбоксильной. Последние два радикала обусловливают уникальные свойства аминокислот – они могут проявлять свойства как кислот, так и щелочей: первые – за счет карбоксильной группы, вторые – за счет аминогруппы.
Итак, мы выяснили, что такое аминокислоты с точки зрения биохимии. Теперь рассмотрим их влияние на организм и применение в спорте. Для спортсменов аминокислоты важны своим участием в протеиновом обмене. Именно из отдельных аминокислот строятся протеины для роста мышечной массы нашего тела – мышечная, скелетная, печеночная, соединительная ткани. Помимо этого, некоторые аминокислоты напрямую участвуют в обмене веществ. К примеру, аргинин участвует в орнитиновом цикле мочевины – уникальном механизме обезвреживания аммиака, образующегося в печени в процессе переваривания белков.
Перечислять можно долго, однако остановимся на аминокислоте, значение которой особенно велико для спортсменов и людей, умеренно занимающихся спортом.
Для чего нужен глютамин
Глютамин – аминокислота, лимитирующая синтез протеина, из которого состоит наша иммунная ткань – лимфатические узлы и отдельные образования лимфоидной ткани. Значение этой системы переоценить трудно: без должного сопротивления инфекциям ни о каком тренировочном процессе говорить не приходится. Тем более, что каждая тренировка – не важно, профессиональная или любительская – это дозированный стресс для организма.
Стресс – необходимое условие, чтобы сдвинуть с места нашу “точку равновесия”, то есть вызвать определенные биохимические и физиологические изменения в организме. Любой стресс – это цепь реакций, мобилизующих тело. В промежуток, характеризующий регресс каскада реакций симпатоадреналовой системы (а именно они и представляют собой стресс), происходит снижение синтеза лимфоидной ткани. По этой причине процесс распада превышает скорость синтеза, а значит, иммунитет ослабевает. Так вот, дополнительный прием глютамина сводит к минимуму этот крайне нежелательный, но неизбежный эффект физической нагрузки
Незаменимые и заменимые аминокислоты
Чтобы понять, для чего нужны незаменимые аминокислоты в спорте, необходимо иметь общие представления о белковом обмене. Потребленные человеком белки на уровне желудочно-кишечного тракта обрабатываются ферментами – веществами, расщепляющими пищу, которую мы употребили.
В частности, белки распадаются сперва до пептидов – отдельных цепочек аминокислот, не имеющих четвертичной пространственной структуры. И уже пептиды распадутся на отдельные аминокислоты. Те, в свою очередь, усваиваются организмом человека. Это значит, что аминокислоты всасываются в кровь и только с этого этапа могут быть использованы в качестве продуктов для синтеза белка тела.
Забегая вперед скажем, что прием отдельных аминокислот в спорте сокращает этот этап – отдельные аминокислоты будут сразу же всасываться в кровь и процессы синтеза, а также биологический эффект аминокислот наступят быстрее.
Всего существует двадцать аминокислот. Чтобы процесс синтеза белка в теле человека стал возможным в принципе, в рационе человека должен присутствовать полный спектр – все 20 соединений.
Незаменимые
Вот с этого момента и появляется понятие незаменимости. К незаменимым аминокислотам относятся те, которые наше тело не способно синтезировать самостоятельно из других аминокислот. А это значит, что появится им, кроме как из продуктов питания, неоткуда. Таких аминокислот насчитывается 8 плюс 2 частично-заменимые.
Рассмотрим в таблице, в каких продуктах содержится каждая незаменимая аминокислота и какова ее роль в организме человека:
В достаточном количестве аминокислоты содержатся в животных источниках белка – рыбе, мясе, птице. При отсутствии таковых в рационе весьма целесообразен прием недостающих аминокислот в качестве добавок спортивного питания, что особенно актуально для спортсменов-вегетарианцев.
Основное внимание последним стоит обратить на такие добавки, как ВСАА – смесь лейцина, валина и изолейцина. Именно по этим аминокислотам возможна “просадка” в рационе, не содержащем животных источников белка. Для спортсмена (как профессионала, так и любителя) это абсолютно не допустимо, так как в долгосрочной перспективе приведет к катаболизму со стороны внутренних органов и к заболеваниям последних. В первую очередь страдает от недостатка аминокислот печень.
Заменимые
Заменимые аминокислоты и их роль рассмотрим в таблице ниже:
| Название | Роль в организме |
| Аланин | Принимает участие в глюконеогенезе печени |
| Пролин | Отвечает за составление прочной структуры коллагена |
| Левокарнитин | Поддерживает кофермент А |
| Тирозин | Отвечает за ферментативную активность |
| Серин | Отвечает за построение природных белков |
| Глютамин | Синтезирует протеины мышц |
| Глицин | Снижает напряжение т уменьшает агрессивность |
| Цистеин | Положительно влияет на текстуру и состояние кожи |
| Таурин | Оказывает метаболическое действие |
| Орнитин | Принимает участие в биосинтезе мочевины |
Что происходит с аминокислотами и протеинами в вашем теле
Аминокислоты, попавшие в кровоток, в первую очередь распределяются по тканям тела, где в них есть наибольшая потребность. Если у вас есть “просадка” по определенным аминокислотам, прием дополнительного количества белка, богатого ими, или прием дополнительных аминокислот, будет особенно полезен.
Синтез белка происходит на клеточном уровне. В каждой клетка есть ядро – самая важная часть клетки. Именно в ней происходит считывание генетической информации и ее воспроизводство. По сути, вся информация о строении клеток закодирована в последовательности аминокислот.
Как выбрать аминокислоты рядовому любителю, умеренно занимающемуся спортом 3-4 раза в неделю? Никак. Они ему просто не нужны.
Более важны для современного человека следующие рекомендации:
Эти элементарные манипуляции принесут гораздо больше, чем добавление в рацион каких бы то ни было добавок. Более того, добавки без соблюдения указанных условий будут абсолютно бесполезны.
Зачем знать, какие аминокислоты вам нужны, если вы питаетесь непонятно чем? Откуда вы знаете, из чего сделаны котлеты в столовой? Или сосиски? Или что за мясо в котлете в бургера? Про начинку для пиццы вообще промолчим.
Поэтому прежде, чем делать вывод о потребности в аминокислотах, нужно начать питаться простыми, чистыми и полезными продуктами и выполнить описанные выше рекомендации.
То же самое касается дополнительного приема белка. Если в вашем рационе присутствует белок, в количестве 1,5- 2 г на килограмм массы тела, никакой дополнительный белок вам не нужен. Лучше потратить деньги на покупку качественных продуктов питания.
Важно также понимать, что протеин и аминокислоты – это не фармакологические препараты! Это всего лишь добавки спортивного питания. И ключевое слово здесь – добавки. Добавляют их по потребности.
Чтобы понять, есть ли потребность, нужно контролировать свое питание. Если вы уже прошли описанные выше шаги и поняли, что добавки все-таки необходимы, первое, что вы должны сделать – пойти в магазин спортивного питания и выбрать соответствующий продукт в соответствии с финансовыми возможностями. Единственное, чего не стоит делать новичкам – это покупать аминокислоты с натуральным вкусом: пить их будет затруднительно по причине чрезвычайной горечи.
Вред, побочные эффекты, противопоказания
Если у вас есть заболевания, характеризующиеся непереносимостью одной из аминокислот, вы об этом знаете с рождения, так же, как и ваши родители. Этой аминокислоты нужно избегать и дальше. Если же этого нет, говорить о вреде и противопоказаниях добавок нет смысла, поскольку это полностью натуральные вещества.
Аминокислоты – составляющая часть белка, белок – привычная часть рациона человека. Все то, что продается в магазинах спортивного питания – не является фармакологическими препаратами! Только дилетанты могут говорить о каком-то вреде и противопоказаниях. По той же причине нет смысла рассматривать такое понятие, как побочные эффекты аминокислот – при умеренному потреблении никаких негативных реакций быть не может.
Трезво подходите к своему рациону и спортивным тренировкам! Будьте здоровы!
Аминокислоты. Общие пути обмена аминокислот. Синтез мочевины.
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Аминокислоты. Общие пути обмена аминокислот. Биосинтез мочевины.
Аминокислоты. Физико-химические свойства
Аминокислоты белые кристаллические вещества, хорошо растворимые в воде. Имеют высокую температуру плавления, в твердом состоянии находятся в виде внутренней соли. Многие сладкие на вкус (гли).
Аминокислоты амфотерные вещества – проявляют свойства кислот и оснований.
К наиболее важным общим реакциям аминокислот относятся реакции:
Специфические реакции аминокислот связаны с наличием функциональных групп в радикале (окислительно-восстановительные реакции цис).
Аминокислоты. Классификация.
Классификация аминокислот по природе радикала:
Классификация аминокислот по количеству карбоксильных и аминогрупп:
Классификация аминокислот по функциональным группам в радикале:
Классификация аминокислот по способности к синтезу:
Аминокислоты. Функции
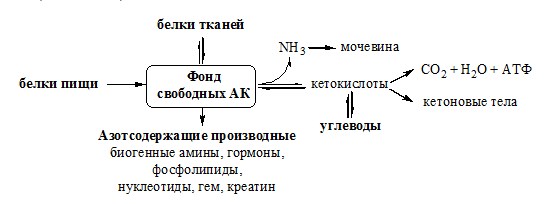
ПУТИ ОБРАЗОВАНИЯ ПУЛА АМИНОКИСЛОТ В КРОВИ
И ЕГО ИСПОЛЬЗОВАНИЕ В ОРГАНИЗМЕ
Большая часть аминокислот организма человека, примерно 15кг, входит в состав белков. Фонд свободных аминокислот организма составляет примерно 35г.
Источниками аминокислот в организме являются белки пищи, белки тканей и синтез АК из углеводов. В сутки у человека распадается на аминокислоты около 400г белков, примерно такое же количество синтезируется. Специальной формы депонирования аминокислот, подобно глюкозе (в виде гликогена) или жирных кислот (в виде ТГ), не существует (исключение – казеин молока). Поэтому резервом аминокислот служат все белки тканей, но преимущественно белки мышц (т.к. их много).
ОБЩИЕ РЕАКЦИИ ОБМЕНА АМИНОКИСЛОТ
Аминокислоты, появившиеся в организме, включаются в общие и специфические реакции обмена.
К общим реакциям обмена аминокислот относят реакции трансаминирования, дезаминирования и декарбоксилирования, биосинтеза белков и рацемизации (L переходы D).
ТРАНСАМИНИРОВАНИЕ (ПЕРЕАМИНИРОВАНИЕ) АМИНОКИСЛОТ
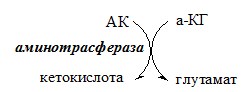
Трансаминирование — реакция переноса α-аминогруппы с аминокислоты на α-кетокислоту, в результате чего образуются новая α-кетокислота и новая аминокислота. Процесс трансаминирования легко обратим, при нем общее количество аминокислот в клетке не меняется.
Реакции катализируют аминотрансферазы, коферментом которых служит пиридоксальфосфат (ПФ) — производное витамина В6 (пиридоксина).
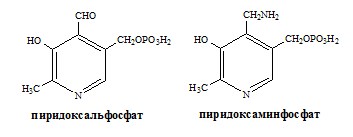
У человека найдено более 10 аминотрансфераз, которые локализуются в цитоплазме и митохондриях клеток. В реакции трансаминирования вступают почти все аминокислоты, за исключением лизина, треонина и пролина.
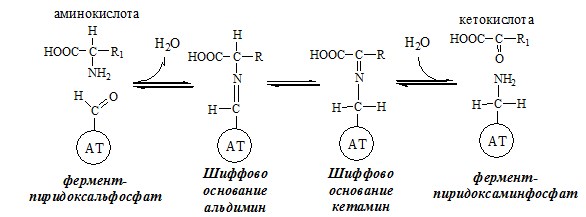
Механизм переаминирования
Вначале, аминоксилота передает свою аминогруппу на пиродоксальфосфат. Аминокислота при этом превращается в кетокислоту, а пиродоксальфосфат – в пиридоксаминфосфат.
Затем, реакции идут в обратную сторону: но уже другая кетокислота, принимает аминогруппу от пиридоксаминфосфата и превращается в новую АК, а пиридоксаминфосфат в пиродоксальфосфат.
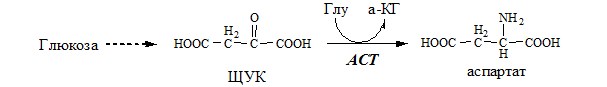
Органоспецифичные аминотрансферазы АЛТ и АСТ
Чаще всего в трансаминировании участвуют аминокислоты и кетокислоты, которых много в организме — глу, ала, асп, α-КГ, ПВК и ЩУК. Основным донором аминогруппы служит глу, а кетогруппы – α-КГ.
Наиболее распространёнными аминотрансферазами в большинстве тканей млекопитающих являются аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (ACT).
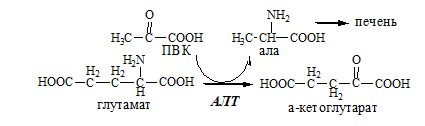
АЛТ катализирует реакцию трансаминирования между ала и α-КГ: ала+α-КГ↔ПВК+глу АЛТ локализуется в цитозоле клеток многих органов, больше всего ее в клетках печени и миокарде.
ACT катализирует реакцию трансаминирования между асп и α-КГ: асп+α-КГ↔ЩУК+глу
ACT имеет как цитоплазматическую, так и митохондриальную формы. Наибольшее ее количество обнаружено в миокарде и печени.
АСТ и АЛТ являются органоспецифичными ферментами, их определяют в крови для диагностики заболеваний печени, сердца и, в меньшей степени, скелетных мышц. Соотношение активностей АСТ/АЛТ называют «коэффициент де Ритиса». В норме он равен 1,33±0,42.
При инфаркте миокарда активность ACT в крови увеличивается в 8—10 раз, а АЛТ — в 1,5—2,0 раза, коэффициент де Ритиса резко возрастает.
При гепатитах активность АЛТ в сыворотке крови увеличивается в – 8—10 раз по сравнению с нормой, a ACT — в 2—4 раза. Коэффициент де Ритиса снижается до 0,6.
Биологическое значение трансаминирования
Реакции трансаминирования обеспечивают синтез и распад амино- и кетокислот, перераспределение аминного азота в тканях организма.
ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
Дезаминирование аминокислот — реакция отщепления α-аминогруппы от аминокислоты, в результате чего образуется соответствующая α-кетокислота и выделяется молекула аммиака.
Дезаминирование бывает прямым и непрямым.
Прямое дезаминирование аминокислоты
Прямое дезаминирование – это дезаминирование, которое происходит в 1 стадию с участием одного фермента. Прямому дезаминированию повергаются глу, гис, сер, тре, цис.
Существует 5 видов прямого дезаминирования аминокислот:
Окислительное дезаминирование – самый активный вид прямого дезаминирования аминокислот.
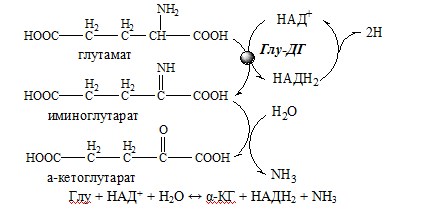
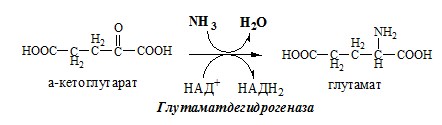
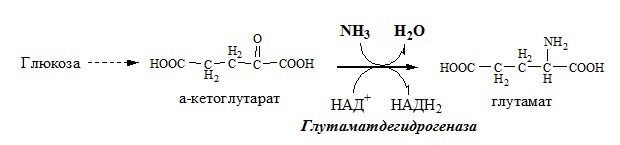
1. Глутаматдегидрогеназа (глу-ДГ) – олигомер, состоящий из 6 субъединиц (молекулярная масса 312 кД), содержит кофермент НАД+. Глу-ДГ катализирует обратимое дезаминирование глу, очень активна в митохондриях клеток практически всех органов, кроме мышц. Глу-ДГ аллостерически ингибируют АТФ, ГТФ, НАДH2, активирует избыток АДФ. Индуцируется Глу-ДГ стероидными гормонами (кортизолом).
Реакция идёт в 2 этапа. Вначале происходит ферментативное дегидрирование глутамата и образование α-иминоглутарата, затем — неферментативное гидролитическое отщепление иминогруппы в виде аммиака, в результате чего образуется α-кетоглутарат. При избытке аммиака реакция протекает в обратном направлении (как восстановительное аминирование α-кетоглутарата).
Глу + НАД+ + Н2О ↔ α-КГ + НАДН2 + NH3
2. Оксидаза L-аминокислот
В печени и почках есть оксидаза L-АК, способная дезаминировать некоторые L-аминокислоты:
Оксидаза L-АК имеет кофермент ФМН. Т.к. оптимум рН оксидазы L-АК равен 10,0, активность фермента очень низка и вклад ее в дезаминирование незначителен.
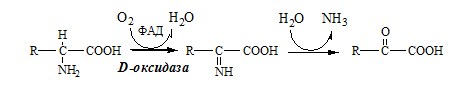
3. Оксидаза D-аминокислот
Оксидаза D-аминокислот также обнаружена в почках и печени. Это ФАД-зависимый фермент, с оптимумом рН в нейтральной среде. Оксидаза D-аминокислот превращает, спонтанно образующиеся из L-аминокислот, D-аминокислоты в кетокислоты.
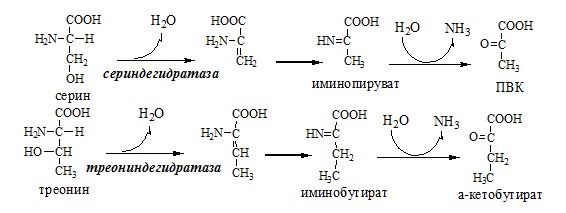
Неокислительное дезаминирование
В печени человека присутствуют специфические пиридоксальфосфатзависимые ферменты сериндегидратаза, треониндегидратаза, катализирующие реакции неокислительного дезаминирования аминокислот серина и треонина.
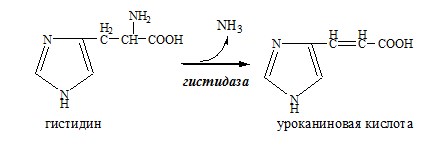
Внутримолекулярное дезаминирование
Внутримолекулярное дезаминирование характерно для гистидина. Реакцию катализирует гистидаза (гистидин-аммиаклиаза). Эта реакция происходит только в печени и коже.
Непрямое дезаминирование (трансдезаминирование) аминокислот
Непрямое дезаминирование – это дезаминирование, которое происходит в 2 стадий с участием нескольких ферментов. Оно характерно для большинства аминокислот, так как они не способны к прямому дезаминированию (нет ферментов).
На первой стадии происходит одна и несколько реакций переаминирования с участием аминотрансфераз, в результате аминогруппа аминокислоты переходит на кетосоединение (α-КГ, ИМФ).
На второй стадии происходит реакция дезаминирования аминосоединения (глу, АМФ), в результате чего образуется аммиак.
Последовательность реакций непрямого дезаминирования зависит от набора ферментов в тканях.
Непрямое дезаминирование в печени
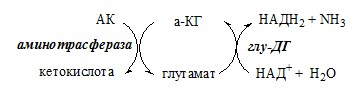
Непрямое дезаминирование аминокислоты происходит при участии 2 ферментов: аминотрансферазы и глу-ДГ. Аминогруппы аминокислоты в результате трансаминирования переносятся на α-КГ с образованием глутамата, который затем подвергается прямому окислительному дезаминированию.
Обе стадии непрямого дезаминирования обратимы, что обеспечивает как катаболизм аминокислот, так и возможность образования практически любой АК из соответствующей α-кетокислоты.
При энергодефиците АДФ активирует Глу-ДГ, что усиливает катаболизм аминокислот и образование а-кетоглутарата, поступающего в ЦТК как энергетический субстрат.
Таким образом, Глу-ДГ играет ключевую роль в регуляции обмена аминокислот и энергии.
Непрямое дезаминирование в мышцах (и нервной ткани)
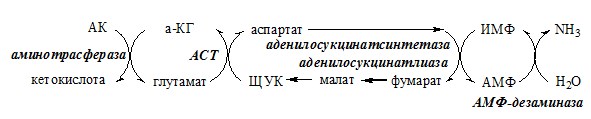
В мышечной ткани активность глу-ДГ низка, поэтому при интенсивной физической нагрузке функционирует ещё один путь непрямого дезаминирования с участием цикла ИМФ-АМФ.
Можно выделить 4 стадии этого процесса:
Этот путь дезаминирования преобладает в мышцах при интенсивной работе, в результате которой накапливается молочная кислота. Выделяющийся аммиак предотвращает закисление среды в клетках, вызванное образованием лактата.
Пути обмена безазотистого остатка аминокислот
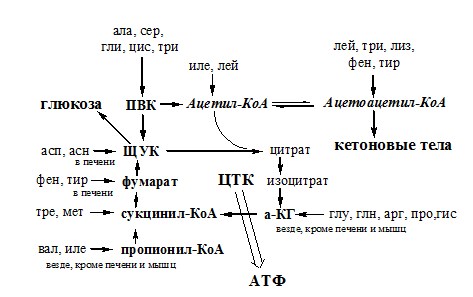
За сутки у человека распадаются примерно 100г АК. Катаболизм всех АК сводится к образованию шести веществ, вступающих в общий путь катаболизма: ПВК, ацетил-КоА, α-кетоглутарат, сукцинил-КоА, фумарат и ЩУК. Эти вещества окисляются в ЦТК для образования АТФ или используются для синтеза глюкозы и кетоновых тел.
Гликогенные аминокислоты – АК, которые превращаются в ПВК и промежуточные продукты ЦТК (а-КГ, сукцинил-КоА, фумарат, ЩУК). Они через ЩУК, используются в глюконеогенезе (ала, асн, асп, гли, глу, глн, про, сер, цис, арг, гис, вал, мет, тре).
Кетогенные аминокислоты – АК, которые в процессе катаболизма превращаются в ацетоацетат (Лиз, Лей) или ацетил-КоА (Лей) и могут использоваться в синтезе кетоновых тел.
Смешанные (глико-кетогенными) аминокислоты – АК, при катаболизме которых образуются метаболит цитратного цикла и ацетоацетат (Три, Фен, Тир) или ацетил-КоА (Иле). Эти АК используются для синтеза глюкозы и кетоновых тел.
ОБМЕН АММИАКА
Аммиак в организме образуется:
Концентрация аммиака
Концентрация аммиака в сыворотке крови в норме 11—35 мкмоль/л. В крови и цитозоле клеток при физиологических значениях рН аммиак переходит в ион аммония — NH4+, количество неионизированного NH3 невелико (
Токсичность аммиака
Аммиак — токсичное соединение. Даже небольшое повышение его концентрации оказывает неблагоприятное действие на организм, и, прежде всего на ЦНС.
Механизм токсического действия аммиака:
Связывание (обезвреживание) аммиака
В связи с токсичностью аммиака в тканях происходит его связывание с образованием нетоксичных соединений – АК и мочевины. Процесс образования и обезвреживания аммиака регулируют в основном ферменты глутаматдегидрогеназа и глутаминсинтетаза.
Обмен глутамата
В мозге и некоторых других органах может протекать восстановительное аминирование α-кетоглутарата под действием глутаматдегидрогеназы, катализирующей обратимую реакцию.
Однако этот путь обезвреживания аммиака в тканях используется слабо, так как глутаматдегидрогеназа катализирует преимущественно реакцию дезаминирования глутамата. Хотя, если учитывать последующее образование глутамина, реакция выгодна для клеток, так как способствует связыванию сразу 2 молекул NH3.
Обмен глутамина
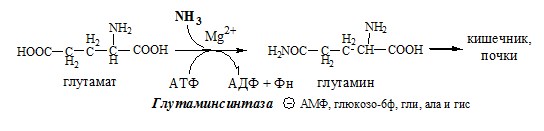
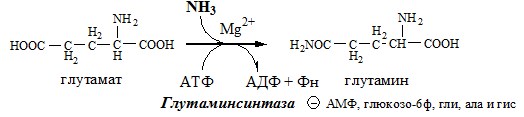
Основной реакцией связывания аммиака, протекающей во всех тканях организма (основные поставщики мышцы, мозг и печень), является синтез глутамина под действием глутаминсинтетазы:
Глутаминсинтетаза находиться в митохондриях клеток, содержит кофактор — ионы Mg2+, является одним из основных регуляторных ферментов обмена АК. Она аллостерически ингибируется АМФ, глюкозо-6ф, гли, ала и гис.
Глутамин, путём облегчённой диффузии, легко проходит клеточные мембраны (для глутамата возможен только активный транспорт), поступает из тканей в кровь и транспортируется в кишечник и почки.
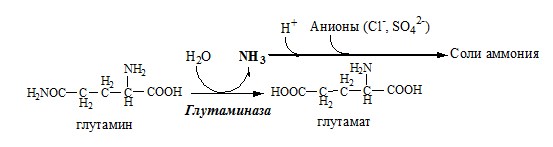
В почках происходит гидролиз глутамина под действием глутаминазы с образованием аммиака:
Аммиак с протонами и анионами образует соли аммония (0,5 г/сут), которые выделяются с мочой. Этот процесс используется для регуляции КОС и сохранения в организме важнейших катионов Na+ и К+. Глутаминаза почек значительно индуцируется при ацидозе, ингибируется при алкалозе.
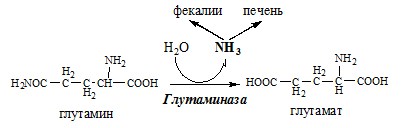
В клетках кишечника также под действием глутаминазы происходит гидролитическое освобождение амидного азота в виде аммиака:
Образовавшийся аммиак поступает через воротную вену в печень или удаляется из организма с фекалиями.
Высокий уровень глутамина в крови и лёгкость его поступления в клетки обусловливают использование глутамина во многих анаболических процессах. Глутамин — основной донор азота в организме. Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосахаров и других соединений.
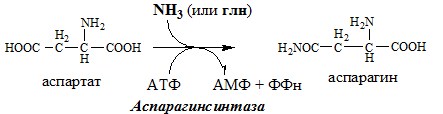
Обмен аспарагина
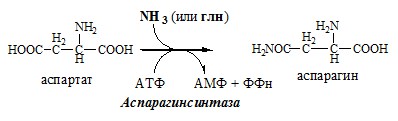
Обезвреживание аммиака в тканях происходит незначительно при синтезе аспарагина под действием глутаминзависимой и аммиакзависимой аспарагинсинтетазы.
Первая функционирует в животных клетках, вторая преобладает в бактериальных клетках, но присутствует и у животных.
Обмен аланина
Из мышц и кишечника избыток аминого азота выводится преимущественно в виде аланина.
В кишечнике:
Глутамат подвергается трансаминированию с ПВК с образованием аланина и α-кетоглутарата. Аланин поступает из кишечника в кровь воротной вены и поглощается печенью.
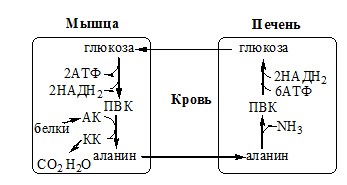
В мышцах:
Образование аланина в мышцах, его перенос в печень связан с обратным переносом в мышцы синтезированной в печени глюкозы.
Этот процесс называется глюкозо-аланиновый цикл:
Он необходим, так как активность глу-ДГ в мышцах невелика и непрямое дезаминирование АК малоэффективно.
Мышцы выделяют особенно много аланина в силу их большой массы, активного потребления глюкозы при физической работе, а также потому, что часть энергии они получают за счёт распада АК. Образовавшийся аланин поступает в печень, где подвергается непрямому дезаминированию. Выделившийся аммиак идет на синтез мочевины, а ПВК включается в глюконеогенез. Глюкоза из печени поступает в ткани и там, в процессе гликолиза, опять окисляется до ПВК.
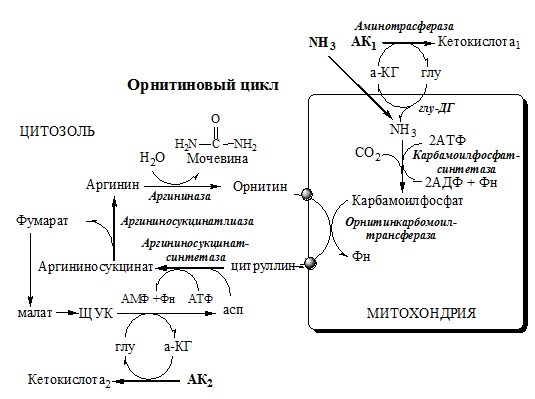
ОРНИТИНОВЫЙ ЦИКЛ
Большая часть свободного аммиака, а также аминного азота в составе (в основном глутамин, аланин) поступают в печень, где из них синтезируется нетоксичное и хорошо растворимое в воде соединение — мочевина. Мочевина является основной формой выведения азота из организма человека.
Синтез мочевины происходит в цикле, который замыкается орнитином. Цикл открыли в 40-х годах XX века немецкие биохимики Г. Кребс и К. Гензелейт.
Мочевина (карбамид) — полный амид угольной кислоты — содержит 2 атома азота, один из аммиака, другой – из асп.
Реакции орнитинового цикла
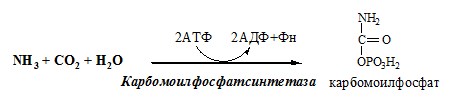
Предварительно в митохондриях под действием карбамоилфосфатсинтетазы I с затратой 2 АТФ аммиак связывается с СО2 с образованием карбамоилфосфата:
(Карбамоилфосфатсинтетаза II локализована в цитозоле клеток всех тканей и участвует в синтезе пиримидиновых нуклеотидов).
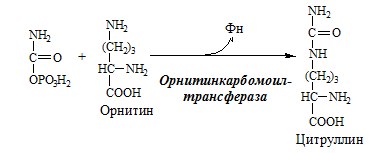
1. В митохондриях орнитинкарбамоилтрансфераза переносит карбамоильную группу карбамоилфосфата на орнитин и образуется — цитруллин:
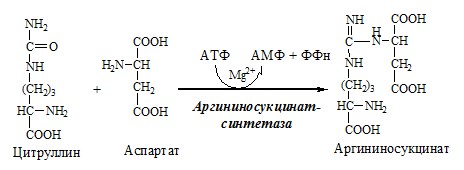
2. В цитозоле аргининосукцинатсинтетаза с затратой 1 АТФ (двух макроэргических связей) связывает цитруллин с аспартатом и образует аргининосукцинат (аргининоянтарная кислота). Фермент нуждается в Mg2+. Аспартат — источник второго атома азота мочевины.
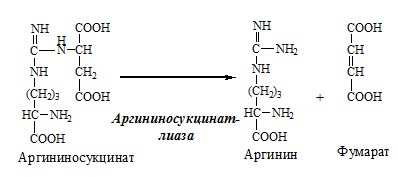
3. В цитозоле аргининосукцинатлиаза (аргининсукциназа) расщепляет аргининосукцинат на аргинин и фумарат (аминогруппа аспартата оказывается в аргинине).
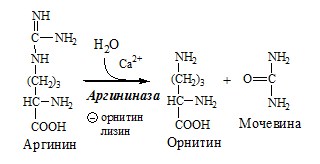
4. В цитозоле аргиназа гидролизует аргинин на орнитин и мочевину. У аргиназы кофакторы ионы Са2+ или Мn2+, ингибиторы – высокие концентрации орнитина и лизина.
Образующийся орнитин взаимодействует с новой молекулой карбамоилфосфата, и цикл замыкается.
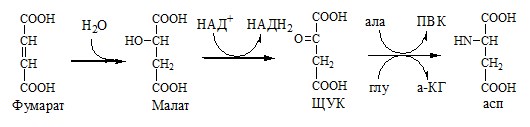
Регенерация аспартата из фумарата
Фумарат, образующийся в орнитиновом цикле, в цитозоле превращается в ЩУК, который переаминируется с аланином или глутаматом с образованием аспартата. Аланин поступает главным образом из мышц и клеток кишечника:
Малат может направиться в митохондрии и включиться в ЦТК.
Пируват, образующийся в этих реакциях из аланина, используется для глюконеогенеза.
Общее уравнение синтеза мочевины:
CO2 + NH3 + асп + 3 АТФ + 2 Н2О → мочевина + фумарат + 2АДФ + АМФ + 2Фн + ФФн
Энергетический баланс орнитинового цикла
На синтез 1 мочевины расходуются 4 макроэргических связи 3 АТФ. Дополнительные затраты энергии связаны с трансмембранным переносом веществ и экскрецией мочевины.
Энергозатраты при этом частично компенсируются:
Орнитиновый цикл в печени выполняет 2 функции:
Полный набор ферментов орнитинового цикла есть только в гепатоцитах. Отдельные же ферменты орнитинового цикла обнаруживаются в разных тканях. В энтероцитах, есть карбамоилфосфатсинтетаза I и орнитинкарбамоилтрансфераза, следовательно, может синтезироваться цитруллин. В почках есть аргининосукцинатсинтетаза и аргининосукцинатлиаза. Цитруллин, образовавшийся в энтероцитах, может поступать в почки и превращаться там в аргинин, который переносится в печень и гидролизуется аргиназой. Активность этих рассеянных по разным органам ферментов значительно ниже, чем в печени.
Выделение азота из организма
Азот выводиться из организма с мочой, калом, потом и с выдыхаемым воздухом в виде различных соединений. Основная масса азота выделяется из организма с мочой в виде мочевины (до 90%). В норме соотношение азотсодержащих веществ в моче составляет: мочевина 86%, креатинин 5%, аммиак 3%, мочевая кислота 1,5% и другие вещества 4,5%. Экскреция мочевины в норме составляет 25 г/сут, солей аммония 0,5 г/сут.
ГИПЕРАММОНИЕМИЯ
Нарушение реакций обезвреживания аммиака может вызвать повышение содержания аммиака в крови — гипераммониемию, что оказывает токсическое действие на организм.
Причинами гипераммониемии могут быть:
1. генетические дефекты ферментов орнитинового цикла в печени;
2. вторичное поражение печени в результате цирроза, гепатита или других заболеваний.
Известны пять наследственных заболеваний, обусловленные дефектом пяти ферментов орнитинового цикла.
Наследственные нарушения орнитинового цикла и их основные проявления
Гиперам-мониемия, тип I
В течение 24-48 ч после рождения кома, смерть
Гиперам-мониемия, тип II
Сцепленный с Х-хромосомой
Гипотония, снижение толерантности к белкам
Гипераммониемия тяжёлая у новорождённых. У взрослых — после белковой нагрузки
Гипераммониемия, атаксия, судороги, выпадение волос
Аргини-носукцинат NH 3
Аргини-носукци-нат, Глн, Ала, Лиз
Снижение активности какого-либо фермента синтеза мочевины приводит к накоплению в крови субстрата данного фермента и его предшественников.
При гипераммониемиях I и II типа происходит накопление карбамоилфосфата в митохондриях и выход его в цитозоль. Это вызывает увеличение скорости синтеза пиримидиновых нуклеотидов (вследствие активации карбамоилфосфатсинтетазы II), что приводит к накоплению оротата, уридина и урацила и выведению их с мочой.
Тяжесть течения заболевания зависит также от степени снижения активности ферментов.
Все нарушения орнитинового цикла приводят к значительному повышению в крови концентрации аммиака (до 6000 мкмоль/л), глутамина и аланина.
Гипераммониемия сопровождается появлением следующих симптомов:
В тяжёлых случаях развивается кома с летальным исходом.
Все симптомы гипераммониемии — проявление действия аммиака на ЦНС.
Для диагностики различных типов гипераммониемии производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, активности фермента в биоптатах печени.
Лечение больных с различными дефектами орнитинового цикла в основном направлено на снижение концентрации аммиака в крови за счёт малобелковой диеты, введения кетоаналогов АК в рацион и стимуляцию выведения аммиака в обход нарушенных реакций:
Обмен аминокислот и аммиака между тканями
Печень
В печень азот поступает в основном в виде аммиака, глутамина, аланина, а меньше в виде других аминокислот в основном из мышц и кишечника. Поглощает аминокислоты с разветвленной цепью (вал, лей, иле). Синтезирует глюкозу в основном из аланина и серина.
Мышцы
Поглощают аминокислоты с разветвленной цепью (вал, лей, иле). Выделяют много аланина и глутамина меньше других аминокислот.
Кишечник
Поглощает глутамин. Выделяет много аланина. С пищей из кишечника поступают все аминокислоты.
Мозг
Поглощает много аминокислот с разветвленной цепью (вал, лей, иле). Выделяет много глутамина.
Почки
Поглощают глутамин. Выделяют много серина и немного аланина.
ДЕКАРБОКСИЛИРОВАНИЕ АМИНОКИСЛОТ И ИХ ПРОИЗВОДНЫХ
Некоторые аминокислоты и их производные могут подвергаться декарбоксилированию – отщеплению α-карбоксильной группы. У млекопитающих декарбоксилируются: три, тир, вал, гис, глу, цис, арг, орнитин, SAM, ДОФА, 5-окситриптофан и т.д. Реакцию необратимо катализируют декарбоксилазы, которые содержат в активном центре пиридоксальфосфат. Механизм реакции похож на реакцию переаминирования.
Продуктами реакции являются СО2 и биогенные амины, выполняющие регуляторные функции (гормоны, тканевые гормоны, нейромедиаторы).
Серотонин
Серотонин образуется из триптофана в надпочечниках, ЦНС и тучных клетках.
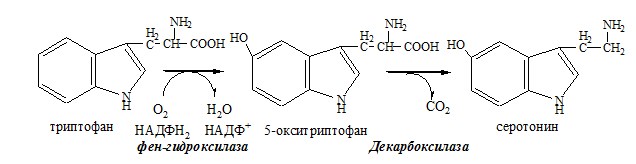
Серотонин – возбуждающий нейромедиатор средних отделов мозга (проводящих путей) и гормон. Стимулирует сокращение гладкой мускулатуры, вазоконстриктор, регулирует АД, температуру тела, дыхание, антидепрессант.
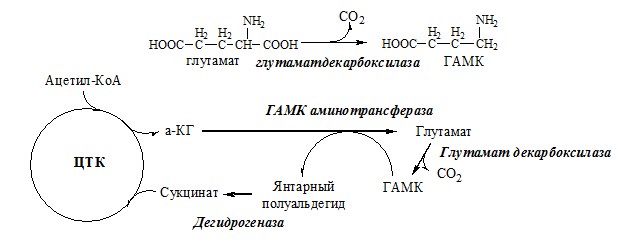
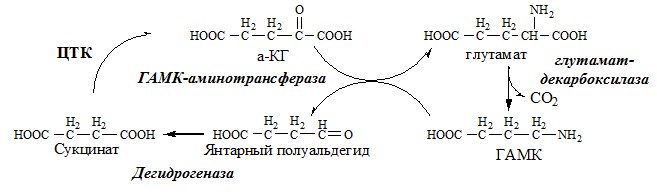
ГАМК
ГАМК образуется и разрушается в ГАМК-шунте ЦТК в высших отдела мозга. Он имеет очень высокую концентрацию.
ГАМК – тормозной нейромедиатор (повышает проницаемость постсинаптических мембран для К+), повышает дыхательную активность нервной ткани, улучшает кровоснабжение головного мозга.
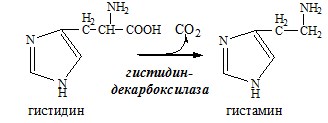
Гистамин
Гистамин образуется в тучных клетках. Секретируется в кровь при повреждении ткани, развитии иммунных и аллергических реакций.
Гистамин – медиатор воспаления, аллергических реакций, пищеварительный гормон:
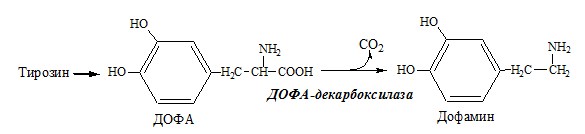
Дофамин
Дофамин образуется (фен → тир → ДОФА → дофамин) в мозге и мозговом веществе надпочечников.
Дофамин – нейромедиатор среднего отдела мозга.
Аминокислоты. Специфические пути обмена аминокислот
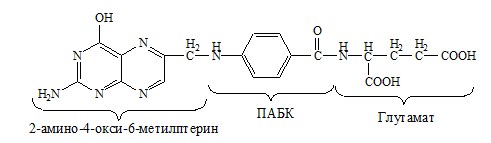
ФОЛИЕВАЯ КИСЛОТА
Значительную роль в обмене ряда АК, синтезе некоторых сложных липидов, нейромедиаторов, гормонов и ряда других веществ играют производные фолиевой кислоты.
Фолиевая кислота широко распространёна в продуктах животного и растительного происхождения, синтезируется микрофлорой кишечника.
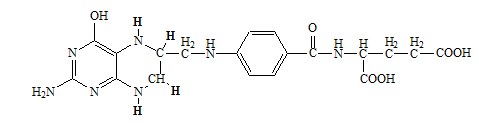
Активная форма фолиевой кислоты – ТГФК. Она образуется в печени при восстановлении фолиевой кислоты с участием фолатредуктазы и дигидрофолатредуктазы, коферментом которых служит НАДФН2.
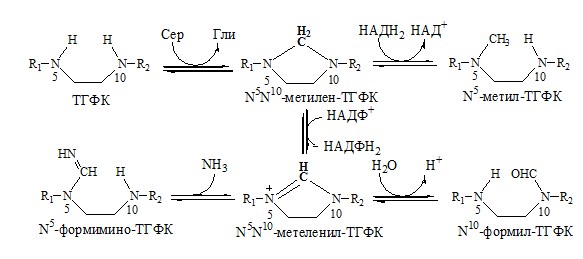
Образование одноуглеродных фрагментов, их взаимопревращения
ТГФК принимает от АК одноуглеродные фрагменты: серин и глицин дают метиленовый фрагмент (-СН2-), гистидин – формимино- и формильный фрагменты.
В составе ТГФК одноуглеродные фрагменты могут подвергаться взаимопревращениям: метиленовая группа превращаться в метенильную (-СН=), формильную (-НС=О), метильную (-СН3) и формиминогруппу (-CH=NH).
Затем ТГФК отдает одноуглеродные фрагменты на:
Недостаточность фолиевой кислоты
Гиповитаминоз фолиевой кислоты возникает редко, его вызывает использование сульфаниламидных препаратов. Сульфаниламиды — структурные аналоги парааминобензойной кислоты, они ингибируют синтез фолиевой кислоты у микроорганизмов, вызывая их гибель. Некоторые производные птеридина (аминоптерин и метотрексат) тормозят рост почти всех организмов, нуждающихся в фолиевой кислоте, их используют для подавления опухолевого роста у онкологических больных.
Гиповитаминоз фолиевой кислоты приводит к:
КОБАЛАМИН (В12)
В12 синтезируется только микроорганизмами, им богаты печень, почки. Активные формы кобаламина – метилкобаламин (цитоплазма) и дезоксиаденозилкобаламин (митохондрии).
Кобаламин участвует:
1. в передачи метила с метил-ТГФК на гомоцистеин при регенерации метионина.
2. в превращениях одноуглеродных фрагментов в составе ТГФК.
3. в метаболизме жирных кислот с нечетным числом атомов С и аминокислот с разветвленной цепью. Перенос протонов в реакциях изомеризации.
Недостаточность В12
Гиповитаминоз возникает при нарушении всасывании В12 (дефицит фактора Касла при пониженной кислотности желудочного сока).
Гиповитаминоз В12 сопровождается:
1. макроцитарной (мегалобластической) анемией: снижение числа эритроцитов, гемоглобина, увеличение размера эритроцитов. Причина — нарушение синтеза ДНК.
2. расстройствами деятельности нервной системы. При распаде жирных кислот с нечетным количеством атомов С и разветвленных АК из-за дефицита В12 накапливается нейротоксичная метилмалоновая кислота.
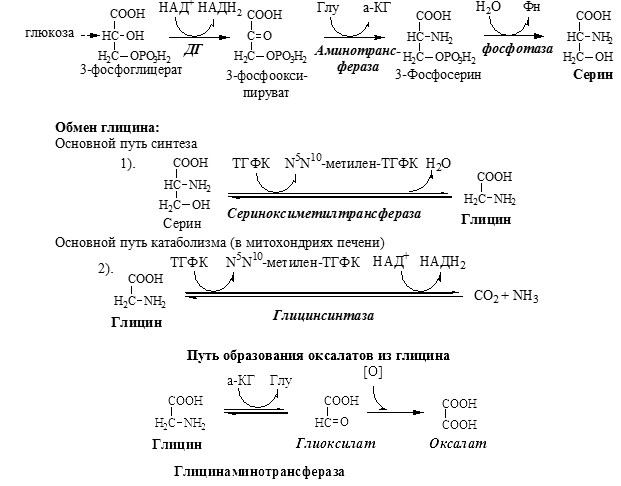
ОБМЕН СЕРИНА И ГЛИЦИНА
Серин и глицин – заменимые аминокислоты.
Синтез серина и глицина. Основной путь катаболизма глицина.
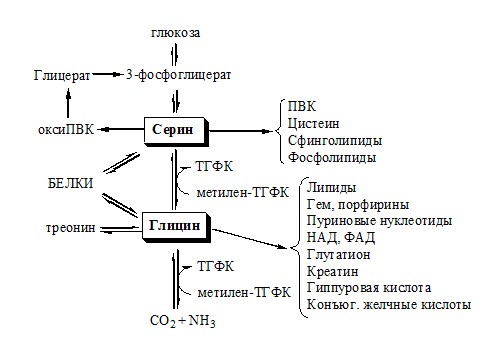
Схема путей обмена серина и глицина
Серии и глицин выполняют в организме человека разнообразные и очень важные функции.
Глицин — важнейший (после ГАМК) тормозной нейромедиатор в спинном мозге, промежуточном мозге и некоторых отделах головного мозга.
Наследственные нарушения обмена глицина
Известно несколько заболеваний, связанных с нарушениями обмена глицина. В их основе лежит недостаточность ферментов или дефект системы транспорта этой АК.
Гиперглицинемия возникает при дефекте глицинрасщепляющей системы. Проявляется повреждением мозга, судорогами, гипотонией, нарушением дыхания.
Глицинурия характеризуется повышенным выделением глицина с мочой (до 1 г/сут) при нормальном содержании его в крови. Причиной является нарушение реабсорбции глицина в почках.
Первичная гипероксалатурия характеризуется постоянно высоким выделением оксалата с мочой, независимо от поступления его с пищей. Дефект глицинаминотрансферазы блокирует превращение глиоксилата снова в глицин. Глицин → глиоксилат → оксалат
Прогрессирует двустороннее образование оксалатных камней в мочевыводящих путях, развиваются нефрокальциноз и инфекция мочевыводящих путей. Больные погибают в детском возрасте от почечной недостаточности или гипертонии.
В состав белков человека входят 2 АК, содержащие серу, — метионин и цистеин. Эти аминокислоты метаболически тесно связаны между собой.
МЕТИОНИН
Метионин — незаменимая аминокислота, может регенерировать из гомоцистеина с участием серина и глицина. Метионин:
1. участвует в синтезе белков организма;
2. является источником метильной группы, используемой в реакциях трансметилирования;
3. является источником атома серы, необходимого для синтеза цистеина;
4. участвует в реакциях дезаминирования;
5. Метионил-тРНК участвует в инициации процесса трансляции.
Образование S-аденозилметионина
Метильная группа в метионине прочно связана с серой, поэтому донором этого одноуглеродного фрагмента служит активная форма метионина – S-аденозилметионин (SAM). (SAM — нестабилен т.к. сера при валентности 2 имеет 3 связи). SAM образуется при присоединении метионина к аденозину с участием метионинаденозилтрансферазы (есть во всех типах клеток). Аденозин образуется при гидролизе АТФ.
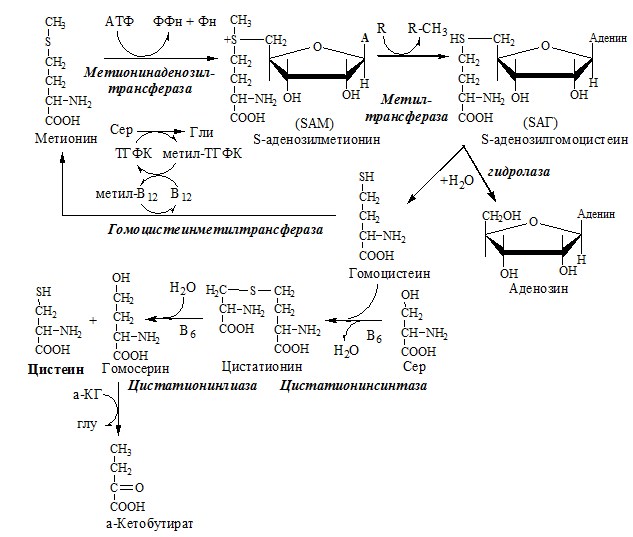
Ресинтез метионина, роль ТГФК и витамина В12.
Связь обменов метионина и цистеина
Реакции трансметилирования с участием S-аденозилметионина
Отщепление метильной группы от SAM и перенос её на соединение-акцептор катализируют ферменты метилтрансферазы. SAM в ходе реакции превращается в S-аденозилгомоцистеин (SAT).
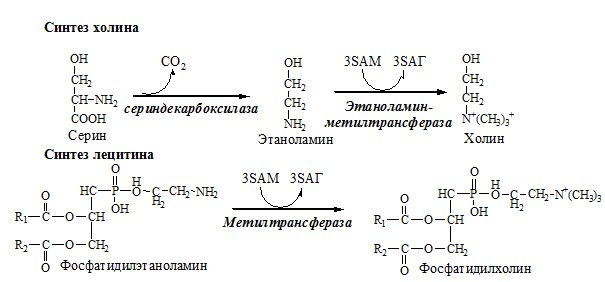
Синтез холина и синтез лецитина
Аналогично синтезируются:
1. из ГАМК → карнитин;
2. из гуанидинацетата → креатин;
3. из норадреналина → адреналин;
4. из карнозина → анзерин;
5. Реакции трансметилирования используются также в синтезе азотистых оснований, инактивации гормонов, нейромедиаторов и обезвреживании ксенобиотиков.
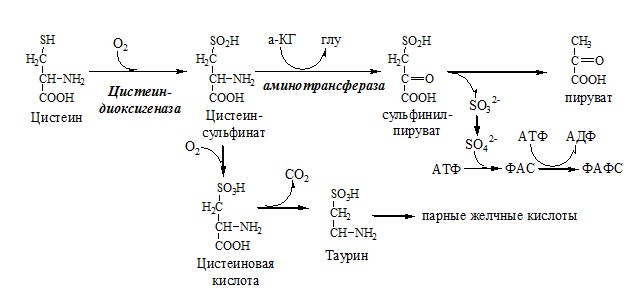
ЦИСТЕИН
Цистеин – серосодержащая условнозаменимая АК. Синтезируется из незаменимого метионина и заменимого серина.
Нарушение синтеза цистеина возникает при гиповитаминозе фолиевой кислоты, В6, В12 или наследственных дефектах цистатионинсинтазы и цистатионинлиазы. Гомоцистеин превращается в гомоцистин, который накапливается в крови, тканях и выделяется с мочой.
Обмен цистеина: схема путей, их значение.
Цистеин:
Образование сульфат-иона, его утилизация (образование ФАФС).
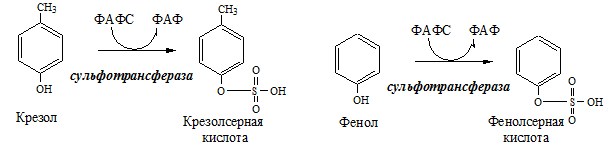
ФАФС используется:
1. В обезвреживании ксенобиотиков:
2. В синтезе гликозаминогликанов (сульфирование ОН групп производных глюкозы, галактозы сульфотрансферазой).
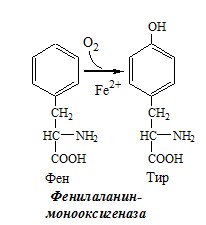
ФЕНИЛАЛАНИН
Фенилаланин — незаменимая АК, которая содержится в достаточных количествах в пищевых продуктах. Фенилаланин идет в основном на синтез белков и тирозина.
Превращение фенилаланина в тирозин необратимо катализирует фенилаланингидроксилаза (монооксигеназа), коферментом которой служит тетрагидробиоптерин (Н4БП), кофактором – Fe2+. Н4БП в результате реакции окисляется в дигидробиоптерин (Н2БП). Регенерация последнего происходит при участии дигидроптеридинредуктазы с использованием НАДФH2.
Реакция необходима для удаления избытка фенилаланина, так как высокие концентрации его токсичны для клеток. Образование тирозина не имеет большого значения, так как недостатка этой аминокислоты в клетках практически не бывает.
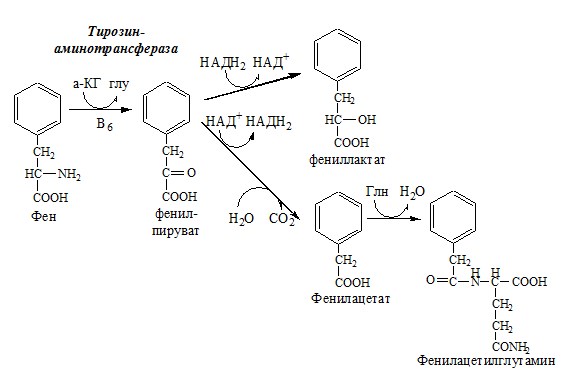
Фенилкетонурия
В печени здоровых людей небольшая часть фенилаланина (10%) превращается в фениллактат и фенилацетилглутамин. При дефекте фенилаланингидроксилазы этот путь катаболизма фенилаланина становится главным, что способствует развитию фенилкетонурии (ФКУ).
Классическая фенилкетонурия— наследственное заболевание, связанное с мутациями в гене фенилаланингидроксилазы (частота 1:10000 новорождённых), которые приводят к снижению активности фермента или полной его инактивации.
При ФКУ концентрация фен повышается в крови в 20—30 раз, в моче — в 100—300 раз по сравнению с нормой. В крови и моче повышается содержание метаболитов альтернативного пути: фенилпирувата, фенилацетата, фениллактата и фенилацетилглутамина.
Проявления фенилкетонурии:
1. нарушение умственного и физического развития;
2. судорожный синдром;
3. нарушение пигментации.
Проявления фенилкетонурии связаны с токсическим действием на клетки мозга высоких концентраций фенилаланина, фенилпирувата, фениллактата. Большие концентрации фенилаланина ограничивают транспорт тирозина и триптофана через гематоэнцефалический барьер и тормозят синтез нейромедиаторов (дофамина, норадреналина, серотонина).
Прогрессирующее нарушение умственного и физического развития у детей, больных ФКУ, можно предотвратить диетой с очень низким содержанием или полным исключением фенилаланина. Если такое лечение начато сразу после рождения ребёнка, то повреждение мозга предотвращается. Считается, что ограничения в питании могут быть ослаблены после 10-летнего возраста (окончание процессов миелинизации мозга), однако в настоящее время многие педиатры склоняются в сторону «пожизненной диеты». При отсутствии лечения больные не доживают до 30 лет.
Для диагностики фенилкетонурии используют качественные и количественные методы обнаружения патологических метаболитов в моче, определение концентрации фенилаланина в крови и моче.
Дефектный ген, ответственный за фенилкетонурию, можно обнаружить у фенотипически нормальных гетерозиготных носителей с помощью теста толерантности к фенилаланину.
ТИРОЗИН
Тирозин — условно заменимая АК, образуется из незаменимого фенилаланина. Содержание тир в пищевых белках достаточно велико.
Тирозин используется в синтезе белков, катехоламинов, тиреоидных гормонов и меланинов.
Обмен тирозина зависит от типа тканей.
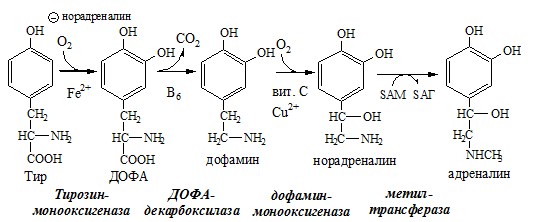
1. Обмен тирозина в надпочечниках и нервной ткани
В мозговом веществе надпочечников и нервной ткани тирозин метаболизирует по катехоламиновому пути с образованием дофамина, норадреналина и адреналина (только в надпочечниках).
Болезнь Паркинсона
Болезнь Паркинсона развивается при снижении активности тирозинмонооксигеназы и ДОФА-декарбоксилазы, что приводит к недостаточности дофамина в чёрной субстанции мозга. Это одно из самых распространённых неврологических заболеваний (частота 1:200 среди людей старше 60 лет). Заболевание сопровождается акинезией (скованность движений), ригидностью (напряжение мышц) и тремором (непроизвольное дрожание).
Дофамин не проникает через гематоэнцефалический барьер и как лекарственный препарат не используется. Для лечения паркинсонизма используют заместительную терапию препаратами-предшественниками дофамина (производными ДОФА) — леводопа, мадопар, наком и др. Также подавляют инактивацию дофамина ингибиторами МАО (депренил, ниаламид, пиразидол и др.).
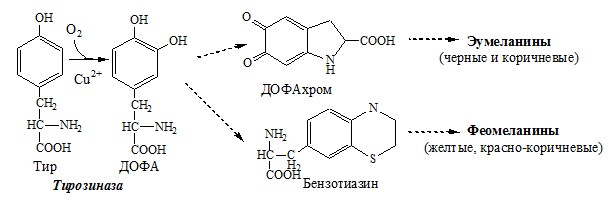
2. Обмен тирозина в меланоцитах
В пигментных клетках (меланоцитах) обмен тирозин идет по меланиновому пути. Из тирозина синтезируются пигменты — меланины 2 типов: эумеланины и феомеланины. Эумеланины (чёрного и коричневого цвета) — нерастворимые высокомолекулярные полимеры 5,6-дигидроксииндола. Феомеланины — жёлтые или красновато-коричневые полимеры, растворимые в разбавленных щелочах.
Меланины присутствуют в сетчатке глаз, в составе волос, в коже. Цвет кожи зависит от распределения меланоцитов и количества в них разных типов меланинов.
Альбинизм
При наследственном дефекте тирозиназы (1:20000) в меланоцитах нарушается синтез меланинов и развивается альбинизм.
Клиническое проявление альбинизма (от лат. albus — белый) — отсутствие пигментации кожи, сетчатки глаз и волос. У больных часто снижена острота зрения, возникает светобоязнь. Длительное пребывание таких больных под открытым солнцем приводит к раку кожи.
3. Превращение тирозина в щитовидной железе
В щитовидной железе из тирозина синтезируются и выделяются гормоны йодтиронины: тироксин (тетрайодтиронин) и трийодтиронин.
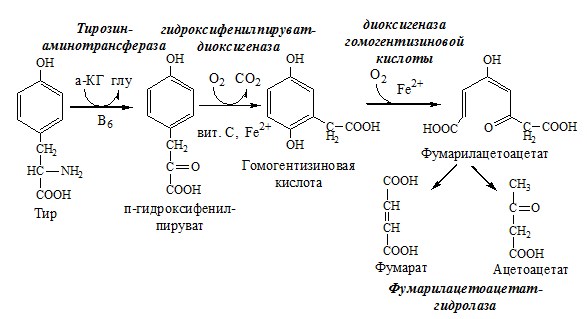
4. Катаболизм тирозина в печени
Катаболизм тирозина происходит в печени по гомогентизиновому пути (схема).
Фумарат может окисляться до СО2 и Н2О или использоваться для глюконеогенеза. Ацетоацетат — кетоновое тело, окисляемое до СО2 и Н2О с выделением энергии.
Алкаптонурия («чёрная моча»)
При наследственном дефекте диоксигеназы гомогентизиновой кислоты (2—5 случаев на 1 млн новорождённых) развивается алкаптонурия. При алкаптонурии происходит накопление в организме гомогентизиновой кислоты, избытки которой выделяются с мочой. На воздухе гомогентизиновая кислота окисляется с образованием тёмных пигментов – алкаптонов.
Клиническими проявлениями болезни, кроме потемнения мочи на воздухе, являются пигментация соединительной ткани (охроноз) и артрит.
Тирозинемии
Некоторые нарушения катаболизма тирозина в печени приводят к тирозинемии и тирозинурии.
Различают 3 типа тирозинемии.
ТРИПТОФАН
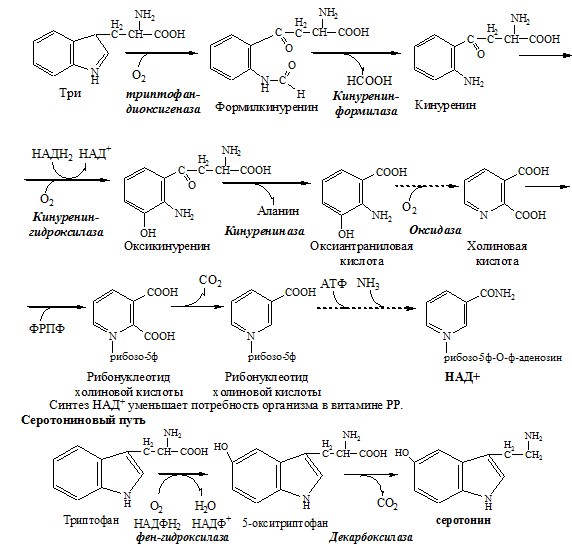
Триптофан – незаменимая АК. В физиологических условиях >95% триптофана метаболизирует по кинурениновому пути и 1% по серотониновому пути.
Схема кинуренинового пути
Серотонин образуется в надпочечниках, ЦНС и тучных клетках.
Серотонин – возбуждающий нейромедиатор средних отделов мозга (проводящих путей) и гормон. Стимулирует сокращение гладкой мускулатуры, вазоконстриктор, регулирует АД, температуру тела, дыхание, антидепрессант.
Образование и использование в организме ГАМК и ГОМК. Антиоксидантные, антигипоксические и адаптогенные свойства Глу, Асп, их клиническое применение.
ГЛУТАМАТ
Синтез глутамата
Глутамат образуется:
1). при восстановительном аминировании α-кетоглутарата глутаматдегидрогеназой:
2). В реакция переаминирования с участием аминотрансфераз:
Использование глутамата
Глутамат содержится в больших количествах в головном мозге, где выполняет разнообразные функции:
Нарушение обмена глутамата приводит к целому ряду патологических нарушений ЦНС: эпилепсии, расстройствах вестибулярной системы, ишемии и др. Глутамат и его аналоги используют как лекарственные средства при хронической недостаточности аминокислотного обмена, вегетососудистой дистонии, эпилепсии (в качестве предшественника ГАМК — тормозного медиатора).
ГЛУТАМИН
Синтез глутамина
Использование глутамина
1. Используется в синтезе белков, углеводов;
2. Источник азота в синтезе пуриновых и пиримидиновых оснований, аспарагина, аминосахаров;
3. Обеспечивает транспорт азота из тканей;
АСПАРТАТ
Синтез аспартата
Использование аспартата
1. Используется в синтезе белков, липидов, углеводов;
2. Участвует в орнитиновом цикле при синтезе мочевины;
3. Участвует в синтезе карнозина, анзерина, пуриновых и пиримидиновых нуклеотидов, N-ацетиласпарагиновой кислоты.
АСПАРАГИН
Синтез аспарагина
Использование аспарагина
1. Используется в синтезе белков, липидов, углеводов;