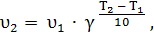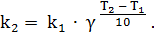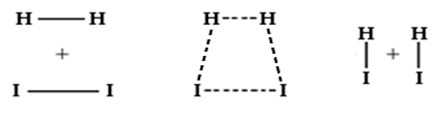Энергия активации
Энергия активации в химии и биологии — минимальное количество энергии, которое требуется сообщить системе (в химии выражается в джоулях на моль), чтобы произошла реакция. Термин введён Сванте Августом Аррениусом в 1889. Типичное обозначение энергии реакции Ea.
Энергия активации в физике — минимальное количество энергии, которое должны получить электроны донорной примеси, для того чтобы попасть в зону проводимости.
В химической модели, известной как Теория активных соударений (ТАС), есть три условия, необходимых для того, чтобы произошла реакция:
При низкой (для определённой реакции) температуре большинство молекул обладают энергией меньшей, чем энергия активации, и неспособны преодолеть энергетический барьер. Однако в веществе всегда найдутся отдельные молекулы, энергия которых значительно выше средней. Даже при низких температурах большинство реакций продолжают идти. Увеличение температуры позволяет увеличить долю молекул, обладающих достаточной энергией, чтобы преодолеть энергетический барьер. Таким образом повышается скорость реакции.
Содержание
Математическое описание
Уравнение Аррениуса устанавливает связь между энергией активации и скоростью протекания реакции:
k — константа скорости реакции, 


С повышением температуры растёт вероятность преодоления энергетического барьера.
Для количественного описания температурных эффектов в химической кинетике для приближённых вычислений кроме уравнения Аррениуса используют правило Вант-Гоффа: повышение температуры на 10 К увеличивает для большинства реакций скорость в 2-4 раза. Математически это означает, что скорость реакции зависит от температуры степенным образом:
где 
Переходное состояние
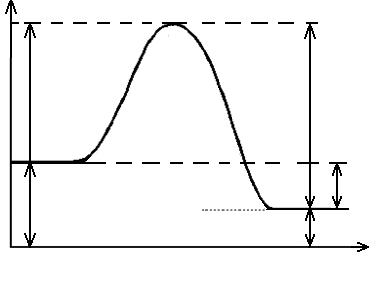
Переходное состояние — состояние системы, при котором уравновешены разрушение и создание связи. В переходном состоянии система находится в течение небольшого (10 −15 с) времени. Энергия, которую необходимо затратить, чтобы привести систему в переходное состояние, называется энергией активации. В многоступенчатых реакциях, которые включают в себя несколько переходных состояний, энергия активации соответствует наибольшему значению энергии. После преодоления переходного состояния молекулы вновь разлетаются с разрушением старых связей и образованием новых или с преобразованием исходных связей. Оба варианта возможны, так как происходят с высвобождением энергии (это хорошо видно на рисунке, поскольку оба положения лежат энергетически ниже энергии активации). Существуют вещества, способные уменьшить энергию активации для данной реакции. Такие вещества называют катализаторами. Биологи же такие вещества называют ферментами. Интересно, что катализаторы таким образом ускоряют ход реакции, самостоятельно в ней не участвуя.
См. также
Ссылки
Полезное
Смотреть что такое «Энергия активации» в других словарях:
ЭНЕРГИЯ АКТИВАЦИИ — ЭНЕРГИЯ АКТИВАЦИИ, наименьшее количество энергии, необходимое для начала химической реакции. По мере того, как в ходе реакции химические связи разрываются или формируются, энергия системы увеличивается по сравнению с энергией исходных веществ,… … Научно-технический энциклопедический словарь
ЭНЕРГИЯ АКТИВАЦИИ — в химии наименьшая энергия, которой должна обладать частица (атом, ион, радикал) для того, чтобы произошла химическая реакция. Одна из основных величин, определяющих скорость реакции при данной температуре (см. Аррениуса уравнение) … Большой Энциклопедический словарь
энергия активации — – средняя избыточная энергия, которой должны обладать реагирующие частицы, чтобы преодолеть потенциальный энергетический барьер, разделяющий исходное и конечное состояния системы. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Энергия активации — кинетический параметр, средняя избыточная энергия, которой должны обладать реагирующие частицы (атомы, элементы) для преодоления потенциального барьера между начальным и исходным состоянием системы. [Ушеров Маршак А. В. Бетоноведение: лексикон. М … Энциклопедия терминов, определений и пояснений строительных материалов
ЭНЕРГИЯ АКТИВАЦИИ — энергетический барьер, который необходимо преодолеть реагирующим атомам для осуществления хим. реакции. В частном случае радиогенных газов Э. а. (Е) определяет возможность перемещения газов по кристаллической решетке. Количество газа, остающееся… … Геологическая энциклопедия
энергия активации — Количество энергии в калориях, требуемое для перевода всех молекул, содержащихся в 1 моле реагирующего субстрата, в переходное состояние [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN activation energy … Справочник технического переводчика
энергия активации — [activation energy] разность между средней энергией частиц (молекул, радикалов, ионов и др.), вступающих в элементарный акт химической реакции, и средней энергией всех частиц реагирующей системы. Энергия активации разных химических реакций… … Энциклопедический словарь по металлургии
ЭНЕРГИЯ АКТИВАЦИИ — – в химической кинетике наименьшая избыточная энергия, которой должны обладать частицы (сталкивающиеся или распадающиеся) для осуществления химического превращения. Энергия активации при гетерофазном окислении титаномагнетита, т.е. для… … Палеомагнитология, петромагнитология и геология. Словарь-справочник.
энергия активации — в химии, наименьшая энергия, которой должна обладать частица (атом, ион, радикал) для того, чтобы произошла химическая реакция. Одна из основных величин, определяющих скорость реакции при данной температуре (см. Аррениуса уравнение). * * *… … Энциклопедический словарь
Энергия активации — Activation energy Энергия активации. Энергия, необходимая для начала металлургического процесса, например, пластической деформации, диффузии, химической реакции. (Источник: «Металлы и сплавы. Справочник.» Под редакцией Ю.П. Солнцева; НПО… … Словарь металлургических терминов
Влияние температуры. Энергия активации
Влияние температуры на скорость химической реакции выражается эмпирическим (то есть выведенным из опытных данных) правилом Вант-Гоффа[8] (1884 г.).
Повышение температуры на каждые 10 градусов увеличивает скорость большинства химических реакций в 2-4 раза.
g – температурный коэффициент скорости реакции, показывающий, во сколько раз изменяется скорость данной реакции при изменении температуры на 10 0 С или 10 К;
υ1 и υ2 – скорости реакции соответственно при температурах Т1и Т2.
Для обычных химических реакций значения температурного коэффициента находятся в пределахот 2 до 4, а для биохимических реакций могут достигать значений 7-9. Именно поэтому колебания температуры тела человека в пределах даже 1 °С сильно сказываются на его самочувствии.
Температура влияет на скорость химической реакции, увеличивая константу её скорости, поэтому выше приведённое уравнение можно представить следующим образом:
По правилу Вант-Гоффа можно лишь примерно оценить влияние температуры на скорость химической реакции. На первый взгляд может показаться, что зависимость скорости реакции от температуры обусловлена увеличением числа столкновений реагирующих веществ. Однако число столкновений с увеличением температуры увеличивается незначительно и не может сравниться с величиной температурного коэффициента скорости химической реакции. Число столкновений в газовой смеси при нормальных условиях (температура 0 ºС, давление 101 325 Па) достигает порядка 10 28 соударений в секунду. Если бы каждое соударение приводило к химическому взаимодействию, скорости реакций были бы огромны. Все реакции должны были бы протекать практически мгновенно. Следовательно, далеко не каждое соударение приводит к химическому взаимодействию. Правило Вант-Гоффа справедливо лишь при небольшом изменении температуры и далеко не для всех реакций. Гораздо более точно описывает влияние температуры на скорость химической реакции теория активации Аррениуса[9] (1889 г.).
Основные постулаты теории активации:
· не каждое столкновение (физическое взаимодействие) приводит к акту химического взаимодействия (химической реакции);
· к химическому взаимодействию приводят лишь те столкновения, в которых участвуют частицы, обладающие энергией, необходимой для такого взаимодействия (энергией активации);
· при соударении частицы должны быть определённым образом ориентированы относительно друг друга.
На рис. 4 представлена энергетическая диаграмма экзотермической реакции А + В = AB.
Энергия активации (Е´а) обратной экзотермической реакции АВ = А + В больше энергии активации (Еа) прямой реакции на величину, равную по модулю тепловому эффекту (энтальпии) реакции ΔНР, то есть Е ‘ а = Еа + |ΔН|. Активированный комплекс [А…В] один и тот же для прямой и для обратной реакции.
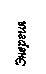 |
| ΣΔН (Продуктов реакции) |
| ΣΔН (Реагентов) |
| ∆HР |
| Еа |
| Е ‘ а |
| АВ |
| А+В |
| Активированный комплекс |
| [ А…В] |
Координата (путь) реакции
Рис. 4. Энергетическая диаграмма экзотермической реакции
Например, для реакции соединения водорода и иода:
а для реакции разложения иодоводорода:
Энергия активации характеризует энергетический барьер, преодоление которого взаимодействующими частицами приводит к образованию продуктов реакции. Энергия активации необходима для возникновения непрочного активированного переходного комплекса [А…В] (рис. 4).
Возникновение и распад такого комплекса можно представить общей схемой на примере образования и распада йодоводорода (рис. 5):
Молекулы исходных веществ [H2…I2] Молекулы продуктов реакции
Рис. 5 Схема возникновения и распада активированного комплекса
Активированный комплекс не является химическим соединением в подлинном смысле этого слова, так как в нём происходит перераспределение химических связей между взаимодействующими атомами. Квантово-химические расчёты показывают, что осуществление реакции через возникновение промежуточного комплекса (переходного состояния) энергетически выгоднее, чем образование новых химических связей после разрыва таковых в молекулах исходных веществ. Такой комплекс неустойчив вследствие его высокой энергии, и быстро распадается, образуя продукты реакции, или исходные вещества.
Энергия активации зависит от природы реагирующих веществ и протекания реакции и не зависит от температуры, если с её изменением не происходит изменения механизма реакции.
Скорость химической реакции зависит от величины энергии активации. Если энергия активации мала, то за определённое время энергетический барьер преодолеет большое число частиц и скорость реакции будет высокой; если же энергия активации велика, то энергетический барьер преодолеет малое число частиц, и реакция будет протекать медленно. Реакции с Еа 0 С) протекает с большой скоростью, характерной для реакций с участием радикалов или ионов (практически мгновенно). Если Еа > 100 кДж/моль, то её скорость реакции при 298 К неизмеримо мала.
Способы активации реагирующих веществ:
· подвод теплоты из окружающей среды (термическая активация);
· воздействия различного рода электромагнитных излучений (свет, проникающая радиация);
· воздействия активных частиц, возникающих при радиоактивном распаде ядер или при электрическом разряде;
· воздействие механической энергии – инициирование некоторых химических реакций ударом или трением (взрыв смеси бертолетовых солей).
Зависимость между константой скорости и энергией активации химической реакции выражается уравнением Аррениуса:
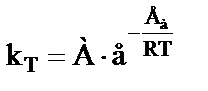
где
| kT | − | константа скорости химической реакции при температуре Т; |
| А | − | предэкспоненциальный множитель (коэффициент Аррениуса), учитывающий частоту столкновения частиц, ориентированных определённым образом; |
| е | − | основание натурального логарифма, равное приблизительно 2,71828…; |
| Еа | − | энергия активации реакции, кДж/моль; |
| R | − | универсальная газовая постоянная, равная 8,31 Дж/(моль × К); |
| Т | − | температура, К. |
Из уравнения Аррениуса следует, что чем больше энергия активации, тем меньше будет константа и скорость химической реакции, так как в системе будет меньшее число активных частиц. В обычных условиях лишь небольшая часть молекул обладает достаточной энергией, чтобы преодолеть энергетический барьер. Это обусловлено тем, что молекулы одного и того же вещества при одинаковых условиях движутся с разной скоростью и поэтому обладают разным запасом кинетической энергии.
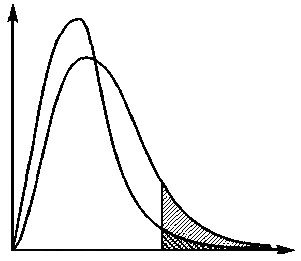
На рис. 6 представлена зависимость относительного числа молекул газа от их энергиипри различных температурах.
| E |
| Ea |
| (Т2 > Т1) |
| NE |
| T2 |
Рис. 6. Зависимость относительного числа молекул газа
от их энергиипри различных температурах
Площадь под каждой кривой равна общему количеству частиц, NЕ – число молекул, обладающих энергией Е. Доли частиц, обладающих при температурах Т1 и Т2 энергией Е ≥ Еа выражаются заштрихованными под соответствующими кривыми площадями.
При подводе теплоты к системе происходит увеличение доли активных молекул, обладающих достаточной энергией для химического взаимодействия. При повышении температуры резко возрастает число активных молекул, и этим обусловлено значительное повышение скорости химической реакции.
В табл. 2 на примере образования воды из водорода и кислорода показана зависимость времени протекания реакции от температуры:
Энергия активации
В процессе протекания реакций горения происходит перегруппировка химических связей между атомами. Например, в реакции 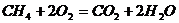
Энергия активации – это то минимальное количество избыточной энергии, которое необходимо иметь реагирующим веществам для разрыва или значительного ослабления внутримолекулярных связей, чтобы началась реакция. На практике энергия активации сообщается реагирующим веществам пламенем спички, зажигалки, запальника, электрической искрой и т.п. Для спички, т.е. для веществ входящих в состав головки спички, также нужна энергия активации – эта энергия сообщается при трении головки о специальную поверхность коробка.
Энергия активации является характеристикой активности молекул при реагировании между собой. Чем меньше энергия активации, тем легче молекулы вступают в реакцию. И наоборот, чем больше энергия активации, тем труднее молекулы вступают в реакцию. Энергию активации можно рассматривать как энергетический барьер, который нужно преодолеть, чтобы произошла реакция. Численное значение Е для большинства газовых смесей лежит в пределах от 80 до 170 кДж/моль.
Различают экзо- и эндотермические реакции. В результате протекания экзотермических реакций теплота выделяется. При эндотермических реакциях теплота поглощается. Все реакции горения горючих газов являются экзотермическими.
Кроме того, реакции горения подразделяются на гомогенные и гетерогенные. Гомогенные реакции –это реакции, протекающие между газами, т.е. когда нет границы раздела фаз. Гетерогенные реакции – это реакции, протекающие на поверхности жидких и твердых тел, т.е. когда есть поверхность раздела фаз. Например, горение угля, мазута и т.п.
1.3 Зависимость скорости химической реакции от различных факторов
Подставим уравнение Аррениуса в формулу 1. В результате получим:
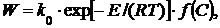
где k0 – предэкспоненциальный множитель (константа);
E – энергия активации, кДж/кмоль;
R – газовая постоянная, кДж/(кмоль· К);
Т – абсолютная температура, К;
С – концентрация реагирующих веществ.
На величину скорости реакции (уравнение 3) влияют следующие факторы: природа реагирующих веществ, температура, концентрация, давление и катализаторы.
Зависимость 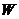

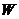

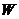
На величину 
Из уравнения 3 видно, что с повышением концентрации 
С повышениемдавления 
Катализаторы ускоряют протекание реакций. Как правило, для ускорения реакций горения используются металлы и их оксиды переходных периодов системы Д.И. Менделеева: хром, марганец, железо, кобальт, родий, осмий, платина и другие. Горение газов протекает достаточно быстро, поэтому при гомогенном горении катализаторы используются редко. В противоположность катализаторам есть вещества замедляющие протекание реакций – это ингибиторы.
1.4 Расчеты горения
Рассмотрим реакцию горения водорода в кислороде: 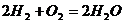
Рассмотрим реакцию горения метана в кислороде: 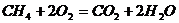
В практических условиях сжигание газа осуществляется в воздухе. Примем состав сухого воздуха: О2 – 21 %, N2 – 79%. Следовательно, 1 м 3 кислорода содержится в 100/21 = 4,76 м 3 воздуха. Или на 1 м 3 кислорода приходится 3,76 м 3 азота. Отсюда условная формула воздуха: (О2 + 3,76N2).
Запишем реакцию горения водорода в воздухе:
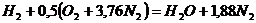
Из уравнения следует, что при нормальных условиях для полного сгорания 1 м 3 водорода требуется 0,5 × 4,76 = 2,38 м 3 воздуха. Таким образом, для сгорания 1 м 3 водорода требуется 2,38 м 3 воздуха. В результате образуются продукты сгорания: 1 м 3 воды в виде пара и 1,88 м 3 азота.
Запишем реакцию горения метана в воздухе:
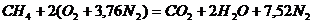
Из уравнения следует, что для полного сгорания 1 м 3 метана необходимо 2 × 4,76 = 9,52 м 3 воздуха. Таким образом, при нормальных условиях для сгорания 1 м 3 метана требуется 9,52 м 3 сухого воздуха. Продукты сгорания содержат 1 м 3 диоксида углерода, 2 м 3 паров воды и 7,52 м 3 азота.
Запишем реакцию горения пропана в воздухе:
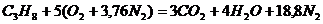
Из уравнения видно, что для полного сгорания 1 м 3 пропана необходимо 5 × 4,76 = 23,8 м 3 воздуха. Таким образом, при нормальных условиях для сгорания 1 м 3 пропана требуется 23,8 м 3 сухого воздуха.
Приведенные расчеты выполнены для стехиометрических уравнений и полученные соотношения воздуха и газа называются стехиометрическими. Например, для горения метана в воздухе стехиометрическое соотношение – 9,52. В реальных условиях воздуха может не хватать для полного сгорания газа или, напротив, воздух подается в избыточном количестве. Для характеристики реальных соотношений воздуха и газа в процессе горения введена безразмерная величина: коэффициент избытка воздуха (окислителя) – коэффициент α. Для стехиометрического соотношения α = 1. Если имеет место недостаток воздуха, то α 1. Например, в процессе горения израсходовано 23 м 3 воздуха и 2 м 3 метана. Подсчитываем коэффициент α. Реальное соотношение воздуха и газа 23/2 = 11,5. Отсюда α = 11,5/9,52 = 1,2.
Выше показано, как можно подсчитывать необходимое количество воздуха для сгорания и определять объем продуктов сгорания для индивидуальных газов. Но обычно используемый газ – смесь различных газов. В этом случае расчет теоретически необходимого объема воздуха (воздуха сухого) ведется по формуле:
где 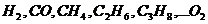
Используемый для сжигания атмосферный воздух содержит влагу, поэтому расчет объема влажного воздуха производят по формуле:
где 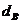
0,00124 – объем 1 г водяного пара.
И, наконец, определяется объем воздуха действительный с учетом величины коэффициента α по формуле:
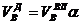
Объем продуктов сгорания газовой смеси определяется по следующим формулам.
Объем диоксида углерода
Объем водяных паров
где N2 – процентное содержание азота в газовой смеси.
Суммарный объем продуктов сгорания
1.5 Цепной механизм процесса горения
Химические уравнения реакций горения газов, рассмотренные выше, не вскрывают механизм реакций, а являются лишь уравнениями итогового баланса. Процесс горения сложный физико-химический процесс, скорость которого определяется интенсивностью физических и химических явлений и особенностями их взаимодействия. Горение – многофакторный процесс, включающий химическую кинетику, термодинамику, тепломассоперенос, газо- и гидродинамику течений. Основной вклад в создании современных представлений о механизме реакций горения внесли академик Н.Н. Семёнов и его школа. За разработку теории цепных реакций Н.Н. Семёнову и английскому учёному С.Н. Хиншелвуду была присуждена Нобелевская премия.
Наиболее изученным является механизм горения водорода в кислороде. Зарождение цепи начинается с эндотермического процесса образования активных центров – радикалов водорода:
Элемент М следует понимать как источник энергии активации. Это может быть открытое пламя, раскаленное тело, электрическая искра и т.п.
Звено превращений состоит из следующих элементарных актов:

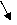


Итогом единичного звена является реакция:
Механизм горения метана представляет собой довольно сложную совокупность цепных реакций с образованием на отдельных стадиях стабильных и нестабильных промежуточных продуктов. Предполагаемый механизм цепного горения метана в кислороде при стехиометрическом соотношении следующий:
НСО + О2 → СО + О + ОН
Итог звена реакции горения метана в кислороде:
Ещё более сложный механизм горения метана в воздухе, особенно при отклонении от стехиометрического соотношения.
1.6 Температура горения газов
Различают следующие температуры горения газов: калориметрическая, теоретическая и действительная.
Калориметрическая температура– это температура продуктов сгорания горючих газов в адиабатических условиях с действительным значением коэффициентом α с действительной температурой газа и воздуха. Калориметрическая температура может быть рассчитана по формуле:
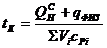
где 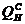
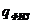
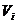
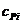
Теплосодержание (энтальпия) воздуха и газа вычисляются по формуле:
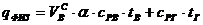
где 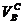
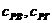
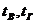
Знаменатель формулы 12 в развернутом виде
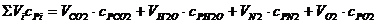
Теплоемкость продуктов сгорания величина не постоянная и увеличивается с повышением температуры, поэтому калориметрическая температура рассчитывается методом итераций (последовательных приближений). Примерные значения калориметрической температуры некоторых газов при сжигании в сухом воздухе при нормальных условиях и коэффициенте α = 1 приведены в таблице 1.2.
Таблица 1.2. Калориметрическая температура горения газов
| Наименование газа | Температура, °С |
| Водород | |
| Метан | |
| Пропан | |
| Ацетилен | |
| Природный газ | |
| Доменный газ | |
| Сжиженный газ |
С увеличением влажности воздуха температура снижается на 25 – 20 градусов на каждый весовой процент влаги. К снижению температуры приводит уменьшение и увеличение коэффициент α относительно α = 1.
Теоретическая температура– это температура продуктов сгорания горючих газов в адиабатических условиях с действительным значением коэффициентом α с действительной температурой газа и воздуха с учетом химической неполноты сгорания и реакций диссоциации. Реакции диссоциации – распад молекул продуктов сгорания под воздействием высокой температуры. Например:
Н2О ↔ Н2 + 0,5О2 – 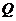
СО2 ↔ СО + 0,5О2 – 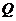
При протекании реакций диссоциации теплота поглощается и в результате температура горения снижается. Теоретическая температура рассчитывается по формуле:
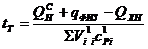
где 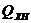
диссоциацию продуктов сгорания;
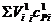
Степень диссоциации определяется по константам диссоциации для каждой реакции. До температуры 1500°С диссоциацию можно не учитывать.
Действительная температура– это температура продуктов сгорания горючих газов в действительных условиях с действительным значением коэффициентом α с действительной температурой газа и воздуха с учетом химической неполноты сгорания и реакций диссоциации. Действительные условия отличаются от адиабатических условий, т.к. всегда есть потери теплоты в окружающую среду.
Действительная температура находится по формуле:

где 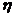
Величина пирометрического коэффициента зависит от печей и их тепловой изоляции. Принимается в пределах от 0,5 до 0,85.
1.7 Температура воспламенения
Процесс возбуждения горения называется воспламенением. Под температурой воспламенения (самовоспламенения) понимается минимальная температура, до которой должна быть нагрета газовоздушная смесь, чтобы начался самопроизвольный процесс горения не требующий больше внешнего подводы теплоты. Тепловое воспламенение носит цепной характер и может заканчиваться взрывом. Температура воспламенения определяется экспериментально. Величина температуры воспламенения зависит от природы газа, от содержания газа в газовоздушной смеси, от давления и других факторов. Температура воспламенения горючих газов в смеси с кислородом всегда меньше, чем в смеси с воздухом. Введение в смесь негорючих (балластных) газов (N2, CO2 и т.п.) приводит к повышению температуры воспламенения. Минимальные значения температуры воспламенения газовоздушных смесей приведены в таблице 1.3.
Таблица 1.3. Минимальная температура воспламенения газовоздушных смесей
| Газ | Температура воспламенения, °С | Газ | Температура воспламенения, °С |
| Водород | Бутан | ||
| Метан | Оксид углерода | ||
| Пропан | Природный газ |
В действительности воспламенение газовоздушной смеси производится зажиганием (вынужденное зажигание). Зажигание или поджигание характеризуется тем, что холодная газовоздушная смесь воспламеняется в одном месте (пламенем спички, раскаленным телом, искрой) и возникшее пламя распространяется по всему объему газовоздушной смеси. Таким образом, зажигание смеси отличается от теплового воспламенения тем, что смесь доводится до температуры воспламенения не во всем объеме одновременно, а только в малой части объема, откуда горение распространяется на весь объем холодной смеси.
1.8 Пределы воспламенения
Смеси горючих газов с воздухом или кислородом воспламеняются и горят только в определенных концентрационных пределах. Различают нижний и верхний пределы воспламенения. Нижний предел соответствует минимальному, а верхний предел – максимальному содержанию газа в газовоздушной смеси при котором происходит воспламенение при зажигании и самопроизвольное распространение пламени. Вне концентрационных пределов газовоздушные смеси не горят и не взрываются. Существование пределов воспламенения объясняется тепловыми потерями при горении. В таблице 1.4 приведены пределы воспламенения газов в смеси с воздухом при 20°С и давлении 760 мм рт. ст.
Таблица 1.4. Концентрационные пределы воспламенения
| Наименование газа | Содержание газа в смеси, % объема | ||
| На пределах воспламенения | При α = 1 | ||
| Нижний | Верхний | ||
| Водород | 4,0 | 75,0 | 29,5 |
| Метан | 5,0 | 15,0 | 9,5 |
| Этан | 3,0 | 12,5 | 5,7 |
| Пропан | 2,2 | 9,5 | 4,0 |
| Бутан | 1,9 | 6,1 | 3,1 |
| Ацетилен | 2,5 | 81,0 | 7,8 |
| Оксид углерода | 12,5 | 74,0 | 29,5 |
| Сжиженный газ | ≈ 2 | ≈ 10 | 3 ÷ 4 |
С увеличением температуры газовоздушной смеси пределы воспламенения расширяются, и температурах, превышающих температуру воспламенения, смеси горят при любом объемном соотношении воздуха и газа.
Пределы воспламенения смеси газов определяются по правилу аддитивности:
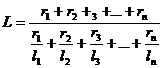
где 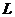
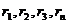
долях или процентах;
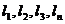
компонентов в газовоздушной смеси, % объема.
Величина коэффициента α на пределах воспламенения для смеси газов рассчитывается по формуле:
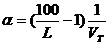
Расчет по формуле 16 для метановоздушной смеси дает α = 0,6 на верхнем пределе и α = 2,0 на нижнем пределе.
1.9 Нормальное распространение пламени
Пламенемназывается зона, в которой протекают реакции горения. Характерным свойством пламени является его свечение. Пламя, возникшее в объеме или в потоке газовоздушной смеси (ГВС), отделяет еще несгоревшую смесь от продуктов горения. Проделаем мысленный эксперимент (рис. 1). Возьмем прозрачную трубку, открытую с одного торца. Заполним трубку газовоздушной смесью (в пределах воспламенения) и воспламеним смесь у открытого торца. Возникнет пламя, которое будет перемещаться вдоль трубки. Продукты сгорания свободно истекают из открытого торца трубки.
Рис. 1. Мысленный эксперимент
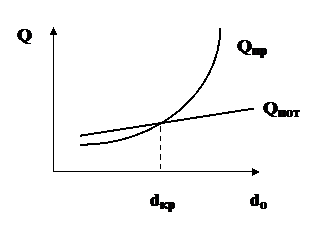
Перемещение пламени вызывается тем, что ГВС перед ним нагревается до температуры воспламенения за счет теплоты, поступающей из пламени, теплопроводностью и диффузией раскаленных продуктов сгорания и радикалов. Линейная скорость, с которой перемещается пламя (фронт горения) по однородной ГВС называется равномерной скоростью распространения пламени (v, м/с).Величина равномерной скорости распространения пламени зависит от физико-химических констант ГВС и от формы фронта горения (диаметра трубки). С увеличением диаметра трубки равномерная скорость увеличивается, т.к. фронт горения искривляется, усиливаются завихрения и конвективные потоки. С уменьшением диаметра трубки равномерная скорость распространения пламенизамедляется и при каком-то значении диаметра процесс горения становится невозможным. Это объясняется тем, что с уменьшением размеров трубки (канала) возрастает отношение периметра к площади сечения. Теплопотери в окружающую среду превышают теплопоступления из объема пламени – горение прекращается. Это наглядно показано на рис. 2.
Рис. 2. Зависимость прихода теплоты Qпр и теплопотерь Qпот от
диаметра трубки (канала)
Для сравнения горючих свойств газов, независимо от диаметра трубки, введено понятие нормальная скорость распространения пламени.Нормальной скоростью распространения пламени (UН , м/с) называется скорость, с которой пламя перемещается по нормали к поверхности фронта горения. Нормальная скорость распространения пламени зависит только от физико-химических констант ГВС и находится по формуле:

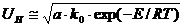
где 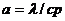
Здесь λ – коэффициент теплопроводности, с – теплоемкость и
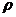
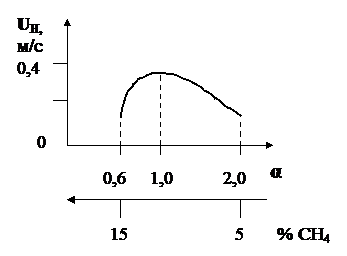
Рис. 3. Зависимость нормальной скорости от коэффициента α
для метановоздушной смеси
Из рис. 3 следует, что величина нормальной скорости возрастает с увеличением коэффициента α, достигает максимума при α ≈ 0,9 а, затем уменьшается. Наглядно видна зона устойчивого воспламенения и горения, которая находится в диапазоне α = 0,6 ÷ 2,0, или от 5% до 15% содержания метана в ГВС.
Скорость распространения пламени в смеси с кислородом всегда выше.
1.10 Экспериментальное определение нормальной скорости
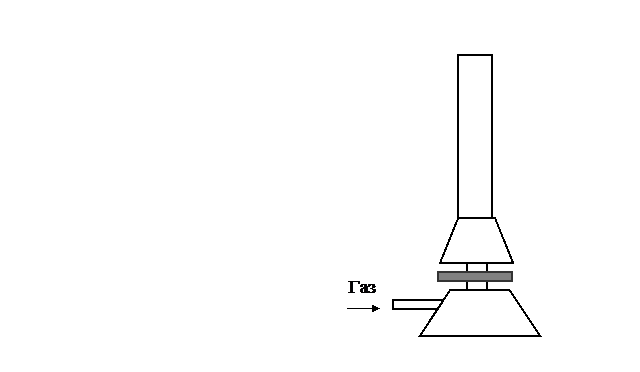
По формуле 17 величина нормальной скорости распространения пламени находится аналитически исходя из физико-химических констант смеси. Однако зачастую эти константы неизвестны, поэтому UН определяют экспериментально. Для эксперимента используется лабораторная горелка Бунзена или Тэклю (рис. 3).
Горелка Бунзена – изобретение Роберта Бунзена (1855). Горелка имеет круглое основание – 1, смеситель (инжектор) – 3 в виде металлической трубки, в нижней части которой имеются отверстия для поступления воздуха и регулятор расхода воздуха – 2. Газ подводится с боку из газопровода.
При работе горелки газ в виде струи с большой скоростью выходит из сопла, создавая разрежение в смесителе. Благодаря этому разрежению, окружающий воздух засасывается (инжектируется) в смеситель и при движении вверх смешивается с газом, образуя горючую смесь, которая поджигается на выходе из устья горелки.
Рис. 3. Лабораторные горелки: а) Бунзена, б) Тэклю:
1 – основание; 2 – регулятор расхода воздуха; 3 – смеситель
Пламя лабораторной горелки имеет два фронта горения. Внутренний фронт – горение происходит за счет первичного воздуха (α Uн. Это означает, что конусный фронт неустойчивый, т.к. пламя сносится по поверхности конуса к вершине. В действительности пламя горелки устойчивое вследствие того, что у основания конуса фронт горения разворачивается в горизонтальную плоскость и образуется кольцевой зажигающий пояс. В зажигающем поясе скорость потока и скорость горения равны, поэтому зажигающий пояс устойчив и воспламеняет поток ГВС, выходящей из устья горелки. С увеличением Wнзажигающий пояс несколько отходит от устья. При этом Uнв зажигающем возрастает, т.к. уменьшается охлаждающее воздействие на пламя устья. И вновь происходит их взаимная компенсация: Wн = Uн.Однако при дальнейшем увеличение Wнможет наступить момент, когда Wнпревысит Uн.В этом случае происходит отрыв и погасание пламени.