Большая Энциклопедия Нефти и Газа
Увеличение поверхности жидкости требует затраты некоторой работы. [2]
Увеличение поверхности жидкости сопровождается возникновением новых участков разреженного поверхностного слоя. При этом должна быть совершена работа против сил притяжения между молекулами. Эта работа представляет собой поверхностную энергию. [3]
Увеличение поверхности жидкости в результате ее распыления увеличивает скорость сушки. [6]
Увеличению поверхности жидкости соответствует переход части молекул из более удаленных от поверхности слоев на поверхность жидкости, связанный с затратой некоторой работы. [8]
Поэтому увеличение поверхности жидкости требует затраты некоторой работы. Энергия, которую нужно сообщить жидкости для увеличения поверхности жидкой фазы, равна коэффициенту поверхностного натяжения о жидкости. [9]
Для увеличения поверхности жидкости необходимо затратить некоторую работу. Величина этой работы, отнесенная к 1 см2 поверхности вещества, и есть поверхностное натяжение; оно равно максимальной полезной работе, затрачиваемой на образование единицы поверхности. [10]
Для увеличения поверхности жидкости необходимо совершить работу против сил поверхностного натяжения. [11]
Поэтому увеличение поверхности жидкости связано с затратой дополнительной энергии. Эта дополнительная энергия и должна быть доставлена при испарении с вогнутой поверхности. [13]
Для увеличения поверхности жидкости требуется затратить некоторую работу. [14]
Для увеличения поверхности жидкости необходимо затратить работу на преодоление притяжения молекул внутрь жидкости, причем величина работы, затрачиваемой на одну молекулу, может быть определена. [15]
Большая Энциклопедия Нефти и Газа
Для увеличения поверхности жидкости необходимо затратить работу на преодоление притяжения молекул внутрь жидкости, причем величина этой работы, которая затрачивается на одну молекулу, может быть определена. [16]
Для увеличения поверхности жидкости нужно преодолеть сиЛу1 внутреннего давления и совершить определенную механическую, работу. [17]
Поэтому увеличение поверхности жидкости связано с затратой дополнительной энергии. Эта дополнительная энергия и должна быть доставлена при испарении с вогнутой поверхности. [18]
При увеличении поверхности жидкости часть ее молекул переходит из глубины на поверхность, при этом совершается работа против сил / и потенциальная энергия поверхностного слоя возрастает. [19]
При увеличении поверхности жидкости ее температура понижается, так как при нагревании поверхностное натяжение уменьшается. [20]
При увеличении поверхности жидкости некоторое число молекул из объема жидкости должно быть поднято в поверхностный слой. Для этого необходимо затратить работу, причем если процесс образования поверхности происходит изотермически, то потенциальная поверхностная энергия равна с обратным знаком энергии, затраченной на ее образование. [21]
При увеличении поверхности жидкости ничего подобного не наблюдается. [22]
Работа по увеличению поверхности жидкости на 1 сад2 называется поверхностным натяжением. Поверхностное натяжение, в частности, приводит к образованию сферических форм капельно-жидких структур. [23]
Совершенная при увеличении поверхности жидкости работа вызвала увеличение энергии поверхностного слоя жидкости. [24]
Заметим, что для увеличения поверхности жидкости необходимо затратить работу, связанную с преодолением сил, обусловливающих внутреннее давление. Работа при обратимом и изотермическом пррцессе, необходимая для создания единицы поверхности, равна удельной свободной энергии поверхности. [25]
Мы видели, что увеличение поверхности жидкости связано с затратой работы. Поэтому чем меньше поверхность жидкости, тем более устойчиво ее состояние. Этим обусловливается, например, шарообразная форма капель, так как шар обладает наименьшей поверхностью при данном объеме. [28]
Заметим, что для увеличения поверхности жидкости необходимо затратить работу, связанную с преодолением сил, обусловливающих внутреннее давление. Работа при обратимом и изотермическом пррцессе, необходимая для создания единицы поверхности, равна удельной свободной энергии поверхности. [29]
Определение коэффициента поверхностного натяжения методом поднятия жидкости в капиллярах
Лабораторная работа №15
поверхностного натяжения методом
поднятия жидкости в капиллярах
Определение коэффициента поверхностного натяжения воды.
Характер движения молекул в жидкостях существенно отличается от движения молекул как в газах, так и в твердых телах. В газах среднее расстояние между соседними молекулами гораздо больше их диаметра. Поэтому при тепловом движении молекулы движутся хаотически. В твердых кристаллических телах молекулы расположены в правильном периодическом порядке и составляют кристаллическую решетку. Этот порядок сохраняется на далекие расстояния (миллионы и миллиарды молекулярных расстояний). Такой порядок называется «дальним порядком». Поскольку плотность твердых тел значительно больше плотности газов, молекулы в кристаллах примыкают друг к другу. Тепловое движение молекул сводится к их колебаниям около положения равновесия. В жидкостях средние расстояния между соседними молекулами несколько больше, чем в кристаллах. Поэтому молекулы жидкости могут отходить от своих правильных положений, расстраивая идеальный порядок, свойственный кристаллам. Тепловое движение молекул в жидкостях сводится к следующему. Молекулы большую часть времени колеблются около своих положений равновесия. Амплитуды колебаний различных молекул различны. Вследствие взаимодействия молекул при тепловом движении энергия некоторых из них может возрасти. Поскольку увеличение энергии соответствует увеличению амплитуды колебаний, то амплитуда колебаний этих молекул может возрасти настолько, что они при наличии свободного места перескакивают в другие положения равновесия и начинают колебаться около них. С увеличением температуры амплитуда колебаний и частота таких перескоков возрастают. Так как расстояния между соседними молекулами в жидкости все-таки малы, то в жидкости сохраняется так называемый «ближний порядок», т. е. порядок в расположении ближайших соседей какой-либо молекулы. Этот порядок размывается по мере удаления от данной молекулы.
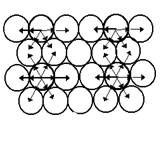
Молекулы, расположенные в поверхностном слое жидкости, находятся в иных условиях по сравнению с молекулами внутри жидкости. Каждая из внутренних молекул окружена со всех сторон другими молекулами и испытывает одинаковое притяжение во всех направлениях. Молекулы, расположенные вблизи поверхности, испытывают со стороны своих соседей притяжение, направленное внутрь и в стороны (рис. 1), но не испытывают уравновешивающего притяжения со стороны прилегающих слоев газообразной формы, содержащих в себе значительно меньшее число молекул.
В результате на поверхностную молекулу действует сила, направленная внутрь жидкости, перпендикулярно ее поверхности. Под действием этой силы молекулы погружаются в жидкость. Вследствие теплового движения небольшая часть молекул вновь выходит на поверхность. Втягивание молекул внутрь происходит с большей скоростью, чем движение молекул к поверхности. Число молекул в поверхностном слое будет непрерывно уменьшаться. Поверхность жидкости будет сокращаться до тех пор, пока не наступит динамическое равновесие, т. е. пока количество молекул, уходящих из поверхностного слоя и возвращающихся в него за одно и то же время, не будет одинаковым. Таким образом, при отсутствии внешних сил поверхность жидкости принимает наименьшее значение, возможное при данном объеме. Как известно, изо всех тел заданного объема наименьшей поверхностью обладает шар, поэтому жидкость под действием только внутренних сил принимает форму шара. Наличие внешних сил приводит к изменению формы жидкости. Для увеличения поверхности необходимо совершить работу, которая затрачивается на вывод молекул из глубины на поверхность.
Очевидно, для изменения поверхности жидкости на величину DS нужно совершить работу, равную
где а — работа, необходимая для вывода одной молекулы на поверхность:
n — число молекул в 1 см2 поверхностного слоя. Величина an = s называется коэффицентом поверхностного натяжения:
Коэффициент поверхностного натяжения s численно равен работе, которую нужно совершить для увеличения поверхности жидкости на единицу площади.
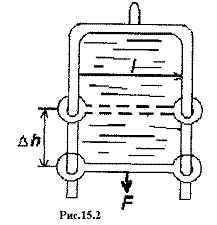
Определим силу поверхностного натяжения. Рассмотрим проволочный каркас, одна из сторон которого может свободно перемещаться (рис. 2). Если поместить этот каркас в мыльный раствор, то на нем образуется мыльная пленка, представляющая собой тонкий слой жидкости с двумя свободными поверхностями. Если отпустить подвижную перекладину, то поверхность пленки сократится. Силы, возникающие при сокращении поверхности жидкости, называются силами поверхностного натяжения. Работа, затрачиваемая против сил поверхностного натяжения, при перемещении подвижной перекладины на величину Dh, равна:
где DS = 2l∙Dh — изменение поверхности пленки с обеих сторон.
Сравнивая формулы (1) и (2), получим
где F/2 — сила, действующая с одной стороны пленки. Таким образом, коэффициент поверхностного натяжения численно равен силе, действующей на единицу длины линии, являющейся границей поверхности жидкости. Эта сила направлена перпенднкулярно любому элементу длины, разграничивающей поверхность жидкости, и касательна к ее поверхности. В системе СГС коэффициент поверхностного натяжения измеряется в дин/см. В cистеме СИ — Н/м.
3. 0писание аппаратуры и метода измерения
Принадлежности: торзионные весы, пластинки, стакан с водой.
3.1. Метод торзионных весов
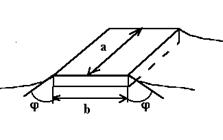
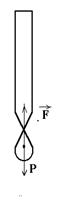
Погрузим в жидкость прямоугольную пластинку, стороны которой равны а и b (рис. З). Угол j между вертикальной поверхностью пластинки и плоскостью, касательной к поверхности жидкости на границе с телом, называется краевым углом. Для того, чтобы пластинку оторвать от поверхности жидкости, нужно приложить силу, равную F1 =P+F,
где Р — вес пластинки, F = 2s(a+b) cosj — сила поверхностного натяжения, действующая по всему периметру пластиннки 2(а+b).
Таким образом, коэффициент поверхностного натажения определится из формулы:
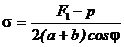
Если смачивание полное, то j = 0 и формула (4 ) принимает более простой вид:
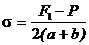
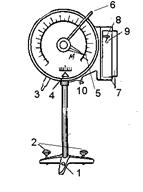
В данной работе F1 и Р определяются с помощью крутильных микровесов, называемых торзионными, пределы измерения которых 0 — 500 мГ. Основным элементом торзионных весов (рис. 4) является плоская спиральная пружина, которая с помощью рычага 8 закручивается под действием силы со стороны взвешиваемого предмета. При этом указатель 4 сместится в сторону от положения равновесия. Весы можно вновь уравновесить рычагом 6, возвратив пружину в первоначальное положение. При этом стрелка 5, жестко скрепленная с рычагом 6, смещается и показывает вес груза. Точность весов равна 1 мГ=9,8·10-3Н.
3. 2. Теория капиллярного метода
В узких стеклянных трубках-капиллярах, опущенных в жидкость, хорошо заметно поднятие или опускание жидкости. Поверхностная пленка жидкости в трубке под действием молекулярных сил жидкости и стекла принимает вогнутую форму (вогнутый мениск). На такой искривленной поверхности силы поверхностного натяжения вызывают добавочное давление DР, обусловленное кривизной поверхности, направленное всегда в сторону вогнутой поверхности. В случае произвольной поверхности жидкости двоякой кривизны дополнительное давление определяется формулой Лапласа:
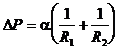
где R1 и R2 — главные радиусы кривизны поверхности, a — коэффициент поверхностного натяжения. Если поверхность сферическая, то
R1 = R2 = R, и формула (6) будет иметь вид:
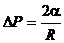
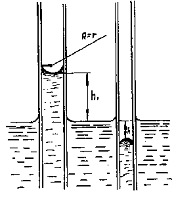
Этим добавочным давлением вызываются явления поднятия (а в случае несмачивающей жидкости — опускания) жидкости в капиллярах. Жидкость поднимается или опускается в капилляре до тех пор, пока добавочное давление не сравняется с гидростатическим давлением поднявшегося или опустившегося столба жидкости (рис. 5).
Если считать, что жидкость полностью смачивает поверхность трубы, то радиус кривизны мениска R совпадает с внутренним радиусом трубки r. По равенству добавочного и гидростатического давлений можно написать:
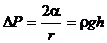
где r — плотность жидкости; h — высота ее поднятия; g — ускорение силы тяжести. Из равенства (7) определяем коэффициент поверхностного натяжения:
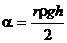
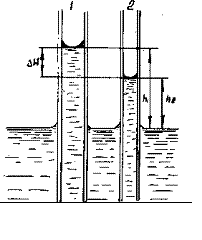
Полученная формула справедлива только при условии полного смачивания стекла жидкостью. Поэтому надо особо строго следить за чистотой капилляра. В данной работе опыт проводится с двумя капиллярами (рис. 6), радиусы которых r1 и r2. В этом случае коэффициент поверхностного натяжения:
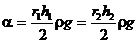
отсюда: 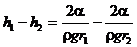
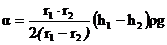
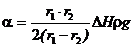
где DН — разность отсчетов между нижними краями менисков в капиллярных трубках.
4. Метод отрыва капли
Примером проявления силы поверхностного натяжения может служить образование капли при медленном вытекании жидкости из трубки. Капля отрывается в тот момент, когда ее вес P = mg становится равным силе поверхностного натяжения F = sl, действующей по контуру длиной l =2pr. Следовательно P=F или, подставляя соответствующие выражения для P и F, получим:
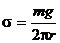
где r — радиус шейки капли, равный внутреннему радиусу трубки.
Для получения достоверного значения массы капли необходимо отсчитать n капель (в стакан общим весом без капель P1 = М1g и определить суммарный вес стакана и воды P2 = М2g. Тогда формула (9) примет вид:
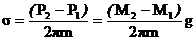
где М1 — масса стакана; М2 — масса стакана с n каплями.
5.1. Метод торзионных весов
1. Устанавливают весы по уровню 1 с помощью винтов 2.
2. С помощью арретира 3 освобождают коромысло весов 8.
3. Устанавливают стрелку 5 на 0 и вращением корректора 10 совмещают указатель 4 с вертикальной чертой на шкале.
4. Открывают крышку весов 7 и подвешивают на крючок 9 пластинку. Уравновешивают весы.
5. Подставляют стакан и осторожно наливают дистиллированную воду до тех пор, пока она не коснется поверхности пластинки.
6. Медленно передвигают рычаг 6 до момента отрыва пластинки от поверхности жидкости. Измерения повторяют 5 раз и находят среднее значение PH2O.
7. Убирают стакан и определяют вес сырой пластинки PH2O. Затем высушивают пластинку.
8. Вычисляют коэффициент поверхностного натяжения по формуле (5).
5.2. Капиллярный метод
1. Установите вертикально капиллярные трубки в общем держателе и погрузите их в стакан с дистиллированной водой, опустив их на 2-3 см ниже поверхности жидкости. Оставьте их в этом положении на несколько минут для основательного смачивания водой. Проследите, чтобы в капиллярах не осталось пузырьков воздуха.
2. Приподнимите трубки до поверхности жидкости, закрепите держатель и отсчитайте с помощью линейки-шкалы высоту подъема воды в капиллярах.
3. Снова опустите трубки глубже и через несколько минут поднимите и повторите отсчеты.
4. Повторите измерения не менее трех раз. Результаты измерений запишите в таблицу.
6 Поверхностная энергия и поверхностное натяжение
Лекция 6. Поверхностная энергия и поверхностное натяжение.
Оценка поверхностного натяжения жидкостей. Методы.
Определение поверхностного натяжения твердых тел.
Адсорбция на границе жидкость-газ.
Рекомендуемые файлы
Изотерма адсорбции. Построение.
Поверхностный слой жидкости, соприкасающийся с другой средой, находится в особых условиях по сравнению с остальной массой жидкости.
Эти особые условия возникают потому, что молекулы поверхностного слоя, в отличии от молекул внутренних слоев, подвергаются неодинаковому притяжению молекулами жидкости и газа.
Каждая молекула внутри жидкости со всех сторон притягивается с одинаковыми силами соседними молекулами, расположенными на расстоянии радиуса сферы действия межмолекулярных сил, как показано на рис. 6.1.
Рис. 6.1. Схема действия межмолекулярных сил внутри жидкости и на ее поверхности.
В результате, силы притяжения компенсируются и равнодействующая сил для молекулы 1 равна 0.
У молекул поверхностного слоя (молекула 2) одна часть сферы действия межмолекулярных сил находится в жидкости, другая – в газовой фазе. Так как плотность газа меньше плотности жидкости, то силы притяжения молекул газа очень малы и равнодействующая всех сил притяжения будет направлена внутрь жидкости перпендикулярно ее поверхности.
Таким образом, поверхностные молекулы жидкости всегда находятся под действием силы, стремящейся втянуть их внутрь и, тем самым, сократить поверхность жидкости.
Этим объясняется шарообразная форма капли жидкости (шар имеет минимальную поверхность).
При увеличении поверхности, например, при растяжении жидкой пленки, некоторое число молекул из внутренних областей жидкости переходит на поверхность. Этот переход молекул из равновесного состояния в особое состояние молекул поверхностного слоя требует затраты внешней работы.
Работа, затрачиваемая на увеличение площади поверхности жидкости, переходит в потенциальную энергию молекул поверхностного слоя – поверхностную энергию.
Поверхностная энергия, отнесенная к единице поверхности, называется поверхностным натяжением (ПН):
где 


Единица измерения ПН [Н/м] соответствует представлению о ПН как о силе, отнесенной к единице длины контура поверхности, направленной вдоль поверхности и стремящейся ее уменьшить.
Так как ПН определяется работой создания единицы площади поверхности, расходуемой на разрыв межмолекулярных связей, то чем прочнее межмолекулярные связи, тем больше ПН жидкости (например, вода ПНводы=71,95 мН/м, бензол ПНбензола=28,2 мН/м при 25 0 С).
С повышением температуры ПН снижается, т.к. ослабляются межмолекулярные связи.
Таким образом, поверхностная энергия – это прямое проявление межмолекулярных взаимодействий.
Молекулы, находящиеся на поверхности жидкости или твердого тела испытывают воздействие неуравновешенных молекулярных сил, вследствие чего получают дополнительную энергию по сравнению с молекулами, которые находятся внутри жидкости или твердого тела.
Проявляет себя поверхностная энергия как сила, которая стремится уменьшить площадь поверхности до минимально возможной величины.
В твердых телах подвижность молекул на поверхности отсутствует, поэтому поверхностная энергия здесь не может наблюдаться в виде поверхностного натяжения. Измерять поверхностную энергию можно лишь косвенными методами.
Дополнительная свободная энергия на поверхности раздела двух конденсированных фаз называется межфазным натяжением.
ПН и межфазное натяжение являются важными характеристиками, потому что они определяют ход важных технологических процессов.
Эти показатели важны для устойчивости дисперсий, суспензий, эмульсий и других дисперсных систем.
Существует ряд независимых методов оценки ПН, среди которых различают статистические и динамические, косвенные и непосредственные.
Оценка ПН жидкостей из родственных
Поскольку ПН есть проявление действия межмолекулярных сил, эта характеристика связана с другими свойствами, в основе которых лежит действие межмолекулярных сил, например, с энергией когезии.
Известно эмпирическое сооотношение между ПН и плотностью энергии когезии (
где 
Связь между ПН, энергией когезии и мольным объемом для низкомолекулярных соединений устанавливает соотношение:
где 


Расчет ПН из аддитивной функции через парахор:


Парахор – аддитивная величина. Понятие парахора ввел Сагден.
Межфазное натяжение на поверхности раздела
твердое тело-жидкость. Смачивание.
Капля жидкости на поверхности твердого тела может вести себя различно (рис. 6.2):
Рис. 6.2. Контактные углы, образованные жидкостями на поверхности твердого тела:

Если жидкость смачивает твердое тело, то она стремится растечься по поверхности.
Контактный угол при этом равен 0 (рис. 6.2а), т.е. при полном смачивании q=0, а cos q=1.
Краевой угол q является мерой смачивания. Он определяется как угол между твердой поверхностью и касательной в точке соприкосновения трех фаз. Угол q отсчитывается в сторону жидкой фазы.
В состоянии равновесия:
Величина 
Уравнение известно как соотношение Юнга-Дюпре, которое устанавливает условие равновесия сил, из которого можно определить ПН твердого тела или межфазное натяжение:
Поверхностные натяжения рассмотрены как силы, приложенные перпендикулярно к единице длины периметра смачивания и действующие по касательной к соответствующим поверхностям (рис. 6.3).
Рис. 6.3. Действие трех сил (пограничных) поверхностного натяжения.
Смачиванию благоприятствует низкая свободная энергия поверхности раздела, высокая поверхностная энергия твердого тела и низкая свободная энергия поверхности жидкости.




Величины 



При этом различают силы когезии (слипания) и адгезии (прилипания).
Первые действуют между молекулами внутри фазы, вторые – в разных фазах.
Работа когезии 
Поскольку при этом образуется две новых поверхности жидкости, то:
Работа адгезии 
(Свободная энергия уменьшается за счет работы сил взаимодействия).
Из этих двух уравнений следует уравнение, известное как уравнение Дюпре:
По этому уравнению вычисляют 



Таким образом силы межфазного взаимодействия (адгезионные силы) стремятся растянуть каплю, а силы когезии стягивают каплю, препятствуя растеканию.
Определение 

Эта величина определяется как значение 



Если Г>0 адсорбцию называют положительной, если Г 0, концентрация растворенного вещества в поверхностном слое будет уменьшаться: Г 2 поверхности, кмоль/м 2 ;

Зная Г можно рассчитать площадь S, приходящуюся на 1 молекулу.
Число адсорбированных молекул на 1 м 2 составляет:
С увеличением Г величина S уменьшается и при 

Пользуясь 



Строят изотерму ПН (зависимость 
По изотерме ПН рассчитывают Г по уравнению Гиббса.
Для этого к кривой 




Рис. 6.5. Построение изотермы адсорбции по изотерме
Каждой концентрации С соответствует отрезок Z на оси ординат.
Длина отрезка, выраженная в единицах ПН равна: 

Подставив полученные значения Z в уравнение:
Используя Z для ряда концентраций, рассчитывают адсорбцию Г.
Строят изотерму адсорбции, откладывая по оси абсцисс С, а по оси ординат Г.
Где сложно провести касательную (в интервале концентраций 0,2-0,15 моль/л) рассчитывают изменение: 


Данные заносят в таблицу:
Значение 
Рис. 6.6. График уравнения Ленгмюра в прямолинейных координатах.
Угол 


Отрезок 
Из этого уравнения определяем 
Из уравнения