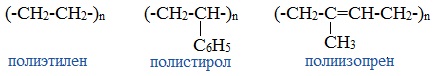Характеристические мономеры, типы и примеры
мономеры это небольшие или простые молекулы, которые составляют основную или существенную структурную единицу более крупных или более сложных молекул, называемых полимерами. Мономер это слово греческого происхождения, что означает обезьяна, один и простой, часть.
Когда один мономер присоединяется к другому, образуется димер. Когда это в свою очередь сливается с другим мономером, оно образует тример и так далее, пока не образует короткие цепи, называемые олигомерами, или более длинные цепи, которые являются так называемыми полимерами..
Мономеры связаны или полимеризуются путем образования химических связей путем совместного использования пар электронов; то есть они связаны ковалентными связями.
На изображении выше кубы представляют собой мономеры, которые связаны двумя гранями (двумя звеньями), образуя падающую башню.
Это связывание мономеров известно как полимеризация. Мономеры одного или разных типов могут быть соединены, и количество ковалентных связей, которые могут быть установлены с другой молекулой, будет определять структуру полимера, который они образуют (линейные, наклонные или трехмерные структуры).
Существует большое разнообразие мономеров, среди которых есть мономеры природного происхождения. Они принадлежат и конструируют органические молекулы, называемые биомолекулами, присутствующими в структуре живых существ..
Например, аминокислоты, которые составляют белки; моносахаридные звенья углеводов; и мононуклеотиды, которые образуют нуклеиновые кислоты. Существуют также синтетические мономеры, которые позволяют разрабатывать бесчисленное множество инертных полимерных продуктов, таких как краски для пластмасс..
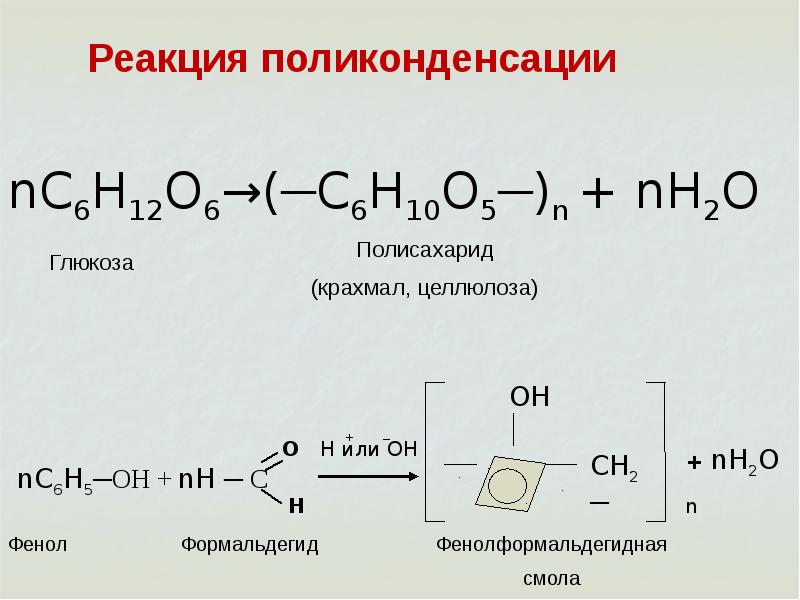
Можно упомянуть два из тысяч примеров, которые можно привести, например, тетрафторэтилен, который образует полимер, известный как тефлон, или мономеры фенол и формальдегид, которые образуют полимер, называемый бакелит..
Характеристики мономеров
Мономеры связаны ковалентными связями
Атомы, которые участвуют в образовании мономера, удерживаются вместе сильными и стабильными связями, такими как ковалентная связь. Кроме того, мономеры полимеризуются или связываются с другими мономерными молекулами через эти связи, придавая прочность и стабильность полимерам..
Эти ковалентные связи между мономерами, могут образовываться в результате химических реакций, которые зависят от атомов, составляющих мономер, наличия двойных связей и других особенностей, которые имеют структуру мономера..
Процесс полимеризации может быть одной из трех следующих реакций: конденсацией, добавлением или свободными радикалами. У каждого из них свои механизмы и способы роста.
Функциональность мономеров и структура Полимера
Мономеры могут быть бифункциональными или полифункциональными, в зависимости от активных или реакционноспособных центров мономера; то есть атомы молекулы, которые могут участвовать в образовании ковалентных связей с атомами других молекул или мономеров.
Эта характеристика также важна, так как она тесно связана со структурой полимеров, которые составляют, как подробно описано ниже.
Бифункциональность: линейный полимер
Мономеры являются бифункциональными, когда они имеют только два сайта связывания с другими мономерами; то есть мономер может образовывать только две ковалентные связи с другими мономерами и образует только линейные полимеры.
Среди линейных полимеров в качестве примера можно упомянуть этиленгликоль и аминокислоты..
Полифункциональные мономеры. Трехмерные полимеры
Есть мономеры, которые могут быть связаны с более чем двумя мономерами и являются структурными единицами большей функциональности.
Они называются полифункциональными и представляют собой те, которые продуцируют разветвленные, сетчатые или трехмерные полимерные макромолекулы; например, полиэтилен.
Скелет или центральная структура
С двойной связью между углеродом и углеродом
Есть мономеры, которые представляют в своей структуре центральный скелет, образованный по крайней мере двумя атомами углерода, соединенными двойной связью (C = C).
В свою очередь, эта цепь или центральная структура имеет присоединенные с боков атомы, которые могут меняться, образуя другой мономер. (R2C = CR2).
Если какая-либо из цепей R модифицируется или заменяется, получается другой мономер. Аналогичным образом, когда эти новые мономеры собираются вместе, они образуют другой полимер.
В качестве примера этой группы мономеров можно упомянуть пропилен (H2C = CH3Н), тетрафторэтилен (F2C = CF2) и винилхлорид (H2C = CClH).
Две функциональные группы в структуре
Хотя есть мономеры, которые имеют одну функциональную группу, существует большая группа мономеров, которые имеют две функциональные группы в своей структуре.
Аминокислоты являются хорошим примером этого. Они имеют амино-функциональную группу (-NH2) и функциональная группа карбоновой кислоты (-СООН), присоединенная к центральному атому углерода.
Эта характеристика того, чтобы быть дифункциональным мономером, также дает способность образовывать длинные цепи полимеров в присутствии двойных связей..
Функциональные группы
В общем, свойства полимеров определяются атомами, которые образуют боковые цепи мономеров. Эти цепи составляют функциональные группы органических соединений.
Существуют семейства органических соединений, характеристики которых определяются функциональными группами или боковыми цепями. Примером является карбоновая кислота, функциональная группа R-COOH, аминогруппа R-NH2, спирт R-OH, среди многих других участвующих в реакциях полимеризации.
Союз одинаковых или разных мономеров
Союз равных мономеров
Мономеры могут образовывать различные виды полимеров. Вы можете объединять те же мономеры или того же типа и генерировать так называемые гомополимеры.
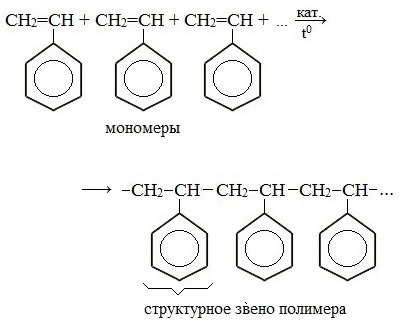
В качестве примера можно упомянуть стирол, образующий мономер полистирола. Крахмал и целлюлоза также являются примерами гомополимеров, образованных длинными разветвленными цепями мономера глюкозы.
Союз разных мономеров
В качестве примера сополимеров можно упомянуть нейлон, полимер, образованный повторяющимися звеньями двух разных мономеров. Это дикарбоновая кислота и молекула диамина, которые соединяются посредством конденсации в эквимолярных пропорциях (равных).
Различные мономеры также могут быть добавлены в неравных пропорциях, таких как образование специализированного полиэтилена, основной структурой которого является 1-октеновый мономер плюс этиленовый мономер.
Типы мономеров
Существует множество характеристик, позволяющих установить несколько типов мономеров, среди которых выделяются их происхождение, функциональность, структура, тип полимера, который они образуют, способ их полимеризации и их ковалентные связи..
Природные мономеры
-Существуют мономеры природного происхождения, такие как изопрен, который получают из сока или латекса растения, и это также мономерная структура натурального каучука.
-Некоторые аминокислоты, вырабатываемые насекомыми, образуют фиброин или белок шелка. Кроме того, есть аминокислоты, которые образуют полимерный кератин, который является белком шерсти, вырабатываемым животными, такими как овцы..
-Среди природных мономеров также имеются основные структурные единицы биомолекул. Например, моносахаридная глюкоза связывается с другими молекулами глюкозы с образованием различных типов углеводов, таких как крахмал, гликоген, целлюлоза и другие..
-Аминокислоты, с другой стороны, могут образовывать широкий спектр полимеров, известных как белки. Это потому, что существует двадцать типов аминокислот, которые могут быть связаны в любом произвольном порядке; и, следовательно, в конечном итоге образует тот или иной белок со своими собственными структурными характеристиками.
-Мононуклеотиды, которые образуют макромолекулы, называемые нуклеиновыми кислотами ДНК и РНК соответственно, также являются очень важными мономерами в этой категории..
Синтетические мономеры
-Среди искусственных или синтетических мономеров (которых много) можно упомянуть некоторые, из которых изготавливаются различные разновидности пластмасс; такой как винилхлорид, который образует поливинилхлорид или ПВХ; и этиленовый газ (Н2C = CH2) и его полиэтиленовый полимер.
Общеизвестно, что из этих материалов можно строить различные контейнеры, бутылки, предметы домашнего обихода, игрушки, строительные материалы и многое другое..
-Тетрафторэтиленовый мономер (F2C = CF2), образующий полимер, известный и коммерчески известный как тефлон.
-Молекула капролактама, полученная из толуола, необходима для синтеза нейлона, среди многих других.
-Существует несколько групп акриловых мономеров, которые классифицируются в зависимости от состава и функции. Среди них акриламид и метакриламид, акрилат, акрил с фтором, среди прочих.
Полярные и полярные мономеры
Эта классификация проводится в соответствии с разницей в электроотрицательности атомов, составляющих мономер. Когда есть заметная разница, полярные мономеры образуются; например, полярные аминокислоты, такие как треонин и аспарагин.
Циклические или линейные мономеры
В соответствии с формой или организацией атомов в структуре мономеров их можно классифицировать как циклические мономеры, такие как пролин, этиленоксид; линейный или алифатический, такой как аминокислота валин, этиленгликоль среди многих других.
примеров
В дополнение к уже упомянутым, доступны следующие дополнительные примеры мономеров:
-И хотя они не были упомянуты, существуют мономеры, структура которых не газированная, а сера, фосфор или атомы кремния..
На конкретных примерах поясните что такое мономер полимер структурное звено степень полимеризации
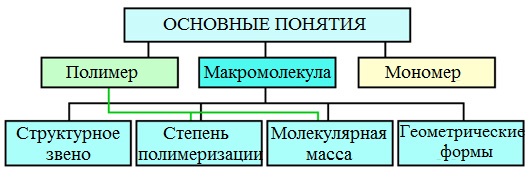
Основные структурные понятия
Для характеристики высокомолекулярных соединений необходимо рассмотреть следующие основные структурные понятия.
Мономер
Мономеры — низкомолекулярные вещества, из которых образуются молекулы полимеров.
Молекулы полимеров являются макромолекулами.
Например, пропилен СН2=СH–CH3 является мономером полипропилена:
а такие соединения, как α-аминокислоты, служат мономерами при синтезе природных полимеров – белков (полипептидов):
Полимер, макромолекула
Высокомолекулярные вещества, состоящие из больших молекул цепного строения, называются полимерами (от греч. «поли» — много, «мерос» — часть).
Например, полиэтилен, получаемый при полимеризации этилена CH2=CH2:
Молекула полимера называется макромолекулой (от греч. «макрос» — большой, длинный).
Молекулярная масса макромолекул достигает десятков — сотен тысяч (и даже миллионов) атомных единиц массы.
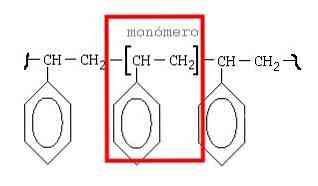
Структурное звено полимера (мономерное звено)
Группа атомов, многократно повторяющаяся в цепной макромолекуле, называется ее структурным звеном.
В формуле макромолекулы это звeно обычно выделяют скобками:
По строению структурного звeна макромолекулы можно сказать о том, какой мономер использован в синтезе данного полимера и, наоборот, зная формулу мономера, нетрудно представить строение структурного звeна.
Строение структурного звена соответствует строению исходного мономера, поэтому его называют также мономерным звеном.
Степень полимеризации
Степень полимеризации (n)
— число, которое показывает, сколько молекул мономеров соединяются в макромолекулу полимера.
В формуле макромолекулы степень полимеризации обычно обозначается индексом «n» за скобками, включающими в себя структурное (мономерное) звено:
Для синтетических полимеров, как правило, n ≈ 102-104; а самые длинные из известных природных макромолекул – ДНК (полинуклеотидов) – имеют степень полимеризации n ≈ 109-1010.
Молекулярная масса макромолекулы и полимера
Молекулярная масса макромолекулы связана со степенью полимеризации соотношением:
М(макромолекулы) = M (звена) × n,
где n — степень полимеризации, M — относительная молекулярная масса
(подстрочный индекс r в обозначении относительной молекулярной массы Мr в химии полимеров обычно не используется).
Для полимера, состоящего из множества макромолекул, понятие молекулярная масса и степень полимеризации имеют несколько иной смысл. Дело в том, что когда в ходе реакции образуется полимер, то в каждую макромолекулу входит не строго постоянное число молекул мономера. Это зависит от того, в какой момент прекратится рост полимерной цепи.




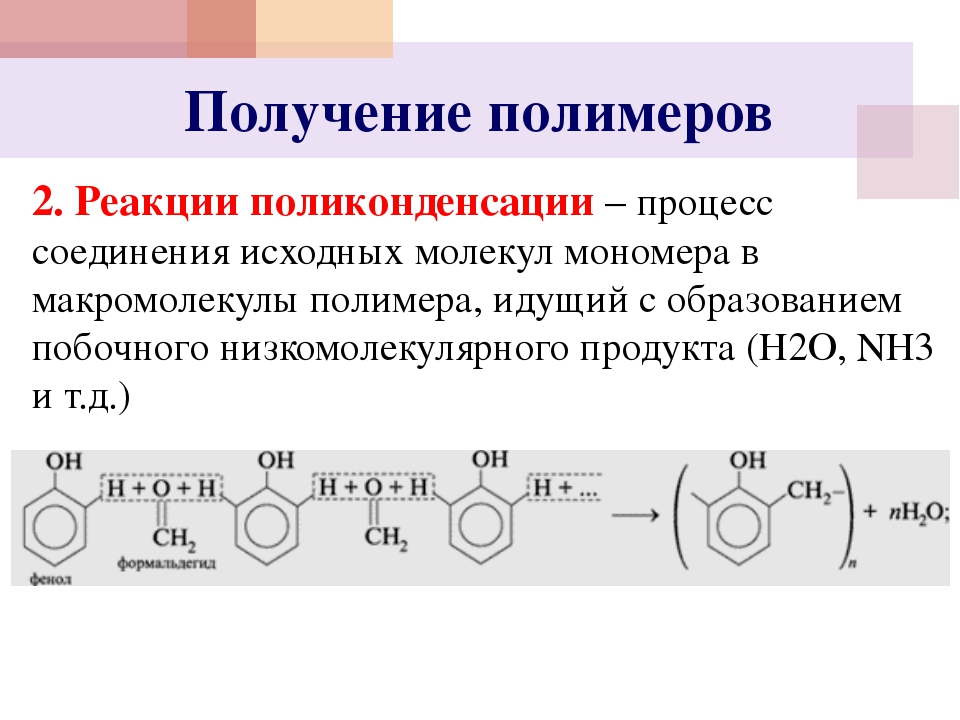

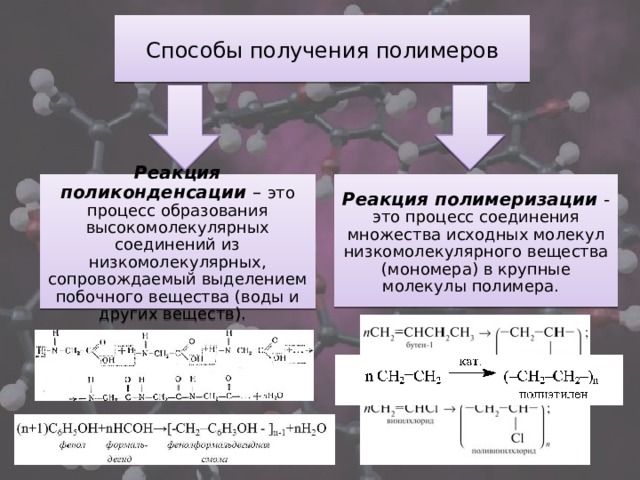

Поэтому в одних макромолекулах мономерных звеньев больше, а в других — меньше. То есть, образуются макромолекулы с разной степенью полимеризации и, соответственно, с разной молекулярной массой (так называемые полимергомологи).
Следовательно, молекулярная масса и степень полимеризации полимера являются средними величинами:
Геометрическая форма макромолекул
Геометрическая форма макромолекулы — пространственная структура макромолекулы в целом.
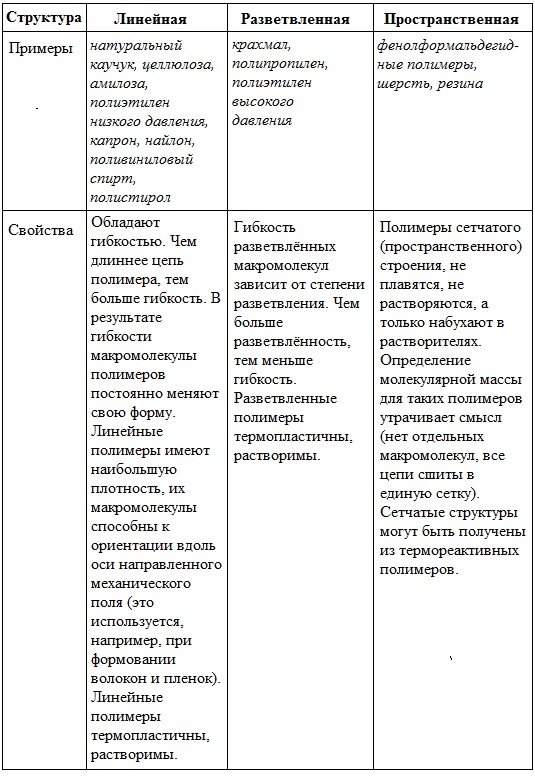
В зависимости от строения углеродной цепи, различают линейные (неразветвленные), разветвленные и пространственные (сетчатые, сшитые) полимеры.
Линейная форма (структурные звенья соединены в длинные цепи последовательно одно за другим) — натуральный каучук, целлюлоза, амилоза (составная часть крахмала), поливиниловый спирт, полистирол, полиэтилен низкого давления, капрон, найлон и др. полимеры:
Разветвленная форма (макромолекулы разветвленных полимеров – это длинные цепи с короткими боковыми ответвлениями) — полиэтилен высокого давления, амилопектин (компонент крахмала):
Пространственная форма (сетчатая, сшитая), при которой длинные линейные молекулы соединены между собой поперечными химическими связями – шерсть, вулканизованный каучук (резина), фенолформальдегидные смолы:
В сетчатых полимерах различные углеродные цепи «сшиты» между собой, и вещество представляет собой одну гигантскую молекулу.
Геометрическая форма макромолекул в значительной степени влияет на свойства полимеров.
Рубрики: Высокомолекулярные соединения
Материалы на основе полимеров
Пластмассы
Пластмассы — материалы на основе полимеров, которые способны под действием нагревания и давления формоваться и сохранять заданную форму после охлаждения.
Помимо высокомолекулярного вещества в состав пластмасс входят также и другие вещества, однако основным компонентом все же является полимер. Благодаря своим свойствам он связывает все компоненты в единую целую массу, в связи с чем его называют связующим.
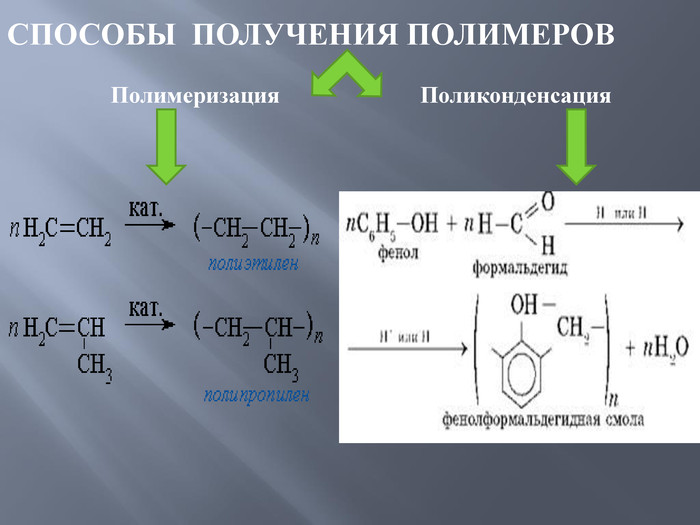


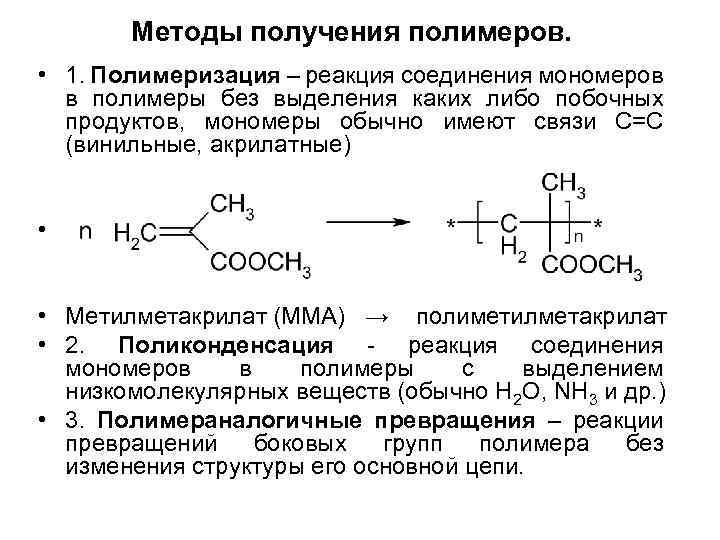



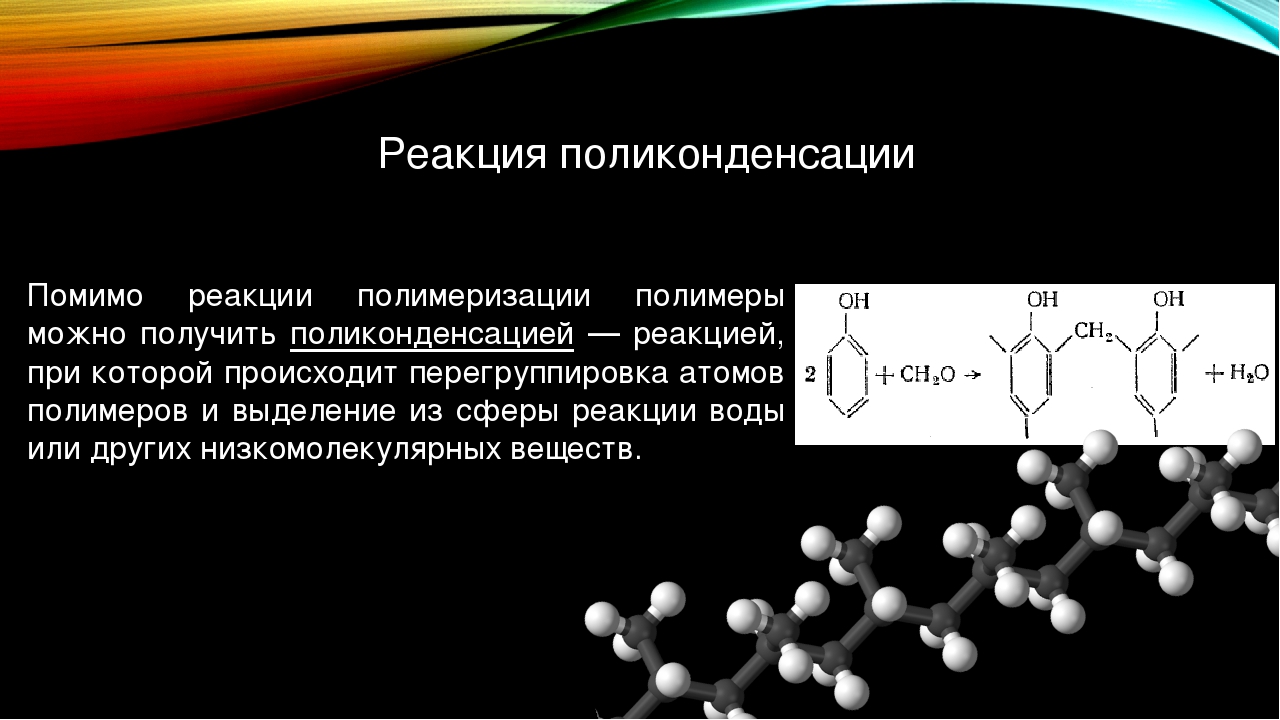

Пластмассы в зависимости от их отношения к нагреванию делят на термопластичные полимеры (термопласты) и реактопласты.
Термопласты — вид пластмасс, способных многократно плавиться при нагревании и застывать при охлаждении, благодаря чему возможно многоразовое изменение их изначальной формы.
Реактопласты — пластмассы, молекулы которых при нагревании «сшиваются» в единую трехмерную сетчатую структуру, после чего изменить их форму уже нельзя.
Так, например, термопластами являются пластмассы на основе полиэтилена, полипропилена, поливинилхлорида (ПВХ) и т.д.
Реактопластами, в частности, являются пластмассы на основе фенолформальдегидных смол.
Каучуки
Каучуки — высокоэлластичные полимеры, углеродный скелет которых можно представить следующим образом:
Как мы видим, в молекулах каучуков имеются двойные C=C связи, т.е. каучуки являются непредельными соединениями.
Каучуки получают полимеризацией сопряженных диенов, т.е. соединений, у которых две двойные C=C связи, разделены друг от друга одной одинарной С-С связью.
Так например, особо зарекомендовавшими себя мономерами для получения каучуков являются:
В общем виде (с демонстрацией только углеродного скелета) полимеризация таких соединений с образованием каучуков может быть выражена схемой:
Таким образом, исходя из представленной схемы, уравнение полимеризации изопрена будет выглядеть следующим образом:
Весьма интересным является тот факт, что впервые с каучуком познакомились не самые продвинутые в плане прогресса страны, а племена индейцев, у которых промышленность и научно-технический прогресс отсутствовали как таковые. Естественно, индейцы не получали каучук искусственным путем, а пользовались тем, что давала им природа: в местности, где они проживали (Южная Америка), произрастало дерево гевея, сок которого содержит до 40-50% изопренового каучука. По этой причине изопреновый каучук называют также натуральным, однако он может быть получен и синтетическим путем.


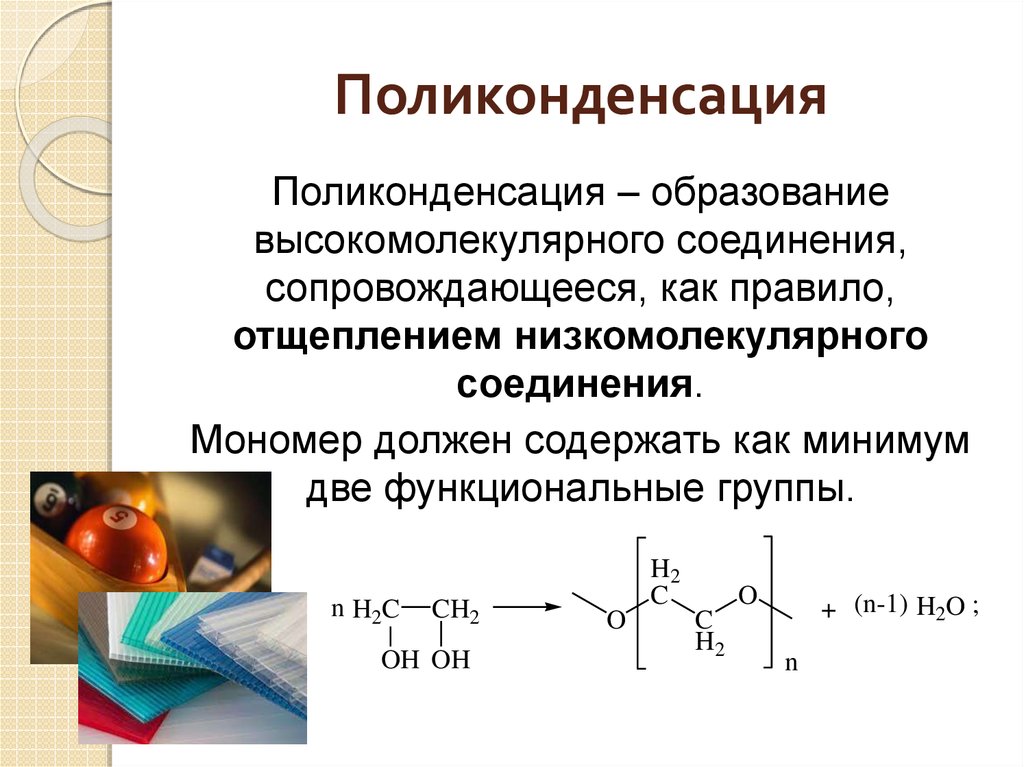





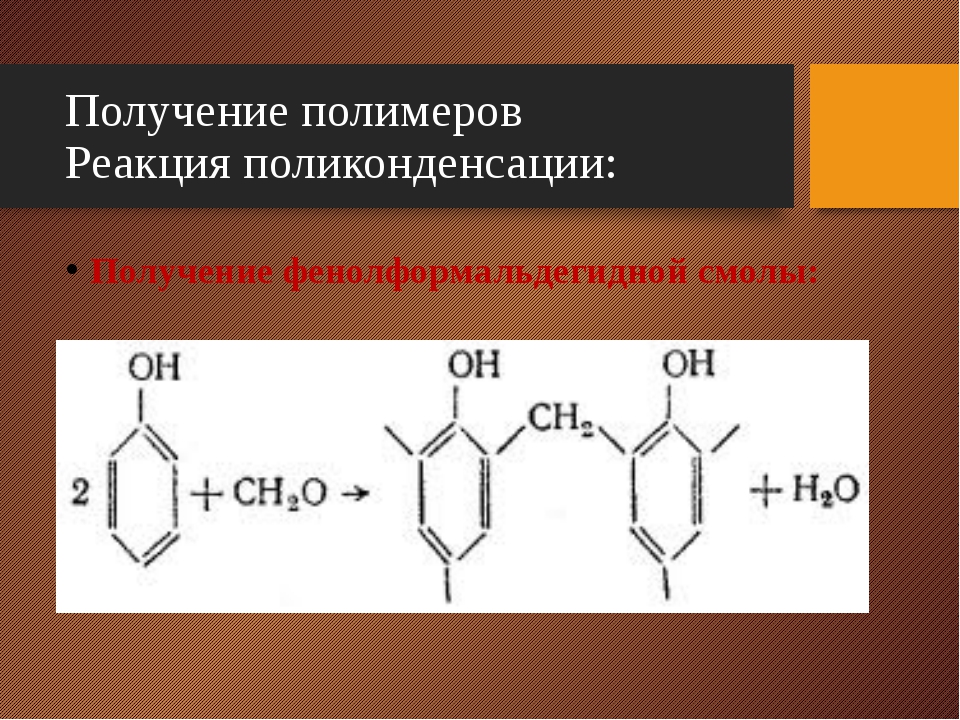
Все остальные виды каучука (хлоропреновый, бутадиеновый) в природе не встречаются, поэтому всех их можно охарактеризовать как синтетические.
Однако каучук, не смотря на свои преимущества, имеет и ряд недостатков. Так, например, из-за того что каучук состоит из длинных, химически не связанных между собой молекул, его свойства делают его пригодным для использования только в узком интервале температур. На жаре каучук становится липким, даже немного текучим и неприятно пахнет, а при низких температурах подвержен затвердеванию и растрескиванию.
Технические характеристики каучука могут быть существенно улучшены его вулканизацией. Вулканизацией каучука называют процесс его нагревания с серой, в результате которого отдельные, изначально не связанные друг с другом, молекулы каучука «сшиваются» друг с другом цепочками из атомов серы (полисульфидными «мостиками»). Схему превращения каучуков в резину на примере синтетического бутадиенового каучука можно продемонстрировать следующим образом:
Волокна
Волокнами называют материалы на основе полимеров линейного строения, пригодные для изготовления нитей, жгутов, текстильных материалов.
Классификация волокон по их происхождению
Искусственные волокна (вискозу, ацетатное волокно) получают химической обработкой уже существующих природных волокон (хлопка и льна).
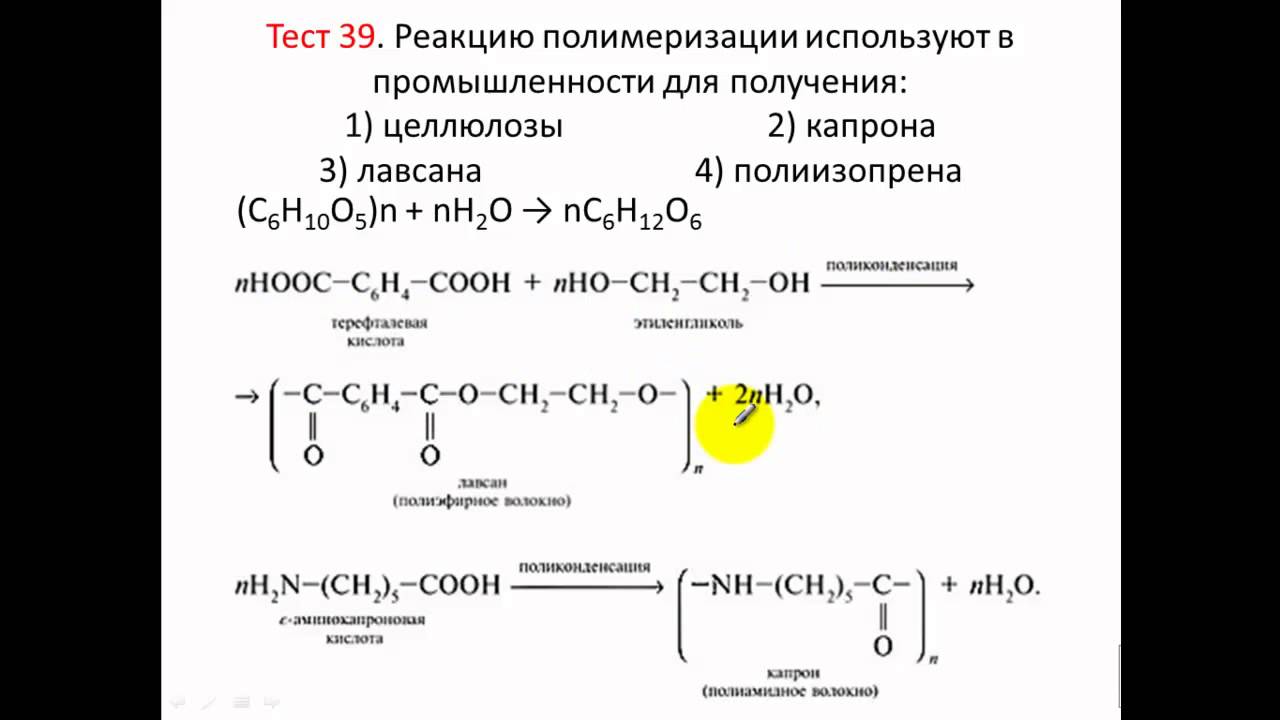
Синтетические волокна получаются преимущественно реакциями поликонденсации (лавсан, капрон, нейлон).
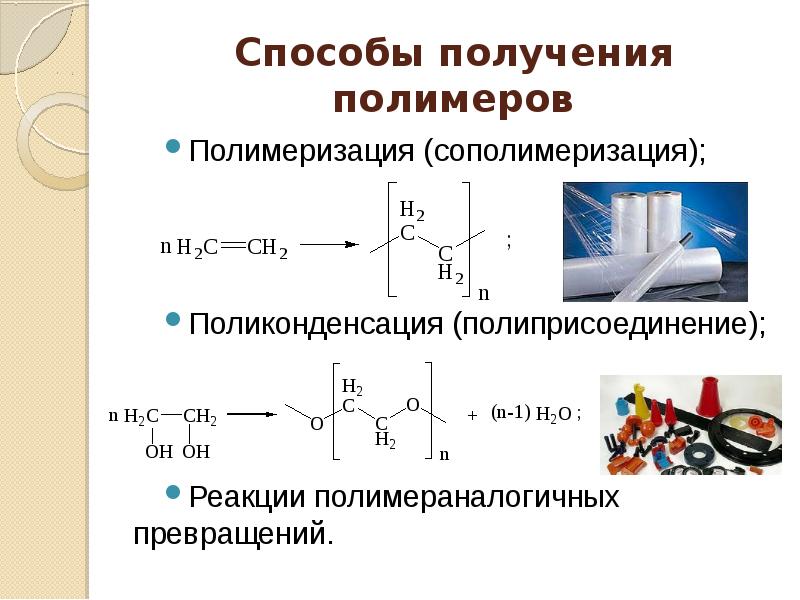
Реакции полимеризации
Реакции полимеризации — это реакции образования полимера путем объединения огромного числа молекул низкомолекулярного вещества (мономера).
Количество молекул мономера (n), объединяющихся в одну молекулу полимера, называют степенью полимеризации.
В реакцию полимеризации могут вступать соединения с кратными связями в молекулах. Если молекулы мономера одинаковы, то процесс называют гомополимеризацией, а если различны — сополимеризацией.
Примерами реакций гомополимеризации, в частности, является реакция образования полиэтилена из этилена:
Примером реакции сополимеризации является синтез бутадиен-стирольного каучука из бутадиена-1,3 и стирола:
На конкретных примерах поясните, что такое мономер, полимер, структурное звено, степень полимеризации.
Другие вопросы из категории
1. калий 2. литий 3. натрий 4. рубидий
4. Оксид элемента Э с зарядом ядра +11 соответствует общей формуле:
1. Э2О 2. ЭО 3. ЭО2 4. ЭО3
5. Характер свойств высшего оксида химического элемента с порядковым номером 6 в Периодической системе:
1. амфотерный 2. кислотный 3. основной
6. Кислотные свойства наиболее ярко выражены у высшего гидроксида:
1. алюминия 2. углерода 3. кремния 4. фосфора
7. Схема превращения C0 → C+4 соответствует химическому уравнению:1. CO2 + CaO = CaCO32. CO2 + H2O = H2CO33. C + 2CuO = 2Cu + CO24. 2C + O2 = 2CO
8.Сокращенное ионное уравнение реакции H+ + OH- = H2O соответствует взаимодействию:
1. гидроксида меди(II) и раствора серной кислоты; 2. гидроксида натрия и раствора азотной кислоты; 3. оксида меди (II) и соляной кислоты; 4. цинка и раствора серной кислоты.
9. Формула вещества, реагирующего с оксидом меди (II):
1. H2O 2. MgO 3. CaCl2 4. H2SO4
10. Элементом Э в схеме превращений Э → Э2О5 → Н3ЭО4 является:
1. азот 2. сера 3. углерод 4. фосфор
Читайте также
фильтрования воздуха, которые используются в быту и на производстве? 3: Что такое центрифугирование? на чем основан этот процесс? где он применяется
4)На примере 1 группы покажи сходство и различие элементов главной и побочной подгрупп?
5) Что такое период?
6) Какие периоды малые?
7)Какие периоды большие?
8)Элементы каких периодов состовляют побочные подгруппы?
9)Элементы какие периодов состовляют главные подгруппы?
10)Какой из элементов:C,N,Si,P As-образуют самое легкое водородное соединение?
11)Химический элемент образует водороное соединение состава H2R и находится в 3 периоде.Назовите элемент?