Наследственный анамнез что это
Сбор семейного анамнеза является важным элементом оценки риска развития онкологических и сердечно-сосудистых заболеваний (ССЗ). У пациентов с отягощенной наследственностью риски обычно выше в 2 раза, а в отдельных случаях и в 4 раза, поэтому у них особенно важно принимать меры по предотвращению заболевания.
Несмотря на то, что генетическая диагностика и определение рисков в последнее время стали более распространенными, отягощенный семейный анамнез до сих пор остается основным методом оценки наследственности в рекомендациях по диагностике и лечению большинства заболеваний.
Анамнез не только указывает на риск заболевания, но и в ряде случаев помогает выбрать оптимальную стратегию наблюдения за пациентом: например, скрининг аневризмы брюшного отдела аорты рекомендуется начинать в 50 лет, если у пациента есть родственник с этим заболеванием.
К сожалению, врачу зачастую не удается качественно собрать семейный анамнез из-за того, что многие пациенты не знают подробности здоровья своих родственников, а информация, которой они владеют, обычно неточна. Кроме того, во время амбулаторного приема врачам не хватает времени для сбора анамнеза. Все это приводит к тому, что исследовательские группы по всему миру разрабатывают решения для получения надежной и точной оценки риска и помогают врачам и пациентам принимать меры на основе собранных данных.
Согласно данным, опубликованным в журнале «Lancet» 5 августа, разработана новая программная платформа для оценки риска развития хронических заболеваний, использующая в числе прочего данные о семейном анамнезе. Программное обеспечение позволяет соединять платформу с электронными медицинскими картами и оказывать поддержку принятия клинических решений врача. Систематический обзор исследований, включавших первичные осмотры 1124 пациентов, показал, что у 66% пациентов высокого риска программа точнее определила риск, чем это было бы сделано ранее, а у 23% ранее анамнез вообще не был бы собран.
Сбор и анализ информации, а также стратификация риска могут выполняться с использованием различных программных платформ. Ранее опыт использования программной платформы показал, что 1184 первичных пациентов заполняли данные о своем семейном анамнезе в среднем 27 минут.
Учитывая такую длительность работы с анкетой, предполагается, что вносить данные пациенты должны без участия врачей. Сообщается, что подобные программы могут стать важным компонентом управления здравоохранением.
Текст подготовил: к.м.н. Круглый Л.Б.
Наследственный анамнез что это
Более столетия тому назад британский врач-ученый Арчибальд Гаррод применил законы наследственности Менделя к наследованию болезней человека и ввел термин «врожденные ошибки метаболизма», создав тем самым раздел биохимической генетики. Тем не менее Гаррод имел в виду больше, чем необычные биохимические изменения у больных с аутосомно-рецессивными нарушениями метаболизма.
Показав свою научную и клиническую проницательность, он предложил значительно более широкое понятие химической индивидуальности, отличающей каждого из нас по состоянию здоровья и предрасположенности к различным болезням вследствие индивидуальных генетических характеристик. И в самом деле, в 1902 г. он писал: «. факторы, определяющие нашу склонность и устойчивостъ к болезням, унаследованы в нашей химической структуре, и даже в молекулярных группах, пришедших из хромосом».
Теперь, более чем 100 лет спустя, в эру геномики человека, у нас есть средства, чтобы оценить важные индивидуальные локусы генотипа и охарактеризовать генетические признаки каждого человека в виде уникальной «химической индивидуальности». Когда станут известны генетические варианты, важные для поддержки здоровья и предотвращения или лечения болезней у каждого человека, и когда это знание будут использовать при принятии важных клинических решений как обычную часть медицинской помощи, мы войдем в эру персонализированной генетической медицины, одну из основных целей проекта «Геном человека».
Тем не менее персонализированная генетическая медицина — только один компонент в широком значении единой службы медицинской помощи больным, когда врачи должны также учитывать индивидуальную историю развития, влияние факторов окружающей среды и общественный опыт при проведении диагностики, консультирования, профилактики и лечения.
Врачи издавна практикуют одну из форм персонализированной генетической медицины, когда собирают семейный анамнез и используют его в клинической практике. Семейный анамнез имеет большое значение в работе с моногенными заболеваниями. Применение известных правил менделирующего наследования позволяет генетикам давать точные оценки риска болезни у родственников больных. Семейная история также важна, когда генетик оценивает риск для комплексных болезней.
Поскольку у родственников имеются общие гены, семейный анамнез дает клиницисту информацию о влиянии на здоровье индивидуальных генетических признаков, что позволяет использовать медицинскую историю родственников как показатель генетической предрасположенности. Кроме того, члены семьи часто имеют общие факторы влияния окружающей среды, например диету и поведение, и, таким образом, родственники могут предоставить информацию как об общих генах, так и общих факторах окружающей среды, способных взаимодействовать, вызывая болезни с многофакторным наследованием.
Наличие родственников первой степени родства с типичной болезнью взрослого возраста, например ИБС, раком молочной железы, опухолями кишечника или простаты, сахарным диабетом II типа, остеопорозом или бронхиальной астмой, — повышает индивидуальный риск для этой болезни приблизительно в 2-3 раза относительно общей популяции.
Чем больше у человека родственников первой степени с многофакторным заболеванием и чем раньше проявляется болезнь у членов семьи, тем больший генетический груз предрасположенности и влияния окружающей среды, вероятно, присутствует в семье пациента, приводя его в группу высокого риска по болезни на основе семейного анамнеза. Например, мужчина с тремя родственниками мужского пола первой степени родства с опухолью простаты имеет в 11 раз более высокий относительный риск развития болезни, чем человек без семейной истории.
Семейный анамнез при оценке риска
I. Высокий риск наследственных болезней:
• Раннее начало болезни у родственников первой степени родства.
• Раннее начало болезни у родственников второй степени (только при ИБС).
• Два пораженных родственника первой степени.
• Один родственник первой степени с поздним или неизвестным началом болезни и больной второй степени родства с ранним началом болезни того же происхождения.
• Два родственника второй степени родства по материнский или отцовской линии, по крайней мере, один с ранним началом болезни.
• Три или более больных родственников по матери или отцу.
• Присутствие семейного анамнеза «умеренного риска» в обеих сторонах родословной.
II. Умеренный риск наследственных болезней:
• Один родственник первой степени родства с поздним или неизвестным началом болезни.
• Два родственника второй степени по одной линии с поздним или неизвестным началом болезни.
III. Средний риск наследственных болезней:
• Отсутствие больных среди родственников.
• Только один больной второй степени родства с одной или обеих сторон родословной.
• Отсутствие семейного анамнеза.
• Приемный ребенок с неизвестным семейным анамнезом
Определение на основе семейного анамнеза того, что человек имеет повышенный риск какого-либо заболевания, может влиять на оказание индивидуальной медицинской помощи. Например, два человека с ГВТ: один с семейной историей необъяснимого ГВТ в относительно молодом возрасте (до 50 лет) и второй без семейной истории любой патологии свертывающей системы, получат разные рекомендации относительно обследования на фактор V Лейдена или мутацию протромбина 20210G>A и противосвертывающей терапии.
Аналогично наличие в семейном анамнезе опухоли толстого кишечника служит основанием для проведения скрининга на опухоли кишечника с применением более сложных методов обследования в возрасте 40 лет, на 10 лет раньше, чем для общей популяции. Дело в том, что совокупная встречаемость болезни у лиц в 40 лет с положительным семейным анамнезом равна риску для 50-летнего человека без такого анамнеза. Увеличение риска будет еще более заметным, если болезнь имеется у двух или более родственников.
Семейный анамнез, к сожалению, сравнительно мало учитывают в клинической медицине. В одном исследовании оказалось, что участковые врачи обсуждают семейную историю только с половиной новых пациентов, и менее чем с четвертью повторных. Только у одного пациента из девяти, наблюдаемых врачами в этом исследовании, в медицинской карте имелась диаграмма родословной.
В другом исследовании, выполненном для проверки состояния медицинской помощи, выяснилось, что наличие у пациента одного или более родственников первой степени родства с болезнью и, следовательно, повышенного риска одного из частых заболеваний взрослого возраста, наследуемого как многофакторный признак, было пропущено почти у двух третей пациентов. Имеет смысл повторить замечание, высказанное выдающимся педиатром и генетиком Бартоном Чайлдсом, приведенное в главе 1: «отсутствие хорошего семейного анамнеза — это плохая медицина».
Конечно, за исключением монозиготных близнецов, никто не обладает всеми одинаковыми генами со своими родственниками. Следовательно, семейный анамнез — лишь косвенное средство оценки вклада индивидуальной комбинации генетических факторов, производимого в развитие болезни. Семейный анамнез так же нечувствителен, как показатель предрасположенности, поскольку он зависит от явной болезни, действительно имеющейся у родственников конкретного пациента.
Будущее принадлежит исследованиям, проводимым независимо от семейной отягощенности, в рамках популяционного скрининга по выявлению вариантов, важных для нормы и патологии, и использованию полученной информации для оценки риска с целью улучшения медицинской помощи конкретному пациенту и его семье. Для применения этой информации необходимо, чтобы генетические факторы были эффективными маркерами фактического риска у конкретного пациента, а сама информация полезна для оказания медицинской помощи.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
«Допрос» в клинике или о том, как собирается анамнез

Ана́мнез (от греч. ἀνάμνησις — воспоминание) — совокупность сведений, получаемых при медицинском обследовании путем расспроса.
1. Жалобы. Бывают основные и второстепенные. Основные жалобы — это, собственно, то, ради чего вам пришлось обратиться к доктору. Дерматологу жалуемся на кожу. Отоларингологу — на боль в ухе и т.д. С этого нужно начинать.
Однако второстепенные жалобы тоже важны. Если у вас повышалась температура, болела голова или резко ухудшилось зрение, стали болеть суставы и вообще любые изменения здоровья — всё это тоже нужно рассказать, даже специалисту, который, казалось бы, «ни при чем».
Он сам решит, что относится к делу. А вот подробное изложение ситуаций, напрямую к здоровью не относящихся (про коммунальщиков, гибэдэдэшников, низкую зарплату, зловредную свекровь и тяжелую жизнь вообще), отнимает время не только у доктора, но и у пациентов в очереди за дверью.
2. Возможные причины. Существует ли причина, с которой вы сами можете связать начало заболевания? Примеры — купил новый стиральный порошок, как только начал носить постиранные им вещи — появились высыпания. Или перенервничал из-за того, что чуть не уволили с работы, или было что-то необычное съеденное или выпитое.
И да, у принимаемых вами лекарств наверняка есть побочные эффекты, и, возможно, причина ухудшения здоровья в этом. Но! Такое случается на самом деле не так часто, как об думают пациенты. А потому торжественно-горестное «я же столько таблеток пью», должное порождать у врача сочувственное уважение к страдальцу, уже не вызывает отклика в очерствевших докторских душах, смиритесь.
3. Длительность болезни. Когда именно вы заболели и как протекала болезнь. Желательно в цифрах. Скажем, болею уже семь дней, а со вчерашнего вечера стало сильно хуже. Или болею третий год, обострения обычно каждой весной, последнее — четвертый день. «Не помню», «примерно», «давно/долго», «когда в позапрошлый раз были в отпуске», «сразу после стационара» — плохие ответы.
4. Что предпринимали по поводу конкретного заболевания. Перечисляются все препараты, травы, БАДы, мази, кремы, физиотерапевтические методы лечения… повторяю — ВСЕ.
Лечились ли «народной» медициной? Стыдно бывает взрослому человеку в таком признаваться, но нужно.
Отдельным списком — то, что принимали параллельно, по поводу других заболеваний: названия лекарств. Ни один доктор не может помнить все коммерческие наименования всех препаратов от всех болезней. Так что если зрелище копающегося доктора в Интернете/ справочнике Видаля Вас раздражает, сделайте список на бумаге.
Особо ответственным товарищам — с действующими веществами (например, соберите все аннотации из упаковок или даже вспомните школьные навыки аппликации и соорудите коллаж из этикеток).
Ответы «не помню», «такие продолговатые», «маленькие желтые», «на букву С, кажется» — ни о чем не говорят. Несколько лучше ответ «в карточке написано»… но и он так себе. Не только потому, что кусок времени врач потеряет на перелистывание талмуда с шифрописью коллег. Но еще и потому, что доктору нужно знать, что из этого вы реально принимали. Может быть, что-то забыли, что-то посоветовали заменить в аптеке, что-то добавили по совету знакомых. Нужна реальная картина.
5. Туберкулез, венерические болезни, гепатиты, ВИЧ-инфицирование. Об этом спросят отдельно. И отвечать нужно правду, даже если пришли, скажем, к мануальному терапевту по поводу коленки.
6. Аллергоанамнез. Случаи любой непереносимости чего бы то ни было (естественно, из того, что едят, пьют, вдыхают, носят на себе, а не более красивой однокурсницы). Особенно важно: непереносимость ЛЕКАРСТВ (сообщите название или хотя бы группу препаратов, каковы были симптомы или точный диагноз, дату).
8. Семейный анамнез: кто из кровных родственников чем болеет (если врач впервые с Вами знакомится, и в карте нет этих сведений), есть ли у кого-либо из кровных родственников такое же заболевание, как у Вас. Напомним, что задавая эти вопросы, врач подразумевает генетическое родство. Так, родители, бабушки/дедушки, дядья и тетки, братья и сестры, кузены и кузины, дети от всех Ваших браков (любого возраста, живущие с Вами или в другом городе, живые или почившие) – родня, а вот муж/жена, свекровь/теща, тесть/свекор и прочие девери/шурины /золовки– нет, даже если Вы «родственные души».
9. «Вредные привычки». Курение – сколько пачек в день и сколько лет? Как часто и как много принимаете алкоголь? и т.д.
10. Обследования. У всех взрослых попросят назвать дату последней флюорографии и RW, у женщин дату последнего посещения гинеколога. (Плохие ответы — «не помню», «тогда когда медкомиссию проходил/а», «кажется, в этом году»). Если проблема, с которой Вы обращаетесь в Центр – не нова, захватите копии результатов прежних консультаций. Анализы, кожные пробы, рентгенограммы и прочее, выписки из стационаров – быстро и четко расскажут Вашему врачу то, что «своими словами» пересказывать трудно и долго.
11. Для деток — информацию про прививки и реакцию Манту. Оптимально – иметь с собою Прививочный сертификат, в который своевременно и полно внесена вся информация, включая названия вакцин.
12. Только для женщин! И это – не дискриминация): У гинеколога (и некоторых других докторов) дам спросят про дату наступления месячных, продолжительность цикла (от первого до первого дня), количество беременностей (считаются все наступившие беременности независимо от того закончились ли они родами, абортом или выкидышем). ВАЖНО! Если Вы беременны или кормите малыша грудью – предупредите об этом и врача и массажиста и косметолога.
13. Другие (известные) болезни. Попросят перечислить все иные болезни, кроме той, по поводу которой вы обратились, особенно если вы на диспансерном учете.
14. Для тех, кому «нужен больничный»: Нетрудоспособность*. Если вам в течение 12 месяцев до момента обращения выдавался больничный (-ные), то спросят, на сколько дней каждый и по какому поводу. Есть ли стойкая потеря трудоспособности (инвалидность).
Несомненно, Вам зададут еще целый ряд других вопросов. Но эти — зададут обязательно. Будьте готовы. Это сократит время на формальности и даст время доктору уделить больше времени основной проблеме.
Леонид Щеботанский — дерматовенеролог высшей категории (Украина), автор популярных медицинских статей в различных изданиях. Ведет свой блог преимущественно на медицинские и общенаучные темы.
Риск носительства заболеваний по родству
Разговор о риске носительства заболеваний по родству следует начать с таких понятий, как гены и хромосомы. Клетки человеческого тела содержат в себе гены, расположенные в нитевидных структурах, называемых хромосомами. В большинстве клеток организма содержится 46 хромосом, из которых ребенок получает 23 от матери и 23 от отца. Они состоят из вещества под названием ДНК.
Изменения в генах и хромосомах приводят к наследственным болезням. У человека могут присутствовать такие мутации, но ввиду наличия двух копий хромосом (полученных от родителей) нормальная копия компенсирует влияние мутированной. Носительство в данном контексте представляет собой ситуацию, когда имеется одна измененная копия в паре хромосом. Это не влияет на здоровье человека, но может отразиться на его потомстве.
Как реализуется риск носительства заболеваний по родству?
Причиной рождения больных детей могут быть:
Способы выяснения риска носительства заболеваний по родству
Вероятность оказаться носителем хромосомной перестройки или генетической патологии повышена у людей с отягощенным семейным анамнезом, а также у родителей детей с подобными наследственными патологиями. Кроме того, существуют болезни, которые характерны для определенной этнической группы или народности.
Для определения риска носительства заболеваний по родству необходимо обратиться к врачу-генетику. На приеме специалист задает вопросы, касающиеся наследственных патологий в семье. Если для исследования имеются основания, врач дает направление на генетический анализ.
Образец крови или слюны направляется в лабораторию, где для оценки риска носительства заболеваний по родству определяется наличие/отсутствие мутации в определенном гене или хромосоме.
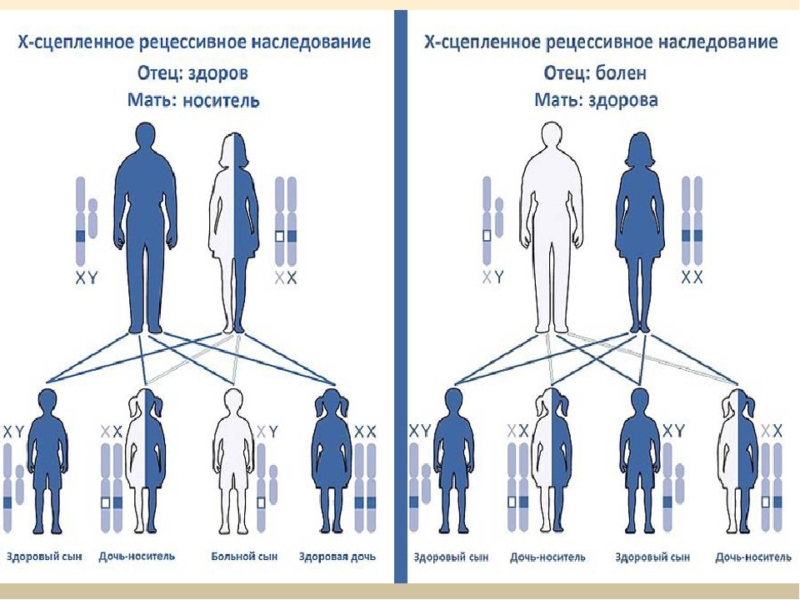
Рождение детей с аутосомно-рецессивной патологией вероятно в том случае, когда оба родителя имеют мутацию в одном и том же гене. При риске носительства заболеваний по родству с X-сцепленным характером вероятно рождение больных сыновей у матери-носительницы, у отца-носителя дочери будут носительницами такой мутации. Женщины редко болеют X-сцепленными болезнями.
Результаты тестирования на риск носительства заболеваний по родству могут оказаться неопределенными. Это может быть связано с присутствием резидального риска (например, для такой болезни, как муковисцидоз), а также с обнаружением мутации, эффект которой неясен.
Что делать, если существует риск носительства заболеваний по родству?
Нужно понимать, что каждый человек является носителем множества генных и хромосомных изменений, но они не обязательно отражаются на его здоровье. Подтверждение того, что женщина или мужчина являются носителем мутации, влияет на принятие решения о рождении детей.
Если оба партнера являются носителями рецессивной патологии либо женщина несет в себе X-сцепленную патологию, то существует несколько вариантов. Выяснить, унаследовал ли ребенок от такого союза генетическую мутацию и будет ли он болеть, позволяет пренатальная диагностика.
Заранее узнать, реализовался ли риск носительства заболеваний по родству, помогает такой метод, как предимплантационная генетическая диагностика. Её проводят в рамках протокола экстракорпорального оплодотворения.
Пройти исследование на риск носительства заболеваний по родству можно в медико-генетическом центре «Геномед».
Скрининг на носительство генетических заболеваний Carrier Screening в г. Москва
Одним из важных генетических исследований, которое рекомендовано сделать при планировании беременности – скрининг на носительство частых аутосомно-рецессивных и X-сцепленных рецессивных заболеваний, также называемый carrier screening.
Принцип наследования генетических заболеваний
При рождении ребенка с наследственным аутосомно-рецессивным заболеванием родители являются здоровыми носителями, то есть у каждого родителя есть нормальный ген и поломанный ген (с мутацией). Носительство заболевания обычно никак не проявляется внешне. Вероятность рождения детей-носителей заболевания будет составлять 50% при каждой беременности, вероятность рождения здоровых детей, не являющимися носителями заболевания, будет составлять 25% при каждой беременности.
Самые частые аутосомно-рецессивные заболевания это:
Частота носительства этих заболеваний очень высока и составляет от 1 на 20 человек до 1 на 60 человек, получается у 1 из 20-60 человек имеется мутация в гене, приводящая к развитию заболевания.
При Х-сцепленном рецессивном типе наследования заболевание проявляется у ребенка при наличии поломанного гена у матери, то есть мать является здоровым носителем. В таком случае существует вероятность рождения больного ребенка (мальчика), которая составляет 25% при каждой беременности. Вероятность рождения здорового ребенка (любого пола), являющийся носителем заболевания – 50%, вероятность рождения девочки-носителя заболевания – 25%.
Зачем будущим родителям проходить Carrier Screening
Клиническая значимость скрининга на носительство генетических заболеваний заключается в том, что с помощью него можно выявить возможное заболевание у будущего ребенка на ранних сроках беременности или до имплантации эмбриона при использовании вспомогательных репродуктивных технологий (ВРТ).
Если в семье у обоих супругов по результатам анализа выявляются мутации (патогенные варианты), вызывающие одно и то же заболевание, в таком случае можно предотвратить рождение больного ребенка.
Для этого проводят:
Кому рекомендовано проходить скрининг на носительство наследственных заболеваний
Американский колледж медицинской генетики и геномики (ACMG) рекомендует проходить скрининг на носительство рецессивных заболеваний:
Как пройти скрининг на носительство
Генетическое исследование назначается врачом-генетиком после консультации, во время которой составляется родословная и рассчитываются риски наследственных заболеваний. Иногда генетиком выявляются случаи семейной наследственной патологии и в таком случае может понадобиться другая диагностика. При отсутствии возможности посетить врача-генетика такой скрининг можно пройти самостоятельно.
Скрининг на носительство рекомендуется проходить либо обоим супругам сразу, либо сначала одному супругу, а затем, если будет выявлен патогенный вариант в одном из генов, второму супругу врач-генетик назначит исследование только на эту мутацию или только на этот ген.
Генетический скрининг на носительство частых рецессивных заболеваний включает в себя 5 этапов:
1. Взятие венозной крови (4 мл) в пробирку с фиолетовой крышкой (с ЭДТА).
2. Заполнение информированного согласия, сопутствующей документации.
3. Отправка биоматериала в генетическую лабораторию.
4. Проведение генетического исследования.
5. Получение результата исследования.
Частые аутосомно-рецессивные заболевания
В 2017 году Американское общество акушеров и гинекологов (ACOG) выпустили рекомендации по исследованию «Скрининг на носительство генетических заболеваний» (1). Основные генетические заболевания, на которые специалисты обратили внимание:
Спинальная мышечная атрофия (СМА)– рекомендовано проводить исследование на носительство СМА всем женщинам, которые планируют беременность или уже беременны.
При наличии в семейном анамнезе больных спинальной мышечной атрофией рекомендуется в первую очередь учитывать результаты генетического исследования заболевшего. Если такое исследование не проводилось или нет возможности узнать результаты, то рекомендуется пройти генетическое исследование делеций гена SMN1.
Муковисцидоз— рекомендовано проводить исследование на носительство муковисцидоза всем женщинам, которые планируют беременность или уже беременны.
Если у пары в семейном анамнезе есть случаи заболевания муковисцидозом, но оба здоровы, следует более детально изучить их родословную и по возможности провести исследование пораженному члену семьи, возможно они являются здоровыми носителями.
Если у супруга муковисцидоз или имеется врожденный дефект – двустороннее отсутствие семявыносящего протока, паре необходимо получить консультацию врача-генетика.
Если у женщины в возрасте до 40 лет наблюдается преждевременное истощение яичников или повышенный уровень фолликулостимулирующего гормона (ФСГ), рекомендуется провести скрининг на носительство ломкой Х-хромосомы, чтобы определить, есть ли у нее премутация в гене FMR1. Пациентам с промежуточными результатами и носителям премутации или полной мутации следует пройти генетическое консультирование для обсуждения риска для их потомков и обсуждения нарушений, связанных ломкой Х-хромосомы.
Генетическое исследование (например, полимеразная цепная реакция) является предпочтительным методом диагностики синдрома ломкой Х- хромосомы и определения числа повторов триплета FMR1 (например, премутаций).