Наследственный гемохроматоз что это
Этиология и встречаемость наследственного гемохроматоза. Наследственный гемохроматоз (MIM №235200) — болезнь накопления железа, встречающаяся у некоторых лиц с гомозиготными или компаундными гетерозиготными мутациями в гене HFE. Большинство пациентов (90-95%) с наследственным гемохроматозом гомозиготны по мутации Cys282Tyr; оставшиеся 5-10% больных — компаундные гетерозиготы по Cys282Tyr и другой мутации, His63Asp. Гомозиготность по мутации His63Asp не ведет к клиническому гемохроматозу, если нет дополнительных причин перегрузки железом.
Частота носительства у белой популяции Северной Америки составляет приблизительно 11% по Cys282Tyr и приблизительно 27% для His63Asp, это означает, что примерно 1 из 330 человек — гомозигота по мутации Cys282Tyr и еще 1 из 135 — ком-паундная гетерозигота по патогенным мутациям в гене HFE. Частота этих мутаций гораздо более низкая среди монголоидов, негроидов и американских индейцев.
Клиническую пенетрантность наследственного гемохроматоза определить трудно; оценки изменяются от 10 до 70%, в зависимости от того, определяется ли наследственный гемохроматоз как органная патология, вызванная накоплением железа, или биохимическим подтверждением повышения насыщения ферритина и уровня трансферрина.
В семейных исследованиях, например, от 75 до 90% гомозиготных родственников больных оказались бессимптомными. Популяционные исследования оценивают пенетрантность наследственного гемохроматоза на основе биохимического подтверждения от 25 до 50%, но пенетрантность может быть более высокой, если выполняется биопсия печени для выявления скрытого цирроза.
Независимо от того, какова пенетрантность, ясно, что мужчины поражаются более часто, чем женщины, и сложные гетерозиготы Cys282Tyr/His63Asp имеют значительно более низкий риск наследственного гемохроматоза, чем гомозиготы Cys282Tyr. Хотя точная величина пенетрантности у гомозигот Cys282Tyr требует окончательного определения, ясно, что пенетрантность неполная.
Патогенез наследственного гемохроматоза
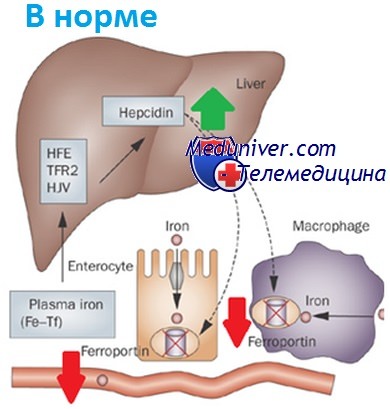
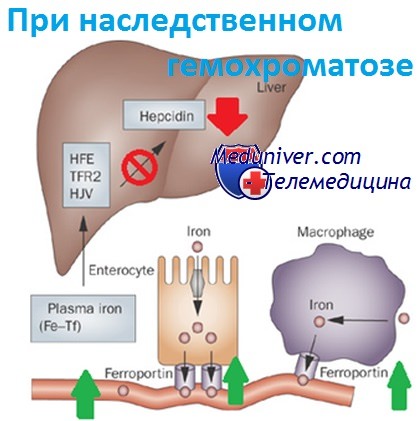
Наследственный гемохроматоз — заболевание, связанное с избытком железа. Запасы железа определяются в основном поглощением его из пищи энтероцитами тонкого кишечника и выходом эндогенного железа из макрофагов, фагоцитирующих эритроциты.
Освобождение железа энтероцитами и макрофагами регулируется циркулирующим гормоном обмена железа, гепсидином, синтезируемым в печени и блокирующим поглощение железа, когда его достаточно. Мутантный белок HFE создает помехи сигналам гепсидина, что приводит к стимуляции энтероцитов и макрофагов к выбросу железа. Таким образом, организм продолжает усваивать железо и использовать его повторно, несмотря на его избыток.
Симптоматика избытка железа развивается лишь у небольшого числа лиц с двумя мутациями в гене HFE. Ранние симптомы включают утомляемость, боли в суставах, снижение либидо и боли в животе. Дополнительные признаки — выявление при обычном обследовании повышенного насыщения трансферрина железом или ферритина. Поздние признаки избытка железа — гепатомегалия, цирроз, печеночно-клеточная карцинома, сахарный диабет, кардиомиопатия, гипогонадизм, артрит и повышенная пигментация кожи. У мужчин симптомы появляются в возрасте 40-60 лет.
Считают, что у женщин симптоматика проявляется вдвое или в десять раз реже, чем у мужчин, симптомы могут не проявиться даже в постменопаузе. Прогноз для пациентов, диагностированных и начавших лечение до развития цирроза печени, отличный. Больные циррозом, получающие эффективное лечение кровопусканиями, все же имеют 10-30% риска развития опухоли печени.
Особенности фенотипических проявлений наследственного гемохроматоза:
• Возраст начала: 40-60 лет у мужчин; в постменопаузе у женщин
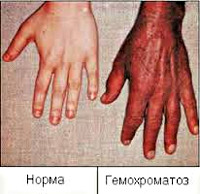
• Утомляемость, слабость, гиперпигментация («бронзовая кожа»), сахарный диабет, цирроз, кардиомиопатия
• Высокая насыщенность трансферрина сыворотки железом
• Высокий ферритин сыворотки
Лечение наследственного гемохроматоза
Индивидуумам с генотипом группы риска следует ежегодно контролировать уровень ферритина сыворотки крови. Если содержание ферритина превышает 50 нг/мл, показано кровопускание для удаления некоторого количества крови и поддержания рекомендованной нормальной концентрации ферритина. Кровопускание повторяют до тех пор, пока не будет достигнута нормальная концентрация ферритина. Невозможность достичь нормальной концентрации ферритина в течение 3 мес от начала кровопусканий — плохой прогностический признак.
Как только концентрация ферритина станет ниже 50 нг/ мл, поддерживающие кровопускания проводят каждые 3-4 мес у мужчин и каждые 6-12 мес у женщин. Больным с клиническими проявлениями и начальной концентрацией ферритина более 1000 нг/мл выполняют биопсию печени для уточнения наличия цирроза. Кровопускания пациентам с биохимическими отклонениями необходимо проводить еженедельно, пока гематокрит не составит 75% начального, а концентрация ферритина станет ниже 50 нг/мл.
Риски наследования наследственного гемохроматоза
Наследственный гемохроматоз — аутосомно-рецессивное заболевание с неполной пенетрантностью. Сибсы больного имеют 25% шанс иметь две мутации. Ребенок больного — облигатный носитель с 5% риском иметь две мутации, если оба родителя европеоиды. Из-за очень низкой пенетрантности этой болезни тотальный популяционный скрининг на наличие мутаций гена HFE не считают целесообразным.
Тем не менее из-за распространенности заболевания, неточной определенности пенетрантности и доступности легкого и эффективного лечения, может оказаться оправданным однократное определение насыщения трансферрина сыворотки и концентрации ферритина среди взрослых мужчин северо-европейского происхождения.
Пример наследственного гемохроматоза. С.Ф., 30-летний ранее здоровый мужчина европейского происхождения, направлен на консультацию в клинику генетики, поскольку у его 55-летнего отца только что диагностирован цирроз печени, вызванный наследственным гемохроматозом. Анамнестические сведения и данные медицинского осмотра в норме.
Насыщение трансферрина железом оказалось 48% (в норме 20-50%). Уровень ферритина сыворотки крови также в норме (
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гемохроматоз. Пигментный цирроз. Бронзовый диабет.
Врачи, лечащие заболевание
У этого заболевания множество названий, но за этой многоликостью прячется опасный враг. Заболевание относительно редкое и требующее исключительного опыта и особого подхода в терапии.
Развитие заболевания связано с избыточным накоплением железа в организме, что проявляется поражением печени, поджелудочной железы, сердца, кожи, суставов, гипофиза.
В развернутой стадии заболевания наблюдаются такие симптомы, как: серые кожные покровы и коричневая пигментация (в области конечностей, лица, шеи и половых органов), сахарный диабет, цирроз печени, хроничечная почечная недостаточность артропатии, импотенция.
Диагноз гемохроматоза устанавливается на основании характерной клинической симптоматики, оценки параметров метаболизма железа (повышение уровней железа и ферритина сыворотки крови; снижение показателей общей железосвязывающей способности сыворотки и трансферрина); результатах генетического тестирования, данных биопсии печени.
Лечение гемохроматоза направлено на удаление из организма избыточного количества железа (с помощью кровопусканий, при применении дефероксамина) и на профилактику возникновения осложнений заболевания.
Выделяют первичный и вторичный гемохроматоз:
В настоящее время известно 5 мутаций, детерминирующих появление этого заболевания.
Типы наследственного гемохроматоза:
Самая распространенная форма наследственного гемохроматоза (более 95% всех случаев) опосредована двумя мутациями в гене HFE, локализованном в 6-й хромосоме (локус 6p21.3): C282Y (замена цистеина в положении 282 на тирозин) и H63D (замена гистидина в положении 63 на аспарагин). Ген детерминирует синтез HFE-белка, который представляет собой гликопротеин (ММ= 37 235 дальтон), сходный по структуре с белками главного комплекса гистосовместимости 1 класса.
Мутации гена HFE приводят к усилению всасывания железа в ЖКТ и его накоплению в тканях организма, что приводит к нарушению функций печени, поджелудочной железы, сердца, гипофиза. Однако клинические проявления заболевания возникают только у половины гомозигот с мутацией C282Y.
Ювенильный гемохроматоз встречается редко. Заболевание манифестирует в возрасте 10-30 лет.
Генетическую основу заболевания составляют мутации гена HJV(локус 7q22), кодирующего синтез рецептора трансферрина-2 (TfR2). Клинические проявления у пациентов с гемохроматозами 2-го и 3-го типов идентичны. Было установлено, что рецептор трансферрина-2 является модулятором продукции гепсидина в ответ на избыток железа в организме. Поэтому у большинства гомозиготных пациентов с мутациями гена, кодирующего синтез рецептора трансферрина-2, уровни гепсидина крайне низкие.
Клиническая симптоматика аутосомно-доминантного гемохроматоза сходна с той, которая наблюдается при гемохроматозе 1-го типа: перегрузка организма железом, сопровождающаяся развитием цирроза печени, сахарного диабета, импотенцией (у мужчин) и аритмиями.
Болезнь быстро прогрессирует, приводя к смертельному исходу вскоре после рождения.
Вторичный гемохроматоз возникает при избыточном поступлении в организм железа (при длительном неконтролируемом лечении препаратами железа, при повторных частых переливаниях крови).
Существует несколько видов вторичного гемохроматоза:
Развивается у людей, которые переносят неоднократные массивные гемотрансфузии по поводу хронических анемий.
К этой группе относятся пациенты с алкогольным циррозом печени, гемохроматозом африканского племени банту. Последний ранее назывался гемосидероз Банту. Его причиной является длительное и избыточное поступление в организм железа с алкогольными напитками, изготавливаемыми в специальных железных сосудах.
Развивается вследствие нарушений метаболизма железа при промежуточной талассемии, у больных циррозом печени после операции портокавального шунтирования, при хронических вирусных гепатитах В и С, при неалкогольном стеатогепатите, при закупорке протока поджелудочной железы, кожной порфирии, при злокачественных новообразованиях.
Возникает при большой талассемии и некоторых видах дизэритропоэтической анемии.
Профилактика
Меры первичной профилактики гемохроматоза не существуют.
Важно как можно раньше установить диагноз, так как лечение гемохроматоза методом кровопусканий позволяет отсрочить или предотвратить появление цирроза печени и увеличить продолжительность жизни пациентов.
С этой целью проводится семейный и популяционный скрининг. В ходе проведения скрининга было установлено, что 78% мужчин (средний возраст 42 года) и 36% женщин (средний возраст 39 лет), являющихся родственниками пациентов с гемохроматозом, являются гомозиготными носителями мутации C282Y и имеют признаки перегрузки железом.
Первичное обследование всех родственников первой степени родства больного гемохроматозом проводится до достижения ими возраста 20 лет путем определения сывороточных показателей метаболизма железа (уровней железа, ферритина, трансферрина, общей железосвязывающей способности сыворотки, коэффициента насыщения ферритина железом).
При наличии лабораторных признаков нарушения метаболизма железа проводится генетическое тестирование с целью выявления мутаций C282Y и H63D.
Если пациент с гемохроматозом или его родственник в возрасте до 40 лет являются гомозиготными носителями мутации C282Y и у них выявлены лабораторные признаки нарушения метаболизма железа, то им рекомендуется проведение кровопусканий.
Если возраст пациента с гемохроматозом или его родственников больше 40 лет, и они являются гомозиготными носителями мутации C282Y, то им производится биопсия печени с целью установления степени ее перегрузки железом.
Биопсия печени проводится также при необходимости подтверждения диагноза и определения стадии заболевания.
Даже при отсутствии в биоптате данных за гемохроматоз родственники пациентов нуждаются в наблюдении с определением железосвязывающей способности сыворотки крови каждые 6-12 месяцев.
При первых признаках заболевания (коэффициент насыщения ферритина железом более 40%), показано проведение кровопусканий.
Симптомы гемохроматоза
Типичные симптомы гемохроматоза проявляются, когда уровень железа в организме достигает критической отметки в 20-40 грамм. Поскольку заболевание развивается очень медленно, то первые тревожные звоночки могут появиться, как правило, к 40-60 годам. На начальных этапах у больных наблюдаются:
Симптомами прогрессирующего гемохроматоза являются:
У женщин в этот период может наблюдаться задержка овуляции или полное прекращение месячных. В запущенных случаях – бесплодие. У мужчин отмечается аномальное увеличение молочных желез, атрофия яичек, а впоследствии – импотенция.
Диагностика гемохроматоза
Диагностика гемохроматоза осуществляется преимущественно лабораторными методами. Основными критериями для подтверждения данного диагноза являются определение уровня железа и железосодержащих белков в плазме крови, а также скорость выведения этого металла с мочой.
Очень часто также применяется биопсия печени и кожи с целью обнаружения специфического пигмента гемосидерина, выделяющегося при распаде гемоглобина.
В отдельных случаях, когда имеет место поражение внутренних органов, врач может назначить ультразвуковое исследование органов брюшной полости, ЭКГ, ЭхоКГ, МРТ печени, рентгенографию суставов и др.
Лечение гемохроматоза
Лечение гемохроматоза – процесс длительный и сложный, осуществляемый в течение всей жизни больного. О полном выздоровлении в данном случае речь не идет, однако при современном уровне развития медицинской науки течение болезни можно существенно замедлить и тем самым облегчить состояние пациента.
При этом заболевании на стадии манифестации с системным накоплением железа (почки, печень, поджелудочная железа, сердце, суставы и другие органы) продолжительность жизни может составлять 4-5 лет. Если же гемохроматоз вовремя диагностировать и помешать его развитию, то течение заболевания в большинстве случаев доброкачественное и может протекать в стадии компенсации десятки лет.
Поначалу у больного сливают по 0,5 литров крови еженедельно, при этом осуществляя контроль за его состоянием. Как только у пациента возникают первые признаки анемии, процедуру выполняют реже, а при необходимости делают перерыв на 3 месяца. Заканчивается курс кровопускания, когда результаты биопсии печени показывают оптимальное содержание железа в тканях этого органа.
Поскольку гемохроматоз является генетически обусловленным заболеванием, стопроцентной защиты от него не существует в принципе. Единственный способ обезопасить себя от его разрушительного влияния – регулярно проходить медицинское обследование и сдавать соответствующие анализы. Особенно это касается тех, у кого есть ближайшие родственники с подобным синдромом.
Гемохроматоз – наследственное полисистемное заболевание, сопровождающееся активным всасыванием железа в ЖКТ и его последующей аккумуляцией во внутренних органах (сердце, поджелудочной железе, печени, суставах, гипофизе). Клиника гемохроматоза характеризуется бронзовой пигментацией кожи и слизистых оболочек, развитием цирроза печени, сахарного диабета, кардиомиопатии, артралгий, нарушения половой функции и т. д. Диагноз гемохроматоза подтверждается при определении повышенной экскреции железа с мочой, высокого содержания железа в сыворотке крови и биоптатах печени, а также с помощью рентгенографии, УЗИ, МРТ внутренних органов. Лечение пациентов с гемохроматозом основано на соблюдении диеты, введении дефероксамина, проведении кровопусканий, плазмафереза, гемосорбции, симптоматической терапии. При необходимости решается вопрос о трансплантации печени и артропластике.
Общие сведения
В этиологическом аспекте выделяют первичный (наследственный) и вторичный гемохроматоз. Первичный гемохроматоз связан с дефектом ферментных систем, приводящим к отложению железа во внутренних органах. В зависимости от генного дефекта и клинической картины выделяют 4 формы наследственного гемохроматоза:
Вторичный гемохроматоз (генерализованный гемосидероз) развивается в результате приобретенной недостаточности ферментных систем, участвующих в обмене железа, и часто ассоциирован с другими заболеваниями, в связи с чем выделяют следующие его варианты: посттрансфузионный, алиментарный, метаболический, смешанный и неонатальный.
Причины гемохроматоза
Первичный наследственный гемохроматоз является заболеванием с аутосомно-рецессивным типом передачи. В его основе лежат мутации гена HFE, расположенного на коротком плече 6-ой хромосомы. Дефект HFE-гена приводит к нарушению трансферрин-опосредованного захвата железа клетками 12-перстной кишки, следствием чего является формирование ложного сигнала о дефиците железа в организме. В свою очередь, это способствует повышенному синтезу железосвязывающего белка DCT-1 энтероцитами и усиленной абсорбции железа в кишечнике (при нормальном поступлении микроэлемента с пищей). В дальнейшем происходит чрезмерное отложение железосодержащего пигмента гемосидерина во многих внутренних органах, гибель их функционально активных элементов с развитием склеротических процессов. При гемохроматозе ежегодно в организме человека накапливается 0,5-1,0 г железа, а проявления заболевания манифестируют при достижении общего уровня железа 20 г (иногда 40-50 г и больше).
Вторичный гемохроматоз развивается в результате избыточного экзогенного поступления железа в организм. Такое состояние может возникать при частых повторных гемотрансфузиях, неконтролируемом приеме препаратов железа, талассемии, некоторых видах анемии, кожной порфирии, алкогольном циррозе печени, хронических вирусных гепатитах В и С, злокачественных новообразованиях, следовании низкобелковой диете.
Симптомы гемохроматоза
Клиническая манифестация наследственного гемохроматоза приходится на зрелый возраст, когда содержание общего железа в организме достигает критических значений (20-40 г). В зависимости от преобладающих синдромов различают гепатопатическую (гемохроматоз печени), кардиопатическую (гемохроматоз сердца), эндокринологическую формы заболевания.
Заболевание развивается постепенно; в начальной стадии преобладают неспецифичные жалобы на повышенную утомляемость, слабость, похудание, снижение либидо. В этой стадии больных могут беспокоить боли в правом подреберье, сухость кожи, артралгии, обусловленные хондрокальцинозом крупных суставов. В развернутой стадии гемохроматоза формируется классический симптомокомплекс, представленный пигментацией кожи (бронзовая кожа), циррозом печени, сахарным диабетом, кардиомиопатией, гипогонадизмом.
Обычно наиболее ранним признаком гемохроматоза выступает появление специфической окраски кожи и слизистых оболочек, выраженной, главным образом, на лице, шее, верхних конечностях, в области подмышек и наружных гениталий, рубцов кожи. Интенсивность пигментации зависит от давности течения заболевания и варьирует от бледно-серого (дымчатого) до бронзово-коричневого цвета. Характерно выпадение волос на голове и туловище, вогнутая (ложкообразная) деформация ногтей. Отмечаются артропатии пястно-фаланговых, иногда коленных, тазобедренных и локтевых суставов с последующим развитием их тугоподвижности.
Практически у всех больных выявляется увеличение печени, спленомегалия, цирроз печени. Нарушение функции поджелудочной железы выражается в развитии инсулинзависимого сахарного диабета. В результате поражения гипофиза при гемохроматозе страдает половая функция: у мужчин развивается атрофия яичек, импотенция, гинекомастия; у женщин – аменорея и бесплодие. Гемохроматоз сердца характеризуется кардиомиопатией и ее осложнениями – аритмией, хронической сердечной недостаточностью, инфарктом миокарда.
В терминальной стадии гемохроматоза развивается портальная гипертензия, асцит, кахексия. Гибель пациентов, как правило, наступает вследствие кровотечения из варикозно расширенных вен пищевода, печеночной недостаточности, острой сердечной недостаточности, диабетической комы, асептического перитонита, сепсиса. Гемохроматоз значительно увеличивает риск развития рака печени (гепатоцеллюлярной карциномы).
Диагностика гемохроматоза
В зависимости от преобладающих симптомов пациенты с гемохроматозом могут обращаться за помощью к различным специалистам: гастроэнтерологу, кардиологу, эндокринологу, гинекологу, урологу, ревматологу, дерматологу. Между тем, диагностика заболевания едина при различных клинических вариантах гемохроматоза. После оценки клинических признаков больным назначается комплекс лабораторно-инструментальных исследований, позволяющих убедиться в правомерности диагноза.
Лабораторными критериями гемохроматоза служат значительное повышение уровня железа, ферритина и трансферрина в сыворотке крови, увеличение выведения железа с мочой, снижение общей железосвязывающей способности сыворотки крови. Диагноз подтверждается с помощью пункционной биопсии печени или кожи, в образцах которых обнаруживается отложение гемосидерина. Наследственная природа гемохроматоза устанавливается в результате проведения молекулярно-генетической диагностики.
С целью оценки тяжести поражения внутренних органов и прогноза заболевания исследуются печеночные пробы, уровень глюкозы крови и мочи, гликозилированный гемоглобин и др. Лабораторная диагностика гемохроматоза дополняется инструментальными исследованиями: рентгенографией суставов, ЭКГ, ЭхоКГ, УЗИ органов брюшной полости, МРТ печени и др.
Лечение гемохроматоза
Основной целью проводимой терапии служит удаление избытка железа из организма и недопущение развития осложнений. Больным с гемохроматозом назначается диета, предусматривающая ограничение пищевых продуктов с высоким содержанием железа (яблок, мяса, печени, гречневой крупы, шпината и пр.), легкоусвояемых углеводов. Запрещается прием мультивитаминов, аскорбиновой кислоты, БАДов, содержащих железо, алкоголя. Для выведения избытков железа из организма прибегают к кровопусканиям под контролем показателей гемоглобина, гематокрита крови, ферритина. С этой же целью могут использоваться экстракорпоральные методы гемокоррекции – плазмаферез, гемосорбция, цитаферез.
Патогенетическая медикаментозная терапия гемохроматоза основана на внутримышечном или внутривенном введении пациенту дефероксамина, связывающего ионы Fe3+. Одновременно проводится симптоматическое лечение цирроза печени, сердечной недостаточности, сахарного диабета, гипогонадизма. При выраженной артропатии определяются показания к проведению артропластики (эндопротезирования пораженных суставов). У пациентов с циррозом решается вопрос о проведении трансплантации печени.
Прогноз и профилактика
Несмотря на прогрессирующее течение заболевания, своевременная терапия позволяет продлить жизнь пациентов с гемохроматозом на несколько десятилетий. При отсутствии лечения средняя продолжительность жизни больных после диагностики патологии не превышает 4-5 лет. Наличие осложнений гемохроматоза (главным образом, цирроза печени и застойной сердечной недостаточности) является прогностически неблагоприятным признаком.
При наследственном гемохроматозе профилактика сводится к проведению семейного скрининга, раннему выявлению и началу лечения заболевания. Избежать развития вторичного гемохроматоза позволяет рациональное питание, контроль за назначением и приемом препаратов железа, проведением переливаний крови, отказ от приема алкоголя, наблюдение за больными с заболеваниями печени и системы крови.
Публикации в СМИ
Гемохроматоз
Гемохроматоз наследственный — нарушение обмена веществ, проявляющееся усиленным всасыванием железа в тонкой кишке и накоплением его в тканях с последующим повреждением и недостаточностью органов. Повышенное накопление железа также может быть связано с другими причинами, например, частыми переливаниями крови или гемолитической анемией. Частота • Распространённость гена, ответственного за гемохроматоз, в Европе: гомозиготы — 0,3%, гетерозиготы — 10% • Заболевание развивается постепенно, и обычно его выявляют в возрасте 40–60 лет • У мужчин клинические проявления развиваются в 10 раз чаще, чем у женщин.
Этиология • Ген, ответственный за развитие наследственного гемохроматоза, локализован в хр. 6 (*235200, 6p21.3, ген HFE, r ) • Отмечена достоверная связь заболевания с типами HLA A3, B7, B14 • Увеличение количества железа в крови может возникнуть при талассемиях, сидеробластической анемии, кожной порфирии, избыточном поступлении железа (например, вследствие приготовления алкогольных напитков в железных сосудах), повторных переливаниях крови.
Патогенез. Механизм усиления всасывания железа при наследственном гемохроматозе неизвестен. Уменьшение всасывания происходит только тогда, когда запасы железа достигают уровня, при котором происходит повреждение тканей. Потеря крови и усиленный расход железа организмом уменьшают запасы железа и задерживают развитие заболевания (кровопускания, менструации и беременность). После уменьшения запасов железа всасывание его в кишечнике вновь усиливается
Патоморфология • Эпидермис истончён, в клетках увеличено содержание меланина • Отложения железа в поджелудочной железе, сердце, гипофизе, суставах • Печень •• Железо, откладывающееся в паренхиме печени, обнаруживают в форме ферритина и гемосидерина. На ранних стадиях — отложения в перипортальных зонах, на поздних стадиях — в эпителии жёлчных протоков, в купферовских клетках, фиброзных перегородках •• Макронодулярный или смешанный цирроз печени.
Клиническая картина
• Пигментация кожи (серая) преимущественно в подмышечных областях, в паху, на открытых частях тела • Астеновегетативный синдром — слабость, апатия • Поражение печени (вплоть до цирроза) •• Увеличение и уплотнение •• Тупые боли в животе, болезненность печени; иногда боли, симулирующие острый живот •• Увеличение селезёнки умеренное •• Печёночная недостаточность, асцит, кровотечение из варикозно-расширенных вен пищевода возникают редко •• У 15–30% больных с циррозом развивается гепатоцеллюлярная карцинома ••• Ухудшение состояния ••• Быстрое увеличение печени ••• Боли в животе ••• Асцит • Поражение поджелудочной железы •• Боли в животе •• Экзокринная недостаточность, диарея •• СД у 2/3 больных • Поражение сердца — рестриктивная кардиомиопатия •• Сердечная недостаточность, отёки •• Нарушения ритма, проводимости • Поражение суставов •• Чаще поражаются мелкие суставы кистей, коленные и тазобедренные суставы •• Артропатия может быть обусловлена синовитом, вызванным отложением пирофосфата кальция • Нарушения репродуктивной функции вследствие поражения гипоталамо-гипофизарной системы и нарушения обмена половых гормонов на фоне поражения печени •• Снижение либидо и потенции (38%) •• Атрофия яичек •• Аменорея (22%) •• Выпадение волос в местах вторичного оволосения.
Лабораторные исследования • Показатели накопления железа •• Насыщение трансферрина (сывороточная концентрация железа, делённая на ОЖСС; выражают в процентах) около 90% (в норме — 30%) •• Сывороточный ферритин: более 200 мг/л для мужчин и 150 мкг/л для женщин ••• Нормальные показатели не исключают избыточного накопления железа ••• Сывороточный ферритин повышен при выраженном некрозе гепатоцитов (освобождение из клеток печени) и некоторых злокачественных опухолях ••• Показатель целесообразно использовать для контроля эффективности лечения •• Концентрация железа в сыворотке крови повышена. Кроме гемохроматоза, повышение сывороточного железа может встретиться при опухолях (например, остром гранулоцитарном лейкозе), частых гемотрансфузиях незадолго до проведения анализа, длительном бесконтрольном приёме препаратов железа • Определение концентрации глюкозы крови и при необходимости — другие тесты для выявления СД • На поздних стадиях заболевания при проведении функциональных пробах печени обнаруживают изменения, характерные для цирроза • Генетическое тестирование.
Инструментальные исследования • Биопсия печени — лучший метод верификации диагноза гемохроматоза •• Позволяет определить стадию фиброза •• Окраска по Перлсу позволяет выявить железосодержащие пигменты. Результаты окрашивания оценивают визуально (от 0 до 4+) в зависимости от процентного содержания окрашенных клеток паренхимы печени •• Количественное определение железа в ткани печени •• Вычисление печёночного индекса железа (содержание железа [мкмоль в 1 г сухой печёночной ткани делят на возраст [в годах]) ••• Печёночный индекс железа позволяет дифференцировать гомозигот (индекс выше 1,9) от гетерозигот (индекс ниже 1,5) и других состояний, сопровождающихся повышенным накоплением железа ••• Индекс не имеет диагностического значения у больных с перегрузкой железа в результате гемотрансфузий • Рентгенография суставов •• Сужение суставной щели •• Субхондральные кисты •• Остеофиты •• При сопутствующей пирофосфатной артропатии — тени отложения пирофосфата кальция в хряще • ЭхоКГ для исключения кардиомиопатии • МРТ позволяет определить степень накопления железа в тканях.
ЛЕЧЕНИЕ
Тактика ведения • Диета (исключение продуктов, содержащих большое количество железа, исключение употребления алкоголя, нежелательно употребление витамина С) • Выведение железа из организма — кровопускания по 500 мл 1–2 р/нед до снижения уровней железа и ферритина сыворотки, а также насыщения трансферрина железом, до нижней границы нормы. После нормализации уровня железа кровопускания по 500 мл 1 раз в 3 мес • Дефероксамин для выведения железа используют только при тяжёлой анемии или гипопротеинемии. Препарат вводят в дозе 20–50 мг/кг/сут в/в, инфузию проводят в течение 10–12 ч. При длительном применении препарата необходимо до и во время лечения проведение офтальмологического обследования • Лечение вторичных поражений (коррекция гормональных нарушений, НПВС — при поражениях суставов и т.д.).
Оперативное лечение • Трансплантация печени при развитии гепатоцеллюлярной карциномы или терминальной стадии цирроза печени • Протезирование суставов при тяжёлой артропатии.
Осложнение • Риск развития первичного рака печени на фоне цирроза выше в 200 раз и при выведении железа он не снижается • Определение концентрации АФП в сыворотке крови 1 раз в 6 мес у больных с циррозом печени в сочетании с УЗИ позволяет диагностировать опухоль на ранней стадии в 80% случаев.
Течение и прогноз определяются степенью и продолжительность перегрузки железом. Неблагоприятные прогностические факторы • Цирроз печени •• СД •• Сердечная недостаточность.
Профилактика • Обследование родственников больного •• Генетическое тестирование •• Тест на гемохроматоз (насыщение трансферрина выше 50% и концентрация ферритина в сыворотке крови более 200 мкг/л у мужчин и 150 мкг/л у женщин) у молодых гомозигот имеет чувствительность 94% и специфичность 86% •• При сохранении повышенных значений хотя бы одного показателя длительное время показано проведение пункционной биопсии печени с определением печёночного индекса железа •• При подтверждении гомозиготности необходимо лечение кровопусканиями даже при отсутствии симптомов заболевания.
Синонимы • Гемомеланоз • Диабет бронзовый • Сидерофилия • Синдром Труазье–Ано–Шоффара • Цирроз пигментный
МКБ-10 • E83.1 Нарушение обмена железа
Код вставки на сайт
Гемохроматоз
Гемохроматоз наследственный — нарушение обмена веществ, проявляющееся усиленным всасыванием железа в тонкой кишке и накоплением его в тканях с последующим повреждением и недостаточностью органов. Повышенное накопление железа также может быть связано с другими причинами, например, частыми переливаниями крови или гемолитической анемией. Частота • Распространённость гена, ответственного за гемохроматоз, в Европе: гомозиготы — 0,3%, гетерозиготы — 10% • Заболевание развивается постепенно, и обычно его выявляют в возрасте 40–60 лет • У мужчин клинические проявления развиваются в 10 раз чаще, чем у женщин.
Этиология • Ген, ответственный за развитие наследственного гемохроматоза, локализован в хр. 6 (*235200, 6p21.3, ген HFE, r ) • Отмечена достоверная связь заболевания с типами HLA A3, B7, B14 • Увеличение количества железа в крови может возникнуть при талассемиях, сидеробластической анемии, кожной порфирии, избыточном поступлении железа (например, вследствие приготовления алкогольных напитков в железных сосудах), повторных переливаниях крови.
Патогенез. Механизм усиления всасывания железа при наследственном гемохроматозе неизвестен. Уменьшение всасывания происходит только тогда, когда запасы железа достигают уровня, при котором происходит повреждение тканей. Потеря крови и усиленный расход железа организмом уменьшают запасы железа и задерживают развитие заболевания (кровопускания, менструации и беременность). После уменьшения запасов железа всасывание его в кишечнике вновь усиливается
Патоморфология • Эпидермис истончён, в клетках увеличено содержание меланина • Отложения железа в поджелудочной железе, сердце, гипофизе, суставах • Печень •• Железо, откладывающееся в паренхиме печени, обнаруживают в форме ферритина и гемосидерина. На ранних стадиях — отложения в перипортальных зонах, на поздних стадиях — в эпителии жёлчных протоков, в купферовских клетках, фиброзных перегородках •• Макронодулярный или смешанный цирроз печени.
Клиническая картина
• Пигментация кожи (серая) преимущественно в подмышечных областях, в паху, на открытых частях тела • Астеновегетативный синдром — слабость, апатия • Поражение печени (вплоть до цирроза) •• Увеличение и уплотнение •• Тупые боли в животе, болезненность печени; иногда боли, симулирующие острый живот •• Увеличение селезёнки умеренное •• Печёночная недостаточность, асцит, кровотечение из варикозно-расширенных вен пищевода возникают редко •• У 15–30% больных с циррозом развивается гепатоцеллюлярная карцинома ••• Ухудшение состояния ••• Быстрое увеличение печени ••• Боли в животе ••• Асцит • Поражение поджелудочной железы •• Боли в животе •• Экзокринная недостаточность, диарея •• СД у 2/3 больных • Поражение сердца — рестриктивная кардиомиопатия •• Сердечная недостаточность, отёки •• Нарушения ритма, проводимости • Поражение суставов •• Чаще поражаются мелкие суставы кистей, коленные и тазобедренные суставы •• Артропатия может быть обусловлена синовитом, вызванным отложением пирофосфата кальция • Нарушения репродуктивной функции вследствие поражения гипоталамо-гипофизарной системы и нарушения обмена половых гормонов на фоне поражения печени •• Снижение либидо и потенции (38%) •• Атрофия яичек •• Аменорея (22%) •• Выпадение волос в местах вторичного оволосения.
Лабораторные исследования • Показатели накопления железа •• Насыщение трансферрина (сывороточная концентрация железа, делённая на ОЖСС; выражают в процентах) около 90% (в норме — 30%) •• Сывороточный ферритин: более 200 мг/л для мужчин и 150 мкг/л для женщин ••• Нормальные показатели не исключают избыточного накопления железа ••• Сывороточный ферритин повышен при выраженном некрозе гепатоцитов (освобождение из клеток печени) и некоторых злокачественных опухолях ••• Показатель целесообразно использовать для контроля эффективности лечения •• Концентрация железа в сыворотке крови повышена. Кроме гемохроматоза, повышение сывороточного железа может встретиться при опухолях (например, остром гранулоцитарном лейкозе), частых гемотрансфузиях незадолго до проведения анализа, длительном бесконтрольном приёме препаратов железа • Определение концентрации глюкозы крови и при необходимости — другие тесты для выявления СД • На поздних стадиях заболевания при проведении функциональных пробах печени обнаруживают изменения, характерные для цирроза • Генетическое тестирование.
Инструментальные исследования • Биопсия печени — лучший метод верификации диагноза гемохроматоза •• Позволяет определить стадию фиброза •• Окраска по Перлсу позволяет выявить железосодержащие пигменты. Результаты окрашивания оценивают визуально (от 0 до 4+) в зависимости от процентного содержания окрашенных клеток паренхимы печени •• Количественное определение железа в ткани печени •• Вычисление печёночного индекса железа (содержание железа [мкмоль в 1 г сухой печёночной ткани делят на возраст [в годах]) ••• Печёночный индекс железа позволяет дифференцировать гомозигот (индекс выше 1,9) от гетерозигот (индекс ниже 1,5) и других состояний, сопровождающихся повышенным накоплением железа ••• Индекс не имеет диагностического значения у больных с перегрузкой железа в результате гемотрансфузий • Рентгенография суставов •• Сужение суставной щели •• Субхондральные кисты •• Остеофиты •• При сопутствующей пирофосфатной артропатии — тени отложения пирофосфата кальция в хряще • ЭхоКГ для исключения кардиомиопатии • МРТ позволяет определить степень накопления железа в тканях.
ЛЕЧЕНИЕ
Тактика ведения • Диета (исключение продуктов, содержащих большое количество железа, исключение употребления алкоголя, нежелательно употребление витамина С) • Выведение железа из организма — кровопускания по 500 мл 1–2 р/нед до снижения уровней железа и ферритина сыворотки, а также насыщения трансферрина железом, до нижней границы нормы. После нормализации уровня железа кровопускания по 500 мл 1 раз в 3 мес • Дефероксамин для выведения железа используют только при тяжёлой анемии или гипопротеинемии. Препарат вводят в дозе 20–50 мг/кг/сут в/в, инфузию проводят в течение 10–12 ч. При длительном применении препарата необходимо до и во время лечения проведение офтальмологического обследования • Лечение вторичных поражений (коррекция гормональных нарушений, НПВС — при поражениях суставов и т.д.).
Оперативное лечение • Трансплантация печени при развитии гепатоцеллюлярной карциномы или терминальной стадии цирроза печени • Протезирование суставов при тяжёлой артропатии.
Осложнение • Риск развития первичного рака печени на фоне цирроза выше в 200 раз и при выведении железа он не снижается • Определение концентрации АФП в сыворотке крови 1 раз в 6 мес у больных с циррозом печени в сочетании с УЗИ позволяет диагностировать опухоль на ранней стадии в 80% случаев.
Течение и прогноз определяются степенью и продолжительность перегрузки железом. Неблагоприятные прогностические факторы • Цирроз печени •• СД •• Сердечная недостаточность.
Профилактика • Обследование родственников больного •• Генетическое тестирование •• Тест на гемохроматоз (насыщение трансферрина выше 50% и концентрация ферритина в сыворотке крови более 200 мкг/л у мужчин и 150 мкг/л у женщин) у молодых гомозигот имеет чувствительность 94% и специфичность 86% •• При сохранении повышенных значений хотя бы одного показателя длительное время показано проведение пункционной биопсии печени с определением печёночного индекса железа •• При подтверждении гомозиготности необходимо лечение кровопусканиями даже при отсутствии симптомов заболевания.
Синонимы • Гемомеланоз • Диабет бронзовый • Сидерофилия • Синдром Труазье–Ано–Шоффара • Цирроз пигментный
МКБ-10 • E83.1 Нарушение обмена железа