Sodium
| Натрий/Natrium (Na) | |
|---|---|
| Атомный номер | 11 |
| Внешний вид простого вещества |  серебристо-белый мягкий металл серебристо-белый мягкий металл |
| Свойства атома | |
| Атомная масса (молярная масса) | 22,989768 а. е. м. (г/моль) |
| Радиус атома | 190 пм |
| Энергия ионизации (первый электрон) | 495,6(5,14) кДж/моль (эВ) |
| Электронная конфигурация | [Ne] 3s 1 |
| Химические свойства | |
| Ковалентный радиус | 154 пм |
| Радиус иона | 97 (+1e) пм |
| Электроотрицательность (по Полингу) | 0,93 |
| Электродный потенциал | -2,71 в |
| Степени окисления | 1 |
| Термодинамические свойства простого вещества | |
| Плотность | 0,971 г/см³ |
| Удельная теплоёмкость | 1,222 Дж/(K·моль) |
| Теплопроводность | 142,0 Вт/(м·K) |
| Температура плавления | 370,96 K |
| Теплота плавления | 2,64 кДж/моль |
| Температура кипения | 1156,1 K |
| Теплота испарения | 97,9 кДж/моль |
| Молярный объём | 23,7 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объемноцентрированая |
| Период решётки | 4,230 Å |
| Отношение c/a | n/a |
| Температура Дебая | 150,00 K |
В воде натрий ведет себя почти так же, как литий: реакция идёт с бурным выделением водорода, в растворе образуется гидроксид натрия.
Содержание
История и происхождение названия
Натрий (а точнее, его соединения) использовался с давних времён. Например, сода (натрон), встречающаяся в природе в водах натронных озёр в Египте. Природную соду древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Плиний Старший пишет, что в дельте Нила соду (в ней была достаточная доля примесей) выделяли из речной воды. Она поступала в продажу в виде крупных кусков, из-за примеси угля окрашенных в серый или даже чёрный цвет.
Натрий впервые был получен английским химиком Хемфри Дэви в 1807 году электролизом твердого NaOH.
Название «натрий» (natrium) происходит от арабского натрун (по-гречески — nitron) и первоначально оно относилось к природной соде. Сам элемент ранее именовался содием (лат. Sodium ).
Получение
Первым способом получения натрия стала реакция восстановления карбоната натрия углем при нагревании тесной смеси этих веществ в железной ёмкости до 1000°C:
Затем появился другой способ получения натрия — электролиз расплава едкого натра или хлорида натрия.
Физические свойства
Натрий — серебристо-белый металл, в тонких слоях с фиолетовым оттенком, пластичен, даже мягок (легко режется ножом), свежий срез натрия блестит. Величины электропроводности и теплопроводности натрия достаточно высоки, плотность равна 0,96842 г/см³ (при 19,7° С), температура плавления 97,86° С, температура кипения 883,15° С.
Химические свойства
Щелочной металл, на воздухе легко окисляется. Для защиты от кислорода воздуха металлический натрий хранят под слоем керосина. Натрий менее активный чем литий, поэтому с азотом реагирует только при нагревании:
При большом избытке кислодрода образуется перокcид натрия
Применение
Металлический натрий широко используется в препаративной химии и промышленности как сильный восстановитель, в том числе в металлургии. Натрий используется в производстве весьма энергоёмких натриево-серных аккумуляторов. Его также применяют в выпускных клапанах грузовиков как теплоотвод. Изредка металлический натрий применяется в качестве материала для электрических проводов, предназначенных для очень больших токов.
В сплаве с калием, а также с рубидием и цезием используется в качестве высокоэффективного теплоносителя. В частности, сплав состава натрий 12 %, калий 47 %, цезий 41 % имеет рекордно низкую температуру плавления −78 °C и был предложен в качестве рабочего тела ионных ракетных двигателей и теплоносителя для атомных энергоустановок.
Натрий так-же используется в газоразрядных лампах высокого давления ДНаТ (Дуговая Натриевая Трубчатая). Эти лампы очень широко применяются в уличном освещении. Они дают ярко-жёлтый свет. Срок службы ламп ДНаТ составляет 12-24 тысяч часов. Поэтому газоразрядные лампы типа ДНаТ незаменимы для городского, архитектурного и промышленного освещения.
Металлический натрий применяется в качественном анализе органического вещества. Сплав натрия и исследуемого вещества нейтрализуют этанолом, добавляют несколько милилитров дистиллированной воды и делять на 3 части, проба Ж. Лассеня (1843), направлена на определение азота, серы и галогенов (проба Бейльштейна)
Хлорид натрия (поваренная соль) — древнейшее применяемое вкусовое и консервирующее средство.
Азид натрия (Na3N) применяется в качестве азотирующего средства в металлургии и при получении азида свинца.
Цианид натрия (NaCN) применяется при гидрометаллургическом способе выщелачивания золота из горных пород, а также при нитроцементации стали и в гальванотехнике (серебрение, золочение).
Хлорат натрия (NaClO3) применяется для уничтожения нежелательной растительности на железнодорожном полотне.
Биологическая роль
В организме находится большей частью снаружи клеток (примерно в 15 раз больше чем в цитоплазме). Это разницу поддерживает натрий-калиевый насос, который откачивает попавший внутрь клетки натрий.
Совместно с калием натрий выполняет следующие функции:
Рекомендуемая доза натрия составляет для детей от 600 до 1700 миллиграмм, для взрослых от 1200 до 2300 миллиграмм. В виде поваренной соли это составляет от 3 до 6 грамм в день.
Натрий содержится практически во всех продуктах, хотя большую его часть организм получает из поваренной соли. Усвоение в основном происходит в желудке и тонкой кишке. Витамин Д улучшает усвоение натрия, однако, чрезмерно соленая пища и пища богатая белками препятствуют нормальному всасыванию. Количество поступившего с едой натрия показывает содержание натрия в моче. Для богатой натрием пищи характерна ускоренная экскреция.
Дефицит натрия у питающегося сбалансированой пищей человека не встречается, однако, некоторые проблемы могут возникнуть при вегетарианских диетах. Временный дефицит может быть вызвано использованием мочегонных, поносом, обильным потением или избыточным употреблением воды. Симптомами нехватки натрия являются потеря веса, рвота, образование газов в желудочно-кишечном тракте, и нарушение усвоения аминокислот и моносахаридов. Продолжительный дефицит вызывает мышечные судороги и невралгию.
Переизбыток натрия вызывает отек ног и лица, а так же повышеное выделение калия с мочой. Максимальное количество соли, которое может быть переработано почками составляет примерно 20-30 грамм, большее количество уже опасно для жизни.
Натрий
Натрий/Natrium (Na), 11
На́трий — элемент главной подгруппы первой группы, третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 11. Обозначается символом Na (лат. Natrium ). Простое вещество натрий (CAS-номер: 7440-23-5) — мягкий щелочной металл серебристо-белого цвета.
Содержание
История и происхождение названия
Натрий (а точнее, его соединения) использовался с давних времён. Например, сода (натрон), встречается в природе в водах натронных озёр в Египте. Природную соду древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Плиний Старший пишет, что в дельте Нила соду (в ней была достаточная доля примесей) выделяли из речной воды. Она поступала в продажу в виде крупных кусков, из-за примеси угля окрашенных в серый или даже чёрный цвет.
Натрий впервые был получен английским химиком Хемфри Дэви в 1807 году электролизом расплава гидроксида натрия.
Нахождение в природе
Получение
Первым промышленным способом получения натрия стала карботермическая реакция восстановления карбоната натрия углем при нагревании тесной смеси этих веществ в железной ёмкости до 1000 °C (способ Девилля) [6] :
С появлением электроэнергетики стал более практичен другой способ получения натрия — электролиз расплава едкого натра или хлорида натрия. В настоящее время электролиз — основной способ получения натрия.
Натрий также можно получить циркониетермическим методом, а также термическим разложением азида натрия.
Физические свойства
Химические свойства
Щелочной металл, на воздухе легко окисляется. Для защиты от кислорода воздуха металлический натрий хранят под слоем керосина.
При горении на воздухе или в кислороде образуется пероксид натрия:
С водой натрий реагирует очень бурно, реакция идёт с выделением водорода, который может самовоспламениться или взорваться, куски металла всплывают на поверхность и могут расплавиться:
Как и все щелочные металлы, натрий является сильным восстановителем и энергично взаимодействуют со многими неметаллами (за исключением азота, иода, углерода, благородных газов):

Натрий более активный чем литий. С азотом реагирует крайне плохо в тлеющем разряде, образуя очень неустойчивое вещество — нитрид натрия (в противоположность нитриду лития):
С разбавленными кислотами взаимодействует как обычный металл:
С концентрированными окисляющими кислотами выделяются продукты восстановления:
Растворяется в жидком аммиаке, образуя синий раствор:
С газообразным аммиаком взаимодействует при нагревании
С ртутью образует амальгаму натрия, которая используется как более мягкий восстановитель вместо чистого металла. При сплавлении с калием даёт жидкий сплав.
Алкилгалогениды с избытком металла могут давать натрийорганические соединения — высокоактивные соединения, которые обычно самовоспламеняются на воздухе и взрываются с водой.
Применение
Металлический натрий широко используется в препаративной химии и промышленности как сильный восстановитель, в том числе в металлургии. Используется для осушения органических растворителей, например, эфира. Натрий используется в производстве весьма энергоёмких натриево-серных аккумуляторов. Его также применяют в выпускных клапанах грузовиков как теплоотвод. Изредка металлический натрий применяется в качестве материала для электрических проводов, предназначенных для очень больших токов.
В сплаве с калием, а также с рубидием и цезием используется в качестве высокоэффективного теплоносителя. В частности, сплав состава натрий 12 %, калий 47 %, цезий 41 % имеет рекордно низкую температуру плавления −78 °C и был предложен в качестве рабочего тела ионных ракетных двигателей и теплоносителя для атомных энергоустановок.
Натрий также используется в газоразрядных лампах высокого и низкого давления (НЛВД и НЛНД). Лампы НЛВД типа ДНаТ (Дуговая Натриевая Трубчатая) очень широко применяются в уличном освещении. Они дают ярко-жёлтый свет. Срок службы ламп ДНаТ составляет 12-24 тысяч часов. Поэтому газоразрядные лампы типа ДНаТ незаменимы для городского, архитектурного и промышленного освещения. Также существуют лампы ДНаС, ДНаМТ (Дуговая Натриевая Матовая), ДНаЗ (Дуговая Натриевая Зеркальная) и ДНаТБР (Дуговая Натриевая Трубчатая Без Ртути).
Металлический натрий применяется в качественном анализе органического вещества. Сплав натрия и исследуемого вещества нейтрализуют этанолом, добавляют несколько миллилитров дистиллированной воды и делят на 3 части, проба Ж. Лассеня (1843), направлена на определение азота, серы и галогенов (проба Бейльштейна)
Хлорид натрия (поваренная соль) — древнейшее применяемое вкусовое и консервирующее средство.
Азид натрия (NaN3) применяется в качестве азотирующего средства в металлургии и при получении азида свинца.
Цианид натрия (NaCN) применяется при гидрометаллургическом способе выщелачивания золота из горных пород, а также при нитроцементации стали и в гальванотехнике (серебрение, золочение).
Хлорат натрия (NaClO3) применяется для уничтожения нежелательной растительности на железнодорожном полотне.
Изотопы натрия
В настоящее время (2012 г.) известно 20 изотопов с массовыми числами от 18 до 37 и 2 ядерных изомера натрия. Единственный стабильный изотоп 23 Na. У большинства изотопов период полураспада меньше одной минуты. Существуют также 2 радиоактивных изотопа с большим периодом полураспада. Это претерпевающий позитронный распад 22 Na с периодом полураспада 2,6027 года, его используют в качестве источника позитронов и в научных исследованиях. 24 Na, с периодом полураспада электронного типа 15 часов, используется в медицине для диагностики и для лечения некоторых форм лейкемии.
Биологическая роль
В высших организмах натрий находится большей частью в межклеточной жидкости клеток (примерно в 15 раз больше чем в цитоплазме клетки). Разность концентраций поддерживает встроенный в мембраны клетки натрий-калиевый насос, откачивающий ионы натрия из цитоплазмы в межклеточную жидкость.
Совместно с калием натрий выполняет следующие функции:
Рекомендуемая доза натрия составляет для детей от 600 до 1700 миллиграммов, для взрослых от 1200 до 2300 миллиграммов в день. В виде поваренной соли это составляет от 3 до 6 граммов в день.
Натрий содержится практически во всех продуктах, хотя большую его часть организм получает из поваренной соли. Усвоение в основном происходит в желудке и тонкой кишке. Витамин Д улучшает усвоение натрия, однако, чрезмерно солёная пища и пища богатая белками препятствуют нормальному всасыванию. Количество поступившего с едой натрия показывает содержание натрия в моче. Для богатой натрием пищи характерна ускоренная экскреция.
Дефицит натрия у питающегося сбалансированной пищей человека не встречается, однако, некоторые проблемы могут возникнуть при вегетарианских диетах и голодании. Временный дефицит может быть вызван использованием мочегонных препаратов, поносом, обильным потением или избыточным употреблением воды. Симптомами нехватки натрия являются потеря веса, рвота, образование газов в желудочно-кишечном тракте, и нарушение усвоения аминокислот и моносахаридов. Продолжительный дефицит вызывает мышечные судороги и невралгию.
Переизбыток натрия вызывает отек ног и лица, а также повышенное выделение калия с мочой. Максимальное количество соли, которое может быть переработано почками составляет примерно 20-30 граммов, большее количество уже опасно для жизни.
Меры предосторожности
В лабораториях небольшие количества натрия (примерно до 1 кг) хранят в закрытых стеклянных банках под слоем керосина, так, чтобы керосин покрывал весь металл. Банка с натрием должна храниться в металлическом несгораемом шкафу (сейфе). Натрий берут пинцетом или щипцами, отрезают скальпелем (натрий пластичен и легко режется ножом) на сухой поверхности (не на столе, а в стеклянной чашке) необходимое количество и остаток тут же возвращают в банку под слой керосина, а отрезанный кусок либо помещают в сухой керосин, либо тут же вводят в реакцию. Прежде чем приступить к работе с натрием, необходимо пройти инструктаж по технике безопасности, лица, впервые приступающие к работе с натрием, должны производить эту работу под наблюдением сотрудников, имеющих опыт такой работы. Обычно в лабораторных условиях для реакций используют количества натрия, не превышающие нескольких десятков грамм. Для демонстративных опытов, например, в школе на уроках химии стоит брать не более одного грамма натрия. После работы с металлическим натрием всю посуду и остатки натрия заливают неразбавленным спиртом и полученный раствор нейтрализуют слабым раствором кислоты. Следует обратить особое внимание, чтобы все остатки и обрезки натрия были полностью нейтрализованы до их выбрасывания, так как натрий в мусорном ведре может вызвать пожар, а в канализационном сливе может вызвать разрушение трубы. Хранить натрий дома и производить с ним какие-либо опыты не рекомендуется.
Натрий
НАТРИЙ, Na (лат. Natrium, от араб. натрун, греч. nitron, первоначально — природная сода * а. sodium, natrium; н. Natrium; ф. sodium; и. sodio), — химический элемент I группы периодической системы Менделеева; атомный номер 11, атомная масса 22,98977; относится к щелочным металлам. В природе встречается один стабильный изотоп 23 Na. Соединения натрия известны с глубокой древности. Металлический натрий впервые получил (1807) английский учёный Г. Дэви.
Физические свойства натрия
Химические свойства натрия
Степень окисления +1. Твёрдый натрий на воздухе быстро окисляется, жидкий — загорается. Хранят под слоем смеси парафина с трансформаторным маслом, бензина или керосина, очищенных от влаги и кислорода, в атмосфере аргона или азота, а также в запаянных стеклянных ампулах. Известен пероксид Na2О2. С водой натрий бурно реагирует с образованием гидроксида и водорода. Натрий, взаимодействуя с галогенами, даёт галогениды, с водородом, серой и азотом (при электрическом разряде) — соответственно гидрид, сульфид и нитрид. Натрий и его гидроксид взаимодействуют с неорганическими кислотами с образованием солей. Натрий растворяется в аммиаке, давая аммиачные комплексы. Известно большое число натрийорганических соединений, используемых в качестве алкилирующих агентов в органическом синтезе. Натрий входит в состав многих сплавов.
Реклама
Нахождение в природе
Получение и применение
Получают натрий термохимическим восстановлением соединений, содержащих этот металл, или электролизом расплавов NaCl с добавлением CaCl2 и BaCl2 и др. или расплавов NaOH с добавлением Na2CO3.
Натрий и его сплавы используются как теплоносители для процессов, требующих равномерного обогрева (например, в ядерных энергетических установках). Na2О2 применяется для получения кислорода в регенерационных устройствах. В металлургической промышленности натрий служит восстановителем при выделении некоторых редких элементов (Ti, Zr, Ta). Натрий — источник свечения в натриевых газоразрядных лампах. Соли натрия находят большое применение в различных отраслях народного хозяйства.
Натрий металлический
Металлический натрий представляет собой мягкий серебристо-белый металл. Токсичен, легко воспламеняем. Благодаря своим химическим свойствам широко используется во многих сферах промышленности.Выпускаемый нашим предприятием продукт соответствует ГОСТ 3273-75 «Натрий металлический технический».
Области применения
Одним из основных направлений применения металлического натрия является синтез регенеративных продуктов, которые необходимы для производства коллективных средств защиты органов дыхания, а также индивидуальных средств защиты, использующихся для нужд Министерства обороны Российской Федерации, а также для гражданских целей МЧС России и Роскосмоса.
Производство
С целью производства металлического натрия, отвечающего всем мировым стандартам, нашим предприятием разработана новая экологически безопасная методология получения продукта, основанная на синтезе физических, химических и технологических процессов.
Конкурентным преимуществом технологического процесса является инновационная процедура предварительной подготовки плава солей в печи специальной конструкции, что позволяет повысить чистоту металлического натрия.
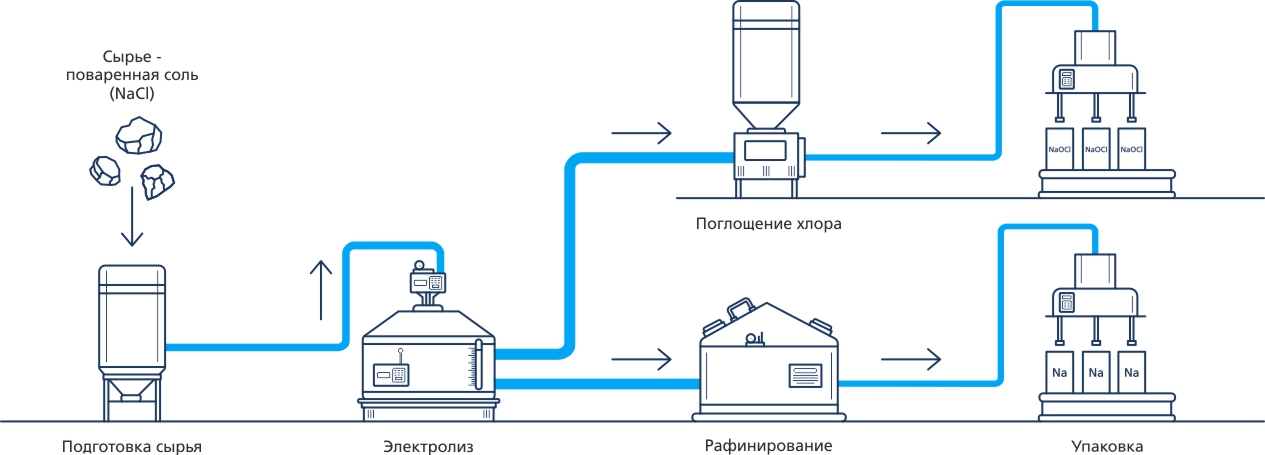
Металлический натрий получают путём электролиза расплава поваренной соли. Производственный процесс включает в себя: сушку поваренной соли, подачу в электролизёр, электролиз с получением газообразного хлора и металлического натрия. При последующих операциях происходит дополнительная очистка натрия и поглощение газообразного хлора с образование гипохлорита натрия.
На каждом производственном участке ведется контроль технологических параметров в соответствии с ГОСТ ISO 9000-2011.
Технологический процесс получения натрия металлического промышленно-безопасен и исключает аварийность.
Экологические свойства и безопасность продукта отвечают нормам Министерства природных ресурсов и экологии Российской Федерации, а также регламентам Евразийского экономического союза.
Отсутствие аналогов предлагаемой технологии позволило предприятию приступить к оформлению патента на полезную модель производства металлического натрия.