Молибдат натрия
| Молибдат натрия | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Молибдат натрия |
| Традиционные названия | Молибденовокислый натрий |
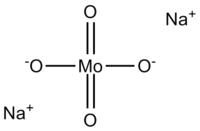
| Химическая формула | Na2MoO4 |
| Физические свойства | |
| Состояние (ст. усл.) | белые кристаллы |
| Молярная масса | 205,92 г/моль |
| Плотность | 3,28; 3,62 г/см³ |
| Термические свойства | |
| Температура плавления | 687; 688 °C |
| Энтальпия образования (ст. усл.) | -1469 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 65 20 ; 84 100 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7631-95-0 |
| Рег. номер PubChem | 61424 |
| SMILES | [O-][Mo](=O)(=O)[O-].[Na+].[Na+] |
| Регистрационный номер EC | 231-551-7 |
| RTECS | QA5075000 |
Молибдат натрия — неорганическое соединение, соль металла натрия и молибденовой кислоты с формулой Na2MoO4, белые кристаллы, растворимые в воде, образует кристаллогидраты.
Содержание
Получение
Физические свойства
Молибдат натрия образует белые кристаллы кубической сингонии, пространственная группа F d3m, параметры ячейки a = 0,9108 нм, Z = 8.
Образует кристаллогидраты состава Na2MoO4•n H2O, где n = 2 и 10.
Применение
Литература
Полезное
Смотреть что такое «Молибдат натрия» в других словарях:
молибдат натрия — молибденовокислый натрий … Cловарь химических синонимов I
Молибдат свинца — Общие Систематическое наименование Молибдат свинца Традиционные названия Молибденовокислый свинец Химическая формула PbMoO4 Физические свойства Состо … Википедия
Молибдат аммония — Общие Систематическое наименование Молибдат аммония Традиционные названия Молибденовокислый аммоний Химическая формула (NH4)2MoO4 Физические свойства … Википедия
Молибдат бария — Общие Систематическое наименование Молибдат бария Традиционные названия Молибденовокислый барий Химическая формула BaMoO4 Физические свойства Состояни … Википедия
Молибдат калия — Общие Систематическое наименование Молибдат калия Традиционные названия Молибденовокислый калий Химическая формула K2MoO4 Физические свойства … Википедия
Молибдат кальция — Общие Систематическое наименование Молибдат кальция Традиционные названия Молибденовокислый кальций Химическая формула CaMoO4 Физические свойства … Википедия
Молибдат магния — Общие Систематическое наименование Молибдат магния Традиционные названия Молибденовокислый магний Химическая формула MgMoO4 Физические свойства Состо … Википедия
Молибдат стронция — Общие Систематическое наименование Молибдат стронция Традиционные названия Молибденовокислый стронций Химическая формула SrMoO4 Физические свойства … Википедия
Алюминат натрия — Общие Систематическое наименование Алюминат натрия Традиционные названия Метаалюминат натрия Химическая формула NaAlO2 Физические свойства Молярная м … Википедия
Гексафтороалюминат натрия — Общие Систематическое наименование Гексафтороалюминат натрия Традиционные названия Фтористый алюминий натрий Химическая формула Na3[AlF6] Физические свойства … Википедия
Натрий молибденовокислый: свойства и применение
Натрий молибденовокислый (молибдат натрия) – это соединение неорганической этимологии, соль металлического Na и молибденовой кислоты.
Данное вещество имеет немалое значение для обменных процессов в живых организмах. Его наличие/отсутствие изрядно влияет на развитие растений и животных. Оно выступает кофактором для ферментов.
Свойства
Молярная масса – 205,92 г/моль, плотность – 3,28, 3,62 г/см³, t плавления – 687, 688 °C. Формула: Na2MoO4.
Получение
Синтез молибденовокислого натрия возможен следующим образом: растворение окиси молибдена в щелочном растворе, или сплавление таких компонентов, как кальцинированная/каустическая сода и оксид молибдена.
Применение

Другие направления активного применения натрия молибденовокислого:
— аграрный комплекс. Служит микроудобрением. Является источником молибдена – незаменимого металлического компонента для большого количества ферментов. Молибден принимает участие в обмене углеводов, азота и фосфора. Не без его помощи синтезируются витамины и хлорофилл. Кроме того, ему под силу ускорить фотосинтез, а также он является составной частью нитратредуктазы – фермента, участвующего в восстановлении нитратов до аммиака в растительных структурах;
— ЛК-производство. Молибдат натрия – один из самых важных компонентов, необходимых для качественного изготовления глазури и пигмента;
— лабораторная практика. Для химических лабораторий и исследовательских учреждений эта соль является очень нужным реагентом в различных химических испытаниях. При сочетании с другими хим. элементами молибдат натрия приводит к образованию новых материалов (например, алкалоидов, чернил и др.), широко применяемых во многих сферах общественной жизнедеятельности. И как аналитический реактив помогает эти самые алкалоиды определять.
К тому же, данное вещество может служить антискейлинговым агентом, выступать промежуточным продуктом, использоваться в качестве смазки и присадки для смазочных материалов, применяться в фармацевтике, производстве бытовой химии (чистящих средств) и уходовой косметики (средств-отбеливателей для кожи и выступающих защитными агентами для волос).
Безопасность
Рассматривая тему «свойства молибдата натрия», нельзя обойти стороной вопрос техники безопасности при обращении с ним.
Итак, имея дело с этим реактивом, помните: ему характерно токсическое воздействие. Может плохо влиять на нервную систему, нарушать обмен веществ, раздражать пищеварительный тракт при проникновении в организм в пылеобразной форме. Несет опасность не только при вдыхании, но и при контакте с кожными покровами. Сильный кашель и болевые ощущения в горле, тошнота, боли в области живота, рвота и диарея – вот признаки того, что при взаимодействии с данным продуктом произошло отравление.
Это вещество принадлежит к третьему классу опасности. Предельно допустимая концентрация в рабочем воздушном пространстве составляет 4 мг/м³. Есть ограничения и по поводу количества данного материала, находящегося в хозяйственно-питьевых водоемах – 0,25 мг/дм³ (по Mo).
Чтобы минимизировать негативное воздействие молибденовокислого натрия на организм, используя его в работе, не забывайте применять СИЗ, главным образом, для защиты лица и рук (респиратор, перчатки из резины, очки). Другие важные защитные мероприятия: соблюдение личной гигиены, обеспечение помещений приточно-вытяжной вентиляцией. Если имеет место лабораторный анализ, выполнять его лучше всего в вытяжном шкафу.
Еще один момент. Нагреваясь, этот реактив поддается разложению, при этом формируются ядовитые газы, в частности окись натрия. Также он вступает в бурные реакции с галогенами. Опасность заключается и в том, что он может привести к пожару и взрыву. Это стоит учитывать при хранении. Избегайте соседства с мощными окислителями и галогенами. Храните данную соль в крытом сухом месте при комнатной t. Не используйте по истечении срока годности, который составляет 12 месяцев со дня изготовления.
Молибдат натрия – вещество важное и, в то же время, требующее внимательного отношения. Чтобы исключить возможные риски, обязательно соблюдайте технику безопасности.
Молибденовокислый натрий (Молибдат натрия)
Продажа
Компания АО «Реахим» на протяжении многих лет предлагает качественную продукцию высокой чистоты и с действующим сроком гарантии. Покупая у нас молибденовокислый натрий и другие реагенты, Вы получаете продукцию, соответствующую стандартам, по низкой цене и с быстрой доставкой в оговоренные сроки.
Общее определение
Молибденовокислый натрий представляет собой кристаллический порошок, необходимый для обмена веществ и развития растений и животных, служит кофактором для ферментов. Является неорганическим соединением, растворяется в воде.
Применение
Молибденовокислый натрий используется в качестве ингибитора коррозии и анти-скейлингового агента, как промежуточная продукция, в лаборатории, как смазочный материал и присадки к смазочным маслам.
Получение
Для синтеза молибдата натрия растворяется оксид молибдена в растворе щелочи или методом сплавления гидроксида натрия с оксидом молибдена.
Идентификация
Название: Молибденовокислый натрий / Sodium molybdate
Синонимы: Молибдат натрия / Disodium molybdate
Формула: MoNa2O4
CAS: 7631-95-0
Физические данные
Пожарная безопасность
При нагревании молибденовокислый натрий разлагается с образованием токсичных газов, включая оксид натрия, и еще бурно реагирует с галогенами. Опасное вещество, может стать причиной пожаров и взрывов.
Влияние на организм
Молибдат натрия опасен при вдыхании и попадании на кожу, он оказывает раздражающее действие, интенсивный кашель и боль в горле, а при проглатывании вызывает тошноту, боли в животе, рвоту, диарею.
Транспортировка и хранение
Для транспортировки используются тары объемом 5 г, 100 г, 500 г.
Важным при хранении является удаленное расстояние от молибденовокислого натрия до сильных окислителей и галогенов. Помещение должно быть крытое с комнатной температурой.
Гарантийный срок
Хранится в течение 1 года от даты производства, в сухом месте.
Анион молибдата (VI) тетраэдрический. Два катиона натрия координируются с каждым анионом.
СОДЕРЖАНИЕ
История
Молибдат натрия впервые был синтезирован методом гидратации. Более удобный синтез осуществляется путем растворения МоО 3 в гидроксиде натрия при 50–70 ° C и кристаллизации отфильтрованного продукта. Безводную соль получают нагреванием до 100 ° C.
Использует
В сельском хозяйстве используется 1 миллион фунтов стерлингов в год в качестве удобрений. В частности, его использование было предложено для лечения Хлыстохвостов в брокколи и цветной капусте в молибденовых-дефицитных почвах. Однако следует проявлять осторожность, потому что при уровне 0,3 ppm молибдата натрия может вызвать дефицит меди у животных, особенно крупного рогатого скота.
Реакции
При взаимодействии с боргидридом натрия молибден восстанавливается до оксида молибдена (IV) с более низкой валентностью :
Молибдат натрия реагирует с кислотами дитиофосфатов:
который далее реагирует с образованием [MoO 3 (S 2 P (OR) 2 ) 4 ].
Безопасность
Молибдат натрия несовместим с щелочными металлами, наиболее распространенными металлами и окислителями. Он взорвется при контакте с расплавленным магнием. Он будет бурно реагировать с межгалогенами (например, пентафторид брома ; трифторид хлора ). Его реакция с горячим натрием, калием или литием раскалена.
Натрий молибдат дигидрат, ч
| CAS | 10102-40-6 |
| Молекулярная формула | H4MoNa2O6 |
| Синонимы | натрий молибденовокислый, 2-водный |
| Температура плавления | 100°C (с разложением) |
| Температура кипения |
Классификация химических реактивов
Чистый («ч.»)
Содержание основного компонента 98% и выше (без примесей). Цвет полосы на упаковке — зелёный.
Чистый для анализа («ч.д.а.», «чда»)
Содержание основного компонента выше или значительно выше 98%. Примеси не превышают допустимого предела для точных аналитических исследований. Цвет полосы на упаковке — синий.
Химически чистый («х.ч.», «хч»)
Содержание основного компонента более 99%. Цвет полосы на упаковке — красный.
Особо чистый («осч»)
Cодержание примесей в таком незначительном количестве, что они не влияют на основные свойства. Цвет полосы на упаковке — жёлтый.
Как купить?
Приобрести у нас реактив можно оформив заказ в 1 клик или по звонку
Как получить свой заказ?
Доставка осуществляется по всей России или самовывозом из г.Королев.
Как оплатить заказ?
Предлагаем более 10 видов оплаты заказа, наличные и безналичные формы







