Неонатальный скрининг новорожденных. Зачем берут кровь из пяточки?
Неонатальный скрининг поможет определить недуги, с которыми мы не в силах бороться при помощи витаминок или соблюдения режима дня.
В этой статье мы расскажем вам о том, что такое неонатальный скрининг новорожденных, для чего его делают. Ведь многих мам волнует вопрос, зачем малышу в роддоме берут кровь из пяточки?
После рождения малыш вступает в жизнь с непривычными для него условиями, нуждаясь в нашей заботе и обереге от заболеваний. Частично свое чадо от «летающих» вирусов и бактерий мы защищаем. Однако существуют недуги, с которыми мы не в силах бороться при помощи витаминок или соблюдения режима дня.
Речь идет о наследственных или врожденных заболеваниях, не выявленных у малыша во время внутриутробного развития. Подробнее о генетических исследованиях до и во время беременности https://www.u-mama.ru/read/waiting/pregnancy/8760.html.
Что такое неонатальный скрининг
Неонатальный скрининг — массовое обследование всех новорожденных детей для раннего выявления наиболее распространенных наследственных или врожденных заболеваний.
Цель: обнаружение у малыша недуга до появления клинических признаков и назначение советующего своевременного лечения.
Правовое регулирование скринингового исследования новорожденных в Российской Федерации
Начиная с 2006 года, в рамках национального проекта «Здоровье» всем новорожденным детям проводят исследование на выявление врожденного гипотиреоза, фенилкетонурии, муковисцидоза, адреногенетального синдрома и галактозмии.
Ранее на протяжении 15 лет проводилось тестирование лишь на врожденный гипотиреоз и фенилкетонурию.
Порядок и сроки выполнения скрининга регламентируются Приказом Минздравсоцразвития России от 22.03.2006 г. № 185 «О массовом обследовании новорождённых детей на наследственные заболевания».
С 2007 года проводится аудиологический скрининг, рано выявляющий нарушения слуха у ребенка первого года жизни.
По Свердловской области перечень расширен до 16 патологий на основании Приказа МЗ СО от 02.03.2012 г. № 166-п «О совершенствовании массового обследования новорожденных детей на наследственные заболевания на территории Свердловской области».
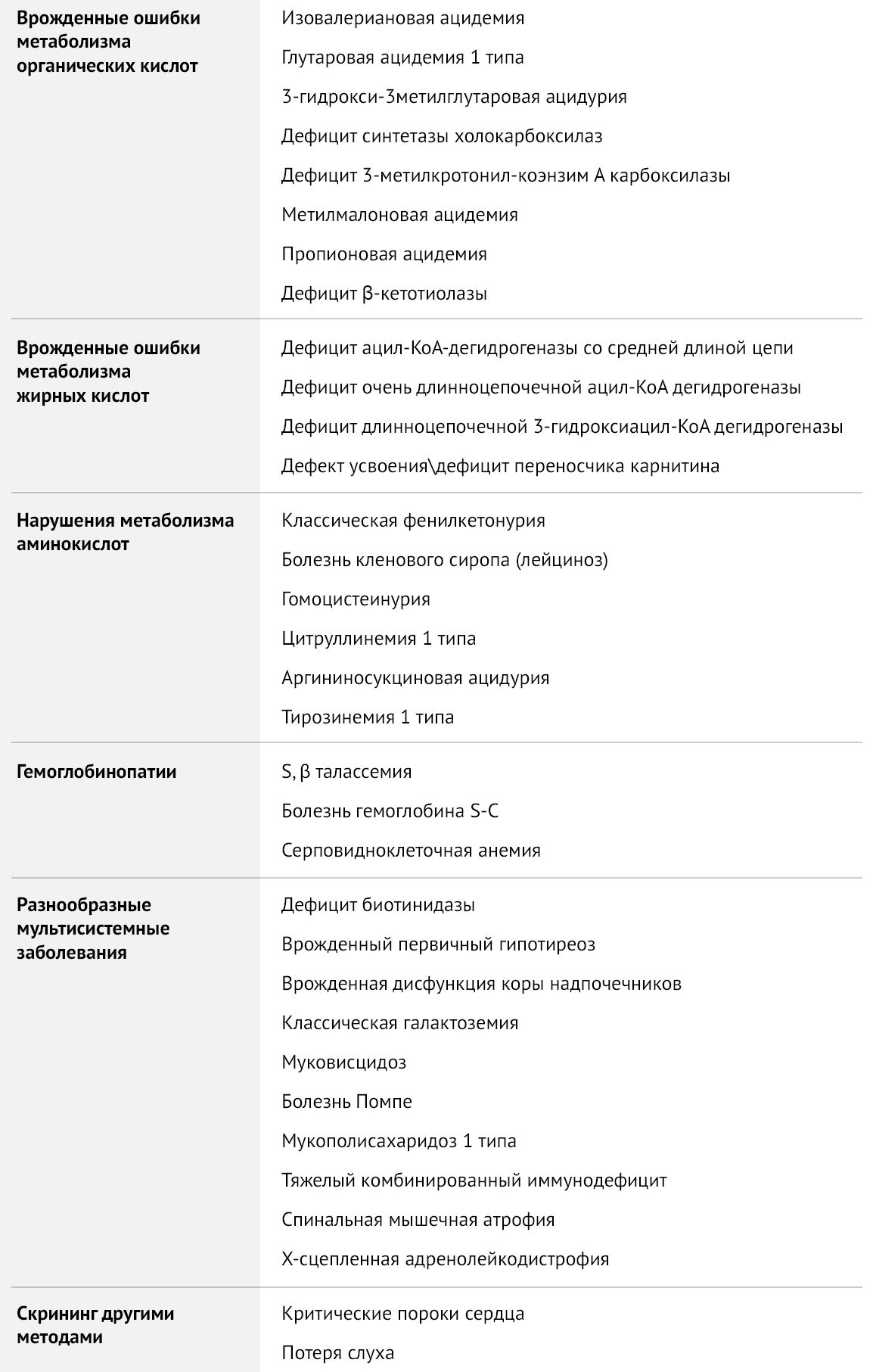
Дополнительные одиннадцать заболеваний:
Сроки и условия проведения неонатального скрининга новорожденных
Исследование выполнятся в родильном доме на четвертый день жизни у доношенного ребенка, у недоношенного малыша — на седьмой или позднее. При тестировании на более ранних сроках возможно получение ложноположительных или ложноотрицательных результатов.
Набирается капелька крови из пятки малыша до кормления утром натощак либо чрез три часа после любого очередного кормления. Затем кровь наносится на тестовые бланки (фильтровальную бумагу) на область специальных кружочков, пропитанных специальным веществом.
Иногда скрининг не проводится в родильном доме — например, при выписке из стационара ранее четвертых суток жизни ребенка. Вам на руки выдается заполненный тест-бланк для забора крови, а в обменной карте указывается, что кровь на скрининг не взята. Набор крови проводится на участке согласно рекомендованным срокам.
Как расцениваются итоги исследования?
Результаты можно узнать в поликлинике по месту жительства через 10 дней после забора анализа.
Ребенок здоров при отрицательных результатах тестирования. Обычно родителей об этом не извещают. Наблюдение за ребенком проводится по возрасту согласно рекомендованным срокам в плановом порядке.
Положительный или сомнительный результат не всегда означает, что ребенок болен.
Скрининг — лишь расчет вероятного риска наличия недуга у крохи. Для уточнения диагноза проводится повторный забор крови. При вновь повышенных показателях ребенка с родителями направляют в медико-генетическую консультацию для тщательного и детального обследования.
Как и когда проводится аудиометрия?
Исследование выполняет отоларинголог (ЛОР-врач) при помощи аудиометра в родильном доме или поликлинике в первые дни жизни ребенка. Если малыш спокойный, то тестирование обычно занимает всего несколько минут. Результат вы получите сразу после его завершения.
Варианты проведения исследования
* В наружный слуховой проход ребенка вводится небольшой микрофон и подается звуковой сигнал, который улавливают клетки в ухе малыша и отправляют ответный сигнал (эхо). При отсутствии проблем со слухом эхо улавливается прибором.
* Малышу надеваются наушники, а к голове прикрепляются электроды. Через наушники подается звуковой сигнал в наружный слуховой проход, активизирующий участки головного мозга, которые отвечают за слух. Их электрическую активность улавливают электроды и передают прибору.
Выявление отклонений на аудиометрии вовсе не означает, что у малыша обязательно имеются проблемы со слухом. Возможно, результаты исследования были искажены из-за того, что кроха во время тестирования был беспокойным, плакал или двигался.
При неудовлетворительном результате аудиометрии в первые дни жизни малыша исследование проводится повторно немного позднее: обычно в месячном возрасте.
Как видите, возможности неонатального скрининга довольно большие, что позволяет рано выявить недуг и назначить лечение.
В следующем материале — описание наиболее часто встречающихся наследственных заболеваний, выявляемых при помощи «пяточного теста»: Неонатальный скрининг: описание основных заболеваний и тактики ведения больных детей
Автор: Корецкая Валентина Петровна, педиатр,
Для чего нужен неонатальный скрининг?
Врачи-неонатологи роддома больницы Вересаева рассказали, для чего нужен неонатальный скрининг, кому положен и когда проводится.
Неонатальный скрининг – важное обследование, позволяющее уже в первые дни жизни ребенка выявить серьезные врожденные патологии. Неофициально его называют «пяточным» тестом, поскольку кровь берется из пяточки и наносится на специальный тест-бланк.
Скрининг, который проводится в массовом порядке всем новорожденным, позволяет исключить такую пятерку серьезных заболеваний, как муковисцидоз (генетическая мутация, поражающая экзокринные железы органов дыхательной и пищеварительной систем); галактоземию (нарушение углеводного обмена), адреногенитальный синдром (нарушения, связанные с избыточной секрецией гормонов коры надпочечников), врожденный гипотиреоз (заболевание щитовидки) и фенилкетонурию (нарушение метаболизма аминокислот).
В Москве список расширен до 11 показателей, в него добавлена диагностика еще шести заболеваний из группы органических ацидурий, аминоацидопатий и нарушений обмена жирных кислот.
Все эти наследственно-генетические заболевания встречаются крайне редко, однако «поймать» их важно вовремя, поскольку их своевременное выявление позволяет избежать необратимых последствий и выбрать правильную тактику лечения.
Обычно скрининг делают в роддоме на четвертый день жизни младенца (для недоношенных малышей срок сдвигается), однако в Москве принята ранняя выписка: и мама с малышом (после естественных родов) могут оказаться дома уже на вторые сутки. Если тест не успеют провести в роддоме, то на руки родителям выдадут специальный бланк, где будет указана необходимость проведения скрининга. В таком случае анализ возьмет патронажная медсестра, которая придет навестить малыша в первые дни.
Анализ берут натощак после «голодной» паузы в три часа.
С февраля 2020 года расширенный неонатальный скрининг на 11 заболеваний доступен всем малышам, родившимся в Москве и получившим свидетельство о рождении в роддоме. Исследование проводится бесплатно.
Анализ готовится быстро. На связь с родителями специалисты выйдут только в случае, если какая-либо патология обнаружится. Однако большинство может забыть о тесте сразу после его выполнения, ведь частота встречаемости скринируемых заболеваний крайне мала.
Можно ли отказаться от неонатального скрининга?
Можно, но не стоит. Ведь именно в первые дни жизни малыша можно выстроить максимально эффективную схему лечения, которая в дальнейшем позволит ребенку избежать тяжелых осложнений и инвалидизации.
Неонатальный скрининг
Неонатальный скрининг, ласково именуемый в нашей стране «пяточка», является одним из первых важных исследований новорожденного. В России скрининг преимущественно направлен на выявление пяти наследственных болезней обмена: фенилкетонурии, врожденного гипотиреоза, врожденной дисфункции коры надпочечников (ВДКН), галактоземии и муковисцидоза. За рубежом этот список расширен до 50 различных заболеваний, в некоторых штатах Америки их свыше 60. Здоровый доношенный новорожденный допускается к скринингу на 4–5 сутки, недоношенный — на седьмой день после рождения. Заболевания, на выявление которых направлен скрининг, никак не проявляют себя в периоде новорожденности, но их ранняя диагностика и своевременно начатое патогенетическое лечение существенно влияют на прогноз и качество жизни ребенка. Помимо исследования крови проводится аудиометрия для оценки слуха и пульсоксиметрия для скрининга пороков сердца, но в данной статье мы преимущественно сосредоточимся на тестировании крови.
Разработка программы скрининга началась в шестидесятых годах прошлого века, когда Роберт Гатри создал технологию тестирования сухих отпечатков крови на фильтровальной бумаге. Первым заболеванием, которое стало кандидатом для массовой диагностики, была фенилкетонурия, так как ее раннее выявление и коррекция питания способны предотвратить развитие тяжелых неврологических нарушений. Затем к скринингу добавилось еще несколько заболеваний: врожденный гипотиреоз, ВДКН, галактоземия и муковисцидоз. Тандемная масс-спектрометрия (ТМС) позволила значительно расширить список заболеваний, добавив к болезням обмена веществ гемоглобинопатии, спинальную мышечную атрофию, тяжелый комбинированный иммунодефицит и др.
Таблица 1 | Рекомендуемая The American College of Obstetricians and Gynecologists (ACOG) скрининг-панель для врожденных заболеваний
В данной статье будут рассмотрены два скрининга, доступные в нашей стране: обязательный, включающий тестирование на пять заболеваний (врожденный гипотиреоз, ВДКН, фенилкетонурия, галактоземия, муковисцидоз) и расширенный скрининг на наследственные нарушения метаболизма.
Обязательный скрининг
На 4–5 сутки после рождения здорового доношенного ребенка или на седьмые сутки жизни недоношенного ребенка проводится тестирование методом «сухого пятна».
Фенилкетонурия (в современной классификации ― ФАГ-зависимая ФКУ) обусловлена мутацией гена фенилаланингидроксилазы и относится к числу аминокислотных аминоацидопатий. В норме фенилаланин (ФА) путем реакций гидроксилирования превращается в тирозин, однако в случае мутации вышеназванного гена активность превращающего фермента снижается, создается дефицит тирозина одновременно с избытком ФА, образующего токсичные метаболиты (фенилацетат, фенилпируват, фениллактат). Снижение образования тирозина влечет за собой нарушение синтеза гормонов щитовидной железы, нейротрансмиттеров и пигментов меланоцитов, а избыток ФА приводит к дисбалансу аминокислот в тканях мозга, обусловленному торможением их всасывания в желудочно-кишечном тракте или нарушением реабсорбции из почечных канальцев, нарушению образования или стабилизации полирибосом, снижению синтеза миелина, норадреналина и серотонина. Также за счет конкурентного ингибирования создается дефицит тирозиназы, что в совокупности с дефицитом тирозина приводит к снижению образования меланина и гипопигментации.
Основной проблемой пациентов с ФКУ являются нарушения функции ЦНС: от сонливости, вялости, отсутствия аппетита в период манифестации в 2–6 месяцев до тяжелых нарушений психомоторного развития в будущем; нередко развиваются атаксия, гиперкинезы, тремор рук, парезы по центральному типу. Единственный способ предотвратить развитие вышеназванных нарушений — назначение гипофенилаланиновой диеты с момента рождения с поддержанием низкого уровня фенилаланина в течение всей жизни.
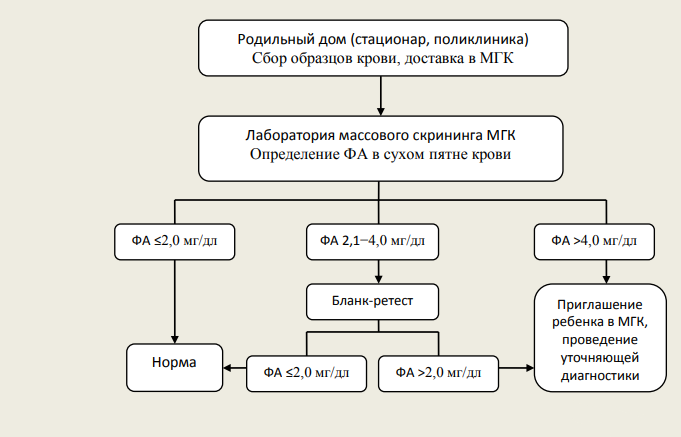
Рисунок 1 | Интерпретация результатов исследования на наличие фенилкетонурии
ВДКН обусловлена дефицитом ферментов и транспортных белков, участвующих в биосинтезе кортизола. Наиболее часто встречается дефицит 21-гидроксилазы, что в свою очередь приводит к дефициту кортизола и альдостерона и ответному увеличению секреции АКТГ и гиперплазии коры надпочечников. В условиях дефицита фермента происходит значительное накопление предшественников гормонов, что приводит к увеличению синтеза тестостерона, не зависящего от 21-гидроксилазы. В итоге у пациента формируется надпочечниковая недостаточность и гиперандрогения. Гормональным маркером дефицита 21-гидроксилазы является уровень 17-гидроксипрогестерона (17-ОНП), определяемый в рамках неонатального скрининга. Результат трактуется как положительный, если при двукратном тестировании образца уровень 17-ОНП у доношенных новорожденных составляет ≥ 20 нг/мл. У недоношенных детей при заборе крови на 7–8 сутки после рождения скрининговый результат трактуется как положительный при следующих уровнях 17-ОНП: на сроке 23–32 недели гестации ― ≥ 65 нг/мл; на сроке 33–36 недель гестации ― ≥ 40 нг/мл.
Врожденный гипотиреоз в большинстве случаев вызван дефектами самой щитовидной железы (первичный гипотиреоз). Причины первичного врожденного гипотиреоза можно в широком смысле классифицировать как неспособность щитовидной железы нормально развиваться (дисгенезия) или неспособность структурно нормальной щитовидной железы производить нормальные количества гормона (дисгормоногенез). Дисгенезия щитовидной железы, охватывающая весь спектр агенеза, гипоплазии и эктопии, является наиболее частой причиной врожденного гипотиреоза. В то время как это заболевание остается наиболее частой причиной врожденного гипотиреоза, частота возникновения дисгормоногенеза за последние несколько десятилетий увеличилась. В то время как на дисгормоногенез приходится только 15 % врожденного гипотиреоза, диагностированного в первые дни скрининга новорожденных, у 30–40 % младенцев, прошедших скрининг по современным протоколам, имеется эктопическая щитовидная железа, соответствующая одной из форм дисгормоногенеза. В отличие от дисгенезии щитовидной железы, при которой моногенная причина присутствует только у небольшого количества пациентов, дисгормоногенез часто возникает из-за генетического дефекта на каком-либо этапе синтеза тиреоидных гормонов.
Учитывая разнообразие функций тиреоидных гормонов в организме человека, врожденный гипотиреоз характеризуется разнообразием клинических проявлений с поражением всех органов и систем. При отсутствии своевременного лечения на первый план выходит задержка психомоторного и речевого развития, затем наступают отставание в физическом развитии и задержка полового развития. Основной задачей скрининга является наиболее раннее выявление детей с подозрением на врожденный гипотиреоз.
Рисунок 2 | Интерпретация результатов исследования на наличие врожденного гипотиреоза
Галактоземия — аутосомно-рецессивное наследственное нарушение обмена углеводов, при котором в организме накапливается избыток галактозы и ее метаболитов. В норме галактоза образуется в результате гидролиза лактозы в кишечнике либо в процессе ферментных реакций, обмена гликопротеинов и гликолипидов. Галактоза является материалом для образования клеточных мембран, нервной ткани, нервных окончаний и т. д. В результате ферментных реакций она превращается в глюкозу, и именно дефицит галактозо-1-фосфатуридилтрансферазы лежит в основе патогенеза данного заболевания. Метаболиты галактозы обладают повреждающим действием. Так, галактитол проникает в хрусталик глаза, приводя к повышению осмотического давления, электролитным нарушениям и денатурации белка с формированием катаракты. Другие метаболиты обладают гепато-, нейро- и нефротоксическим действиями, а также вызывают гемолиз эритроцитов. Тормозящее влияние метаболитов галактозы на углеводный обмен приводит к гипогликемии.
Рисунок 3 | Интерпретация результатов исследования на наличие галактоземии
Муковисцидоз — аутосомно-рецессивное заболевание, связанное с мутацией гена МВТР (трансмембранного регулятора муковисцидоза). МВТР является хлорным каналом, мутации гена которого нарушают не только транспорт, но и секрецию ионов хлора. При затруднении их прохождения через клеточную мембрану увеличивается реабсорбция натрия железистыми клетками, нарушается электрический потенциал просвета, что вызывает изменение электролитного состава и дегидратацию секрета желез внешней секреции. В результате выделяемый секрет становится чрезмерно густым и вязким. Поражаются все экзокринные железы организма: печень, поджелудочная железа, мочеполовая система, но наиболее ярко муковисцидоз проявляет себя со стороны органов дыхания, провоцируя бронхообструкцию, дыхательную и сердечную недостаточность, легочную гипертензию.
Рисунок 4 | Интерпретация результатов исследования на наличие муковисцидоза
Расширенный скрининг
Органические ацидемии — группа аутосомно-рецессивных наследственных заболеваний обмена, в основе патогенеза которых лежит дефицит ферментов, участвующих в метаболизме белков, что приводит к повышению уровня кетоновых тел, обладающих токсическим действием на различные органы и ткани, в частности, на ЦНС. Данные заболевания манифестируют уже в стадии декомпенсации, как правило, в период с первой недели до первого года жизни. Триггерами служат стресс, длительное голодание, инфекционные заболевания, иммунизация, реже — чрезмерное употребление белковой пищи. Проявляются преимущественно неврологической симптоматикой: нарушение сознания вплоть до комы, эпилептические приступы, нарушение мышечного тонуса, у детей старшего возраста — нарушения психоречевого развития, атаксия, очаговые неврологические симптомы, синдром Рейе (острая печеночная недостаточность, сочетающаяся с энцефалопатией), психические расстройства.
Нарушения окисления жирных кислот — врожденный дефект метаболизма из-за нарушения либо митохондриального β-окисления, либо транспорта жирных кислот с использованием карнитинового транспортного пути. Проявления зависят от нарушения метаболизма конкретной кислоты, но все они имеют общие черты и требуют схожей тактики лечения. В периоде новорожденности метаболические нарушения проявляются тяжелой кардиомиопатией, гипокетотической гипогликемией, дисфункцией печени в первые несколько дней или недель жизни, часто заканчиваясь летально. В младенческом и детском возрасте характерны эпизоды летаргии и рвоты, развивается дисфункция печени и гипокетотическая гипогликемия, энцефалопатия, что может привести к внезапной младенческой смерти. У подростков и во взрослом возрасте дебютируют эпизодическим рабдомиолизом, мышечной слабостью, миалгией. Лечение включает отказ от голодания, симптоматическую терапию развившихся осложнений и включение в рацион добавок, если это необходимо.
Аминоацидопатии
Болезнь кленового сиропа (она же лейциноз) — наследственное заболевание, обусловленное дефицитом дегидрогеназы кетокислот с разветвленной цепью и нарушением метаболизма лейцина, изолейцина, валина (аминокислоты с разветвленной цепью, АКЦР). Повышение уровня АКЦР и их метаболитов, в частности, кетокислот, приводит к кетоацидозу, атрофии ткани головного мозга, нарушению окислительного фосфорилирования в дыхательной цепи митохондрий. Избыток лейцина обладает нейротоксическим эффектом, вызывая дисфункцию астроцитов, апоптоз нейронов и блокируя транспорт через гематоэнцефалический барьер аминокислот, важных для синтеза нейротрансмиттеров.
Гомоцистеинурия — наследственное заболевание из группы аминоацидопатий, обусловленное нарушением метаболизма серосодержащих аминокислот, в частности, метионина. Дефицит цистатион-b-синтазы нарушает преобразование метионина в цистеин. Высокий уровень гомоцистеина связан с образованием некротически-дегенеративных участков в почках, селезенке, слизистой оболочке желудка и сосудах, активацией XII фактора свертывания, способствующего тромбообразованию.
Тирозинемия 1 типа — заболевание, обусловленное дефицитом фумарилацетоацетатгидролазы, в результате чего происходит накопление высокотоксичных фумарил- и малеилацетоацетата, обладающих гепатотоксическим и канцерогенным действием. Конечные метаболиты — сукцинилацетон и сукцинилацетоацетат — являются митохондриальными токсинами, тормозящими фосфорилирование и блокирующими цикл Кребса. Накопление токсинов приводит к прогрессирующему заболеванию печени с развитием печеночной недостаточности, цирроза, тубулопатии с формированием ренальной тубулопатии, гипофосфатемического рахита, синдрома Фанкони. Острая тирозинемия сопровождается развитием гипертрофической кардиомиопатии. Кроме того, нарушается путь синтеза порфирина, ингибируется синтез порфобилиногена, что приводит к кризам, проявление которых напоминает порфирию. Все пациенты подвержены высокому риску развития гепатоцеллюлярной карциномы, вторичной по отношению к циррозу. Без своевременного лечения дети погибают в возрасте 10 лет.
Скрининг новорожденным из пятки стандартный на 5 наследственных заболеваний и расширенный, 43 показателя
В детском медицинском центре «Санаре» проводится неонатальный скрининг на базе лаборатории Морозовской детской городской клинической больницы.
Суть скрининга в том, что выявляются достаточно часто встречающиеся в популяции заболевания, успех лечения которых целиком и полностью зависит от раннего начала терапии. В терапии этих состояний определяющую роль играет именно время и грамотный подход.
Согласно Приказу № 185 Минздравсоцразвития РФ от 22.03.2006 «О массовом обследовании новорожденных детей на наследственные заболевания», скрининг новорожденных проводится на 5 наследственных заболеваний:
Процедура забора крови для неонатального скрининга
Образец крови у новорожденного ребенка берется таким же способом, как для неонатального скрининга на фенилкетонурию, галактоземию, гипотиреоз, адреногенитальный синдром и муковисцидоз.
Исследование можно провести и для детей старшего возраста!
Если забор крови производится у ребенка старше 1 года, то кровь для проведения исследования берется из пальца.
Для новорожденного ребенка можно использовать пятна крови, которые были взяты для неонатального скрининга, у ребенка старшего возраста забор производится на специальный индивидуальный бланк-фильтр.
Неонатальный скрининг новорожденных: анализ, который спасает жизнь
В Московском центре неонатального скрининга, функционирующем в Морозовской детской больнице, ежегодно более 100 000 новорожденных проходят диагностику на тяжелые наследственные заболевания.
Исследование включает в себя тестирование 11 врожденных болезней: муковисцидоз, галактоземия, врожденная дисфункция коры надпочечников, врожденный гипотиреоз, фенилкетонурия, глутаровая ацидурия тип 1, тирозинемия тип 1, лейциноз, метилмалоновая/пропионовая ацидурия, недостаточность биотинидазы, недостаточность среднецепочечной ацилКоА дегидрогеназы жирных кислот.
«Отсутствие родственников с врожденной и наследственной патологией, к сожалению, не является гарантом рождения здорового ребенка, поэтому важно, чтобы родители не отказывались от проведения исследований. Наследственные заболевания представляют серьезную угрозу для здоровья и жизни детей. Благодаря ранней диагностике и вовремя начатому лечению малышу можно помочь справиться с тяжелыми проявлениями недуга. Наиболее ранний способ диагностики врожденных нарушений обмена веществ — неонатальный скрининг новорожденных. Он позволяет выявить опасную болезнь до появления симптомов, тем самым предотвратив развитие угрожающих жизни осложнений», — отметила заведующий медико-генетическим отделением Морозовской детской больницы, врач-генетик Татьяна Кекеева.
Как сообщила врач, анализ крови собирается у всех новорожденных в родильных домах города. Образцы крови из пяточки детей берут по истечении трех полных суток с момента рождения и направляют на исследование в Московский центр неонатального скрининга.
«Если признаков заболеваний не выявлено, результаты анализов не направляются ни в роддом, ни родителям новорожденного. Если выявлено повышение определенных показателей, ребенку показан немедленный повторный анализ. В случае выявления превышения показателей и в повторном анализе, наши сотрудники связываются с медицинским учреждением или с родителями малыша и приглашают их пройти уточняющую диагностику», — рассказала Татьяна Кекеева.
При подтверждении диагноза ребенок с наследственным заболеванием наблюдается у врача специалиста Морозовской больницы до 18 лет. Пациентам назначаются специализированные лекарственные препараты и лечебное питание, выписываются льготные рецепты.
Московский центр неонатального скрининга работает более пяти лет. Здесь анализируются данные обо всех родившихся в Москве детях с наследственными болезнями обмена, что позволяет оперативно выявить заболевание и своевременно назначить терапию.
Кроме того, специалисты центра консультируют детей в случае подозрения на другую моногенную патологию, хромосомные нарушения и проводят семейные консультации при подготовке к беременности и во время беременности (оценка рисков развития заболеваний у плода).