Вирус гепатита С, РНК HCV генотипирование (типы 1а, 1b, 2, 3, 4)
Описание
Вирус гепатита С, HCV ПЦР real-time генотипирование (типы 1а, 1b, 2, 3, 4) — определение вируса гепатита С в сыворотке крови и определение генотипов ВГС 1а, 1b, 2, 3, 4 методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени».
Метод ПЦР — позволяет идентифицировать в биологическом материале искомый участок генетического материала и обнаружить единичные молекулы ДНК вируса, не выявляемые другими методами. Принцип метода основан на многократном увеличении числа копий, специфичного для данного возбудителя участка ДНК.
С помощью ПЦР-анализа можно диагностировать инфекцию в остром периоде и выявлять случаи носительства.
Вирус гепатита С
Исследование позволяет выявить присутствие РНК вируса гепатита С (субтипы 1a, 1b, 2a, 2b, 2c, 2i, 3) и идентифицировать генотипы 1a, 1b, 2, 3 (субтипы a/b).
Вирус гепатита С (ВГС) поражает клетки печени, а также некоторые клетки крови (нейтрофилы, моноциты, В-лимфоциты).
Вирус гепатита С подразделяют на 6 генотипов, каждый из которых, в свою очередь подразделяется на субтипы. Генотипы 1, 2 и 3 являются самыми распространенными в мире. В Российской Федерации чаще распространен генотип 1b, чем 1a, далее с убывающей частотой — 3, 1a, 2.
Генотипирование вируса гепатита С
Генотип вируса гепатита С является наиболее важным фактором, от которого зависит эффективность и тактика противовирусного лечения хронического гепатита С. Знание генотипа вируса используется для планирования продолжительности курса лечения, что особенно важно, учитывая широкий спектр побочных действий применяемых препаратов интерферона и плохую переносимость терапии многими пациентами. Генотипирование вируса гепатита C должно выполняться всем пациентам до начала противовирусной терапии, в целях планирования ее продолжительности, прогнозирования эффективности, в отдельных случаях — для расчета дозы противовирусных препаратов.
Основной путь передачи вируса гепатита С — кровь (препараты для переливания элементов крови и плазмы, донорские органы, нестерильные шприцы, иглы, инструменты), реже — заражение половым путём.
Острый вирусный гепатит
Острый вирусный гепатит, как правило, протекает бессимптомно и в большинстве случаев остаётся невыявленным. У 60–85 % инфицированных развивается хроническая инфекция, которая увеличивает риск развития цирроза, печёночной недостаточности и гепатоцеллюлярной карциномы.
Лечение при различных генотипах вируса гепатита С
Генотип 1 хуже поддаётся лечению, чем генотипы 2 и 3. Кроме того, биопсию печени важнее провести именно при генотипе 1. Повышенные дозы препаратов интерферона рекомендованы для пациентов с 1-м и 4-м генотипами. Курс терапии у таких пациентов должен быть продлён до 48 недель даже при отсутствии вируса в крови более 24 недель. В случае успешности лечения, которая подтверждается снижением вирусной нагрузки крови (
ПЦР-диагностика Ковид-19
Пандемия коронавируса, охватившая весь мир, считается наиболее масштабной и опасной за всю историю человечества. Согласно последним данным, на начало декабря 2021 года общее число заболевших превышает 270 миллиона человек, из числа которых свыше 5,3 млн. погибших.
Врачи по всему миру прикладывают максимум усилий, направленных на предотвращение распространения инфекции, а также сокращение смертности среди населения.
Для наилучшей эффективности противоэпидемических мероприятий важно подобрать наиболее экономную и информативную систему тестирования, именно такой является ПЦР-диагностика.
Посредством выделения РНК вируса возможно обнаружить возбудитель в организме человека даже при его минимальной концентрации. Благодаря этому удается начать лечение заблаговременно, предотвратив прогрессирование Ковид-19 до тяжелых форм или убедиться в том, что человек полностью здоров. Сегодня такая возможность имеется и у пациентов нашей клиники.
Принцип проведения ПЦР-диагностики на Ковид-19
ПЦР или полимеразная цепная реакция – современный метод лабораторных исследований, который позволяет с предельной точностью выявлять различные инфекции в организме человека, включая Ковид-19. Результаты анализа максимально точны, исключается даже вариант ложноположительного теста. Однако в отношении COVID-19, в силу новизны и недостаточной изученности вируса, точность ПЦР-диагностики составляла в начале эпидемии порядка 80%. На сегодняшний день точность ПЦР-теста составляет 99.6%.
Суть метода заключается в обнаружении молекул РНК вируса во взятом биологическом материале. В отношении диагностики коронавируса исследуемым биоматериалом становится мазок слизистой ротоглотки и носоглотки.
Особое внимание при этом уделяется именно РНК SARS-CoV-2, то есть рибонуклеиновой кислоте, являющейся носителем генетической информации вируса. Но даже если при первом исследовании РНК вируса не выявлены, подозрения все же могут оставаться (что не связано с возможной погрешностью).
Как известно, инкубационный период в случае Ковид-19 составляет 14 дней, по этой причине полностью исключить болезнь удается после проведения повторной диагностики. При этом все же стоит отметить главное преимущество ПЦР-тестов – это один из самых точных и чувствительных методов диагностики инфекционных заболеваний. Это значит, что проведение даже единичного исследования с высокой долей вероятности даст точный результат и позволит определить, болен ли человек на момент забора биоматериала.
Специфика анализа РНК SARS-CoV-2 (КОВИД, COVID-19)
Анализ на РНК SARS-CoV-2 (КОВИД, COVID-19) можно назвать стандартный ПЦР-тест на коронавирус. В данном случае выполнение исследования занимает 1 день с момента забора биоматериала. В случае положительного результата исследования человек считается инфицированным. Если же РНК коронавируса не выявлена, тест отрицателен, можно с уверенностью говорить о том, что человек не является носителем вируса.
Специфика анализа РНК SARS-CoV-2 (КОВИД, COVID-19) (CITO)
РНК SARS-CoV-2 (КОВИД, COVID-19) (CITO) – схожее по принципу забора биоматериала и методу проведения исследование. Разница заключается лишь в скорости, припиской «CITO» обозначается экспресс-тест, который, в отличие от стандартного метода исследования, проводится в течение нескольких часов. Несмотря на то, что результат будет готов уже спустя 3-4 часа, это не влияет на показатели точности, но такой вариант диагностики обходится дороже.
Особенности забора биоматериала
Процесс забора биоматериала – важнейший этап в ПЦР-диагностике. Крайне важно получить чистый образец, ведь от этого зависит точность и результативность исследования. К счастью, для проведения ПЦР-тестов на Ковид процесс взятия мазка из носоглотки и ротоглотки предельно прост и не требует предварительной подготовки со стороны пациента:
Экспресс-тест NowCheck COVID-19 AG – набор исследований для максимально быстрой и простой диагностики новой коронавирусной инфекции. Тест позволяет выявить антигены COVID-19 в слизи из носоглотки методом ИХА (иммунохроматографии). По точности и достоверности он приближен к анализу ПЦР, но в отличие от него не требует специальных условий и оборудования.
Тест зарегистрирован в реестре медицинских изделий и имеет медицинское регистрационное удостоверение РФ. Метод, который лежит в основе исследования, получил одобрение Министерства здравоохранения России.
Диагностика занимает в среднем 15-30 минут, что позволяет максимально быстро заподозрить коронавирусную инфекцию и принять решение о госпитализации.
Показания к проведению исследования
ПЦР-диагностика коронавируса с предельно высокой на сегодняшний день точностью позволяет получить ответ на конкретный вопрос – болеет ли человек коронавирусом в данным момент. Это исследование не позволяет узнать, переболели вы ранее или нет.
Таким образом, учитывая текущие карантинные меры во многих странах, данный метод диагностики особенно актуален для людей, которые собираются поехать за границу или возвращаются домой.
В таких реалиях показаниями к проведению ПЦР теста являются:
Сертификация
Лаборатория, проводящая данное исследование обладает всеми необходимыми сертификатами для проведения ПЦР-диагностики на COVID-19 (коронавирус). Лабораторные исследования проводятся согласно международным стандартам на современном диагностическом оборудовании.
Заключение о проведенном исследовании выдается пациенту на специальном бланке с печатями, подтверждающими действительность документа.
Данная страница не существует!
Услуги инфекционной клиники
Диагностика, профилактика и лечение
Фиброэластометрия и УЗ-диагностика молочных желез, щитовидной железы, мошонки, брюшной полости
Биохимия. Анализ крови: общий, клинический. Анализы на витамины, микроэлементы и электролиты. Анализ на ВИЧ-инфекцию, вирусные гепатиты, бактерии, грибки и паразиты
Максимально точное определение выраженности фиброза печени неинвазивным методом при помощи аппарата FibroScan 502 TOUCH
Гинеколог в H-Сlinic решает широчайший спектр задач в области женского здоровья. Это специалист, которому вы можете полностью доверять
Дерматовенерология в H-Сlinic — это самые современные и эффективные алгоритмы диагностики и лечения заболеваний, передающихся половым путем, грибковых и вирусных поражений, а также удаление доброкачественных невусов, бородавок, кондилом и папиллом
Возможности вакцинопрофилактики гораздо шире Национального календаря прививок. H-Clinic предлагает разработку плана вакцинации и современные высококачественные вакцины в наличии
Терапевт в H-Сlinic эффективно решает задачи по лечению заболеваний, которые зачастую могут становиться большой проблемой при наличии хронического инфекционного заболевания
Врач-кардиолог H-Сlinic проведет комплексную диагностику сердечно-сосудистой системы и при необходимости назначит эффективное терапию. Сердечно-сосудистые проблемы при инфекционных заболеваниях, требуют специфичных подходов, которые мы в состоянии обеспечить
Наша цель — новое качество вашей жизни. Мы используем современные диагностические алгоритмы и строго следуем наиболее эффективным протоколам лечения.
Общая терапия, Инфекционные заболевания, Гастроэнтерология, Дерматовенерология, Гинекология, Вакцинация, УЗИ и фиброэластометрия, Кардиология, Неврология
Биохимия, Общий/клинический анализ крови, Витамины и микроэлементы/электролиты крови, ВИЧ-инфекция, Вирусные гепатиты, Другие инфекции, бактерии, грибки и паразиты, Комплексы и пакеты анализов со скидкой
В наличии и под заказ качественные бюджетные решения и препараты лидеров рынка лечения инфекционных болезней. Аптека H-Clinic готова гибко реагировать на запросы наших клиентов. Мы поможем с оперативным поиском препаратов, которые обычно отсутствуют в сетях.
Не детектируется что это рнк
Своевременная и качественная диагностика – один из ключевых факторов в борьбе с COVID-19: диагностика необходима и для оценки общей эпидемиологической ситуации, и в случае принятия решения по каждому конкретному пациенту. По данным сайта стопкоронавирус.рф на 12.05.2020 г. проведено более более 5,8 миллионов тестов на наличие нового коронавируса. Цифра огромная. Однако, насколько достоверны результаты? Появляется все больше историй о типичной картине COVID-19 при отрицательных анализах. Почему так может происходить?
Сначала поговорим о ПЦР-тестах, которые специфически выявляют РНК вируса в пробах.
Взятие пробы для ПЦР
Показано, что для выявления нового коронавируса подходят смывы из носоглотки – из ротоглотки вероятность ложноотрицательного анализа немного выше [ 1 ]. Один из важнейших аспектов – время взятия материала. Проведенные исследования показывают, что при взятии материала у больного в первый день проявления симптомов COVID-19 положительный диагноз поставят с вероятностью 94 %, а вот к 10-му дню это будет всего лишь 67 %! [ 2 ].
Существует четкая закономерность: чем позже от возникновения симптомов взят материал, тем меньше шансов обнаружить в нем вирусную РНК.
Есть и хорошие новости: в течение первой недели от возникновения симптомов носоглоточные смывы имеют порядок от 100 000 до 1 000 000 копий вирусной РНК в 1 мл, что делает их легко обнаруживаемыми даже не самыми чувствительными системами. Исследования также показали, что вирусная нагрузка в верхних дыхательных путях может быть одинаковой у людей с проявленной симптоматикой и при бессимптомном течении болезни [ 3 ].
Транспортировка и хранение проб для ПЦР
Точность разных ПЦР-тест-систем
После попадания образцов в лабораторию правильность диагноза будет зависеть во многом от тест-системы, которую там используют. На сегодняшний день помимо двух тест-систем, разработанных еще в январе в ГНЦВБ «Вектор», зарегистрировано 8 ПЦР-тест систем [ 5 ]:
Из них системы «Вектора» и «Вектор-Беста» (последняя через сеть лабораторий «Инвитро» [ 6 ]) используются для исследования проб от государственных медицинских организаций. Здесь хочется отметить, что система «Вектора» не содержит в своем составе внутреннего контрольного образца, который должен добавляться во все пробы для контроля правильности выделения РНК и реакции обратной транскрипции [ 7 ]. Отсутствие такого контроля может также потенциально приводить к некоторому количеству ложноотрицательных результатов. Хорошая новость заключается в том, что остальные зарегистрированные тест-системы имеют в своем составе внутренний контроль, а также, по-видимому, обладают более высокой чувствительностью, т.е. дают меньше ложноотрицательных результатов.
Таким образом, в городах, где представлены сетевые лаборатории, есть возможность сдать анализ частным образом и надеяться на точность проведения процедуры. В первые дни появления симптоматики точность будет выше.
Экспресс-системы
Что касается экспресс-тест-систем, то есть опасения, что созданные в сжатые сроки «уникальные» тесты по своему качеству будут уступать системам, основанным на обычной ПЦР. Насколько надежны эти системы покажет время, однако уже сейчас количество ложноотрицательных результатов ПЦР в совокупности с длительностью ожидания результата привело к тому, что в клиниках страны диагноз стали ставить не на основе ПЦР-анализа, а на основе результатов компьютерной томографии (КТ).
КТ
Преимущество КТ-диагностики при наличии клинической картины – это скорость постановки диагноза и более высокая чувствительность по сравнению с реальностью ПЦР-диагностики: 97,2 % против 83,3 % согласно данным небольшого китайского исследования [ 12 ]. Начиная с 4-5 дня заболевания можно различить так называемый симптом «матового стекла», на стадии прогрессирования такие участки консолидируются, возникает симптом «булыжной мостовой», «обратного ореола», а в пиковая стадии – «белое легкое» [ 13 ]. Возникает закономерный вопрос: отличается ли картина пневмонии, вызванной именно новым коронавирусом, от заболеваний другой вирусной природы. Ответ – нет. Вирусные пневмонии, будь то аденовирус, грипп или другие респираторные вирусы, выглядят на КТ одинаково.
Однако в условиях пандемии, когда подавляющее большинство вирусных пневмоний имеют коронавирусную природу, использование КТ для диагностики становится более чем оправданным. В последней версии методических рекомендаций Минздрава по профилактике, диагностике и лечению COVID-19 указано, что «наличие клинических проявлений в сочетании с характерными изменениями в легких по данным КТ или обзорной рентгенографии органов грудной клетки вне зависимости от результатов однократного лабораторного исследования на наличие РНК SARS-CoV-2 и эпидемиологического анамнеза» является клинически подтвержденным случаем COVID-19 [ 14 ]. Отметим также, что объем поражения легких при РГ и КТ может не иметь прямой корреляции с клинической тяжестью заболевания.
ИФА (иммуноферментный анализ)
ПЦР-тест-системы, как и КТ-диагностика выявляет COVID-19 в острой фазе. Однако весьма актуальна и информация об уже переболевших, на основании которой можно судить об охвате населения заболеванием, а также о числе бессимптомных случаев. Ответы на эти, а также на многие другие вопросы, может дать тест-система на антитела. На сегодняшний день разработкой таких тест-систем помимо «Вектора» занимаются такие организации как «Вектор-Бест», «НПО «Диагностические системы», ФНКЦ ФХМ ФМБА России, «МБС-Технологии», а также «Генетико» и Институт молекулярной биологии РАН [5]. К сожалению, тест-системы на антитела требуют намного больших усилий и времени на разработку, чем ПЦР-системы, а их чувствительность и специфичность оставляет желать лучшего. Так, проведенное в США исследование доступных система на антитела показало, что лишь 3 из 14 систем дают надежные результаты (т.е. не более 1% ложноположительных результатов), но при этом их чувствительность не превышает 90% относительно положительных контрольных образцов [ 15 ]. Какова будет чувствительность и специфичность разрабатываемых российских систем – пока неизвестно.
Итак, самое разумное, что вы можете сказать клиентам:
Регистрируйся на нашем сайте и получай доступ ко в сем материалам о COVID-19 в специальном разделе.
Отвечаем на вопросы в прямых эфирах Вконтакте: https://vk.com/pharmznanie
Обсудить последние новости со всеми коллегами России вы можете в чатах:
Двуликие геномы! Что такое амбисенсные вирусные РНК?
Двусмысленные вирусные геномы содержат участки как положительной, так и отрицательной «полярности»
здесь и далее рисунки Андрея Занкевича
Автор
Редактор
Статья на конкурс «Био/Мол/Текст»: Некоторые РНК-вирусы человека, животных и растений демонстрируют чудеса организации структуры генома, который, хотя и представлен одноцепочечной молекулой РНК, кодирует две трансляционные рамки, направленные в разные стороны. Что это за вирусы, и как им это удаётся? Давайте попробуем разобраться.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Напомним, что РНК (рибонуклеиновая кислота) — это такая молекула, представляющая собой одну цепочку нуклеотидов. В составе каждого нуклеотида присутствует остаток моносахарида рибозы. На сегодняшний день известно множество разных типов РНК, которые выполняют совершенно разные функции: от кодирования клеточных белков (мРНК) до противовирусной защиты (некоторые микроРНК) [1–5]. РНК, входящие в состав многих вирусов, могут иметь ряд оригинальных функций, таких как регуляция времени экспрессии различных вирусных генов путем изменения пространственной организации цепи РНК или привлечение клеточных белковых комплексов.
Биологи привыкли думать об РНК главным образом как о «молекуле-посреднике» между ДНК и белком. Именно молекулы матричной РНК (мРНК) распознаются рибосомами — молекулярными машинками, расшифровывающими последовательность РНК в процессе синтеза белка. мРНК имеют в своем составе кодирующие последовательности и, как правило, некодирующие области на 5′- и 3′-концах. Для мРНК эукариот характерно наличие особой кэп-структуры (которая узнается рибосомой) на 5′-конце и полиаденозиновой последовательности на 3′-конце («ключик» для выхода из ядра, вдобавок повышающий стабильность такой мРНК). мРНК называют РНК положительной полярности, или (+)РНК, то есть РНК, с которой не нужно проводить никаких дополнительных операций — у нее есть всё, что нужно для «посадки» рибосомы и последующей трансляции! У некоторых вирусов встречаются молекулы РНК отрицательной полярности, или (–)РНК, несущие комплементарные кодирующим последовательностям участки. В таком случае для образования вирусной мРНК необходима эта самая (–)РНК, а также вирусный фермент, осуществляющий матричный синтез комплементарной РНК-цепи.
Но бывает ли такое, что в пределах одной молекулы РНК одна ее часть, кодирующая некоторый белковый продукт, имеет положительную полярность, в то время как другая часть цепи представлена участком отрицательной полярности, кодирующим другой белок? Могла ли такая молекула возникнуть в процессе эволюции живых форм?
Ответ — да! И для того, чтобы разобраться, как функционируют такие молекулы, нам предстоит погрузиться в таинственный мир вирусов.
Давным-давно, в далекой-далекой галактике.
Сегодня очень популярна гипотеза «РНК-мира» [6], указывающая на РНК как на главного кандидата в прародители жизни на нашей планете. Поскольку РНК может как кодировать информацию, так и проявлять иногда каталитическую (рибозимную) активность (то есть специфически ускорять протекание определенных химических реакций), молекулы РНК, включающие обе эти функции, вполне могли бы являться первыми объектами живой природы, так как при наличии субстрата они способны реплицировать сами себя.
Как известно, все формы жизни обладают определенной наследственностью, которая определяет степень генетической идентичности живых объектов. В качестве молекул, ответственных за поддержание такой наследственной идентичности, выступают нуклеиновые кислоты (ДНК и РНК). Клеточные формы жизни для хранения и передачи информации используют только один тип нуклеиновых кислот — дезоксирибонуклеиновую кислоту (ДНК), в то время как вирусы в качестве основной молекулы наследственности могут использовать либо ДНК, либо РНК.
В случае ДНК-содержащих вирусов реализуется, как правило, Центральная догма молекулярной биологии в классическом виде: попав в клетку, ДНК удваивается в процессе репликации вирусного генома, на матрице ДНК в ходе транскрипции синтезируются мРНК, которые затем прочитываются рибосомой, синтезирующей по ним вирусные белки, то есть осуществляется трансляция. Далее вирусные белки ассоциируются с ДНК-геномом вируса в вирусную частицу (вирион), которая способна заражать новые клетки.
Очевидно, что РНК-содержащие вирусы используют иные стратегии размножения и, следовательно, реализации своего генома. Непривычные для большинства биологов молекулярные механизмы, которые используются такими вирусами, вероятно, унаследованы от далеких предков из того самого РНК-мира.
Размножение РНК-вирусов подразумевает использование разных типов РНК:
Немного истории
Первым найденным РНК-вирусом стал бактериофаг f2, инфицирующий бактерию кишечную палочку (Escherichia coli) [7]. Выделенная геномная РНК фага f2 имела свойства мРНК, то есть она распознавалась рибосомой и могла транслироваться. На родственном РНК-бактериофаге Qβ была изучена РНК-зависимая РНК-полимераза (RdRp), которая, как оказалось, может синтезировать цепь РНК на матрице другой цепи РНК, то есть осуществлять репликацию вирусного РНК-генома! В ходе работы с РНК-бактериофагами f2 и его родственником Qβ были получены общие представления о биологии таких РНК-вирусов [8].
РНК, способную распознаваться рибосомой с осуществлением синтеза белка, назвали «(+)РНК». Эта РНК, попав в клетку-хозяина, может сразу использоваться в качестве мРНК для синтеза вирусных белков. У многих вирусов такая (+)РНК инфекционна сама по себе, т. к. кодирует все нужные для полноценной вирусной инфекции белки, включая RdRp, осуществляющую репликацию генетического материала вируса.
После РНК-бактериофагов были найдены (+)РНК-вирусы животных, такие, как вирус полиомиелита [9], [10], представитель группы пикорнавирусов. Подобные вирусы не содержат репликативных белков в составе вирусной частицы (вириона).
Вирус везикулярного стоматита (VSV), как и вирус полиомиелита, был также одним из первых исследованных РНК-вирусов животных, однако в составе вириона нашли фермент RdRp, синтезирующий комплементарную (антигеномную) цепь РНК [11]. Антигеномная цепь является интермедиатом репликации и не участвует в трансляции. Матрицами для синтеза белка в данном случае выступают более короткие вирусные мРНК (субгеномные РНК), транскрибируемые с геномной цепи. Хотя антигеномная РНК не транслируется, ее последовательность совпадает с последовательностями мРНК, поэтому говорят, что она имеет ту же полярность — положительную. Итак, в рассматриваемом случае антигеномная и субгеномные цепи являются (+)РНК, а геномная РНК играет роль матрицы для синтеза (+)РНК и оттого называется «РНК противоположной полярности», то есть «(–)РНК». У (–)РНК-вирусов как раз такая РНК в качестве геномной упаковывается в вирион вместе с вирусной RdRp, которая ответственна за матричный синтез антигеномной и субгеномных (+)РНК после проникновения в клетку. Cреди (–)РНК вирусов выделяют вирусы с несегментированным геномом (вирион содержит одну молекулу (–)РНК, вместе с RdRp необходимую для инфекции; порядок Mononegavirales) и сегментированным геномом (для инфекции необходимо несколько разных молекул геномной РНК, каждая из которых связана со своей молекулой RdRp; порядок Articulavirales). Хорошо известный вирус гриппа А является представителем второй группы. Каждая (–)РНК (геномный сегмент), упакованная в вирусную частицу, «обёрнута» молекулами белка нуклеокапсида NP, в комплексе с которым образуется РНП (рибонуклеопротеин). Также в этот комплекс входит мультисубъединичная RdRp.
Встречаются вирусы, геном которых представлен двухцепочечной РНК. Как и в случае (–)РНК-вирусов, у дцРНК-вирусов во время репликации в клетке первым делом происходит синтез (+)цепи. Вирусные частицы этой группы также включают в свой состав RdRp.
Наша статья посвящена очень занятной группе вирусов, имеющих «двусмысленный РНК-геном». Сегментированная природа генома роднит их с представителями порядка Articulavirales, однако, в отличие от последних, один или два РНК-сегмента являются «(±)РНК». Такие РНК называют амбисенсными: это значит, что в пределах одной молекулы РНК есть последовательности, по смыслу соответствующие мРНК ((+)участки), а также участки отрицательной полярности ((–)участки), то есть комплементарные мРНК. Согласно таксономии, вирусы с двусмысленным РНК-геномом определяют в семейства Bunyaviridae и Arenaviridae.
Исторически одним из первых выделенных вирусов с двусмысленной РНК был флебовирус — вирус лихорадки долины Рифт (RVFV) [12]. Открытие амбисенсной природы РНК некоторых вирусов [13], [14] пришлось на период, когда были достаточно хорошо исследованы (+)- и (–)РНК-содержащие вирусы, что и позволило предположить возможность «двусмысленной» молекулы РНК в составе таких вирусов.
Вирусы с двусмысленным РНК-геномом из семейства Bunyaviridae
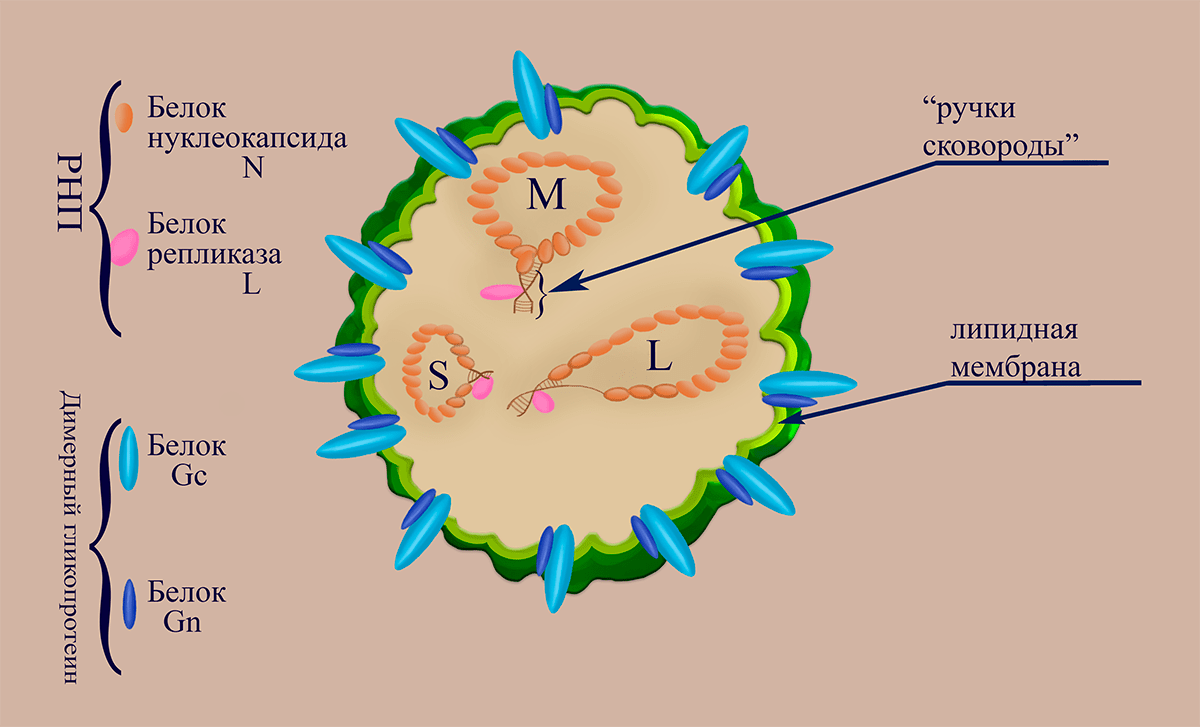
Вирусные частицы (вирионы) Bunyaviridae диаметром от 80 до 130 нанометров могут иметь изменчивую (плеоморфную) форму. Липопротеидная оболочка, образованная фосфолипидной мембраной и вирусными гликопротеинами Gn и Gc, содержит внутри три нуклеокапсида (рибонуклеопротеина, состоящих из молекулы РНК (сегмента), «одетой» в молекулы белка нуклеокапсида N, и ассоциированной с ней одной молекулы репликазы L (RdRp)). Три сегмента РНК-генома, несущих на концах комплементарные участки (благодаря которым РНК «циклизуются» в вирионе), получили названия в соответствии с длинами их нуклеотидной последовательности: L (large,
7000 нуклеотидных остатков), M (medium,
3000 н.о.), S (small,
1000 н.о.) (рис. 1.). В семействе встречаются (–)РНК-вирусы (роды Orthobunyavirus, Hantavirus и Nairovirus), имеющие концептуальную схожесть молекулярной стратегии репликации с таковой, например, вируса гриппа. Однако вирусы семейства Bunyaviridae не имеют матриксного белка — широко распространенного типа полипротеинов, встречающегося у большинства липид-содержащих РНК-вирусов животных и человека.
Рисунок 1. Схематичное изображение структуры вириона флебовирусов
В семействе Bunyaviridae роды Phlebovirus, Tospovirus и Tenuivirus являются вирусами с двусмысленным РНК-геномом и, в отличие от остальных представителей семейства, имеют чуть более длинный S-сегмент генома (РНК S) (±)полярности. Род Tospovirus имеет вдобавок (+)участок на РНК M, который делает и эту РНК амбисенсной.
Флебовирусы
Вирусы рода Phlebovirus выделяют практически по всему миру и относят к нетаксономической группе арбовирусов, распространяющихся в членистоногих переносчиках и в позвоночных, на которых питаются переносчики. Члены этого рода переносятся кровососущими членистоногими. Инфекции не обходят стороной человека: вирусы сицилийской и неаполитанской москитных лихорадок широко распространены по территории Средиземноморья [15]. Среди симптомов таких инфекций — продолжительная сильная лихорадка, тошнота, рвота, диарея и головные боли. Вирус Тосканы, также переносимый москитами, обладает способностью проникать в нервную ткань и, вдобавок к вышеперечисленным симптомам, вызывает асептический менингит и менингоэнцефалит. Флебовирусы, переносимые клещами, например, вирус Бханджа, вирус тяжелой лихорадки с синдромом тромбоцитопении, или вирус Хартленд, вызывают серьезные вспышки инфекций среди людей [16].
Эти вирусы получили свое имя от латинского названия москитов (Phlebotominae), которые являются их основными переносчиками. Вирионы флебовирусов имеют диаметр 100-125 нанометров. Внутри вириона находятся три вирусных рибонуклеопротеина (вРНП), содержащих геномные сегменты, однако для вируса лихорадки долины Рифт (RVFV) было показано [17], что вирионы также могут содержать ещё три дополнительных вРНП, образованных цепочками антигеномных РНК, комплементарных геномным вирусным РНК. Рецептор-распознающий аппарат вирусов представлен гетеродимерами гликопротеинов Gn и Gc, которые организованным способом распределены по мембране вириона.
Структура генома флебовирусов
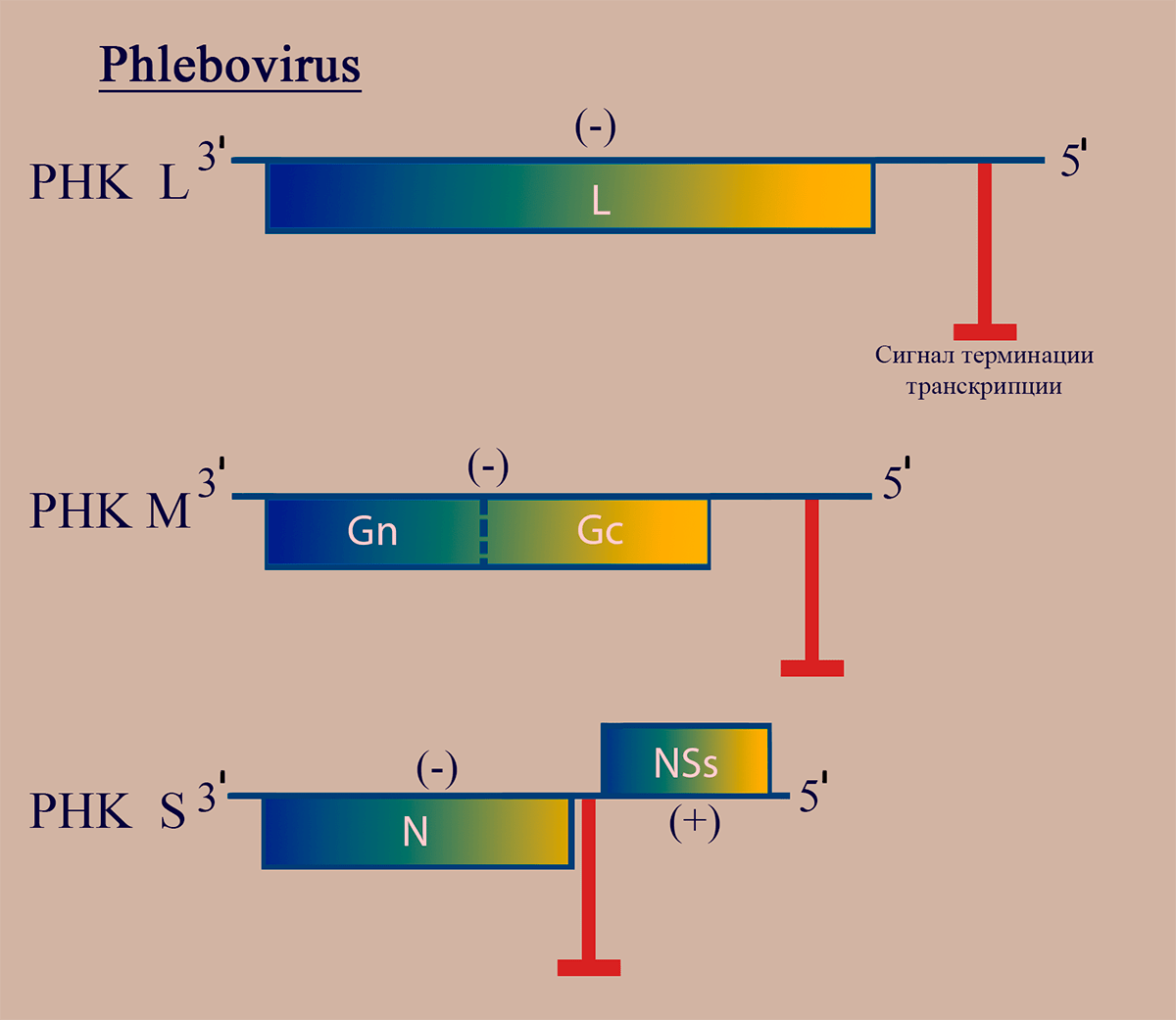
Геном флебовирусов как и других представителей семейства Bunyaviridae, включает три молекулы РНК: PHК L, РНК M, РНК S, имеющие на 5′- и 3′- концах уникальные для каждого геномного сегмента комплементарные последовательности. РНК L (–)полярности кодирует белок репликазы L. (–)РНК M кодирует предшественник гликопротеинов G1 и G2. (±)РНК S кодирует белок нуклеокапсида N на (–)полярном участке (ближе к 3′) и неструктурный белок NSs на (+)полярном участке (ближе к 5′) (рис. 2).
Рисунок 2. Схема структуры генома флебовирусов. Отмечены участки РНК, обладающие (–)- и (+)полярностью. Пунктирной линией обозначен сайт протеолиза белкового продукта.
NSs выполняет ряд функций, среди которых подавление индукции интерферона, усиление репликации и транскрипции вирусной РНК и определение круга хозяев [18]. NSs через цепочку белковых факторов способен приводить к инактивации противовирусной протеинкиназы R организма-хозяина [19].
При одевании вирусных РНК белок N распознаёт последовательность на ее 5′-конце. В вирионе каждая молекула РНП закольцована за счет комплементарных взаимодействий 5′- и 3′-концевых последовательностей (образование т.н. «ручек сковороды»). Таким образом, сегменты генома организуются в шпилечные структуры с короткими (около 12 пар нуклеотидных остатков) стебельками и большими (весь остальной геном) петлями, которые покрыты белком N.
Главный промотор транскрипции и репликации располагается в области спаренных 5′- и 3′-концевых участков («ручки»). Транскрипция и репликация генома флебовирусов осуществляются репликазой L (RdRp).
Как вирусы «воруют» у клеток кэп для синтеза своих мРНК?
Зрелая мРНК эукариот на 5′-конце имеет т.н. кэп — 7-метилгуанозин-5′-трифосфат, соединенный с соседним нуклеотидом 5′,5′-трифосфатной связью. Такая структура делает 5′-конец устойчивым к многим 5′-экзонуклеазам (ферментам, которые «едят» цепочку нуклеотидов с 5′-конца), но самое важное — она распознается рибосомой и необходима для осуществления трансляции.
Кажется, что синтез белков вирусов эукариот возможен только в том случае, если вирусные мРНК имеют кэп. Разные группы вирусов решают «вопрос кэпа» по-разному: кто-то использует ковалентно-пришитый к 5′-концу белок, имитирующий кэп, кто-то имеет образованные вторичными структурами РНК внутренние сайты посадки рибосом (IRES), кто-то может кодировать свои системы кэпирования или привлекать клеточный аппарат созревания РНК. В случае (±)РНК-вирусов, равно как и для многих (–)РНК-вирусов, имеет место процесс, называемый «стащить кэп» (cap snatching). Рассмотрим этот механизм на примере флебовирусов.
Белок L имеет РНК-полимеразную (т.е. может синтезировать комплементарную РНК-цепь) и эндонуклеазную (т.е. может разрезать цепочку нуклеиновой кислоты в определенных сайтах) активности. Последняя направлена на создание разрыва в 5′-нетранслируемой области (НТО) клеточных мРНК, что ведет к декэпированию этих мРНК. Продукт этого «откусывания», короткая кэпированная РНК, используется в дальнейшем в качестве затравки для транскрипции вирусной РНК в цитоплазме. После осуществления такого разрыва вирусная репликаза вместе с 5′-концевым фрагментом клеточной мРНК запускает транскрипцию на матрице геномной вирусной РНК [18]. Таким образом синтезируются способные взаимодействовать с рибосомами субгеномные вирусные РНК. Подход «стащить кэп» не используется для репликации вирусных РНК, то есть для синтеза геномных и антигеномных РНК.
Механизмы транскрипции и репликации РНК флебовирусов
Транскрипция кодирующей белок N последовательности на РНК S, как и для генов других геномных сегментов, происходит с участием геномной (–)РНК по принципу «стащить кэп», а мРНК, кодирующая белок NSs (закодирован в (+)последовательности РНК S), транскрибируется по этому же принципу, но с антигеномной цепи. То есть (+)участок геномной цепи не способен сразу распознаваться рибосомой — для трансляции этого участка необходимо сначала синтезировать полноразмерную антигеномную РНК, с нее — содержащую клеточный кэп субгеномную РНК, и только на субгеномную РНК «сядет» рибосома.
Остановка транскрипции (–)участка РНК S определяется межгенным сигналом терминации. Похожие сигналы терминации находятся в 5′-концевой области РНК M и РНК L. В результате синтезируются кэпированные, но неполиаденилированные (и, следовательно, не такие стабильные, как клеточные мРНК) субгеномные РНК [18]. Также было показано [17], что в инфицированных клетках наблюдается ранняя экспрессия белка NSs, к тому же при детальном анализе состава вирионов обнаружили, что в вирусную частицу может упаковываться как три геномных цепи, так и еще три антигеномных цепи. Считается, что антигеномная РНК S присутствует в вирионе для осуществления ранней транскрипции мРНК, кодирующей NSs, поскольку этот неструктурный белок способен регулировать клеточные процессы, и чем раньше он начнёт работать в зараженной клетке, тем интенсивнее будет протекать вирусная инфекция.
Когда белка N накапливается некоторое «пороговое» количество, происходит переключение режима работы белка L с транскрипционного на репликационный, в результате чего синтезируются не субгеномные РНК, а антигеномные. Инициация репликации не требует затравок клеточной природы, полимеризация комплементарной цепи начинается с одного рибонуклеотида, который и является затравкой [18]. Репликация прекращается, когда репликаза доходит до конца геномной цепи. Геномные РНК синтезируются по аналогичной схеме с антигеномных цепей. Все вышеописанные процессы протекают в цитоплазме — для эффективных транскрипции, репликации, созревания гликопротеинов и, в конце концов, формирования вирусных частиц необходимо образование «вирусных фабрик», представляющих собой трубчатые структуры, образованные мембранами комплекса Гольджи. Такие «фабрики» позволяют повысить локальную концентрацию компонентов репликации вируса [20].
Жизненный цикл флебовирусов
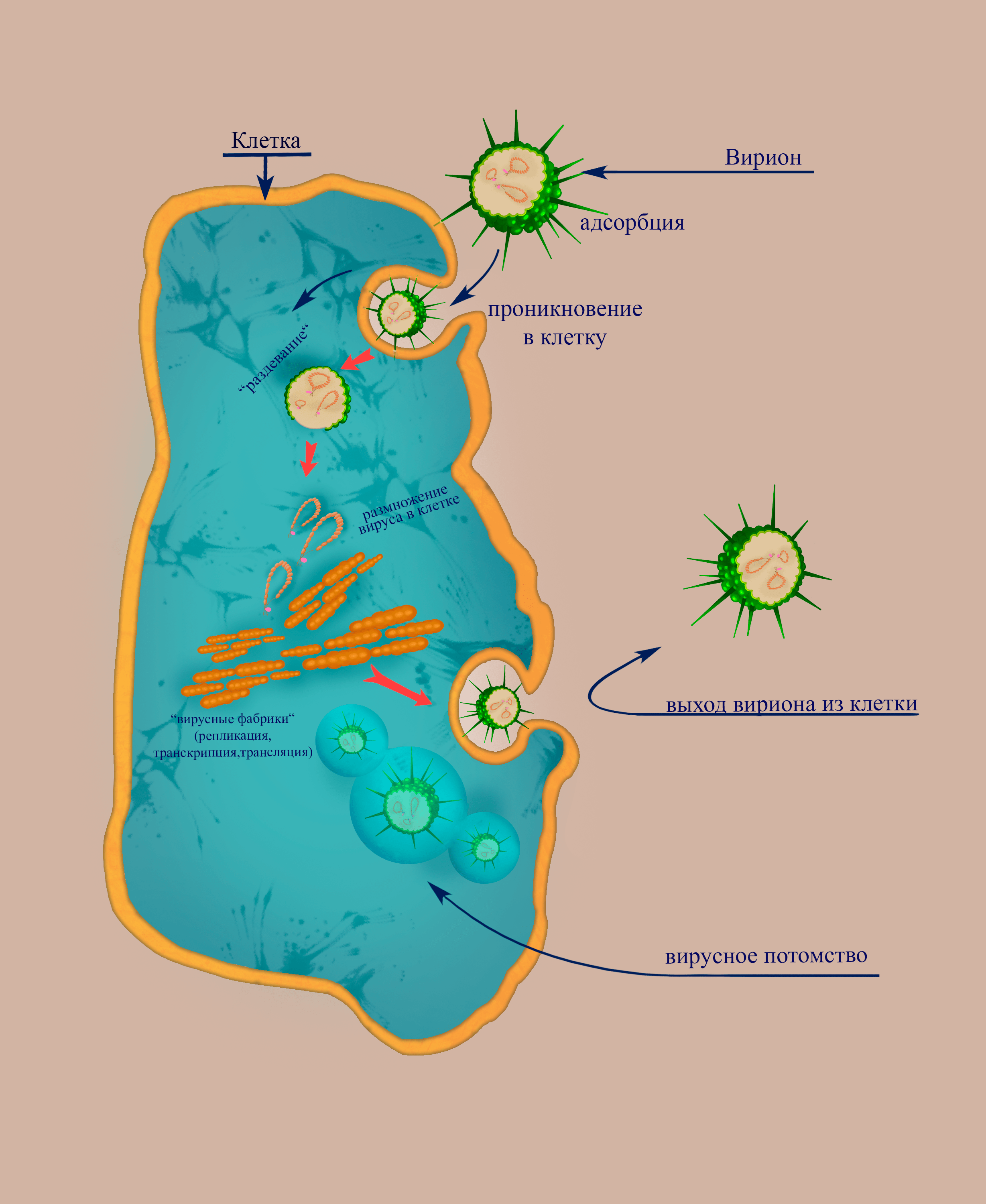
Жизненный цикл состоит из следующих стадий (рис. 3):
Рисунок 3. Схема, демонстрирующая основные этапы цикла флебовируса
Тосповирусы и тенуивирусы
Тосповирусы имеют сходную с флебовирусами структуру вириона. Они являются патогенами растений, использующими в качестве переносчика и второго хозяина трипсов, отряд мелких насекомых-фитофагов [21] и способными к межклеточному транспорту через плазмодесмы в растениях благодаря наличию транспортного белка NSm. Этот белок не входит в состав вириона и синтезируется в течение короткого периода на ранних стадиях инфекции. Он способен связываться с белком нуклеокапсида N, вирусной РНК и клеточными белками, оказываясь ответственным не только за межклеточный транспорт вРНП, без упаковки в вирион, но и за образование вышеупомянутых «вирусных фабрик» в клетке, что в совокупности сказывается на степени вирулентности тосповирусов [22].
Название рода Tospovirus происходит от сокращения названия вируса пятнистого увядания томатов (tomato spotted wilt virus, ТоSWV), впервые выделенного в 1930 году из зараженных растений томата. Этот вирус имеет очень широкий спектр хозяев и важное хозяйственное значение, борьба с ним ведется, в основном, за счет контроля численности трипсов.
Структура генома тосповирусов и тенуивирусов
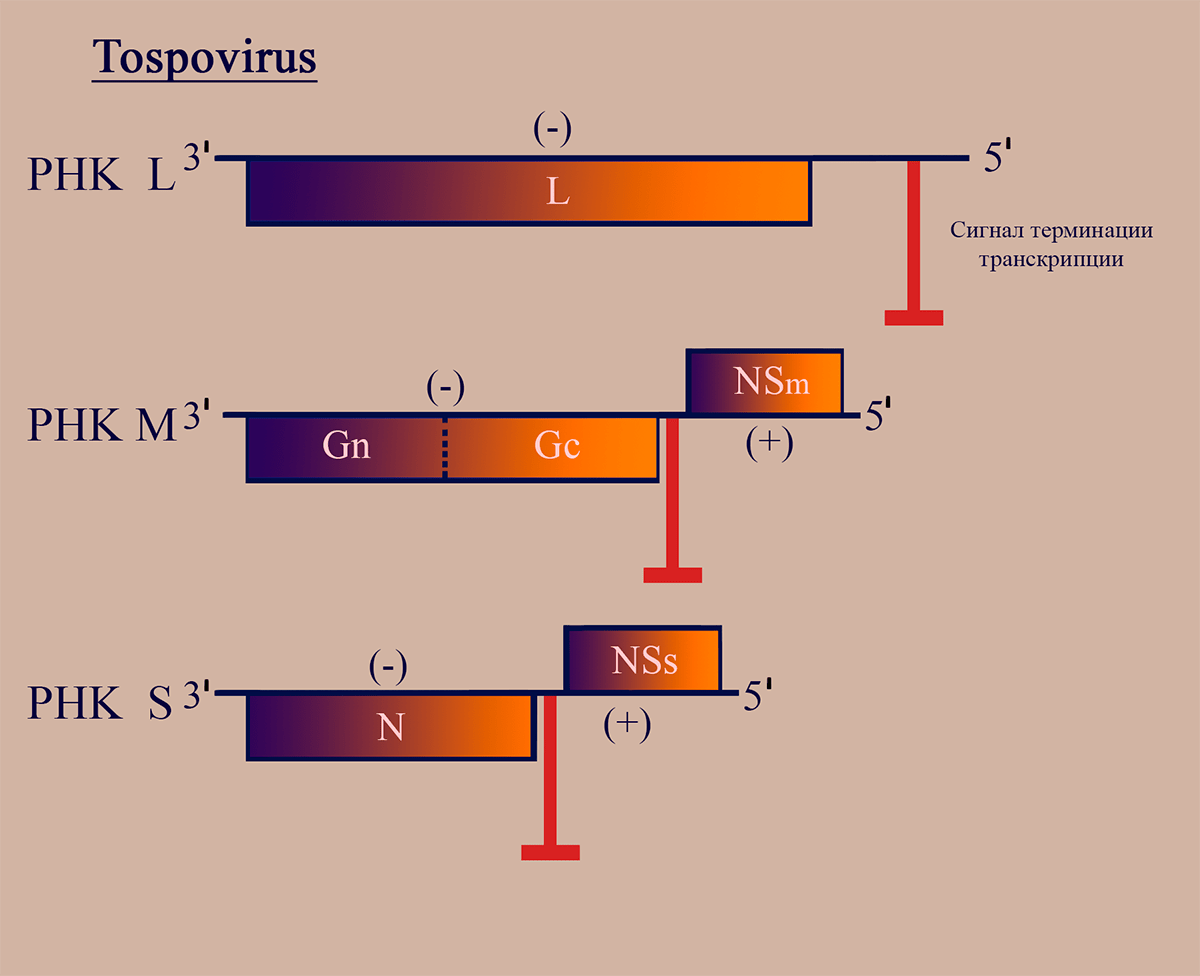
Представители родов Тospovirus и Tenuivirus (тенуивирусы близки к тосповирусам, но не имеют липидной оболочки) являются единственными известными РНКвирусами растений с двусмысленным геномом [23]. Геном тосповирусов представлен тремя РНК-сегментами: большим, средним и малым (L, M, S). РНК L кодирует репликазу L. РНК S, подобно таковой у флебовирусов, кодирует белок нуклеокапсида N в (–)области и неструктурный белок NSs в (+)области. Эти области не пересекаются, они разделены межгенным некодирующим участком, содержащим сигналы терминации транскрипции. М-сегмент генома имеет принципиально отличную от РНК М флебовирусов структуру, являясь амбисенсной РНК. РНК М тосповирусов имеет область (–)полярности, в которой находится последовательность, кодирующая мРНК GnGc — предшественника поверхностных гликопротеинов, а также участок (+)полярности в 5′-области, кодирующий белок межклеточного транспорта NSm. Эти последовательности также разделены межгенным участком (рис. 4). Механизмы транскрипции и репликации РНК этих вирусов сходны с таковыми у флебовирусов [18].
Рисунок 4. Схема структуры генома тосповирусов. Отмечены участки РНК, обладающие (–)- и (+)полярностью. Пунктирной линией обозначен сайт протеолиза белкового продукта.
Отдельного внимания заслуживает неструктурный белок, закодированный в S-сегменте генома тосповирусов — NSs. Основной его функцией является супрессия противовирусного сайленсинга РНК, системы малых интерферирующих РНК [5], [24], распознающих вирусные РНК, что приводит к деградации последних [25]. Логично предположить, что синтез такого белка должен происходить как можно раньше, поэтому, возможно, по аналогии с белком NSs флебовирусов, ранняя транскрипция такой последовательности происходит в результате наличия в вирионе, помимо геномной цепи РНК S, еще и соответствующей ей антигеномной.
Вирусы с двусмысленным РНК-геномом из семейства Arenaviridae
Помимо семейства Bunyaviridae, амбисенсные РНК имеют представители семейства Arenaviridae. Аренавирусы являются таксономической группой вирусов позвоночных с сегментированным двусмысленным РНК-геномом. Вирусы, инфицирующие млекопитающих, определены в род Mammarenavirus, а заражающие рептилий — в роды Reptarenavirus и Hartmanivirus [26].
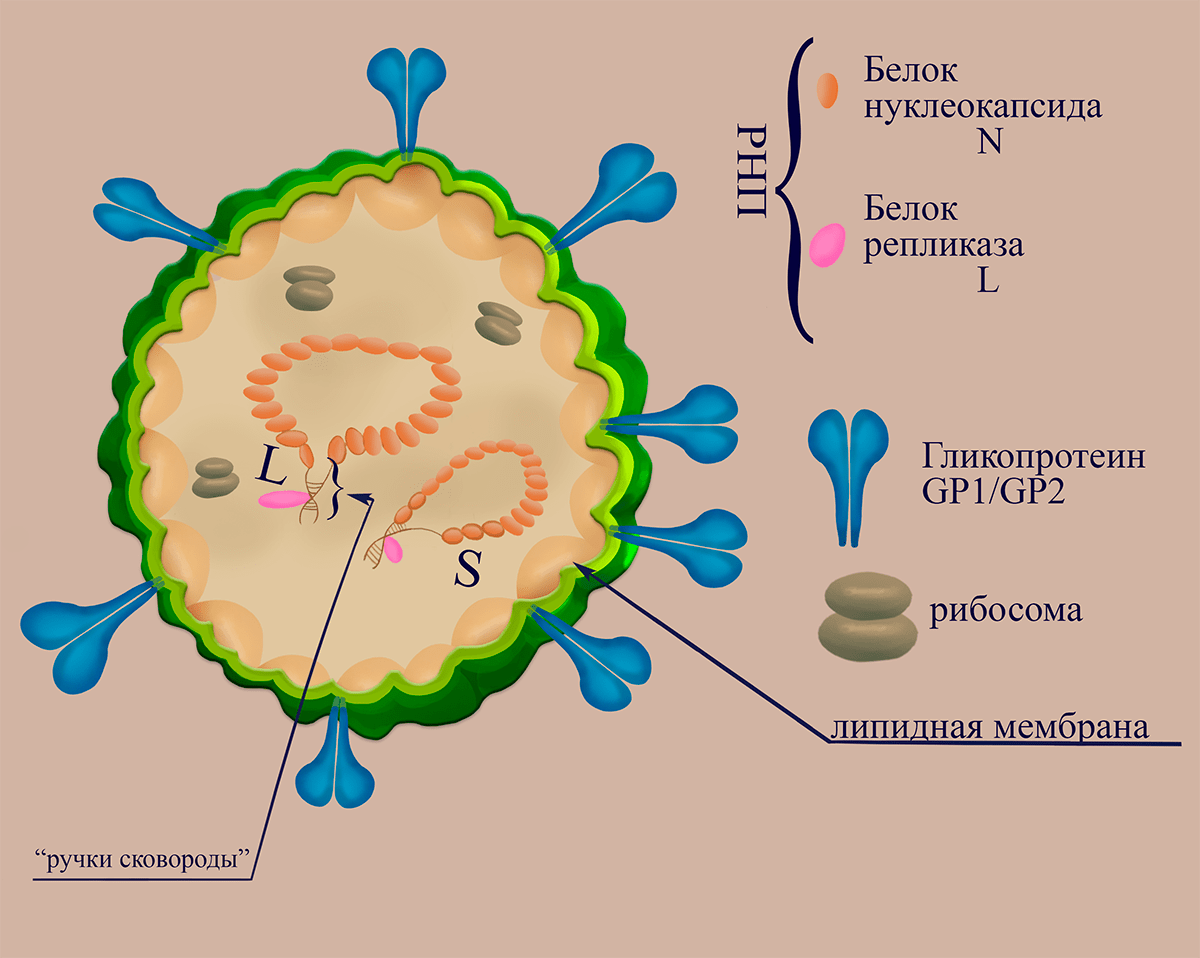
Вирионы аренавирусов, как и рассмотренных выше буньявирусов, плеоморфны, а их диаметр может варьировать от 40 до 200 нанометров в зависимости от вида, однако и частицы одного вида могут заметно различаться по размерам [27]. Границы вириона представлены липопротеидной оболочкой — производной клеточной мембраны, модифицированной равномерно распределёнными гликопротеиновыми комплексами (гетеродимерный гликопротеин GP1/GP2). Гликопротеины синтезируются в виде предшественника, который разрезается примерно пополам клеточной протеиназой на рецептор-распознающую субъединицу GP1 и трансмембранную субъединицу GP2. Последняя ответственна за слияние мембран при проникновении в цитоплазму [28]. В вирионе гликопротеины ассоциированны с лежащими на внутренней стороне мембраны молекулами матриксного белка Z, выстилающего внутреннюю поверхность мембраны, и белка нуклеокапсида N. Белок N способен связываться с РНК, распознавать кэп и ингибировать интерфероновый ответ. Структурный белок Z в клетке выполняет ряд функций (в том числе ингибирование трансляции клеточных мРНК и подавление апоптоза), являясь фактором созревания вирусных частиц (отвечает за инициацию сборки вирионов и за их отпочковывание).
Во время сборки вирусных частиц при формировании внешней оболочки иногда происходит захват субъединиц клеточных рибосом, по всей видимости, не играющих роли в вирусной инфекции (рис. 5).
Рисунок 5. Схематичное изображение структуры вириона аренавирусов
Значительная часть представителей семейства вызывает хронические и, как правило, бессимптомные инфекции у грызунов. При контакте человека с такими вирусами может развиваться острая и тяжелая инфекция, часто — геморрагическая лихорадка (например, в случае инфекции вирусом лихорадки Ласса, LasV). Вирус лимфоцитарного хориоменингита (LCMV), первый выделенный аренавирус, является нейроинвазивным. Попав в организм человека (например, через выделения грызунов), вирионы с током крови преодолевают гематоэнцефалический барьер центральной нервной системы и вызывают воспаления мозговых оболочек [29].
Структура генома аренавирусов
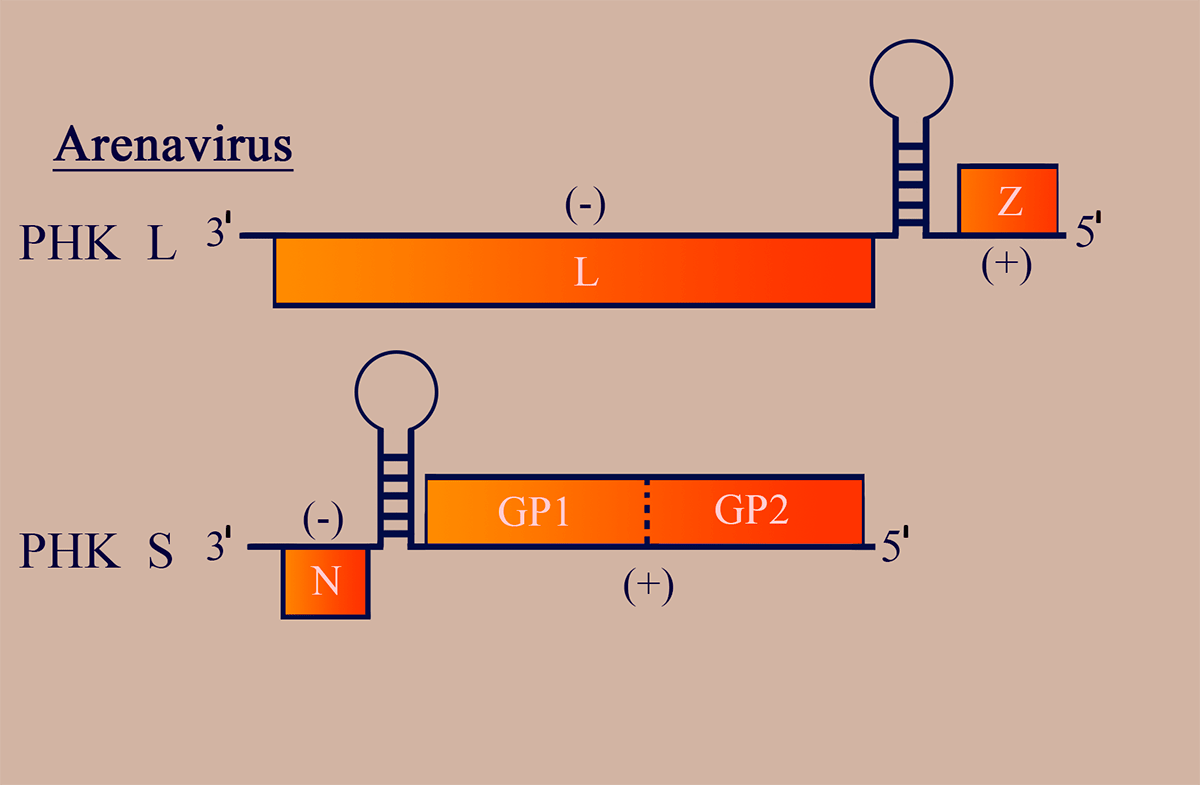
Геном аренавирусов имеет ряд особенностей и представлен двумя сегментами (РНК L
3000 н.о.), циклизованными уже известными нам «ручками сковороды» и закрученными в спиральный рибонуклеопротеиновый комплекс (рис. 6). Обе молекулы РНК — двусмысленные!
Рисунок 6. Схема структуры генома аренавирусов. Отмечены участки РНК, обладающие (–)- и (+)полярностью. Пунктирными линиями обозначены сайты протеолиза белковых продуктов.
РНК L на (–)участке несет последовательность, комплементарную гену репликазы L, и рамку матриксного и регуляторного белка Z на (+)участке в 5′-концевой части геномной РНК.
РНК S кодирует белок нуклеокапсида N в области (–)полярности и содержит рамку считывания GP1GP2 — предшественника поверхностных гликопротеинов GP1/GP2 (также в 5′-концевой части геномного сегмента).
(–)- и (+)участки разделены межгенными сайтами, образующими прочные вторичные структуры шпилечного характера. На 5′-конце геномных и антигеномных цепей присутствует сигнал инициации инкапсидации (то есть «одевания» РНК вирусными белками с образованием вРНП), распознаваемый белком N [18].
Транскрипция и репликация генома аренавирусов
Оба процесса проходят в цитоплазме инфицированной клетки. Транскрипция начинается при участии репликазы L по уже описанному выше для флебовирусов принципу «стащить кэп» (cap snatching). Терминация транскрипции обусловлена наличием соответствующего сигнала в стабильных шпильках межгенного пространства геномной или антигеномной РНК. Вирусные субгеномные РНК не полиаденилируются [18].
Переключение на репликацию связано с наличием белка N: когда его накапливается такое количество, что он начинает покрывать строящиеся цепи РНК, это, вероятно, влияет на конформацию репликазы и приводит к проскоку сигналов терминации транскрипции в виде межгенных шпилек. РНК S при репликации накапливается в больших количествах, так как нужно много копий белка нуклеокапсида, а также гликопротеинов (для экспрессии последних необходим предварительный синтез антигеномной РНК).
Заключение
Принимая во внимание всё вышеизложенное, можно сделать выводы относительно общих особенностей вирусов, содержащих амбисенсную РНК. Геном таких вирусов является сегментированным, и хотя бы один сегмент представлен амбисенсной РНК. Каждый геномный сегмент содержит комплементарные 3′- и 5′-концевые последовательности, образующие «ручки сковороды». В составе этого не очень протяженного дуплекса в геномной РНК присутствует главный промотор транскрипции и репликации, распознаваемый репликазой L. 5′- концевые последовательности геномных и антигеномных молекул РНК связываются белком нуклеокапсида N. Затравкой для синтеза вирусных мРНК, как и в случае типичных вирусов с сегментированным (–)РНК-геномом, является «откушенный» кэпированный фрагмент клеточной мРНК.
Что же касается самих амбисенсных РНК, они содержат последовательности отрицательной полярности в 3′-части и положительной полярности в 5′-части геномной цепи. Терминация транскрипции в таких двусмысленных РНК связана с наличием соответствующих сигналов в межгенном участке. При этом (+)участок амбисенсной РНК не может сразу выступать в качестве мРНК, необходим последовательный синтез антигеномной, а только потом субгеномной РНК положительной полярности. Все эти процессы занимают определенное время, поэтому вопрос «отсрочки» синтеза белков из (+)участка геномной РНК может решаться для вируса путем включения в зрелую вирусную частицу, помимо геномной (±)РНК, ещё и антигеномной (±)РНК.
Такая необычная организация двусмысленных геномных сегментов является интересным способом представления двух кодирующих последовательностей в одном геномном сегменте. На примере вирусов с двусмысленными РНК-геномами заметно, насколько изобретательной может быть эволюция вирусных РНК. Поскольку вирусы с двусмысленными РНК-геномами до сих пор удерживают определенную нишу, можно утверждать, что такой способ кодирования обладает некоторыми преимуществами по сравнению с более привычным для родственных вирусов способом, использующим только (–)РНК-сегменты.
Как возникли амбисенсные РНК и почему поддержались отбором, до сих пор остается одной из загадок современной вирусологии.
И как сказал один известный принц: «Есть многое на свете, друг Горацио, что и не снилось нашим мудрецам!»
Благодарности от автора
Я благодарю доктора биологических наук, профессора кафедры вирусологии биологического факультета МГУ им. М.В. Ломоносова Аграновского Алексея Анатольевича за интересные и содержательные лекции по молекулярным процессам РНК-вирусов и вдохновение на написание данной статьи. Также выражаю благодарность художнику Андрею Занкевичу, чьи наглядные и яркие иллюстрации украшают данную статью.