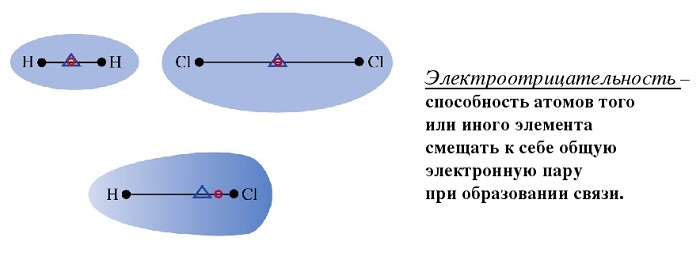
Полярные и неполярные молекулы (Пример)
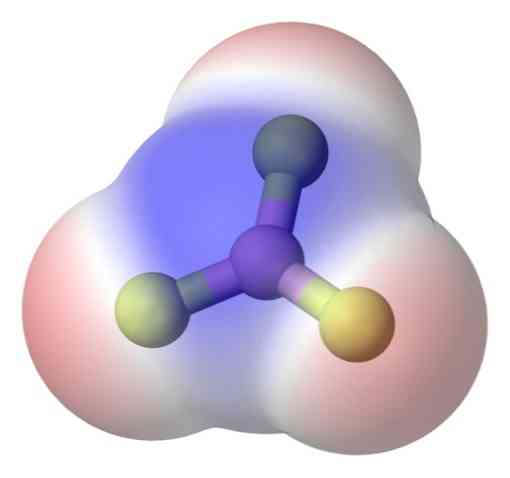
Полярные молекулы это соединения молекулы которых характеризоваться электрическим дипольным моментом. Примеры полярных молекул: вода — H2O, аммиак — NH3, диоксид серы — SO2.
Неполярные молекулы это соединения электроны которых одинаково распределяются между атомами в молекуле вещества или ихнее расположение в молекуле симметрично, поэтому дипольные заряды компенсируют друг друга.
Примеры неполярных молекул: любой из двухатомный газ H2, N2, O2, Cl2, углекислый газ — CO2 и другие.
ЧТО ТАКОЕ ПОЛЯРНЫЕ И НЕПОЛЯРНЫЕ МОЛЕКУЛЫ
Во всякой молекуле имеются как положительно заряженные частицы — ядра атомов, так и отрицательно заряженные — электроны.
Для каждого рода частиц (или, вернее, зарядов) можно найти такую точку, которая будет являться как бы их «электрическим центром тяжести».
Эти точки называются полюсами молекулы. Если в молекуле электрические центры тяжести положительных и отрицательных зарядов совпадут, то молекула будет неполярной.
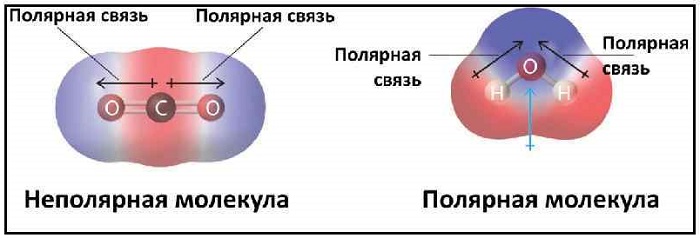
Пример неполярной молекулы
Рис.. Схемы полярной и не полярной молекул: а — полярная молекула; б—неполярная молекула.
Но если молекула построена несимметрично, например состоит из двух разнородных атомов, то, как мы уже говорили, общая пара электронов может быть в большей или меньшей степени смещена в сторону одного из атомов.
Очевидно, что в этом случае, вследствие неравномерного распределения положительных и отрицательных зарядов внутри молекулы, их электрические центры тяжести не совпадут и получится полярная молекула (рис.).
Полярные молекулы это
Полярные молекулы являются диполями. Этим термином обозначают вообще всякую электронейтральную систему, т. е. систему, состоящую из положительных и отрицательных зарядов, распределенных таким образом, что их электрические центры тяжести не совпадают.
Расстояние между электрическими центрами тяжести тех и других зарядов (между полюсами диполя) называется длиной диполя.
Длина диполя характеризует степень полярности молекулы. Понятно, что для различных полярных молекул длина диполя различна; чем она больше, тем резче выражена полярность молекулы.
На практике степень полярности тех или иных молекул устанавливают путем измерения так называемого дипольного момента молекулы т, который определяется как произведение длины диполя l на заряд его полюса е:
Величины дипольных моментов связаны с некоторыми свойствами веществ и могут быть определены экспериментальным путем.
Рис. 2. Схемы строения молекул СO2 и CS2
Ниже приведены дипольные моменты молекул некоторых неорганических веществ.
Дипольные моменты
Дипольные моменты некоторых веществ
Хлористый водород……. 1,04
Двуокись углерода……. 0
Йодистый водород…….. 0,38
Окись углерода ……. 0,11
Определение величин дипольных моментов позволяет сделать много интересных выводов относительно строения различных молекул. Рассмотрим некоторые из этих выводов.
Как и следовало ожидать, дипольные моменты молекул водорода и азота равны нулю; молекулы этих веществ совершенно симметричны и следовательно, электрические заряды в них распределены равномерно.
Отсутствие полярности у двуокиси углерода и у сероуглерода показывает, что их молекулы также построены симметрично. Строение молекул этих веществ схематически изображено на рис. 2.
Несколько неожиданным является наличие довольно большого дипольного момента у воды. Так как формула воды аналогична формулам двуокиси углерода и сероуглерода, то следовало ожидать, что её молекулы будут построены так же симметрично, как и молекулы CS2 и СО2.
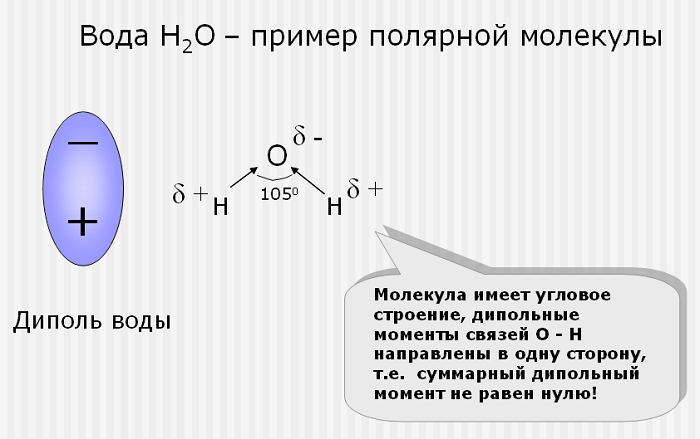
Рис. 3. Схема строения молекулы воды.
Почему молекула воды полярная
Ввиду экспериментально установленной полярности молекул воды (полярности молекул) это предположение приходится отбросить.
В настоящее время молекуле воды приписывают несимметричное строение (рис. 3): два атома водорода соединены с атомом кислорода так, что их связи образуют угол около 105°.
Аналогичное расположение атомных ядер имеется и в других молекулах такого же типа (H2S, SO2), обладающих дипольными моментами.
Полярностью молекул воды объясняются многие ее физические свойства.
Статья на тему Полярные и неполярные молекулы
Похожие страницы:
Понравилась статья поделись ей
Характеристика неполярных молекул, способы их идентификации и примеры
аполярные молекулы это те, которые представляют в своей структуре симметричное распределение своих электронов. Это возможно, если разность электроотрицательности его атомов мала или если электроотрицательные атомы или группы отменяют свои эффекты в молекуле.
Не всегда «аполярность» абсолютна. По этой причине молекулы полярной полярности иногда считаются неполярными; то есть он имеет дипольный момент μ, близкий к 0. Здесь вводится территория родственника: как низко должно быть μ, чтобы молекула или соединение считались неполярными?
Чтобы лучше решить эту проблему, у вас есть молекула трифторида бора, BF3 (верхнее изображение).
Атом фтора является гораздо более электроотрицательным, чем атом бора, и поэтому связи B-F являются полярными. Однако молекула BF3 является симметричным (тригональная плоскость) и включает в себя векторное подавление трех моментов B-F.
Таким образом, неполярные молекулы также генерируются, даже при наличии полярных связей. Генерируемая полярность может быть уравновешена существованием другой полярной связи, такой же величины, как и предыдущая, но ориентированной в противоположном направлении; как это происходит в БФ3.
Характеристики аполярной молекулы
симметрия
Чтобы эффекты полярных связей подавляли друг друга, молекула должна иметь определенную геометрическую структуру; например, линейный, самый простой для понимания с первого взгляда.
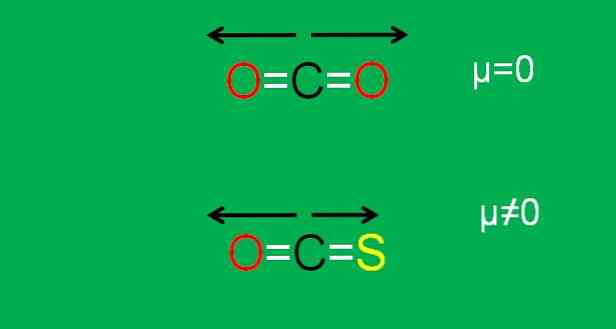
Предположим, что вместо СО2 у вас есть молекула COS (O = C = S), называемая карбонил сульфид.
Теперь это уже не аполярная молекула, поскольку электроотрицательность серы меньше, чем у кислорода; и, следовательно, дипольный момент C = S отличается от дипольного момента C = O. В результате COS является полярной молекулой (насколько полярной является мука из другого мешка).
Нижнее изображение в графической форме суммирует все, что только что было описано:
Обратите внимание, что дипольный момент связи C = S меньше, чем у связи C = O в молекуле COS.
электроотрицательность
Электроотрицательность по шкале Полинга имеет значения от 0,65 (для франка) до 4,0 (для фтора). В целом, галогены имеют высокую электроотрицательность.
Когда разность электроотрицательности элементов, образующих ковалентную связь, меньше или равна 0,4, она называется неполярной или неполярной. Однако единственными молекулами, которые действительно неполярны, являются молекулы, образованные связями между одинаковыми атомами (такими как водород, H-H)..
Межмолекулярные силы
Чтобы вещество растворилось в воде, оно должно электростатически взаимодействовать с молекулами; взаимодействия, которые неполярные молекулы не могут сделать.
В неполярных молекулах их электрические заряды не ограничены на одном конце молекулы, а распределены симметрично (или однородно). Поэтому он не может взаимодействовать через диполь-дипольные силы.
Напротив, неполярные молекулы взаимодействуют друг с другом посредством дисперсионных сил Лондона; это мгновенные диполи, которые поляризуют электронное облако атомов соседних молекул. Здесь молекулярная масса является преобладающим фактором в физических свойствах этих молекул.
Как их идентифицировать?
-Возможно, одним из лучших методов идентификации неполярной молекулы является ее растворимость в различных полярных растворителях, поскольку она обычно плохо растворяется в них..
-В общем, неполярные молекулы имеют газообразную природу. Они также могут образовывать несмешивающиеся жидкости с водой.
-Аполярные твердые частицы характеризуются мягкостью.
-Дисперсионные силы, которые удерживают их вместе, обычно слабы. Из-за этого их температуры плавления или кипения имеют тенденцию быть ниже, чем у соединений полярной природы..
-Аполярные молекулы, особенно в жидкой форме, являются плохими проводниками электричества, поскольку у них нет чистого электрического заряда.
примеров
Благородные газы
Хотя они не являются молекулами, благородные газы считаются неполярными. Предполагая, что в течение двух коротких периодов времени два его атома взаимодействуют, He-He, это взаимодействие можно рассматривать (наполовину) как молекулу; молекула, которая была бы неполярной по природе.
Двухатомные молекулы
Двухатомные молекулы, такие как H2, бром2, я2, Cl2, O2, и F2, они неполярные. Они имеют в качестве общей формулы А2, А-А.
углеводороды
Что если бы А была группой атомов? Это было бы раньше других неполярных соединений; например, этан, СН3-СН3, чей углеродный скелет является линейным, C-C.
Метан, СН4, и этан, С2H6, они неполярные молекулы. Углерод имеет электроотрицательность 2,55; в то время как электроотрицательность водорода составляет 2,2. Поэтому существует дипольный вектор низкой интенсивности, ориентированный от водорода к углероду.
Но из-за геометрической симметрии молекул метана и этана сумма дипольных векторов или дипольных моментов в их молекулах равна нулю, поэтому на молекулах нет полного заряда.
В целом то же самое происходит со всеми углеводородами, и даже когда в них присутствуют ненасыщенности (двойные и тройные связи), они считаются неполярными или низкополярными соединениями. Аналогично, циклические углеводороды представляют собой неполярные молекулы, такие как циклогексан или циклобутан..
другие
Молекулы углекислого газа (СО2) и сероуглерод (CS)2) являются неполярными молекулами, оба с линейной геометрией.
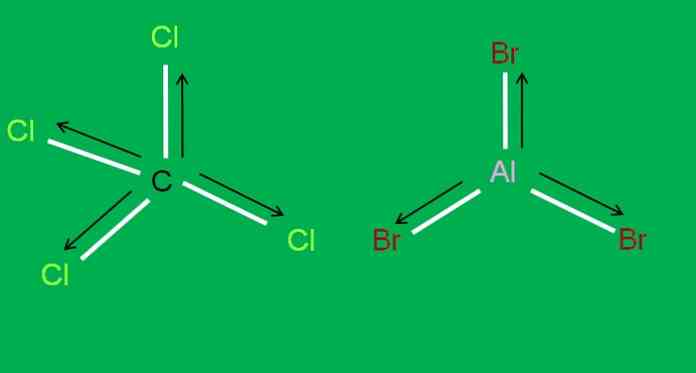
Также у нас есть следующие молекулы CCl4 и AlBr3, оба неполярные
В трибромиде алюминия, AlBr3 это происходит так же, как с BF3, в начале статьи. Между тем, для четыреххлористого углерода, CCl4, геометрия тетраэдрическая и симметричная, так как все звенья C-Cl равны.
Аналогично, молекулы с общей формулой CX4 (CF4, CI4 и CBr4) они тоже неполярные.
И, наконец, неполярная молекула может даже иметь восьмигранную геометрию, как в случае гексафторида серы, SF6. Фактически, он может иметь любую геометрию или структуру, если он симметричен и его электронное распределение однородно.
Полярные и неполярные молекулы – две группы, на которые подразделяются все диэлектрики.
Полярные по-другому называются дипольными. А неполярные являются нейтральными или бездипольными.
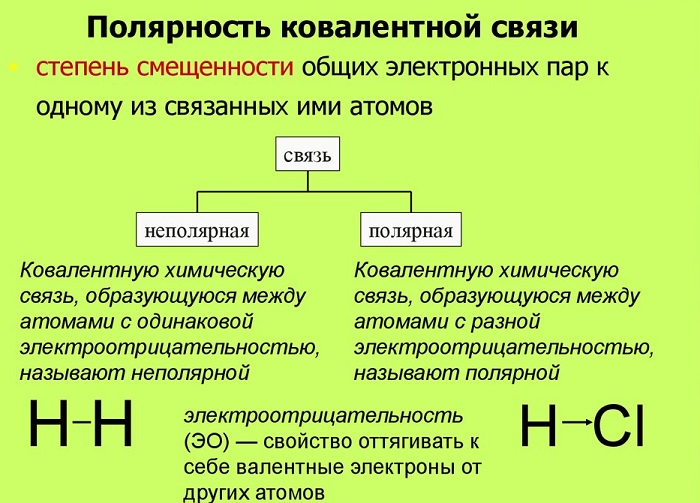
Что такое полярность в химии
Полярность – свойство, показывающее изменение распределения электронной плотности около ядер, если сравнивать с изначальным ее распределением в образующих данную связь нейтральных частицах.
Поляризуемость — способность поляризоваться под воздействием электрического поля.
Мерой полярности называется электрический момент диполя. В нейтральных соединениях он равен нулю. Его значение зависит от разности электроотрицательностей элементов.
Длина диполя — расстояние между его полюсами. Данная характеристика также влияет на степень полярности.
Любое соединение состоит из ядра (положительные частицы) и электронов (отрицательные частицы). И положительные, и отрицательные частицы имеют свой электрический центр тяжести.
Если центры тяжести частиц совпадают, то соединение считается неполярным. Если же полюса не накладываются друг на друга, то в этом случае речь идет о дипольной связи.
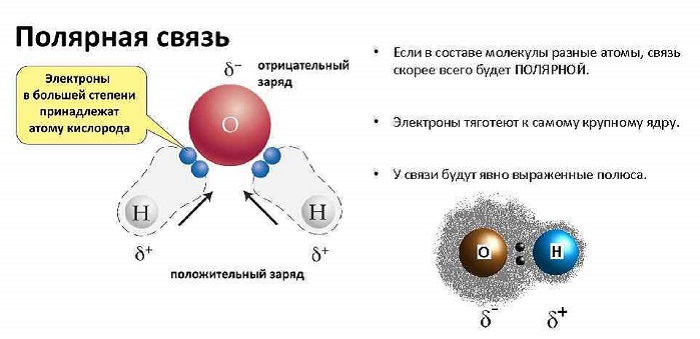
Примеры полярных молекул
Эта связь образуется, если вещество состоит из атомов разных элементов и ассиметрична (имеются неспаренные электроны). Такие соединения имеют угловую, изогнутую геометрическую форму.
Примеры неполярных молекул
Эта связь также может встречаться в соединениях, состоящих из атомов разных элементов и при этом являющихся симметричными (линейные, тетраэдрические и т. д.). Такими веществами являются: BeH2, BF3, CH4, CO2(углекислый газ) и SO3.
При нейтральной связи электронное облако равномерно распределяется между ядрами всех атомов данного вещества. Поэтому ядра действуют на него в равной мере.
Как определить полярность молекулы и от чего она зависит
Чтобы определить, является ковалентная связь дипольной или нет, необходимо посмотреть на химическую формулу вещества.
Если молекула состоит из атомов одного и того же вещества, то она в любом случае нейтральна.
Если же молекулярное строение является сложным, то речь может идти как о полярной, так и неполярной ковалентной связи. Это зависит от геометрической формы.
Неполярные молекулы что значит
ХИМИЯ ЕГЭ | Химический кампус | Регина Ли запись закреплена
Полярная молекула или неполярная?
#ХимКампус_статья
Такие вопросы попадаются в тренировочных заданиях по теме «Химическая связь». Важно заметить, что полярная связь не равно полярная молекула! Полярность определяется неравномерным распределением электронной плотности вокруг молекулы.
Если электронная плотность распределена равномерно, то молекула считается неполярной. Если какой-то участок молекулы перетягивает на себя эту электронную плотность, то молекула – полярная (появляется разные полюсы – области частичного заряда).


Полярная молекула имеет асимметричную форму, неподеленную электронную пару или центральный атом, связанный с другими атомами с разными значениями электроотрицательности. Обычно полярная молекула содержит ионные или полярные ковалентные связи. Приведем примеры:
Полярные молекулы часто гидрофильны («любят воду») и растворимы в полярных растворителях. Полярные молекулы часто имеют более высокие температуры плавления, чем неполярные молекулы с аналогичными молярными массами. Это связано с межмолекулярными силами между полярными молекулами, такими как водородная связь!

Неполярные молекулы образуются либо тогда, когда электроны одинаково распределяются между атомами в молекуле, либо когда расположение электронов в молекуле симметрично, так что дипольные заряды компенсируют друг друга. Приведем примеры неполярных молекул:
Неполярные молекулы обладают некоторыми общими свойствами. Они, как правило, нерастворимы в воде при комнатной температуре, гидрофобны («боятся воды») и способны растворять другие неполярные соединения.
Мы помним золотое правило «подобное растворяется в подобном». Это означает, что полярные растворители растворяют полярные вещества, и наоборот. Это объясняет, почему спирт и вода полностью смешиваются (как полярные) и почему масло и вода не смешиваются (неполярные с полярными).
Дополнительную информацию и объяснение на примерах можно почитать в файлике ниже!
Элементарная физика
2.1 Полярные и неполярные молекулы
Диэлектриками (или изоляторами) называются вещества, не способные проводить электрический ток. Идеальных изоляторов в природе не существует. Bce вещества хотя бы в ничтожной степени проводят электрический ток. Однако вещества, называемые диэлектриками, проводят ток 
Ecли диэлектрик внести в электрическое поле, то это поле и сам диэлектрик претерпевают существенные изменения. Чтобы понять, почему это происходит, нужно учесть, что в составе атомов и молекул имеются положительно заряженные ядра и отрицательно заряженные электроны.
Так как положительный заряд всех ядер молекулы равен суммарному заряду электронов, то молекула в целом электрически нейтральна. Если заменить положительные заряды ядер молекул суммарным зарядом +q, находящимся в центре «тяжести» положительных зарядов, а заряд всех электронов – суммарным отрицательным зарядом –q, находящимся в центре «тяжести» отрицательных зарядов, то молекулу можно рассматривать как электрический диполь с электрическим моментом, определяемым формулой (7.1)
У симметричных молекул 
У несимметричных молекул 
Под действием внешнего электрического поля заряды в неполярной молекуле смещаются друг относительно друга: положительные по направлению поля, отрицательные против поля. B результате молекула приобретает дипольный момент, величина которого, как показывает опыт, пропорциональна напряженности поля. B рационализованной системе коэффициент пропорциональности записывают в виде 




Процесс поляризации неполярной молекулы протекает так, как если бы положительные и отрицательные заряды молекулы были связаны друг с другом упругими силами. Поэтому говорят, что неполярная молекула ведет себя во внешнем поле как упругий диполь.
Действие внешнего поля на полярную молекулу сводится в основном к стремлению повернуть молекулу так, чтобы ее дипольный момент установился по направлению поля. На величину дипольного момента внешнее поле практически не влияет. Следовательно, полярная молекула ведет себя во внешнем поле как жесткий диполь.
К диэлектрикам относятся еще и вещества (NaCl, KCl, KBr, …), молекулы которых имеют ионное строение. Ионные кристаллы представляют собой пространственные решетки с правильным чередованием ионов разных знаков. В этих кристаллах нельзя выделить отдельные молекулы, а рассматривать их можно как систему двух вдвинутых одна в другую ионных подрешеток. При наложении на ионный кристалл электрического поля происходит некоторая деформация кристаллической решетки или относительное смещение подрешеток, приводящее к возникновению дипольных моментов.
Таким образом, внесение всех трех групп диэлектриков во внешнее электрическое поле приводит к возникновению отличного от нуля результирующего электрического момента диэлектрика, или, иными словами, к поляризации диэлектрика. Поляризацией диэлектрика называется процесс ориентации диполей или появления под воздействием внешнего электрического поля ориентированных по полю диполей.
Соответственно трем группам диэлектриков различают три вида поляризации:
электронная, или деформационная, поляризация диэлектрика с неполярными молекулами, заключающаяся в возникновении у атомов индуцированного дипольного момента за счет деформации электронных орбит;
ориентационная, или дипольная, поляризация диэлектрика с полярными молекулами, заключающаяся в ориентации имеющихся дипольных моментов молекул по полю. Естественно, что тепловое движение препятствует полной ориентации молекул, но в результате совместного действия обоих факторов (электрическое поле и тепловое движение) возникает преимущественная ориентация дипольных моментов молекул по полю. Эта ориентация тем сильнее, чем больше напряженность электрического поля и ниже температура;
ионная поляризация диэлектриков с ионными кристаллическими решетками, заключающаяся в смещении подрешетки положительных ионов вдоль поля, а отрицательных – против поля, приводящем к возникновению дипольных моментов.