Тимома
Тимома – гетерогенная группа новообразований, различных по гистогенезу и степени зрелости, берущих начало из эпителиальной ткани вилочковой железы. Варианты клинического течения тимомы могут быть различны: от бессимптомного до выраженного (компрессионный, болевой, миастенический, интоксикационный синдром). Топографо-анатомический и этиологический диагноз устанавливается с помощью лучевых методов (рентгенография, КТ средостения), трансторакальной пункции, медиастиноскопии, исследования биоптата. Лечение хирургическое: удаление тимомы вместе с вилочковой железой и жировой клетчаткой переднего средостения, дополненное по показаниям химиолучевой терапией.
Общие сведения
Тимома – органоспецифическая опухоль средостения, происходящая из клеточных элементов мозгового и коркового вещества тимуса. Термин «тимома» был введен в употребление в 1900 году исследователями Grandhomme и Scminke для обозначения различных опухолей вилочковой железы. Тимомы составляют 10-20% всех новообразований медиастинального пространства. В 65-70% случаев тимомы имеют доброкачественное течение; инвазивный рост с прорастанием плевры и перикарда отмечается у 30% пациентов, отдаленное метастазирование – у 5%. Несколько чаще тимомы развиваются у женщин, болеют преимущественно лица 40-60 лет. На детский возраст приходится менее 8% опухолей тимуса.
Причины формирования опухолей вилочковой железы неизвестны. Предполагается, что тимомы могут иметь эмбриональное происхождение, быть связаны с нарушением синтеза тимопоэтина или иммунного гомеостаза. Факторами, провоцирующими рост и развитие опухоли, могут служить инфекционные заболевания, радиационное воздействие, травмы средостения. Замечено, что тимомы часто сочетаются с различными эндокринными и аутоиммунными синдромами (миастенией, дерматомиозитом, СКВ, диффузным токсическим зобом, синдромом Иценко-Кушинга и др.).
Строение и функции вилочковой железы
Вилочковая железа, или тимус располагается в нижней части шеи и переднем отделе верхнего средостения. Орган образован двумя асимметричными долями – правой и левой. В свою очередь, каждая доля представлена множеством долек, состоящих из коркового и мозгового вещества и заключенных в соединительнотканную строму. В вилочковой железе различают два типа ткани – эпителиальную и лимфоидную. Эпителиальные клетки секретируют тимические гормоны (тимулин, a-, b-тимозины, тимопоэтины и пр.), лимфоидная ткань состоит из Т-лимфоцитов различной степени зрелости и функциональной активности.
Таким образом, вилочковая железа одновременно является железой внутренней секреции и органом иммунитета, обеспечивающим взаимодействие эндокринной и иммунной систем. После 20 лет тимус подвергается возрастной инволюции; после 50 лет паренхима тимуса на 90% замещается жировой и соединительной тканью, сохраняясь в виде отдельных островков, лежащих в клетчатке средостения.
Классификация тимом
В онкологии различают три типа тимом: доброкачественную, злокачественную тимому 1-го типа (с признаками атипии, но относительно доброкачественным течением) и злокачественную тимому 2-го типа (с инвазивным ростом).
В зависимости от удельного веса лимфоидного компонента в тимоме дифференцируют лимфоидные (более 2/3 всех клеток опухоли представлено Т-лимфоцитами), лимфоэпителиальные (Т-лимфоциты составляют от 2/3 до 1/3 клеток) и эпителиальные тимомы (Т-лимфоцитами представлено менее 1/3 всех клеток).
Основываясь на степени инвазивного роста, выделяют 4 стадии тимомы:
Симптомы тимомы
Клинические проявления и течение тимомы зависит от ее типа, гормональной активности, размеров. Более чем в половине случаев опухоль развивается латентно и обнаруживается во время профилактического рентгенологического исследования.
Инвазивные тимомы вызывают компрессионный медиастинальный синдром, который сопровождается болями за грудиной, сухим кашлем, одышкой. Сдавление трахеи и крупных бронхов проявляется стридором, цианозом, дыхательной недостаточностью. При синдроме компрессии верхней полой вены возникает одутловатость лица, синюшность верхней половины туловища, набухание шейных вен. Давление растущей опухоли на нервные узлы обусловливает развитие синдрома Горнера, осиплость голоса, элевацию купола диафрагмы. Сдавливание пищевода сопровождается расстройством глотания – дисфагией.
По различным данным, от 10 до 40% тимом сочетаются с миастеническим синдромом. Больные отмечают снижение мышечной силы, быструю утомляемость, слабость мимических мышц, двоение в глазах, поперхивание, нарушения голоса. В тяжелых случаях может развиться миастенический криз, требующий перехода к ИВЛ и зондовому питанию.
В поздних стадиях злокачественной тимомы появляются признаки раковой интоксикации: лихорадка, анорексия, снижение массы тела. Нередко тимоме сопутствуют различные гематологические и иммунодефицитные синдромы: апластическая анемия, тромбоцитопеническая пурпура, гипогаммаглобулинемия.
Диагностика
Диагностика тимомы проводится торакальными хирургами с привлечением онкологов, рентгенологов, эндокринологов, неврологов. При клиническом осмотре может выявляться расширение вен грудной клетки, выбухание грудины в проекции опухоли; увеличение шейных, надключичных, подключичных лимфоузлов; признаки компрессионного синдрома и миастении. Физикальное исследование обнаруживает расширение границ средостения, тахикардию, свистящие хрипы.
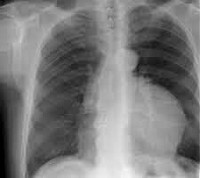
На рентгенограмме грудной клетки тимома имеет вид объемного образования неправильной формы, расположенного в переднем средостении. КТ грудной клетки значительно расширяет объем информации, полученный при первичной рентгендиагностике и в ряде случаев позволяет поставить морфологический диагноз. Уточнение локализации и взаимоотношения новообразования с соседними органами при КТ средостения позволяет в дальнейшем выполнить трансторакальную пункцию опухоли средостения, что чрезвычайно важно для гистологического подтверждения диагноза и верификации гистологического типа тимомы.
Для визуального исследования средостения и выполнения прямой биопсии проводится диагностическая медиастиноскопия, парастернальная торакотомия или торакоскопия. Диагноз миастении уточняется с помощью электромиографии с введением антихолинэстеразных препаратов. Дифференциально-диагностические мероприятия позволяют исключить другие объемные процессы в средостении: загрудинный зоб, дермоидные кисты и тератомы средостения.
Лечение тимом
Лечение опухолей вилочковой железы проводится в отделениях торакальной хирургии и онкологии. Хирургический метод является основным в лечении тимомы, поскольку только тимэктомия обеспечивает удовлетворительные отдаленные результаты. При доброкачественных тимомах оперативное вмешательство заключается в удалении опухоли вместе с вилочковой железой (тимомтимэктомия), жировой клетчаткой и лимфатическими узлами средостения. Такой объем резекции диктуется высоким риском рецидива опухоли и миастении. Операция выполняется из срединного стернотомического доступа.
При злокачественных новообразованиях тимуса операция может дополняться резекцией легкого, перикарда, магистральных сосудов, диафрагмального нерва. Послеоперационная лучевая терапия показана при II и III стадиях тимомы. Кроме этого, облучение является ведущим методом лечения неоперабельных злокачественных тимом IV стадии. В настоящее время большее значение в лечении инвазивных тимом получает трехэтапное лечение, включающее неоадъювантную химиотерапию, резекцию опухоли и лучевую терапию.
В послеоперационном периоде у больных, перенесших тимэктомию, может случиться миастенический криз, который требует проведения интенсивной терапии, трахеостомии, ИВЛ, длительного назначения антихолинэстеразных препаратов.
Отдаленные результаты лечения доброкачественных тимом хорошие. После удаления опухоли исчезают или значительно уменьшаются симптомы миастении. У больных злокачественной тимомой, прооперированных на ранних стадиях, 5-летняя выживаемость достигает 90%, на III стадии – 60-70%. Неоперабельные формы онкологического заболевания имеют плохой прогноз с летальностью 90% в течение ближайших 5 лет.
ЗАБОЛЕВАНИЯ ВИЛОЧКОВОЙ ЖЕЛЕЗЫ И ИХ ЛЕЧЕНИЕ
В. Л. Маневич, В. Д. Стоногин, Т. Н. Ширшова, И. В. Шуплов, С. В. Момотюк
Публикация посвящается памяти Василия Дмитриевича Стоногина (1933-2005)
Заболевания вилочковой железы изучаются врачами различных специальностей: невропатологами, эндокринологами, иммунологами, гемато¬логами, хирургами, патогистологами и др. Проблема миастении является относительно изученной; в последние годы установлено участие вилочковой железы в таком жизненно важном процессе, как выработка (регулировка) иммунитета.
Опухоли и кисты вилочковой железы, миастения и некоторые аутоиммунные заболевания требуют хирургического лечения. Значительный вклад в этот сложный раздел внесли отечественные и зарубежные хирурги (А. Н. Бакулев и Р. С. Колесникова; В. Р. Брайцев; Б. К. Осипов; Б. В. Петровский; М. И. Кузин и соавт.; С. А. Гаджиев и В. Васильев; Viets, и др.).
Из 66 больных 65 были оперированы: 62 произведена радикальная и 3 эксплоративная операция.
Клиника миастении хорошо известна, однако правильный диагноз больному с миастенией нередко ставят после продолжительного наблюдения. У 32 из 44 наших больных правильный диагноз был поставлен только через 6-8 месяцев после появления первых признаков заболевания. Это объяс¬няется малой выраженностью клинической картины миастении в начальной стадии и плохой осведомленностью практических врачей, к которым впервые обращаются за помощью больные миастенией (невропатологи, окулисты, отоларингологи, терапевты).
При выраженной генерализованной форме миастении диагноз не труден. В начальной стадии и в случаях, когда миастения носит локализован¬ный характер (бульбарная, глазная, скелетно-мышечная, глоточно-лицевая), у наших больных предполагались самые разнообразные диагнозы, вплоть до подозрения на симуляцию. Считаем необходимым подчеркнуть особую важность прозериновой пробы, имеющей дифференциально-диагностическое значение. У больных миастенией внутримышечная инъекция 1-2 мл 0,05% раствора прозерина устраняет мышечную слабость и быструю утомляемость, в то время как при миопатиях и мышечной слабости, вызванных другими причинами, инъекция прозерина не дает эффекта. Имеют значение динамометрия, эргометрия и электромиография.
Общепризнано, что лечение миастении должно проводиться комплексно с участием 3-4 специалистов: невропатолога, терапевта-эндокринолога, анестезиолога-реаниматолога и хирурга. На основании большого клинического материала (сотни оперированных и наблюдаемых в отдаленном периоде) авторы подчеркивают преимущество оперативного лечения миастении перед консервативным (М. И. Кузин; А. С. Гаджиев и соавт., и др.). Результаты оперативного лечения лучше, если операцию производят впервые 2-2,5 года от начала заболевания. В более поздние сроки операция оказывается менее эффективной. Отсюда вытекает особая важность ранней диагностики миастении.
Наличие у больного выраженной клинической картины прогрессирующей миастении является показанием к операции, так как все консервативные методы лечения, включая и рентгенотерапию, дают лишь временное улучшение.
Вопрос о необходимости предоперационной рентгенотерапии нельзя считать окончательно решенным. Только 5 из наших больных перед операцией получали рентгеновское облучение, причем каких-либо улучшений в течении послеоперационного периода мы у них не отметили. У больных, оперированных по поводу злокачественной тимомы с явлениями миастении, предоперационное облучение играет важную роль в ближайшем исходе операции и в какой-то степени влияет на сроки наступления рецидива заболевания (М. И. Кузин и соавт.).
Большинство операций по поводу миастении нами выполнено из переднего доступа путем полной срединной продольной стернотомии. Наиболее ответственным моментом операции является отделение железы от левой плечеголовной вены. Ранение этого сосуда опасно из-за массивного кровотечения и возможной воздушной эмболии. В одном случае произошло ранение этой вены, закончившееся благополучно (был наложен боковой сосудистый шов). При операции следует избегать наложения зажимов на железистую ткань, раздавливания её.
У 3 наших больных было сочетание миастении и загрудинного зоба. Произведены тимэктомия и субтотальная струмэктомия.
У 26 больных во время операции была повреждена медиастинальная плевра, в том числе у 8 больных с обеих сторон. Осложнений, связанных с операционным пневмотораксом, не было. Если во время операции плевра не повреждена, переднее средостение дренируется одной резиновой трубкой, конец которой выводят в нижний угол раны или через отдельный прокол ниже мечевидного отростка и соединяют с отсосом. Вслед за тимэктомией трахеостома (превентивно) была наложена 5 больным.
Если сама операция тимэктомии по сравнению с другими торакальными операциями не представляет особой сложности, то течение послеоперационного периода у ряда больных сопровождается осложнениями, на 1-м месте среди которых стоит миастенический криз. Поэтому операции по поводу миастении возможны только в тех учреждениях, где можно обеспечить круглосуточное наблюдение анестезиолога-реаниматолога, а также многодневную аппаратную вентиляцию лёгких.
Вопрос о назначении антихолинэстеразных препаратов в послеоперационном периоде окончательно не решен. С целью уменьшения гиперсекреции бронхов лучше назначать прозерин с небольшими дозами атропина.
Тяжелый миастенический криз с расстройством дыхания, сердечной деятельности, глотания и т. д. наблюдали в первые дни после операции у 26 больных. Вывести из криза консервативными мероприятиями удалось 7 больных; 19 больным была наложена трахеостома с переводом их на аппаратное дыхание, длительность которого составляла от 3 до 40 суток. Через трахеостому систематически круглосуточно аспирируют слизь из трахеобронхиального дерева. Питание больных, находящихся на аппаратном дыхании, осуществляется через зонд. Помимо медикаментозного лече¬ния, применения кислорода, использования дыхательной гимнастики, в последние годы всем больным миастенией в послеоперационном периоде проводится лечебный массаж всего тела, повторяемый несколько раз в день.
Трахеостомическую трубку удаляют после того, как у больного стойко восстанавливается самостоятельное дыхание.
Среди наших больных мы наблюдали 3 (2 мужчин и 1 женщину, все старше 40 лет) с липотимомой. У них опухоль была небольших размеров, с ровными четкими границами; опухоль была расценена нами как доброкачественная. Заболевание сопровождалось умеренно выраженными явлениями миастении. Один из этих больных поступил с жалобами на слабость и быструю утомляемость; при дальнейшем обследовании у него была выявлена тяжелая гипопластическая анемия. Больной оперирован; в ближайшем послеоперационном периоде отмечены благоприятные результаты.
Из 15 наших больных с доброкачественными тимомами у 9 (4 мужчин и 5 женщин) были явления миастении, у остальных опухоль ничем себя не проявляла и была выявлена случайно.
Больной М., 19 лет, поступил 17.III.1966 года. Жалоб нет. После окончания средней школы при прохождении медицинского обследования для поступления в учебное заведение у него рентгенологически было выявлено опухолевое образование в переднем средостении. Признаков миастении нет. Пневмомедиастинография: в переднем средостении со всех сторон окутанное газом образование продолговатой формы размером 15*5 см, с участками просветления в центре; заключение: опухоль вилочковой железы, возможно, с участками распада. Произведена тимэктомия. Гистологически: злокачественная тимома ретинулоклеточного типа. Проведена послеоперационная рентгенотерапия. Осмотрен через 4 года после операции:, жалоб нет, состояние хорошее, признаков рецидива нет.
Дифференциальный диагноз доброкачественных и злокачественных тимом нередко бывает трудным. Злокачественная тимома по рентгенологическим признакам напоминает лимфогранулематоз и лимфосаркому. В отличие от этих образований тимома располагается непосредственно за грудиной, обычно бывает овально-сплющенной или конусовидной формы. Всякая тимома, протекает она с явлениями миастении или без них, подлежит удалению, В литературе имеются указания, что каждую тимому следует рассматривать как потенциально злокачественную опухоль (Б. В. Петровский; Seybold и соавт., и др.).
Вопрос о возможности изолированного поражения вилочковой железы лимфогранулематозом представляется спорным. Мы наблюдали 2 больных, у которых до операции был установлен диагноз “опухоль вилочковой железы”. После операции, при гистологическом исследовании препаратов, диагноз был изменен: изолированное поражение лимфогранулематозом вилочковой железы. Принимая во внимание указания о возможности изолированного поражения вилочковой железы на ранних стадиях заболевания (С. А. Гаджиев и В. В. Васильев), оба эти наблюдения мы отнесли к патологии вилочковой железы. После операции за больными ведётся наблюдение в течение 5 лет. Признаков рецидива и генерализации процесса нет.
Заболевание, заключающееся в сочетании патологии вилочковой желе¬зы и гипопластической анемии, которая возникает вследствие избирательного поражения костного мозга без изменения продукции лейкоцитов и тромбоцитов, впервые описано Кацнельсоном в 1922 году. Позже было предположено, что вилочковая железа влияет на гемопоэтическую функцию костного мозга, регуляцию состава белковых фракций, состояние лимфоидной системы и т. д. (Soutter и соавт.). С тех пор опубликованы данные некоторых авторов об отдельных операциях на вилочковой железе при различных болезнях крови (А. Н. Бакулев, 1958; Chaemers и Boheimer, и др.). К настоящему времени нами произведены 4 операции тимэктомии у больных гипопластической анемией. О результатах этих операций говорить пока рано, так как после них прошел небольшой срок. Ближайшие результаты удовлетворительные у 3 больных.
1) Бакулев А. Н., Колесникова Р. С. Хирургическое лечение опухолей и кист средостения. М., 1967.
2) Брайцев В. Р. Врожденные дизонтогенетические образования средостения и легких. М., 1960.
3) Гаджиев С. А., Догель Л. В., Ваневский В. Л. Диагностика и хирургическое лечение миастении. Л., 1971.
4) Гаджиев С. А., Васильев В. Мед газета, 1973, №15.
5) Кузин М. И. Клин мед, 1969, № 11, с. 6.
6) Кузин М. И., Успенский Л. В., Волков Б. П. Вести, хир., 1972, №7, с.48.
7) Осипов Б. К. Хирургические заболевания легких и средостения. М., 1961.
8) Петровский Б. В. Хирургия средостения. М., 1960.
9) Andгus W., Fооt N., J. thorac. Surg., 1937, v. 6. p. 648.
10) Chaemers G., Boheimer K., Brit. med. J., 1954, v.2, p.1514.
11) Pope R., О s g о о d R., Am. J. Path., 1953, v. 20, p. 85.
12) S е у b о 1 d W., D о n a 1 d М. С., J. thorac. Surg. Clagett C. et al., 1950, v. 20, p.195.
13) Soutter G., Sommers Sh. R e 1 m о n Ch. et al. Ann. Surg., 1957, v. 146, p. 426.
14) Viets H., Brit. med. J., 1950, v. 1, p.139.
| 1) Виктор Львович Маневич – профессор, доктор медицинских наук, 2-я кафедра клинической хирургии ЦОЛИУв. |  |
| 2) Василий Дмитриевич Стоногин – доцент 2-й кафедры хирургии ЦОЛИУв, заведующий учебной частью кафедры, кандидат медицинских наук. E-mail: svas70@mail.ru |  |
Любое копирование материала запрещено без письменного разрешения авторов и редактора.
Работа защищена Федеральным законом о защите авторских прав РФ.
Самый загадочный орган иммунной системы
Вплоть до средних веков одним из претендентов на роль телесного вместилища души считался тимус. В наши дни самой удивительной особенностью этого органа называют его склонность к раннему старению и полной деградации с возрастом. Почему так происходит? Если взрослые могут обходиться без этой железы, то зачем она нужна детям?
Вилочковая железа
Тимус относится к центральным элементам иммунной системы. Свое название железа получила в честь душистого растения чебрец (Thymus), из клеток которой было выделено азотистое основание тимин, входящее в состав ДНК. Это небольшой орган розовато-серого цвета, мягкой консистенции, расположенный в центральной части грудной клетки. Он покрыт капсулой из плотной соединительной ткани, от которой в глубину отходят перемычки, делящие его на дольки. Верхние, более узкие, концы долей выходят за пределы грудной полости, иногда достигая щитовидной железы. Доли тимуса напоминают двузубую вилочку, что и дало название этому органу — «вилочковая железа».
Если тимус недостаточно развит, как, например, при таком генетическом заболевании, как синдром ДиДжорджи, то у детей развивается врожденный иммунодефицит. Болезнь приводит к уменьшению количества Т-лимфоцитов в крови и проявляется повышенной чувствительностью к вирусным, грибковым и некоторым бактериальным инфекциям. Иногда в зрелом возрасте наблюдается особое нарушение иммунологических процессов, связанное с патологией тимуса и других лимфоидных органов, что может быть причиной внезапной смерти от наркоза во время операции.
Его задача — обнаружить клетки, которые в силу различных повреждений превратились в чужеродные, например, под воздействием вируса
Клетки-няньки и школа для лимфоцитов
В отличие от костного мозга, который дает начало практически всем клеткам иммунной системы (эритроцитам, тромбоцитам, гранулоцитам, моноцитам, лимфоцитам), тимус «специализируется» на продукции исключительно Т-лимфоцитов. Буква Т в названии указывает 
Часовые клеточного иммунитета
На внешней оболочке Т-лимфоцитов находятся белки, распознающие специфичные молекулы тканевой совместимости данного организма. Т-лимфоцит похож на часового, который охраняет организм от чужаков, спрашивая «пароль» у каждой клетки, встречающейся на его пути. Его задача — обнаружить клетки, которые в силу различных повреждений превратились в чужеродные, например, под воздействием вируса. Если клетка выглядит подозрительно, то она незамедлительно подлежит разрушению. Для выполнения этой функции Т-лимфоциты должны быть способны распознать собственные антигены тканевой совместимости, специфичные для каждого организма. При этом Т-лимфоциты не должны реагировать на аутоантигенные пептиды, связанные с собственными антигенами тканевой совместимости. Из широчайшего спектра вариантов антигенов тканевой совместимости лишь немногие экспрессированы на клетках данного индивида и нуждаются в распознавании Т-лимфоцитами. Именно поэтому селекция тимоцитов сопровождается большими энергетическими затратами и 95% гибелью. Зато зрелые периферические Т-лимфоциты живут долго и способны отвечать клональной экспансией в случае встречи со специфическим чужеродным антигеном.
Размеры тимуса являются максимальными в детском возрасте, но после начала полового созревания этот орган подвергается значительной атрофии и инволюции
Инволюция тимуса
Размеры тимуса являются максимальными в детском возрасте, но после начала полового созревания этот орган подвергается значительной атрофии и инволюции. У новорожденного тимус уже полностью развит и в течение первого года жизни достигает максимальных размеров — 25 см3: его длина составляет 5 см, ширина — 4 см, толщина — 6 мм. У 6-месячного ребенка масса тимуса достигает от 12 до 20 г, что составляет 0,5% массы тела. Сложная структура и напряженное функционирование железы сохраняются в течение первых 2–3 лет жизни. Самая высокая продукция Т-лимфоцитов происходит до 2 лет, а затем быстро уменьшается. Тимус продолжает расти до наступления половой зрелости, достигая максимального размера (длина до 7,5–16 м) и массы (35–40 г), а после 14–15 лет начинается процесс инволюции. К 20 годам половина функционирующей ткани тимуса замещается жировой тканью и у 25-летних масса железы уменьшается до 25 г с сохранением ее общих очертаний. В течение первых 50 лет жизни ежегодно теряется по 3% истинно тимической ткани. К 50–60 годам инволюция тимуса завершается, его масса составляет менее 15 г, а к 70–75 — около 6 г. Атрофии подвергаются главным образом латеральные участки железы и отчасти нижние, так что железа у взрослого человека принимает более удлиненную форму. По мере инволюции тимус утрачивает былой цвет и за счет увеличения в нем доли стромы и жировых клеток становится более желтым. Вместе с деградацией органа значительно уменьшается и почти полностью прекращается выработка Т-лимфоцитов, с чем отчасти связывают снижение иммунитета у лиц пожилого возраста.
Почему тимус деградирует?
Из всех органов иммунной системы только для тимуса характерна возрастная инволюция. Однако следует отметить, что количество Т-лимфоцитов долгое время сохраняется на достаточном уровне. Дело в том, что значительную часть популяции Т-лимфоцитов составляют долгоживущие клетки, которые не нуждаются в постоянном обновлении. Более того, зрелые Т-лимфоциты подвергаются так называемой колониальной экспансии, то есть избирательной пролиферации при встрече со своим антигеном, за счет чего их численность увеличивается, поэтому количество Т-клеток может поддерживаться во взрослом организме и при отсутствии тимуса. Кроме того, иммунная система располагает некоторыми компенсаторными возможностями для замещения отдельных функций недостающих Т-лимфоцитов. Да и в целом необходимость в генерации новых Т-лимфоцитов с возрастом снижается. Первичные контакты с инфекционными агентами происходят в основном в первые годы жизни, а в дальнейшем встреча с новыми патогенами случается не так часто, поэтому энергозатраты на содержание тимуса становятся нецелесообразными. К тому же постоянная активность тимуса с возрастом чревата развитием стрессовой гиперчувствительности иммунной системы, имеющей патологические последствия.
Тимусзависимая старость
Как видим, возрастная инволюция тимуса не вызывает катастрофического снижения иммунитета. Однако встреча с вирусами кори или ветрянки приводит к более тяжелым осложнениям у взрослых по сравнению с детьми, у которых тимус функционирует в полную силу. Не зря именно в течение первых трех лет жизни, то есть в период «расцвета» тимуса, врачи стараются вакцинировать ребенка против всех наиболее опасных и частых инфекционных заболеваний: туберкулеза, полиомиелита, дифтерии, столбняка, коклюша, кори. В этом возрасте иммунная система организма, как правило, отвечает на введение вакцины выработкой активного иммунитета, в частности путем формирования клонов долгоживущих Т-клеток. Благодаря этому впоследствии при встрече с болезнетворным микроорганизмом включается сигнал колониальной экспансии, активирующий Т-лимфоциты. Несмотря на это, предполагают, что возрастное ослабление иммунной системы, проявляющееся в виде слабой устойчивости к инфекциям, невосприимчивости к вакцинам и аутоиммунным заболеваниям, обусловлено прежде всего старением тимуса. Ведь разнообразные инфекции атакуют человека на протяжении всей его жизни, и «запастись» специфичными иммунными клетками на все случаи практически невозможно, да и запас Т-лимфоцитов постепенно исчерпывается.
Из всех органов иммунной системы только для тимуса характерна возрастная инволюция. Однако следует отметить, что количество Т-лимфоцитов долгое время сохраняется на достаточном уровне
Можно ли «омолодить» тимус?
Фактически тимус начинает деградировать с первых лет жизни, однако это становится заметно в период полового созревания. Закономерно, что инволюция тимуса напрямую связана с влиянием половых гормонов. Отмечено, что инволюцию тимуса способны замедлить пептиды шишковидной железы. Аналогичным образом действует ее гормон мелатонин, способный даже вызывать «омоложение» органа. Поскольку с возрастом ткань тимуса заменяется жировыми клетками, логично, что тимус довольно хорошо восстанавливается при соблюдении низкокалорийной диеты. Способствует этому, скорее всего, «гормон голода» — грелин, правда, у него есть побочный эффект в виде ослабления сексуальной мотивации. У людей старше 70 лет отмечен более разнообразны набор Т-клеточных рецепторов по сравнению с теми, которые еще не преодолели 70-летний рубеж. Удивительно, что продукция Т-лимфоцитов тимусом, пусть и в небольшом количестве, сохраняется даже у людей 100-летнего возраста. При этом у долгожителей менее выражены популяции клеток-клонов — то есть клеток, произошедших от одного активированного Т-лимфоцита. Возможно, именно эти особенности иммунитета позволяют долгожителям лучше противостоять инфекциям и быть более здоровыми. При этом возникает «тимусная селекция», в результате которой люди со сниженным иммунитетом реже становятся долгожителями.
Теперь понятно, почему тимус деградирует с возрастом. Во-первых, производство каждого Т-лимфоцита является слишком энергозатратным процессом. Во-вторых, клетки, прошедшие все этапы созревания, дифференцировки и отбора, могут жить долго и в случае необходимости размножаться клонированием. В-третьих, специфичные наборы клеточных рецепторов практически на все случаи чужеродных антигенов способны сформироваться в течение первого десятилетия жизни, а затем шанс столкнуться с новым инфекционным агентом значительно уменьшается. В-четвертых, подвергать организм иммунологическому стрессу без острой на то необходимости не только нецелесообразно, но и крайне опасно
Татьяна Кривомаз, канд. биол. наук
Список литературы находится в редакции