Нейробластома
Что такое нейробластома?
Чаще всего нейробластома возникает в брюшной полости и часто развивается в нервной ткани надпочечников, которые располагаются над верхней частью почек.
нейробласты
Нейробласты — это клетки, рост которых происходит на очень ранних этапах развития плода, как только ребенок начинает формироваться в теле матери. Эти клетки созревают с образованием нервных клеток симпатической нервной системы (СНС). Иногда в развитии нейробластов происходят отклонения, которые могут формировать опухоли. Как правило, нейробластомы обнаруживаются в основных органах симпатической нервной системы, расположенных по обе стороны спинного мозга и в надпочечниках.
Нейробластома обычно диагностируется у детей младше 5 лет. Это самая распространенная опухоль у грудных детей. На ее долю приходится 50% случаев рака у грудных детей и 7–10% всех случаев детского рака. Каждый год в США диагностируется около 650 новых случаев.
Лечение нейробластомы зависит от стадии заболевания (от того, насколько опухоль успела распространиться от первичного очага). Некоторым детям достаточно только хирургической операции. Пациентам с более тяжелым течением заболевания требуется интенсивное лечение, включающее хирургическую операцию, химиотерапию, лучевую терапию и/или иммунотерапию.
Факторы риска и причины возникновения нейробластомы
Определенные факторы могут повышать риск развития нейробластомы. Такие опухоли наиболее часто развивается у детей младшего возраста, несколько чаще у мальчиков, чем у девочек.
У небольшого числа пациентов (1-2%) отмечается наследственная нейробластома. Эта разновидность заболевания может передаваться из поколения в поколение. Наследственная нейробластома чаще всего вызывается изменением, или мутацией в генах ALK или PHOX2B. У детей с наследственной нейробластомой вероятность передачи заболевания своим детям составляет 50%.
Признаки и симптомы нейробластомы
Признаки и симптомы нейробластомы зависят от расположения опухоли и возраста ребенка. К ним относятся:
Другие симптомы нейробластомы могут включать в себя хроническую диарею, изменения движений глаз, высокое кровяное давление, головную боль, кашель, затрудненное дыхание, жар, образование гематом или синдром Горнера.
Синдром Горнера
| Расположение опухоли | Симптомы |
|---|---|
| Глаз | Экзофтальм, темные круги вокруг глаз («глаза енота»), слепота, синдром Горнера |
| Шея | Уплотнение или отек, синдром Горнера |
| Живот | Уплотнение, потеря аппетита, рвота, запор |
| Таз | Нарушение функции тазовых органов, нарушение работы кишечника или мочевого пузыря |
| Спинной мозг | Слабость, паралич |
Диагностика нейробластомы
Для диагностики нейробластомы применяются различные виды процедур и исследований. К ним относятся:
Изображение нейробластомы, полученное в ходе сканирования с МЙБГ.
Нейробластома левого надпочечника что это
Нейробластома и пограничные (смежные) опухоли по происхождению представляют собой ткани нервного гребня в мозговом веществе надпочечника (хромаффинная ткань) и симпатической нервной системе. Это необычная опухоль, способная иногда к спонтанному регрессу у младенцев.
Существуют различные варианты болезни — от доброкачественного (ганглионеврома) до злокачественного (нейробластома).
Нейробластому наиболее часто обнаруживают в возрасте до 5 лет. У большинства детей выявляют абдоминальное объёмное образование, но первичная опухоль может находиться где-либо по ходу симпатического ствола от шеи до таза. Классически абдоминальные поражения имеют надпо-чечниковое происхождение, но при манифестации заболевания объёмное образование часто бывает большим, пересекает срединную линию и окружает магистральные кровеносные сосуды и лимфатические узлы.
Паравертебральные опухоли могут проникать через межпозвонковое отверстие и вызывать сдавление спинного мозга. После 2-летнего возраста клинические симптомы главным образом, бывают результатом метастатической болезни: болевой синдром в костях, миелодепрессия, потеря массы тела и недомогание.
Диагноз часто можно выставить на основании характерных клинических и радиологических признаков и повышения содержания катехоламинов в моче (VMA, гомованилиновая кислота). Диагноз обычно подтверждают биопсией, метастазы выявляют при исследовании образцов костного мозга, сканировании костей и MIBG (метайодобензилгуа-нидин) сцинтиграфией.
MIBG — меченный радиоактивным изотопом специфичный для опухоли агент — обеспечивает чувствительную визуализацию, позволяющую оценить стадию болезни и проводить мониторинг ответа на лечение. Роль его терапевтического использования не установлена.
Самые важные прогностические клинические особенности — возраст и стадия болезни на момент постановки диагноза. К сожалению, большинство детей старше 1 года манифестируют при уже запущенной стадии болезни и имеют плохой прогноз. Всё шире используют информацию о биологических особенностях нейробластомы для терапии и прогноза.
Сверхэкспрессия онкогена «N-myc» свидетельствует о делении материала в хромосоме 1 (del 1р) и об увеличении генетического материала в хромосоме 17q в клетках опухоли; это свидетельствует о более плохом прогнозе.
Немногих детей с локализованными первичными поражениями без метастазов можно излечить с использованием только хирургического метода. Для большинства больных в запущенных случаях главенствующую роль играет химиотерапия. Детям, дающим хороший начальный ответ, может быть показана консолидация с химиотерапией высокой дозы с предварительным сохранением стволовых клеток, взятых из периферической крови.
К сожалению, риск рецидива высок и перспектива лечения для детей с метастазами всё ещё остаётся немного выше 30%.
Скрининг повышенного содержания катехоламинов в моче для идентификации бессимптомных форм болезни у маленьких детей в принципе выполним, но нет никаких свидетельств того, что это уменьшает смертность, данную процедуру не осуществляют в Великобритании.
Пример нейробластомы у ребенка. Джека, 2-летнего мальчика, мать привела к врачу общей практики вследствие общего плохого самочувствия и отсутствия аппетита. Незадолго до этого ребёнок неохотно стал гулять и иногда кричал, когда его брали на руки. Раньше он нормально спал, однако теперь его сон нарушился, а бабушка Джека заметила, что мальчик стал бледным и потерял в весе.
При осмотре врач общей практики подтвердил неважное самочувствие ребёнка и забеспокоился, обнаружив возможную опухоль в верхней части брюшной полости. Мальчика срочно госпитализировали в местную клинику, где ему провели УЗИ, подтвердившее наличие абдоминальной опухоли, кроме того, была выявлена гипертензия. МРТ-исследование подтвердило наличие очень большой опухоли в верхней части брюшной полости, которая находилась в сложном взаимоотношении с левой почкой и крупными сосудами, предположительно нейробластомы.
Последующие исследования подтвердили инфильтрацию костного мозга опухолевыми клетками, а положительный результат MIBG-сканирования, показывающего захват в первичном и отдалённых очагах, согласовывался с наличием метастазов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Нейробластома плода. Возможности пренатальной диагностики и прогноз
УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Введение
Обычно поражение изолированное, с вовлечением одного надпочечника, двустороннее поражение встречается редко [5]. Иногда антенатально появляются метастазы в печень, кожу, костный мозг и редко в ворсинки плаценты [6]. В этом случае плацента выглядит объемной, но метастатические очаги могут не определяться макроскопически, а диагностируются лишь при гистологическом исследовании. Сосуды ворсинок плаценты содержат скопления клеток нейробластомы, но инвазия стромы наблюдается исключительно редко [7]. Описаны случаи метастазирования в пуповину с последующей гибелью плода [8]. Нейробластомы преимущественно состоят из нейробластов. Макроскопически очаги опухоли хорошо очерчены, но могут инфильтрировать окружающие ткани, капсула отсутствует.
В литературе описан ранний случай диагностики нейробластомы в 19 нед беременности, однако обычно пренатальный диагноз устанавливается при ультразвуковом исследовании в промежутке от 26 до 39 нед гестации [8].
Первое сообщение о пренатальной диагностике нейробластомы датировано 1983 г. [9]. Ультразвуковая картина зависит от размеров, локализации и секреторной активности опухоли. Нейробластомы часто не диагностируются пренатально из-за их малых размеров. При ультразвуковом исследовании нейробластома визуализируется как образование, расположенное забрюшинно, между почкой и диафрагмой, смещающее почку книзу и латерально. Структура ее смешанная, с солидными и кистозными компонентами [10, 11]. В очагах больших размеров могут определяться дегенеративные признаки: кистозные изменения, кровоизлияния, кальцификаты [11, 12]. Иногда имеют место гидронефроз и многоводие, а также водянка плода.
Смещение нижней полой вены визуализирующимся образованием кпереди следует расценивать как признак забрюшинного происхождения этого образования [13]. Кроме того, при больших размерах опухоль надпочечника может смещать окружающие органы.
Цветовое допплеровское картирование помогает идентифицировать питающий опухоль сосуд, отходящий непосредственно от аорты, однако такой единственный сосуд может и не визуализироваться [13].
Как правило, антенатальная диагностика метастазов возможна исключительно редко, так как специфических поражений плаценты при ультразвуковом исследовании не отмечается, описано лишь неспецифическое ее утолщение [14]. В диагностике метастазов может быть информативной МРТ плода.
Геморрагические опухоли надпочечников могут осложняться анемией плода, неиммунной водянкой плода или массивной инвазией печени [10]. Предложены различные объяснения этиологии развития водянки плода: избыточная продукция катехоламинов, приводящая к гипертензии и сердечной недостаточности у плода; вовлечение в патологический процесс печени, вызывающее нарушение венозного возврата и развитие гипопротеинемии [14]; инвазия эритропоэтической ткани клетками опухоли, приводящая к развитию тяжелой анемии или даже гиперсекреции альдостерона корой надпочечников. Кроме того, описано возникновение водянки плода вторично к появлению метастазов в плаценту. Отек плаценты вследствие механического эффекта большого образования может развиваться в некоторых случаях нейробластомы без метастазирования в плаценту [6].
Кроме того, опухоли надпочечников больших размеров могут приводить к дистоции во время родов [8].
Следует помнить и о материнских осложнениях. Очень редко гиперпродукция катехоламинов опухолью надпочечников плода может вызывать избыточное потоотделение, развитие гипертензии и преэклампсии у матери, материнского миррор-синдрома при поражении плаценты [12, 14, 15]. Кроме того, развитие таких материнских осложнений, как правило, связано с высоким уровнем неонатальной смертности, достигающим 70% [1].
Сонографическое установление стадии опухолевого процесса у плода затруднено, но есть сообщения, что при отсутствии симптомов преэклампсии у матери риск широко диссеминированного процесса невысок [8].
Обнаружение кальцификатов в опухоли при ультразвуковом исследовании сочетается с лучшим прогнозом, вероятно, вследствие того, что кальцификаты являются свидетельством произошедшего некроза опухоли [12].
Нейробластома in situ может не проявлять себя клинически и даже подвергаться спонтанной регрессии [17, 18].
Течение заболевания у пациентов с нейробластомой, диагностированной пренатально, обычно благоприятное, особенно при изолированном поражении надпочечников [8]. Методом лечения (с хорошими результатами) является хирургическое удаление опухоли непосредственно после рождения [19], химиотерапия показана только в случаях существенного прогрессирования заболевания [20]. Пациенты с «благоприятными» признаками заболевания (небольшие размеры опухоли, ее кистозная структура, отсутствие прогрессирования) должны тщательно наблюдаться и подвергаться хирургическому лечению только при отсутствии регресса образования [11].
Материалы и методы
В качестве иллюстрации приводим одно из наших клинических наблюдений.
Пациентка Т., 40 лет, обратилась для проведения планового скринингового ультразвукового исследования в 32 нед. В ходе предыдущих исследований в 13 и 19 нед патологии не было выявлено.
Супруги здоровы, профессиональных вредностей не имеют. Наследственность не отягощена. Настоящая беременность пятая. В анамнезе двое нормальных родов, два медаборта. На учете в женской консультации пациентка состояла с 6 нед. Беременность протекала без существенных осложнений. Лишь в срок 6-7 нед была диагностирована угроза невынашивания.
Ультразвуковое обследование проводилось на УЗ-сканере SonoAce-X8 (Medison).
Результаты
При ультразвуковом исследовании обнаружен один живой плод мужского пола. Гестационный срок составил 31 нед 4 дня. Фетометрические показатели соответствовали данному сроку, за исключением окружности живота, превышающей 95-й процентиль за счет гепатомегалии. Нарушений фето-плацентарного кровотока не было выявлено. Патологических изменений плаценты и околоплодных вод не отмечено.
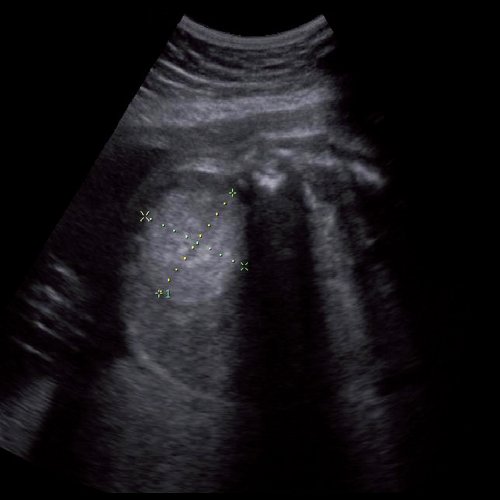
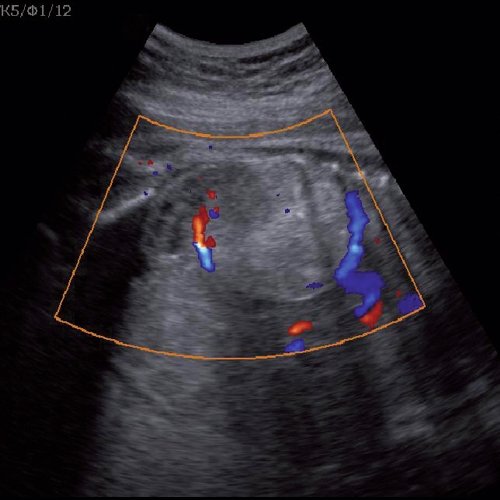
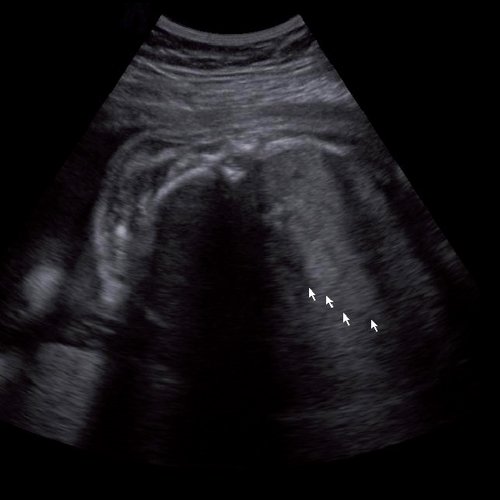
Под диафрагмой справа визуализировалось гиперэхогенное опухолевидное образование несколько неоднородной солидной структуры, с четкими ровными контурами, размером 50x38x35 мм. К нижнему полюсу данного образования прилежала правая почка, имеющая нормальные размеры, форму и структуру. Нижняя полая вена была смещена кпереди и влево. Обращала на себя внимание выраженная гепатомегалия, причем структура печени не была однородной. Она содержала множественные гиперэхогенные включения размерами до 17 мм, окруженные тонким гипоэхогенным периферическим ободком. Цветовое допплеровское картирование(ЦДК) демонстрировало интенсивную периферическую васкуляризацию опухоли (рис. 1-3).
Рис. 1. Нейробластома правого надпочечника плода. Беременность 31 нед 4 дня.
Рис. 2. Кровоток в нейробластоме плода. Цветовое допплеровское картирование. Отчетливо виден питающий сосуд, огибающий образование по его периферии. К нижнему полюсу образования прилежит интактная почка плода.
Был поставлен диагноз: беременность 31 нед 4 дня. Опухоль правого надпочечника плода с метастазами в печень. Рекомендовано динамическое ультразвуковое наблюдение за темпами роста новообразования и возникновением возможных осложнений.
В срок 32 нед 4 дня была диагностирована антенатальная гибель плода. Родился мертвый ребенок, мужского пола весом 2480 г, длиной 45 см.
Обсуждение
Кровоизлияние в надпочечники, как правило, выглядит эхогенным или неоднородной структуры образованием, иногда может быть полностью анэхогенным и характеризуется изменением ультразвуковой картины при динамическом исследовании, постепенно превращаясь в анэхогенное кистозное образование, в котором с течением времени отмечается утолщение его стенки [13] и образуются кальцификаты. Энергетический допплер демонстрирует полную аваскулярность такого образования. В нашем случае образование имело повышенную эхогенность, несколько неоднородную структуру. При ЦДК в опухоли регистрировался преимущественно периферический кровоток.
Опухоль Вильмса поражает почку (чаще правую), которая в представленном случае была интактна.
Экстралобарная легочная секвестрация является преимущественно левосторонним супраренальным образованием с четким наружным контуром, как правило, гиперэхогенной однородной структурой неправильной формы. Выявляется эта патология уже во II триместре беременности, при ЦДК определяется питающий сосуд.
Тератомы (в том числе и забрюшинной локализации) всегда представлены образованиями неоднородной солиднокистозной структуры вследствие их гистологического строения.
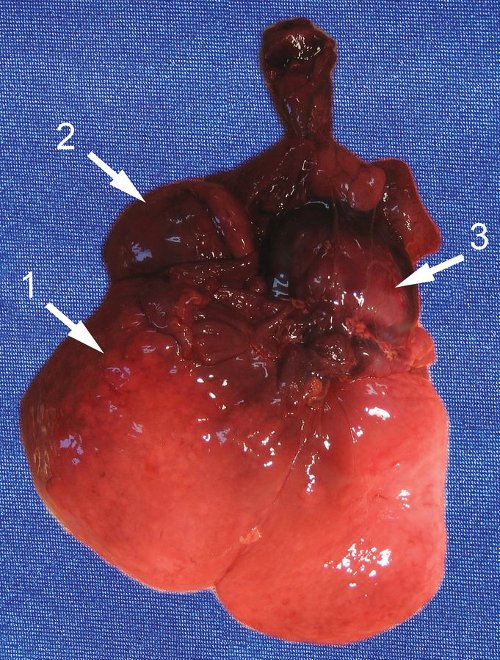
Таким образом, обнаруженное нами образование было отнесено к опухоли надпочечника даже при отсутствии классической картины нейробластомы. Обращали на себя внимание большой размер опухоли и отсутствие выраженных осложнений в виде многоводия, застойной сердечной недостаточности, нарушения фето-плацентарного кровотока. При этом относительно ранняя манифестация (выявление данного комплекса изменений уже в 31 нед), не совсем типичная ультразвуковая морфология опухоли, наличие выраженной гепатомегалии и множественных метастазов позволяли сделать вывод о злокачественном течении заболевания, что, видимо, и обусловило антенатальную гибель плода. В итоге диагноз был подтвержден патоморфологическим исследованием. У недоношенного плода мужского пола живот увеличен в объеме. Справа в забрюшинном пространстве определяется округлое образование (опухоль) размером 50?35?30 мм, эластичной консистенции. Спереди и снизу к опухоли прилежит почка, плотно с ней спаянная. Опухоль исходит из правого надпочечника, который находится на ее верхнем полюсе в виде «шапочки». На разрезе опухоль однородная, желтовато-серая. Левые надпочечники и почка обычного вида. Печень значительно увеличена, занимает около 1/2 объема брюшной полости, доли четко не дифференцируются. Поверхность печени коричневато-красная. На разрезах определяются множественные плотные эластичные узлы диаметром до 15 мм бледно-желтого цвета (рис. 4, 5).
Нейробластома
В 1910 году Wright доказал, что развивается она из эмбриональных нейробластов симпатической нервной системы и дал ей настоящее название. Это наиболее частая экстракраниальная солидная бластома, встречающаяся у детей, и составляет 14% всех новообразований детского возраста.
Несмотря на определенные успехи в лечении детей с этим заболеванием, все еще имеется много проблем, особенно при наличии отдаленных метастазов у детей старше 1 года. Последние, уже при установлении первичного диагноза, встречаются в 70% случаев.
Число неустановленных зон первичного развития опухоли было в 17% случаев. Нейробластома имеет тенденцию к метастазированию в определенные зоны, такие как кости, костный мозг, лимфатические узлы. Редко отсевы опухоли встречаются в коже и печени; как исключение, поражается головной мозг. Нейробластомы раннего детского возраста обладают удивительной способностью, а именно, способностью к спонтанному созреванию в ганглионеврому. Интересно, что Нейробластома нередко случайно, при микроскопическом исследовании обнаруживается у маленьких детей, погибших от неопухолевых заболеваний. Это говорит о том, что ряд этих бластом протекает бессимптомно и спонтанно регрессирует.
Что провоцирует / Причины Нейробластомы:
Многие исследователи полагают, что нейробластома возникает в том случае, когда нормальные эмбриональные нейробласты не созревают в нервные клетки или клетки коры надпочечников. Вместо этого, они продолжают расти и делиться.
Нейробласты могут полностью не созреть к моменту рождения ребенка. В действительности, показано, что небольшие скопления нейробластов часто выявляются у младенцев до 3-месячного возраста. Большинство таких клеток в итоге созревают в нервные клетки и не образуют нейробластому. Иногда нейробласты, остающиеся у младенцев, продолжают расти и образуют опухоль, которая может даже метастазировать в различные органы. Однако многие такие опухоли, в конце концов, созревают или исчезают.
По мере роста ребенка вероятность созревания таких клеток уменьшается, а вероятность формирования нейробластомы увеличивается. При достижении нейробластомой больших размеров и появлении симптомов созревание клеток прекращается, они продолжают расти и распространяться, если не проводится лечение.
У некоторых онкологических больных имеются мутации (изменения) ДНК, которые они унаследовали от одного из родителей, что повышает риск развития опухоли. Некоторые полагают, что некоторые семейные случаи нейробластом возникли в результате наследуемых мутаций гена, угнетающего опухолевый рост.
Большинство нейробластом не являются следствием наследуемых мутаций ДНК. Они вызваны мутациями, приобретенными в ранний период жизни ребенка. Эти мутации присутствуют в опухолевых клетках родителя ребенка и не передаются детям. Причины, вызывающие изменения ДНК, приводящие к возникновению нейробластом, не известны.
Патогномоничными хромосомными нарушениями являются делеция короткого плеча хромосомы 1 с нарушением функции локуса 1 р 31-32. К нарушениям кариотипа относят гиперплоидию или диплоидию опухолевой ДНК. У 30% заболевших в клетках нейробластомы выявляют амплификацию и (или) экспрессию N-myc онкогена, что достоверно коррелирует с неблагоприятным прогнозом (резистентность к полихимиотерапии, склонность процесса к генерализации и т.д.).
Заслуживает внимания исследование клинико-генетических аспектов нейробластом. В литературе описаны случаи возникновения множественных нейробластом различной локализации у двух братьев. Была сделана попытка объяснить семейные случаи нейробластом, медуллобластом и глиом с точки зрения гипотезы о двух мутациях. Предполагается, что в некоторых случаях, одна мутация наследуется, а вторая появляется в соматической клетке; в других случаях обе мутации происходят в одной соматической клетке.
Исследователи, активно работающие в области эпидемиологии опухолей у детей, сообщают, что увеличенный риск заболевания раком коррелирует с врожденными уродствами и врожденной иммунологической недостаточностью.
Патогенез (что происходит?) во время Нейробластомы:
Неоплазмы развиваются из симпатических ганглиев. Различают три типа опухолей, отличающихся друг от друга степенью дифференциации.
Нейробластома является недифференцированной формой неоплазмы состоящей из мелких круглых клеток с темно-пятнистыми ядрами. Часто могут встречаться розетки и характерные нейрофибрилы. В опухоли обнаруживаются геморрагии и участки кальцификации.
Симптомы Нейробластомы:
Первоначальные симптомы нейробластомы не имеют специфичности и могут имитировать различные педиатрические заболевания. Это объясняется, во-первых, возможностью поражения опухолью и метастазами нескольких зон организма ребенка, а также метаболическими нарушениями, обусловленными ростом этих опухолевых очагов.
Клиническая картина зависит от места образования опухоли, локализации метастазов, количества продуцируемых опухолевой тканью вазоактивных веществ.
Растущая инфильтрирующая опухоль, располагающаяся на шее, в грудной клетке, брюшной и тазовых полостях, может, прорастая и сдавливая окружающие ее структуры, давать соответствующий симптомокомплекс.
При локализации в области головы и шеи первыми симптомами могут быть появление пальпируемых опухолевых узлов и развитие синдрома Горнера. Развиваясь в грудной клетке, она может стать причиной нарушения дыхания, дисфагии, сдавления вен.
Первым сигналом наличия опухоли в брюшной полости может быть наличие в ней пальпируемых опухолевых масс, в то время как новообразования таза могут проявляться нарушением акта дефекации и мочеиспускания.
Нейробластомы, прорастающие через межвертебральные отверстия со сдавлением спинного мозга (опухоли в виде «гантели»), вызывают характерные неврологические симптомы, к которым можно отнести такие, как вялый паралич конечностей и/или нарушение мочеиспускания с напряженным мочевым пузырем.
К основным клиническим проявлениям нейробластомы относятся:
• опухоль в брюшной полости
• отёк
• похудание,
• боли в костях, обусловленные метастазами
• анемия
• лихорадка.
Основные жалобы предъявляются на боль (30-35 % случаев), лихорадку (25-30 % случаев), потеря веса (20 % случаев). При росте опухоли в заднем средостении дети жалуются на постоянный кашель, дыхательные расстройства, дисфагию и постоянные срыгивания; наблюдается деформация грудной стенки. При поражении костного мозга вызывает анемию и геморрагический синдром. При росте опухоли в ретробульбарном пространстве возникает характерный «синдром очков» с экзофтальмом. Если нейробластома возникает в забрюшинном пространстве, то она быстро врастает в спинномозговой канал, пальпируясь как бугристая, несмещаемая опухоль каменной констистенции. При распространении опухоли из грудной полости в забрюшинное пространство через диафрагменные отверстия она принимает вид песочных часов или гантели. Метастазы нейробластомы в кожу имеют вид синюшно-багровых узлов с плотной консистенцией.
Клинические симптомы, обусловленные метастазами также весьма многообразны. У новорожденных первым признаком развития метастазов является быстрое увеличение печени, иногда сопровождающееся образованием на коже узлов голубоватого цвета и поражением костного мозга.
У детей более старшего возраста развитие метастазов может вызвать боли в костях и увеличение лимфатических узлов. Иногда заболевание имеет признаки, характерные для лейкемии, т. е. у детей развиваются анемия и кровоизлияния на слизистых оболочках и коже, что обуславливается панцитопенией, вызванной поражением костного мозга клетками нейробластомы.
Метаболические изменения, развивающиеся в результате роста опухоли, ведут к появлению ряда общих симптомов. Так, в результате повышения уровня катехоламинов и, иногда, вазоактивных интестинальных пептидов (VIP) у детей могут появляться приступы потливости и бледности кожных покровов, сопровождающиеся жидким стулом и гипертензией. Эти симптомы могут проявляться независимо от локализации бластомы, и их интенсивность снижается при успешном лечении больного.
Стадия нейробластомы
В литературе встречается довольно большое число систем стадирования нейробластомы. Из них до 1988 года наиболее популярными были классификация, предложенная в США группой по изучению рака у детей (CCSG, Evans et al., 1971); система TNM, разработанная Международным противораковым союзом (INSS, 1987).
В 1988 году была предложена модифицированная система стадирования нейробластомы, в которую были включены элементы обеих указанных классификаций (INSS, Brodeur et al., 1988).
Диагностика Нейробластомы:
Важным тестом в диагностике и дифференциальной диагностике нейробластом является определение суточной экскреции с мочой катехоламинов, их предшественников и метаболитов (ванилминдальной и гомованилиновой кислот). У детей с нейробластомой, в отличие от других опухолей, наблюдается резкое повышение экскреции указанных веществ почти в 85% случаев. Кроме того, в крови или моче больного определяются и другие опухолевые маркеры: нейроно-специфическая энолаза, ферритин и ганглиосайды.
Их определение является не только ценным диагностическим тестом, но и может помочь в объективизации данных и динамике опухолевого процесса после лечения.
Хорошее понимание синтеза и метаболизма катехоламинов имеет большое значение для клинических целей, как при установлении диагноза, так и в ходе лечения больного и последующего наблюдения за ним. В последние 20 лет определение уровня в моче ванилилминдальной и гомованилиновой кислот стало рутинным методом для указанных целей. Однако некоторые вопросы, касающиеся значимости этого теста еще продолжают обсуждаться.
Так, например, некоторые исследователи предлагают использование определения катехоламинов с целью «массового» скрининга.
В Японии обследовали более полумиллиона младенцев. В результате было выявлено 25 детей с бессимптомно текущей нейробластомой. 92% из них наблюдается длительные сроки без рецидива заболевания.
В США и Европе также наметилась тенденция к проведению аналогичной программы. Однако имеются и определенные недостатки этого метода, связанные с тем, что благодаря скринингу, определяются также дети с новообразованиями, которые могли бы спонтанно регрессировать.
Спорным остается вопрос о прогностическом значении уровней ванилилминдальной и гомованилиновой кислот у детей с нейробластомой. В ранних сообщениях указывалось, что высокий их Уровень обязательно ассоциируется с плохим прогнозом, в то время как в более поздних работах не было найдено значимой связи с прогнозом.
Поэтому, определение NSE при диагностике должно оцениваться с большой долей осторожности. Однако этот тест имеет определенное прогностическое значение. В частности, низкие уровни содержания NSE увязываются с хорошим прогнозом, а у детей с диссеминированной формой заболевания, т. е. прогностически неблагоприятной, отмечают высокие уровни содержания сывороточной NSE.
Необходимо подчеркнуть, что нейроно-специфическая энолаза является недостаточно специфичным маркером нейробластомы.
Ферритин. У детей с нейробластомой наблюдается повышение уровня ферритина, который снижается в процессе лечения и нормализуется в период ремиссии. Полагают, что повышение содержания ферритина в сыворотке крови происходит по следующим причинам: из-за повышения количества неиспользуемого железа, обусловленного анемией; из-за увеличения синтеза ферритина нейробластоматозными клетками с последующей секрецией в плазму.
Отмечается, что количество этого маркера почти не увеличивается у детей с нейробластомой I и II стадий, но оно заметно изменяется у больных с III и IV стадиями заболевания. Evans et al. (1987) выделили три группы больных, имевших различный прогноз течения заболевания:
— хороший, при нормальном содержании ферритина в сыворотке и возрасте менее 2-х лет; в этой группе прожило 93% детей;
— умеренный, при нормальном уровне ферритина и возрасте 2 года и старше; 2 года без признаков заболевания наблюдалось
58% больных;
— плохой, при повышенном содержании ферритина; двухлетняя продолжительность жизни у этих детей была 19%.
Кроме клинического и лабораторного обследования ребенка, обязательно выполнение костно-мозговой пункции или трепанобиопсии грудины и крыла подвздошной кости. Полученные аспираты или биоптаты изучаются цитологически, иммунологически или с помощью проточной цитометрии. Отмечено, что при этом они должны быть получены не менее, чем из 4-х зон. Лучевые методы исследования являются одними из решающих в клинической диагностике.
Ультразвуковое исследование должно всегда выполняться первым, при подозрении или наличии опухоли в брюшной или тазовой полостях. Повторная эхография, компьютерная томография проводятся перед решением вопроса о первичном или отсроченном оперативном вмешательстве. Данные, полученные при этом, помогают уточнить локализацию, распространенность опухоли и ее связь с интра- и экстраперитонеальными структурами тазовой и брюшной полостей, а также выявить наличие в ней мелких кальцинатов, которые не определяются обычной рентгенографией. Возможно также выполнение абдоминальной аортографии, нижней венокаваграфии, которые могут помочь в уточненной диагностике распространенности забрюшинных нейробластом.
Заключительным этапом клинической диагностики заболевания является аспирационная биопсия с цитологическим, иммунологическим исследованием пунктата. Кроме того, аспираты могут быть изучены с помощью проточной цитометрии.
При диагностике отдаленных метастазов нейробластомы необходимо, кроме костного мозга, тщательное обследование костей скелета, которые часто ими поражаются, особенно у детей в возрасте 2 года и старше. При стандартной рентгенографии, выполненной во время первичной диагностики, костные метастазы выявляются в 50-60% случаев. Проведение радиоизотопного исследования с использованием радиоактивного технеция (99 mTc ) повышает этот показатель до 80%. В последние годы для диагностики нейробластом предложено проведение радиоизотопного исследования с применением метайодобензилгванидина (131-J-mJBG), аналога гванетедина, меченного йодом-131. Скенирование, проведенное после введения этого препарата, позволяет выявить первичную остаточную и рецидивную опухоль, наличие метастатического поражения костного мозга, костей, лимфатических узлов и мягких тканей. В обзорном сообщении, содержащем данные о 550 больных нейробластомой было показано, что более чем 90% этих опухолей способны накапливать 131-J-MJBG.
При динамическом наблюдении за детьми после лечения необходимо уделять пристальное внимание поиску метастатического поражения костного мозга и костей, используя сцинтиграфию с метайодобензилгванидином, аспирационную и трепанобиопсию. Для этих целей используется также ЯМР-томография.
Следует отметить, что за последние 10 лет, в связи с развитием ультразвуковой, компьютерной и ЯМР-томографии и радиоизотопной сцинтиграфии, значительно повысилась точность диагностики заболевания, определения его стадии и возможности эффективного наблюдения за детьми после лечения.
Лечение Нейробластомы:
Несмотря на то, что нейробластома интенсивно изучается клиницистами и экспериментаторами уже более 100 лет, лечение этого заболевания остается важной проблемой детской онкологии. Выбор стратегии лечения, по крайней мере, зависит от двух факторов:
— прогностических признаков, выявленных у детей во время установления диагноза заболевания;
— реакции опухоли на лечение.
Химиотерапия
Ninane (1990) приводит следующие схемы противоопухолевого лекарственного лечения детей с нейробластомой.
До 1980 года ряд химиотерапевтических режимов состоял из винкристина и циклофосфамида с или без адриамицина. Результаты лечения с использованием этих схем оказались разочаровывающими для детей старше 1 года с местнораспространенной опухолью, так как 2 года переживало только 10% детей. Добавление цисплатины, вепезида и тенипозида привело к повышению начального противоопухолевого эффекта, но мало сказалось на отдаленных результатах.
В последние годы для повышения результатов химиотерапии были предложены высокодозные схемы лечения с пересадкой костного мозга).
Отметим следующее:
1. Использование высоких доз мелфалана в виде единственного Препарата позволяло получить результаты, по своему эффекту мало отличающиеся от результатов, которые наблюдались после интенсивной полихимиотерапии или комбинации ее с тотальным облучением.
2. Смертность из-за токсичности проводимого лечения была наименьшей в группе больных, которым проводилось только введение высоких доз мелфалана.
Необходимо отметить, что указанное лечение проводилось в виде консолидирующей терапии у детей с распространенными формами заболевания. Было показано, что больные с полной или значительной регрессией опухоли после начальной химиотерапии имели лучшие показатели 2 летней продолжительности жизни по сравнению с теми, у которых опухоль мало реагировала на начальное лечение.
Интересные данные о многолетнем наблюдении за больными с нейробластомой, подвергшимися интенсивной химиотерапии были представлены Philip et al. (1990) и Dini et al. (1990).
Оперативное лечение
Оперативное лечение широко используется для радикального удаления ограниченной первичной опухоли. Кроме того, в последние годы оперативному вмешательству подвергаются больные с местнораспространенными или метастатическими нейробластомами. После начальной химиотерапии нередко возникает возможность радикального удаления первичной опухоли и метастазов вследствие их значительной регрессии. В ряде случаев прибегают и к повторным оперативным вмешательствам, если первичная операция оказалась нерадикальной, но затем опухоль уменьшилась после проведения дополнительной химиотерапии.
Лучевая терапия
В настоящее время, в связи с прогрессивным развитием противоопухолевой лекарственной терапии, роль традиционного лучевого лечения больных нейробластомой уменьшилась. Это связано еще и с тем, что эта опухоль в основном поражает маленьких детей, облучение которых несет опасность отдаленных лучевых повреждений.
Все же в некоторых клинических ситуациях имеются показания к ее применению. Во-первых, лучевое лечение может быть проведено при нерадикальном оперативном удалении первичной опухоли и ма¬лой эффективности химиотерапии, во-вторых, при наличии местнораспространенной неоперабельной первичной или метастатической опухоли, не реагирующей на современные курсы химиотерапии.
Величина дозы излучения, прежде всего, зависит от возраста ребенка и величины остаточной опухоли. По мнению Tereb, Tent, при облучении ребенка до года адекватной дозой могут быть 10 Гр, подведенных в течение двух недель (по 1 Гр за фракцию). Jacobson (1984), поддерживая эту точку зрения, рекомендует дозу в 12 Гр за две недели.
Нередко после подведения указанных доз опухоль либо полностью регрессирует, либо значительно уменьшается в размерах. В последнем случае становится возможным оперативное удаление остатков нейробластомы. Симптоматический эффект может быть достигнут после однократного облучения в дозе 5 Гр, но в случаях относительно удовлетворительного состояния ребенка лучше использовать курс облучения с разовой дозой 3 Гр, подводимых за 5 фракций.
При лучевом лечении необходимо захватывать всю опухоль или ее ложе с 2 см прилежащих тканей.
Полагаем, что вопрос о применении лучевой терапии больных нейробластомой должен решаться в каждом случае индивидуально. При этом необходимо учитывать возможный непосредственный эффект на растущую опухоль. Например, даже при больших нерезектабельных опухолях бывает достаточно подвести дозу излучения в 10-15 Гр за 2-3 недели (1 Гр ежедневно), чтобы добиться эффекта за счет спонтанного их созревания.
При опухолях заднего средостения с использованием фотонов или электронов в зону облучения необходимо включать всю опухолевую массу и грудные позвонки на всю их ширину, для предупреждения деформации позвоночника. По достижении верхнего предела лучевой толерантности спинного мозга, необходима его защита. При этом необходимо помнить, что толерантность его меняется с возрастом. Также необходима тщательная защита плечевых суставов. При нейробластомах в настоящее время облучения всей брюшной полости используется редко, так как у больных с III стадией заболевания обычно применяют агрессивную полихимиотерапию.
При облучении тазовой области пристальное внимание уделяется защите тазобедренных суставов. У девочек необходимо, по возможности, выводить из зоны действия прямого пучка ионизирующего излучения яичники путем оперативного их перемещения. Последнее предохраняет ребенка от стерилизации и сохраняет его гормональную функцию.
Некоторые схемы лечения детей с нейробластомой в зависимости от стадии заболевания
Стадия I. Выполнение радикального оперативного удаления опухоли бывает достаточным для излечения больного. Тем не менее, эти дети нуждаются в динамическом наблюдении, так как возможны рецидивы заболевания или отдаленные метастазы.
Стадия IIА. При этой стадии нейробластомы излечения больного, так же как и при I стадии, можно достичь с помощью оперативного удаления опухоли.
Два исследования показали, что без признаков рецидива прошло 100% детей как получавших послеоперационное лечение, так и не получавших его (Ninane et al., 1982; Hayes et al., 1983). Исключение составила «гантелеподобная» форма паравертебральной нейробластомы, при которой необходимо проведение адекватного химиолучевого лечения.
Стадия IIВ. При этой стадии заболевания лечение должно начинаться с химиотерапии с последующим оперативным вмешательством. Трудно однозначно сказать, есть ли необходимость ее применения у детей до 6 месяцев, так как течение заболевания в этом возрасте достоверно благоприятно.
Стадия III (опухоль нерезектабельна) и стадия IV. Лечение детей с этими стадиями заболевания весьма трудная задача и решается, в основном, исходя из опыта конкретного специализированного отделения детской онкологии. Однако можно указать на два основных принципа к подходу терапии:
1. Необходима агрессивная тактика хирургического лечения при III стадии заболевания.
2. Дети с IV стадией в возрасте старше 1 года нуждаются в интенсивной высокодозной химиотерапии с пересадкой костного мозга.
Стадия IVa. В основном, при этой стадии заболевания проводится химиотерапия (несколько курсов циклофосфамида и винкристина), до и после оперативного вмешательства, выполняемого для удаления первичной опухоли.
Пример блоков полихимиотерапии, используемых в современных протоколах
CAV-Pt (протокол N 3891, CCG, США)
Цисплатин по 60 мг/м2 в 1-й день,
VP-16 по 100 мг/м2 в 3-й, 6-й день.
Циклофосфан по 900 мг/м2 в 4-й, 5-й день
Доксорубицин по 30 мг/м2 в 3-й день.
Интервал 3 нед
Прогностичекие факторы
Эти факторы получены в результате выявления достоверной связи между продолжительностью жизни больных после лечения с возрастом, стадией и биологическими параметрами опухоли. Используя многофакторный анализ, Evans et al. (1987) определили, что комбинация таких признаков, как возраст, стадия, уровень сывороточного ферритина и морфологического строения нейробластом, позволяет выделить три группы детей с различным прогнозом:
— благоприятную, в которой более 80% больных живут более 2-х лет;
— промежуточную;
— неблагоприятную, в которой только около 20% детей наблюдаются 2 года.
Возраст при установлении заболевания является единственным важным прогностическим фактором. Так, у детей до 1 года течение заболевания всегда благоприятно. Далее, значимыми признаками, влияющими на прогноз, являются стадия и первичная локализация нейробластомы.
При этом хотелось бы отметить, что 80% детей поступают в специализированную клинику на III-IV стадиях заболевания.
Профилактика Нейробластомы:
В настоящее время не существует рекомендаций по предотвращению развития нейробластомы, так как нет факторов риска, которые можно было бы избежать.
При наличии семейных случаев нейробластомы необходима консультация генетика для уточнения риска возникновения данной опухоли у ребенка.