Нейтропения после химиотерапии что делать
ФГБУ “Онкологический научный центр им. Н.Н. Блохина” РАМН, Москва
Одним из наиболее частых и опасных побочных эффектов цитостатической терапии
является нейтропения. Цитостатики, действуя на быстроделящиеся клетки, затрагивают и систему кроветворения. Циркулирующие нейтрофилы живут в среднем 6–9 часов, и система гемопоэза постоянно вырабатывает около 50 млн этих клеток в 1 минуту для замещения выбывших. Снижение
продукции нейтрофилов после воздействия химиопрепаратов приводит к быстрому уменьшению содержания этих клеток в периферической крови, что повышает риск развития инфекционных осложнений.
Длительная нейтропения зачастую не позволяет проводить химиотерапию (ХТ) в запланированные сроки, заставляет редуцировать дозы цитостатиков, что в свою очередь снижает эффективность противоопухолевого лечения. Кроме того, инфекционные осложнения на фоне нейтропении в
отсутствие адекватной терапии характеризуются стремительным течением и высокой летальностью. В связи с этим существует необходимость тщательной оценки миелотоксического потенциала современных режимов химиотерапии и выявления групп больных с высоким риском развития нейтропении, которым требуется профилактическое назначение колониестимулирующих факторов (КСФ).
Повышенный риск развития инфекции на фоне нейтропении обусловил выделение симптомокомплекса
“фебрильная нейтропения” (ФН). Согласно руководству NCCN (National Comprehensive Cancer Network) [1], ФН характеризуется повышением температуры в ротовой полости выше 38,5 °С при однократном измерении или выше 38,0 °С при двух последовательных измерениях в течение 2 часов при абсолютном числе нейтрофилов (АЧН) в крови менее 0,5 × 109/л или ожидаемом снижении 10 дней или ФН
после ХТ; вовлечение в опухолевый процесс костного мозга; лучевая терапия в анамнезе; недавно перенесенное оперативное вмешательство; наличие раневого процесса; плохой соматический статус пациента; нарушение функции печени и почек; пневмония; присоединившаяся грибковая инфекция.
Риск развития инфекционных осложнений у больных нейтропенией обусловлен не только уменьшением АЧН, но и нарушением функциональных свойств нейтрофилов (ослабление хемотаксиса и фагоцитоза; нарушение экзогенной продукции ростовых факторов, таких как интерлейкин-1,
интерлейкин-3, гранулоцитарно-макрофагального КСФ, Г-КСФ; изменение активности ферментов; снижение образования активных форм кислорода).
Оценка риска развития ФН должна проводиться перед каждым курсом ХТ. Если пациент в течение предыдущего цикла ХТ перенес эпизод ФН или дозолимитирующей нейтропенической инфекции и проводимая ХТ направлена на выздоровление, проведение последующих курсов ХТ в прежних дозах влечет за собой “высокий риск” развития ФН. В таких случаях необходимо рассмотреть вопрос об использовании КСФ. Если пациент перенес эпизод ФН, несмотря на использование КСФ, NCCN рекомендует провести редукцию доз химиопрепаратов во время последующих циклов или изменить
режим ХТ.
Эти рекомендации основаны на результатах крупных рандомизированных исследований, показавших, что риск развития ФН может быть значи-тельно снижен благодаря проведению первичной профилактики с использованием КСФ.
Vogel и соавт. [4] в двойном слепом рандомизированном плацебо-контролируемом многоцентровом
исследовании установили, что при первом и всех последующих циклах ХТ профилактическое назначение КСФ (пегилированный филграстим) значительно снижает риск развития ФН при режимах ХТ, которые прежде ассоциировались с “высоким риском” этого осложнения. В исследование
были включены больные РМЖ, получавшие доцетаксел 100 мг/м2 каждые 3 недели. Пациентки были распределены в 2 группы: 1-я группа (465 жен-щин) получала инъекции плацебо; 2-я группа (463 женщины) – пегфилграстим подкожно (вводился через 24 часа после завершения цикла ХТ). В группе
плацебо частота развития ФН составила 17 %, в группе пегфилграстима – 1 %. Потребность в госпитализации уменьшилась с 14 до 1%, а в использовании внутривенной антибактериальной терапии (АБТ) – с 10 до 2 % (p 50·× 109/л Граноген следует немедленно отменять.
Успех лечения ФН во многом зависит от раннего распознавания возможной инфекции и раннего начала терапии. Нейтропения значительно ослабляет иммунный ответ организма, что не позволяет развиваться характерным клиническим проявлениям инфекции, затрудняя ее клиническую диагностику у онкологических больных. Гипертермия у пациентов с нейтропенией часто бывает единственным
признаком инфекционного процесса.
Согласно клиническим рекомендациям ESMO, необходимо проводить тщательные первичный осмотр и
обследование на выявление возможных очагов инфекции [8]:
1. Наличие длительно стоящего центрального венозного катетера.
2. Симптомы и признаки наличия инфекции дыхательной системы, сердечно-сосудистой системы,
желудочно-кишечного тракта, кожных покровов, мочеполовой системы, центральной нервной системы.
3. Данные о предшествующих положительных результатах микробиологического анализа.
4. Рутинные лабораторные и инструментальные исследования:
• общий и биохимический анализы крови, коагулограмма, С-реактивный белок;
• посев крови (минимум 2 раза), включая посев из центрального венозного катетера; микроскопическое исследование и посев мочи;
• микроскопическое исследование мокроты и ее посев;
• микроскопическое исследование кала и его посев (при диарее);
• исследование очагов инфекции на коже (аспират, биопсия, мазок);
• рентгенография органов грудной клетки.
5. Дальнейшие исследования (при длительной и глубокой нейтропении): компьютерная томография органов грудной клетки (если лихорадка сохраняется, несмотря на адекватную АБТ, более 72 часов).
Немедленный подсчет формулы крови для установления числа нейтрофилов параллельно с другими исследованиями, представленными выше, имеют ключевое значение для определения необходимости начала ранней терапии ФН.
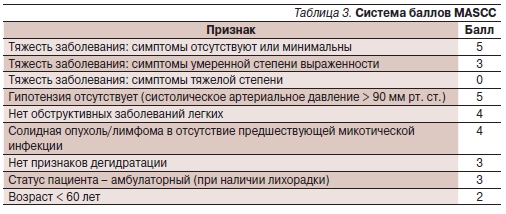
Международной ассоциацией поддерживающей терапии при раке (MASCC) разработан прогностический индекс [9, 10]. Он позволяет быстро оценивать риск осложнений – до того, как станет известно содержание нейтрофилов в крови пациента. Эффективность данного метода подтверждена во многих проспективных исследованиях.
Критерии индекса MASCC представлены в табл. 3.
Показателем “низкого риска” осложнений является сумма баллов > 21. Частота серьезных осложнений при этом не превышает 6 %, а смертность – 1 %. При сумме баллов
1. Crawford J, Althaus D, et al. National Comprehensive Cancer Network. Myeloid growth factors clinical practice guidelines in oncology. J Nat Compreh Cancer Network 2005;3:540–55.
2. ASCO Recommendations for the use of hematopoietic colony-stimulating factors: evidencebased,
clinical practice guidelines. J Clin Oncol 1994;12:2471–250.
3. Zielinski CC, Awada A, Cameron DA, et al. The impact of new European Organisation for Research and Treatment of Cancer guidelines on the use of granulocyte colony-stimulating factor on the management of breast cancer patients. Eur J Cancer 2008;44: 353–65.
4. Vogel CL, Wojtukiewicz MZ, Carroll RR, et al. First and subsequent cycle use of pegfilgrastim prevents febrile neutropenia in patients with breast cancer: a multicenter, double-blind, placebo-controlled phase III study. J Clin Oncol2005;23:1178–84.
5. Timmer-Bonte JN, de Boo TM, Smith HJ, et al. Prevention of chemotherapyinduced febrile neutropenia by prophylactic antibiotics plus or minus granulocyte colony-stimulating factor in small cell lung cancer: a Dutch randomized phase III study. J Clin Oncol 2005;23:7974–84.
6. Yoshida M, Ohno R. Antimicrobial prophylaxis in febrile neutropenia. Clin Infect Dis 2004;39 (1):65–7.
7. Cullen M, Steven N, Billingham L, et al. Antibacterial prophylaxis after chemotherapy for solid tumours and lymphomas. N Engl J Med 2005;353:988–98.
8. Минимальные клинические рекомендации Европейского общества медицинской онкологии (ESMO). М., 2010. C. 375–91.
9. Klastersky J, Paesmans M, Rubenstein E B et al. The Multinational Association for Supportive Care in Cancer risk index: a multinational scoring system for identifying low-risk febrile neutropenic cancer patients. J Clin Oncol 2000; 18:3038–51.
10. Innes H, Lim SL, Hall A, et al. Management of febrile neutropenia in solid tumours and lymphomas
using the Multinational Association for Supportive Care in Cancer (MASCC) risk index: feasibility and safety in routine clinical practice. Supp Care Cancer 2008;16:485–491.
11. Vidal L, Paul M, Ben Dor I, et al. Oral versus intravenous antibiotic treatment for febrile neutropenia
in cancer patients: a systematic review and meta-analysis of randomized trials. J Antimicrob Chemother 2004;54:29–37.
12. Kovacs J, Masour H. Evolving health effects of Pneumocystis: one hundred years of progress of diagnosis and treatment. JAMA 2009;301:2578–85.
13. 13 Wolf H-H, Leithauser M, Maschmeyer G, et al. Central venous catheter-related infections in hematology and oncology. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol 2008;87:863–76.
14. Raad I, Kassar R, Dany G, et al. Management of the catheter in documented catheterrelated coagulase-negative staphylococcal bacteremia: remove or retain? Clin Infect Dis 2009;49:1187–194.
15. Kim SH, Kang CI, Kim HB, et al. Outcomes of hickman catheter salvage in febrile neutropenic cancer patients with Staphylococcus aureus bacteremia. Infect Control Hosp Epidemiol 2003;24:897–904.
16. Walsh TJ, Teppler H, Donowitz GR, et al. Caspofungin versus liposomal amphotericin B for empirical antifungal therapy in patients with persistent fever and neutropenia. N Engl J Med 2004;351:1391–402.
17. Herbrecht R, Denning DW, Patterson TF, et al. Voriconazole versus amphotericin B for primary therapy of invasive aspergillosis. N Engl J Med 2002;347:408–15.
18. Dockrell DH. Salvage therapy for invasive aspergillosis. J Antimicrob Chemother 2008;61:41–4.
19. Schmutzhard E, Williams KJ, Vukmirovits G, et al. A randomised comparison of meropenem with cefotaxime or ceftriaxone for the treatment of bacterial meningitis in adults. Meropenem Meningitis Study Group. J Antimicrob Chemother 1995;36:85–97.
Инфекционные осложнения, лейкопения и нейтропения
Инфекционные осложнения, лейкопения и нейтропения
Инфекции вызываются ростом различных микроорганизмов, например, бактерий, вирусов или грибов, внутри человеческого организма. Инфекции могут начинаться в любом органе, но наиболее часто они возникают в тех частях организма, которые тесно соприкасаются с внешней средой, например в коже, слизистых оболочках пищеварительного тракта (полость рта, пищевод, кишечник), дыхательных путей (гортань, трахея, бронхи, легкие) и органах мочеполовой системы. В норме организм защищен от большинства возбудителей инфекционных заболеваний иммунной системой, которая способна эффективно уничтожать микроорганизмы.
Однако в период проведения противоопухолевой терапии возможно нарушение функционирования иммунной системы – такие методы лечения, как лучевая терапия, химиотерапия, а также некоторые «таргетные» препараты способны повреждать костный мозг, в котором образуются клетки, необходимые для функционирования иммунной системы – лейкоциты. Выделяют множество форм лейкоцитов, к наиболее важным из них относятся нейтрофилы – клетки, играющие главную роль в сопротивляемости организма при «столкновении» с возбудителями бактериальных инфекций. Плохое питание, недостаток сна и стресс также ослабляют иммунную систему.
Степень выраженности угнетения функции иммунной системы отражает количество нейтрофилов в крови. В норме их количество превышает 2,0*10^9 клеток на 1 литр крови (также можно встретить обозначение 2000 клеток на 1 мкл) Снижение их количества обозначают термином «нейтропения». В зависимости от выраженности нейтропении выделяют следующие степени её тяжести:
К характерным симптомам инфекции относятся: лихорадка (повышение температуры до 38 oC и выше), появление кашля или боли в горле, диарея, боль в ушах или в области пазух носа, кожная сыпь, появление боли при мочеиспускании или изменение цвета мочи, выделения из половых путей и т.д. Обязательно проконсультируйтесь со своим лечащим врачом в случае возникновения вышеперечисленных симптомов.
Стоит учитывать, что прием некоторых лекарственных препаратов, например нестероидных противовоспалительных средств, таких, как парацетамол, аспирин, ибупрофен, а также глюкокортикостероидов (дексаметазон, метилпреднизолон, преднизолон и т.д.) может снижать температуру тела и маскировать другие симптомы инфекции. Это может привести к тяжелым последствиям, обязательно сообщите вашему лечащему врачу, если вы принимали или принимаете постоянно эти или другие препараты с аналогичным механизмом действия.
Для диагностики нейтропении используется общий (клинический) анализ крови, кровь для анализа забирается из пальца или из вены. В случае, если подозревается развитие инфекции, в зависимости от её клинической картины проводятся дополнительные методы обследования, например, анализ мочи, кала, рентгенография легких, УЗИ брюшной полости и т.д.
Инфекционные осложнения и «фебрильная» нейтропения у онкологических пациентов являются опасными и потенциально жизнеугрожающими осложнениями. Пациентам, получающим противоопухолевое лечение, рекомендуется регулярно (например, 1 раз в неделю) контролировать показатели общего анализа крови, рекомендуется всегда иметь при себе антибактериальные препараты. Обратитесь к врачу за получением дополнительной информации.
Что я могу сделать для того, чтобы предотвратить развитие инфекции?
Ваш лечащий врач даст вам рекомендации по необходимым мерам предосторожности в процессе лечения, например следующие:
Лечение и профилактика нейтропении
В случае, если нейтропения в процессе лечения развивается снова и снова, или в процессе проведения терапии отмечалось развитие инфекционных осложнений Ваш врач может принять решение о снижении (редукции) доз противоопухолевых препаратов. Уменьшение дозы противоопухолевых препаратов снижает их негативное влияние на процессы кроветворения и во многих случаях позволяет предотвратить развитие нейтропении.
В клиническую практику внедрены также т.н. «гранулоцитарные колониестимулирующие факторы (Г-КСФ)», например филграстим, пэг-филграстим и т.д. Г-КСФ способствует процессам образования клеток иммунной системы в костном мозге.
Как правило, Г-КСФ вводятся через 24-72 часа после химиотерапии подкожно или внутривенно. Их применение позволяет эффективно поддерживать количество нейтрофилов и лейкоцитов в крови и проводить более агрессивную химиотерапию. Большинство пациентов делают себе эти уколы самостоятельно, наиболее удобным является введение под кожу живота. В сети Интернет опубликовано множество обучающих материалов по технике их выполнения (например). Обсудите со своим лечащим врачом целесообразность применения Г-КСФ в вашем индивидуальном случае.
ВНИМАНИЕ! Инфекционные осложнения, возникающие в ходе проведения противоопухолевого лечения, могут представлять собой непосредственную угрозу для жизни. Не занимайтесь самолечением, обратитесь к врачу.
Осложнения во время химиотерапии. Нейтропения
Во время химиотерапии у пациента обычно возникают осложнения разной степени выраженности. Опытный врач обязательно объяснит, как избежать побочных эффектов лечения или снизить их интенсивность, но есть вещи, о которых нужно помнить всегда.
Нейтропения — это снижение количества циркулирующих в крови нейтрофилов, подвида лейкоцитов (белых кровяных клеток), которые отвечают за непосредственный контакт с инфекционным возбудителем и его уничтожение. Другими словами, нейтрофилы — это защита нашего организма.
Нейтропения при химиотерапии возникает из-за повреждения быстроделящихся клеток костного мозга и, как следствие, недостаточного количества нейтрофилов в крови. В целом это нормальный процесс — костный мозг восполняет дефицит, но глубина и длительность нейтропении зависит от множества факторов: в большей степени от режима химиотерапии, возраста пациента и его сопутствующей патологии.
Количество нейтрофилов обычно начинает снижаться примерно через неделю после начала каждого цикла химиотерапии. Уровень нейтрофилов достигает нижней точки через 7-14 дней после лечения. Это явление носит название «надир» и является точкой наибольшего риска по развитию инфекции. Затем количество нейтрофилов снова начинает расти — костный мозг возобновляет нормальную выработку нейтрофилов. Но для достижения нормального уровня может потребоваться 3-4 недели.
Снижение абсолютного числа нейтрофилов (АЧН) ниже 0,5 тыс/мкл (нижний порог нормы 2 тыс/мкл) чревато риском развития инфекции, в том числе и тяжелой. И чем старше пациент, тем выше риск.
Одно из самых важных и потенциально опасных осложнений химиотерапии — фебрильная нейтропения. Ее можно избежать, если знать, что делать.
При нейтропении системная реакция организма на инфекцию чаще всего сначала ограничена лихорадкой. Вот почему важно регулярно сдавать общий анализ крови в процессе химиотерапии и следить за температурой тела. Если при химиотерапии возникло повышение температуры выше 38°C на фоне снижения АЧН ниже 0,5 тыс/мкл, нужно незамедлительно сообщить об этом лечащему врачу, начать лечение антибиотиками широкого спектра и гранулоцитарными колониестимулирующими факторами.
Ранее считалось, то все пациенты в таком состоянии должны быть госпитализированы. Сегодня есть определенные прогностические калькуляторы, которые определяют возможность лечиться амбулаторно, но с четкими рекомендациями по мониторингу состояния.
Фебрильная нейтропения — это опасное состояние, которое без лечения может осложниться сепсисом и даже летальным исходом.
Быстрые факты о нейтропении
1. Нейтропения может угрожать жизни.
В России статистика по нейтропении, возникающей вследствие проведения химиотерапии, не ведется. Но в США, где анализируют эти данные, нейтропения становится причиной госпитализации 60 000 онкологических пациентов ежегодно. Каждый 14-й пациент умирает от осложнений, связанных с этим состоянием.
2. Дни повышенного риска.
Нейтропения может развиться через 7-12 дней после начала каждого цикла химиотерапии.
3. Почему вы находитесь в зоне риска развития нейтропении?
Химиотерапия убивает как ненормальные (раковые), так и нормальные (в том числе ответственные за иммунитет) клетки в вашем организме. Когда это случается, риск развития инфекционного заболевания увеличивается.
4. Инфекции при нейтропении могут быстро прогрессировать.
Контролируйте температуру тела. Немедленно свяжитесь с врачом, если на фоне химиотерапии у вас поднялась температура выше 38°С.
Если предполагается госпитализация, обязательно сообщите врачам, что у вас онкологическое заболевание и вы проходите химиотерапию.
5. Как вы можете предотвратить инфекцию:
НЕЙТРОПЕНИЯ — осложнение, снижающее эффективность химиотерапии
ЖУКОВА Людмила Григорьевна
д.м.н., профессор РАН, заместитель директора МКНПЦ им. А.С. Логинова по онкологии, член правления RUSSCO и АОР, председатель группы клинических рекомендаций по диагностике и лечению рака молочной железы МЗ РФ, член ASCO, ESMO
Что такое нейтропения и какая она бывает?
Нейтропения — это термин, определяющий снижение числа нейтрофилов. Нейтрофилы — это разновидность белых клеток крови, которые отвечают, в том числе, и за защиту организма от инфекционных агентов. Снижение их количества ниже определенного порога называется нейтропенией. В норме считается, что их должно быть 2000. Когда они снижаются до 1500 и ниже, это не опасно, но это уже нейтропения второй степени тяжести. Когда их число становится меньше 1000, это нейтропения третьей степени тяжести. Все, что ниже 1500, не позволяет в большинстве случаев проводить очередной курс лекарственного цитостатического лечения. Снижение числа нейтрофилов до 500 клеток и менее — то, что трактуется врачом как нейтропения четвертой степени тяжести, и может стать состоянием, которое несет угрозу уже не столько для продолжения лечения, но в том числе представляет непосредственную угрозу жизни пациента и требует очень серьезных и быстрых дополнительных медицинских вмешательств.
Поэтому, когда пациент получает лекарственное лечение по поводу злокачественного новообразования или
проходит другой вид противоопухолевой терапии, который сопровождается снижением числа нейтрофилов, у нас (у врачей) возникает термин «у Вас нейтропения», дальше следуют слова «степень тяжести нейтропении». Пациенту важно знать, что эти степени тяжести означают. Например, услышав от врача, что у него нейтропения второй степени тяжести, пациент должен задать вопрос: «А можно ли мне лечиться дальше? Могу ли я безопасно продолжать прием препаратов, приходить на следующий курс?» Если он слышит, что у него нейтропения 3 степени тяжести, это однозначный факт, что лечение необходимо прервать.
Дозолимитирующая нейтропения — это та нейтропения, которая не дает проводить заданный запланированный режим с заданной дозоинтенсивностью — с соблюдением доз и сроков проведения.
Должно быть понимание, что диагностированная нейтропения четвёртой степени тяжести несет в себе тревогу как для пациента, так и для врача, потому что требует определенного алгоритма незамедлительных действий.
Что такое фебрильная нейтропения?
Фебрильная нейтропения — это нейтропения 4 степени тяжести, сопровождающаяся повышением температуры тела. Фебрильный — это значит с лихорадкой.
Пороговым значением температуры, которая требует серьезного внимания, считается 38,5°С однократно либо 38,3°С на протяжении нескольких часов, но обратите внимание, что это касается температуры, измеренной в ротовой полости. Поскольку чаще всего мы измеряем, по старинке, температуру тела в подмышечной впадине, здесь цифры могут быть даже ниже. Температура выше 37,8 градусов по Цельсию меня, как врача, начинает тревожить, и когда я даю напутственные рекомендации своим пациентам, именно эту цифру я ставлю пороговой, после которой пациент должен принять определенные меры безопасности.
Фебрильная нейтропения — это уже жизнеугрожающее состояние, которое может повлечь за собой риски для здоровья и жизни пациента, касающиеся не только непосредственно ситуации снижения числа нейтрофилов:
Наслоившаяся лихорадка на фоне низкого числа нейтрофилов чаще всего обусловлена какой-то присоединившейся инфекцией, потому что клеток, которые с ней должны бороться, катастрофически мало. Эта ситуация опасна прямо сейчас именно этим. В последующем, в результате данного факта, нарушается режим лечения: он может просто быть отложен. Это еще полбеды. Обычно это приводит к изменению дозы, к снижению дозы, а снижение дозы это, к сожалению, в последующем выливается уже в потерю эффективности. Повторный случай развития фебрильной нейтропении — прямая причина отмены лечения.
Почему необходимо профилактировать развитие нейтропении на фоне лечения раннего рака молочной железы?
Рак молочной железы является нозологией, особенно ранний рак молочной железы, для которой принципиальным является проведение правильных режимов в правильных дозах и правильные сроки в неоадъювантном и адъювантном лечении (то есть либо до операции, либо после операции, соответственно). Проведенный в полном объеме — и только в полном объеме с соблюдением доз и сроков лечения — весь запланированный курс химиотерапии позволяет увеличить продолжительность жизни. Мы сейчас говорим не о чем-то таком, мы говорим о месяцах, о годах жизни.
К счастью, в последнее время для улучшения результатов терапии именно раннего рака молочной железы — это уже подтверждено в серьезных крупномасштабных исследованиях — применяются более «жесткие» режимы лекарственного лечения, которые позволяет улучшить отдаленные результаты, то есть увеличить количество излеченных, выживших и живущих без проявления болезни пациентов. Но эти режимы, которые так и называются дозоуплотненные, предполагают уменьшение интервалов между введениями. Обычно все привыкли, что после введенного курса химиотерапии планируется какой-то интервал — 3-4 недели, за который обычно пациент восстанавливается и готов к следующему введению: восстанавливаются показатели крови (прежде всего нейтрофилы), потому что, как мы уже с вами обсуждали до этого, есть пороговый, безопасный уровень нейтрофилов, который позволяет продолжать/начинать следующий цикл лечения. При невозможности его достижения мы не можем начать терапию, что приводит к отсрочке запланированного цикла.
Проведенные опросы показывают, что, к сожалению, до 40% клиницистов предпочитают модифицировать режимы, а не делать что-то другое. Как мы уже установили, модификация режима, изменение интервалов между циклами, снижение дозы приводят к потере эффективности проведенного лечения. Было доказано, например, что снижение дозы адъювантной химиотерапии, назначаемой при раннем раке молочной железы на 15%, уже приводит к существенному уменьшению продолжительности жизни, а снижение дозы на 35% и более, то есть на треть, полностью нивелирует значение этой химиотерапии. Выживаемость больных такая же, как будто им вообще не проводили химиотерапию.
Поэтому с внедрением в нашу повседневную практику дозоуплотненных режимов химиотерапии и принимая во внимание, что нормальный костный мозг любого человека в большинстве случаев не успевает восстановиться за этот короткий интервал, нужно что-то с этим делать, чтобы в нужное время в нужной дозе провести нужный цикл лечения. Режимы химиотерапии, которые используются именно при лечении раннего рака молочной железы, когда мы действительно даем шанс и должны сделать так, чтобы вылечить пациента (мы говорим не о метастатической болезни, где совершенно другие цели и принципы терапии), стимулируют развитие нейтропении 3-4 степеней тяжести.
Развившаяся нейтропения, как правило, приводит к изменению режима лечения (а именно снижению доз препаратов) и к удлинению интервалов между циклами. Если ничего не делать или делать по факту, когда уже случилась беда, а не заблаговременно, мы теряем эффективность лечения, полностью сводим на ноль все наши усилия. Поэтому уже давно стало очевидным, что для того, чтобы соблюсти запланированный режим лечения, нужно применять
специальные препараты. Это препараты под названием гранулоцитарные колониестимулирующие факторы (Г-КСФ). Препараты, которые помогают нашему костному мозгу обеспечить циркуляцию в организме нормального количества нейтрофилов для того, чтобы предотвратить развитие инфекционных осложнений.
В начале мы применяли Г-КСФ для сокращения сроков развившейся нейтропении — периода времени, когда показатели нейтрофилов по анализу крови очень низкие, на фоне которых проводить химиотерапию опасно и нельзя.
Длительное время, к сожалению, отношение к этой группе препаратов класса Г-КСФ у нас было достаточно потребительское: мы применяли Г-КСФ для сокращения сроков развившейся нейтропении — периода времени, когда показатели нейтрофилов по анализу крови очень низкие, на фоне которых проводить химиотерапию опасно и нельзя. Использовали тогда, когда уже случилась нейтропения, чтобы побыстрее восстановить показатели крови и сократить период восстановления до минимума: укольчик, который, конечно же, приведет к выбросу нейтрофилов, и в анализе крови все будет замечательно и даже иногда ужасно. На этом фоне мы со спокойной совестью и для галочки, что все показатели в норме, проводили химиотерапию. Этого быть не должно, категорически не должно этого быть. Мы должны начинать курс лечения на нормально восстановившихся показателях, но не этим путем.
Это еще ладно, если применяются Г-КСФ. Каждый день я сталкиваюсь с тем, что для того, чтобы провести очередной курс лечения, пациенты используют иногда даже по рекомендации моих коллег, глюкокортикостероиды: дексаметазон, преднизолон — это препараты, которые имеют массу позитивных моментов, но имеют и массу негативных последствий. Самое главное, они никогда не должны использоваться для того, чтобы «подогнать» показатели крови под те, на которых мы можем безопасно проводить очередной курс лечения. Но это хотя бы лекарственные препараты.
Бывает, для контроля показателей крови, начинают применять кто во что горазд: начиная от сметаны с пивом и заканчивая деринатами и прочей какой-то непонятной для меня субстанцией, которая, поверьте, в инструкции даже близко не имеет не то что показаний профилактики и лечения нейтропении, а просто вообще не используется при химиотерапии и курации гематологической токсичности, а может применяться только в местном виде. Не знаю, как можно поднять нейтрофилы, прикладывая к больному месту ампулу с какой-то целебной субстанцией. Мы стараемся донести до наших пациентов и до наших коллег, что для того, чтобы соблюсти дозовую интенсивность, как дозоуплотненного, так и стандартного режима химиотерапии при лечении раннего рака молочной железы, не нужно использовать «бабкины методы», заговоры и прочие снадобья. Нужно вспомнить о том, что есть хорошо изученная и доказанная возможность первичной профилактики нейтропении.
Профилактика заключается в том, что в нужное время после проведенного курса химиотерапии должен использоваться колониестимулирующий фактор. Варианты этого подхода сейчас различны.