Точность методов определения патологий плода на ранних сроках беременности
Клиническая картина хромосомных патологий:
Хромосомные аномалии одна из самых актуальных проблем здравоохранения, по данным ВОЗ:
По состоянию на 2021 год в России применяется несколько методов определения генетических патологий плода:
Ранний пренатальный скрининг
Инвазивная диагностика
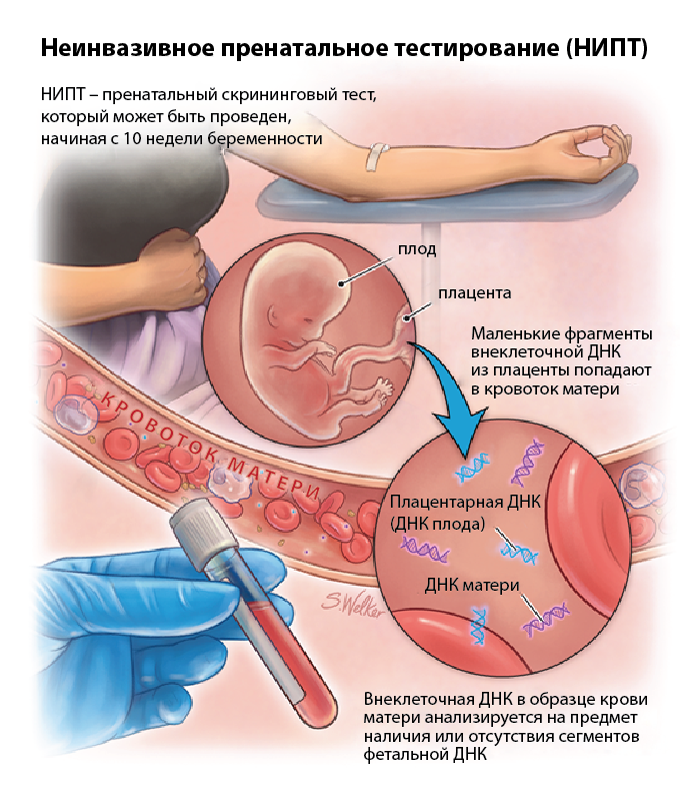
Неинвазивное пренатальное тестирование
Ранний пренатальный скрининг
Или по другому комбинированный скрининг I триместра. В России широкое применение РПС по международному стандарту было инициировано Минздравсоцразвития России только в 2009 г. с поэтапным внедрением нового алгоритма диагностики хромосомных патологий плода в субъектах страны в период с 2010 по 2014 [1].
Данный вид диагностики был разработан фондом медицины плода (FMF) и подразумевает под собой проведение ультразвукового исследования и анализа сывороточных маркеров материнской крови (бетта-ХГЧ и PAPP-A). Расчет риска, с учетом индивидуальных особенностей беременной (возраст матери и срок беременности) происходит с помощью унифицированной программы “Astraia” (Астрайя).
Каждая беременная женщина, которая встает на учет знает, что данный вид скрининга предстоит ей в период с 11 до 14 недель. По результатам скрининга женщина может получить как низкий риск рождения ребенка с патологией, так и высокий (граница 1:100).
Какова же точность скрининга I триместра, который проводят каждой беременной женщине в России:
Стоит отметить что 20% детей рожденных с синдромом Дауна (с трисомией 21) были рождены в группе низкого риска. [3]
Также сравнительный анализ показал, что комбинированный скрининг эффективнее исследования только биохимических или ультразвуковых маркеров (87% вместо 71%) [4].
Инвазивная пренатальная диагностика
Данный вид диагностики включает в себя процедуру забора разного вида биоматериала (в зависимости от срока беременности) из полости матки с помощью пункции под контролем УЗИ. Среди беременных процедуру часто называют “прокол”, длительность процедуры (подготовки и самой пункции) от 5 до 7 минут.
У инвазивной пренатальной диагностики есть свои ограничения и риски осложнений [5]:
По данным FMF риски Скидка 50% на тест ДНК отцовство
ООО «Медикал Геномикс» Лицензия № ЛО-69-01-002086 от 06.10.2017
Юр. адрес: г. Тверь, ул. Желябова, 48
ООО «Лаб-Трейдинг», ИНН: 6950225035, ОГРН: 1186952017053, КПП:695001001
Юр. адрес: г. Тверь, ул. 1-Я За Линией Октябрьской Ж/Д, 2, оф. 22
Скрининг показал риск синдрома Дауна у плода
13 Янв Скрининг показал риск синдрома Дауна у плода
Мне сорок лет, четвертый ребенок. Во время беременности на скринингах мне поставили высокий риск Синдрома Дауна у малыша — сначала 1:6, потом 1:4 и 1:2.
Высокий риск считается уже от 1:250, поэтому, когда я увидела эти цифры, у меня потемнело в глазах.
На УЗИ носовую кость сначала не видели, а потом она была значительно меньше нормы: в два раза меньше самого минимального значения.
Я бросилась искать информацию о синдроме, рисках и вообще всем, что с этим связано. Информацию собирала в интернете на сайтах и форумах, что-то мне рассказывали люди, которые воспитывали или общались с детками, у которых такой синдром.
Я хочу поделиться своим опытом, потому что возможно кто-то также, как и я, окажется в ситуации, когда не знаешь, что делать, у кого спрашивать, и от этого незнания голова разрывается на части. Эмоциональную сторону я намеренно опущу, потому что то напряжение, в котором я была эти полгода, описать невозможно.
Первый скрининг делается на сроке 11-13 недель и включает в себя УЗИ и анализ крови на ряд показателей. На УЗИ смотрят воротниковую зону, носовую кость, кровоток.
У меня носовую кость на тринадцатой неделе не обнаружили и отправили в ЦПСИР переделать через неделю. Через неделю кость также не увидели. Все другие показатели были в норме. В анализе крови при учете первого УЗИ ХГЧ была чуть выше нормы (2,57 при норме 0,5- 2,5 моль), при учете второго УЗИ – 2,7 моль. Повышенный ХГЧ также считается маркером СД у ребенка. Меня отправили к генетику тут же в соседний кабинет. Генетик очень сухим языком еще раз повторила цифры и рекомендовала сделать амниоцентез, то есть анализ, когда иглой берется амниотическая жидкость и считают хромосомы.
На более ранних сроках, 9-13 недель, делают биопсию хориона, но я уже не успевала. На более позднем – после 22 недель – кардоцентез, когда берут кровь из пуповины ребенка.
Что я поняла уже постфактум: после 35 лет коэффициент риска с каждым годом сильно возрастает. То есть в мои 40 лет он уже 1:75 просто априори без анализов и УЗИ. А в 48 лет он будет гораздо больше. При норме УЗИ на чуть повышенный хгч никто бы не обратил внимания, но 40 лет, отсутствие носовой кости и 2,7 вместо 2,5 моль в итоге превратились в риск 1:4.
Я сделала неинвазивный тест — сдала анализ крови Пренетикс на определение распространенных хромосомных аномалий. Результат пришел отрицательный. Я решила не делать амниоцентез, хотя сдала все анализы и была готова. На следующий день мы улетали, а это все-таки маленькая операция, рекомендуется покой и есть небольшая, но угроза выкидыша. Я читала о таких случаях, причем, когда женщина теряла здорового ребенка. Плюс я приняла решение оставить малыша в любом случае, и результат бы уже ничего не решил.
Первый раз носовую кость увидели на экспертном УЗИ в 16 недель, она была 2 мм и отставала где-то на месяц.
Все это время я мониторила интернет и искала информацию. На одном из форумов был опрос мам, у которых родились дети с СД, о том, когда они узнали о диагнозе. Результаты получились примерно такие: 40% мам имели риски на скрининге или даже знали о диагнозе, сдав анализ, но решили рожать. У 40% и скрининг, и УЗИ были в норме. И 20% не делали никаких исследований.
В интернете я нашла несколько ложноположительных результатов неинвазивных тестов, но ни одного ложноотрицательного. У одной моей знакомой были плохие целых два анализа – биопсия хориона и неинвазивный тест, показавший не СД, но другую патологию. Только амниоцентез снял все риски.
Когда я пришла в ЦПСИР на второй скрининг в 21 неделю, меня отругали, что я отказалась от амниоцентеза, сказали, что неинвазивные тесты — это ерунда и таких ложноотрицательных результатов бывает достаточно. В частности, есть мозаичная форма СД, когда часть клеток имеют дополнительную 21ую хромосому, а часть нет, и эту форму могут не диагностировать, если в анализ попадут клетки с обычным рядом хромосом. На этом скрининге носовая кость была 5,1 мм при минимуме 5,7, и риск уже 1:2. В 32 недели носовая кость была в два раза меньше допустимого минимума.
В роддоме на УЗИ уже перед родами меня стали пугать, что у ребенка гиперэхогенный кишечник, что является одним из маркеров генетических патологий, но срок уже был 41 неделя и, скорее всего, в кишечнике у ребенка был меконий.
Также говорили, что неинвазивный тест надо было делать развернутый, не на четыре распространенные патологии, так как гипоплазия носовой кости (слишком маленькая кость) — это маркер не только СД, но и других генетических отклонений.
Первой моей фразой после рождения ребенка была: «Есть ли у него нос?».
Нос был, причем вполне приличный.
Родился обычный ребенок.
Я сейчас задаю себе вопрос: а нужны ли эти скрининги? Я понимаю, что есть другие патологии, кроме Синдрома Дауна, более сложные и опасные, и, возможно, для их диагностики на раннем сроке скрининг очень важен. Но сколько женщин с риском СД у ребенка решили не ждать 16 недель и амниоцентеза и сделали аборт, чтобы не упустить время?
Амниоцентез делается на сроке 16-18 недель, какое-то еще время нужно для получения результата. В итоге срок уже большой и женщину отправляют на искусственные роды. Я даже писать не буду о том, как они происходят: это страшно.
Что бы я точно добавила в том же ЦПСИРЕ или консультациях — это должность психолога, который должен сидеть в кабинете рядом с генетиком и по-человечески объяснять и рассказывать женщине все за и против в любом решении, которое она примет.
Мне повезло — рядом оказались люди, которые поддержали меня, рассказали, что даже если риск подтвердится и у ребенка будет СД — это не так страшно, как описывают врачи по старым исследованиям, проводившимся в интернатах, где и обычные дети не будут психологически здоровыми. Но скольких женщин, особенно в глубинке, убеждают делать аборт при риске, значительно меньшем, чем у меня?
Что касается финансовой стороны исследований: все скрининги, инвазивные анализы, амниоцентез и другие делаются бесплатно в рамках ОМС, неинвазивный пренатальный тест «Пренетикс» стоил 29 000 рублей, периодически на него бывают скидки до 10 000 рублей. Расширенный анализ будет стоить около 60 000 рублей. Также и неинвазивные, и инвазивные анализы определяют пол ребенка.
За экспертное УЗИ я заплатила 5500 рублей.
Очень надеюсь, что все, написанное выше, поможет не унывать женщинам, которые оказались в ситуации, похожей на мою. Риск — это всего лишь риск, а не диагноз. И машина, и люди могут ошибаться.
Ранняя диагностика синдрома Дауна: распространенные заблуждения и статистика
Еще в 1866 году Лэнгдон Даун заметил, что у пациентов с синдромом, которые получил название по фамилии ученого, маленький нос, плоское широкое лицо, толстая шейная складка. С возникновением ультразвука стали появляться более глубокие исследования в этой области, и диагностировать синдром Дауна стало возможным уже у эмбрионов. Главный врач Клиники МАМА Виктория Викторовна ЗАЛЕТОВА рассказывает об истории этих исследований и новейших достижениях.
Врачи всего мира работают в условиях определенной догматики: стопроцентной методики дородовой диагностики синдрома Дауна на данный момент не существует. Фактор риска присутствует всегда. И усилия специалистов разных областей во многих странах направлены на то, чтобы сделать его минимальным.
Одним из важнейших критериев — или ультразвуковых маркеров — при диагностировании синдрома Дауна у эмбрионов является толщина воротникового пространства (ТВП). У любого плода на сроке 11-14 недель можно ее измерить. Было замечено, что у 75% эмбрионов с синдромом Дауна ТВП больше, чем у обычных плодов. Позже были открыты не менее важные ультразвуковые маркеры: длина носовых костей, оценка кровотока в венозном протоке и на трикуспидальном клапане.
Риск, что у ребенка будут присутствовать какие-либо хромосомные аномалии, есть всегда. По синдрому Дауна он составляет порядка 1 на 500. Чем старше мама, тем больше риск (риск резко возрастает после 35 лет).
Доктор Николаидес, основатель Фонда Медицины Плода, и его коллеги в Лондоне в первом триместре беременности выявляют до 95% плодов с синдромом Дауна. Но есть так называемые «нечувствительные дауны» — они «нечувствительны» к этой диагностике. Их количество по данным Фонда Медицины Плода порядка 5%. Это те эмбрионы, которые пройдя биохимический и ультразвуковой скрининг показали абсолютно нормальные значения.
В последние годы пренатальная диагностика хромосомных патологий плода совершенствуется. Был разработан метод ДНК секвенирования клеток плода из крови матери. На 9-ой—10-ой неделе беременности пациентка сдает кровь, из которой «вылавливаются» клеточки эмбриона. И эти клетки анализируются на присутствие основных хромосомных патологий. Данный метод тоже имеет погрешность и не может поставить окончательный диагноз. Но ДНК секвенирование позволяет определить необходимость инвазивной диагностики.
Проведение преимплантационной генетической диагностики эмбрионов (ПГД) в рамках программ ЭКО так же является высокотехнологичной методикой выявления основных хромосомных аномалий, в том числе синдрома Дауна. Исследование позволяет заподозрить проблему на самом раннем этапе и не переносить в полость матки эмбрионы с заведомо лишней хромосомой. Но ПГД как и ДНК-секвенирование имеет свой процент ложно-положительных и ложно-отрицательных результатов. Поэтому в последствии для исключения риска хромосомных патологий требуется проведение комбинированного скрининга с дальнейшей инвазивной диагностикой. Инвазивная методика несет определенные риски по потере беременности, но только это исследование дает более точные результаты.
Комбинированный скрининг в первом триместре позволяет заподозрить патологию плода. Это вспомогательный метод, целью которого является выявление группы риска на основе ультразвуковых и биохимических маркеров. У 75% плодов с синдромом Дауна может быть расширено воротниковое пространство, у 25% оно будет нормальное. У 35-40% плодов с хромосомной патологией наблюдается аномальный венозный кровоток — у остальных он будет нормальный. Поэтому нужна комплексная оценка. Чем больше маркеров рассматривается, тем больше вероятность правильного заключения по этому эмбриону. По-прежнему во всем мире идет поиск новых маркеров. Все врачи пренатальной ультразвуковой диагностики очень этим озабочены, каждый год появляются новые исследования на эту тему.
На основе первого скрининга формируется группа риска. Но это еще не означает наличие синдрома Дауна у эмбриона, речь о подозрении. При расчете индивидуального риска отнесение к группе с высокой вероятностью присутствия заболевания в том числе может произойти из-за возрастного фактора, могли сказаться сывороточные маркеры, отражающие гормональный фон. Что касается расширения воротникового пространства, помимо синдрома Дауна, порядка 50-ти патологий сопровождаются этим признаком.
Практика такова: ложно-положительные и ложно-отрицательные результаты присущи любому скрининговому исследованию. Стопроцентная точность невозможна, это вспомогательный метод для выявления группы риска. Последующие исследования — консультация генетика, инвазивные методики и консилиум врачей разных специальностей — дают возможность подтвердить или опровергнуть диагноз.
У специалистов в этой области существует профессиональное определение «российские плоды с синдромом Дауна очень сложны для диагностики». В отличие от европейских плодов с синдромом Дауна они очень часто попадают в окно нормальных значений толщины воротникового пространства, длины носовой кости и пр. Их сложно выявить. Дело в том, что на территории нашей страны смешалось много наций. В наших жилах течет очень разная кровь, велико присутствие генов монголоидной расы. А при анализе ультразвуковой картины учитываются национальные особенности. И зачастую отклонение от нормативных значений можно принять за этнические черты.
Статистически в популяции на 100 000 плодов только 200 будут иметь синдром Дауна. При этом еще 200 будут иметь другие хромосомные дефекты и 99 600 будут иметь нормальный набор хромосом. Таким образом у порядка 5% эмбрионов воротниковое пространство, как ключевой показатель, будет выше нормативных значений.
Акушер-гинеколог, ведущий беременность, основываясь только на данных ультразвукового исследования и на уровне биохимических маркеров, не может судить, есть ли у плода синдром Дауна. После комбинированного скрининга пациентка направляется в медико-генетический центр. Для подтверждения или опровержения диагноза потребуется консультация врача-генетика и инвазивная пренатальная диагностика.
Врач-генетик анализирует уровень сывороточных маркеров, собирает анамнез, анализирует ультразвуковое исследование и, возможно, назначает повторный ультразвук у врача экспертного уровня. Если высокий риск присутствия хромосомной патологии подтверждается, следующий этап — это инвазивная пренатальная диагностика. В зависимости от срока беременности выделяют хорионбиопсию (на сроке от 11 до 15 недель) и амниоцентез.
Хорион — это будущая плацента, для анализа берут ее образец, в этом материале выявляют клетки плода и исследуют их ДНК. Амниоцентез выполняется после 15 недель — для анализа берется амниотическая жидкость (жидкость, в которой находится плод), в ней также выделяются клетки плода.
Инвазивное исследование назначается только при выявлении высокого риска по результатам комбинированного скрининга — 1:100 и выше (1:50, 1:20). Дело в том, что у каждой инвазивной методики есть процент потерь беременности. Он приблизительно равен 1%. То есть после проведения процедуры одна из ста пациенток может потерять беременность. Поэтому проведение инвазивного исследования должно быть оправдано высокими рисками появления ребенка с хромосомными аномалиями.
Инвазивные методы исследование дают порядка 90-99% точности в определении хромосомной патологии плода. Проводить или не проводить инвазивный тест, оставлять или прерывать беременность после подтверждения подозрений — окончательное решение остается за будущими родителями. Им предстоит оценить все риски, возможные последствия и принять итоговое решение. Долг врача — предоставить пациентке максимально полную информацию, дать предполагаемый прогноз. Но решение судьбы беременности и ответственность за будущее ребенка все-таки лежит на его родителях.
В 21 веке планирование и рождение детей происходит в принципиально изменившихся реалиях. Новые возможности медицины по диагностике, ухудшение экологической ситуации, повышение возраста первой беременности. Все эти факторы значительно меняют сам подход к рождению детей. Сегодня вынашивание ребенка требует от женщины достаточно высокой компетентности в медицинских, социальных и даже правовых вопросах. Все большее значение приобретает подготовка к зачатию. Поэтому мировая медицина однозначна в своих рекомендациях: планирование любой беременности стоит начинать с консультации репродуктолога. Обращаясь в Клинику МАМА, вы можете быть уверены, что получите полный цикл диагностических и лечебных услуг европейского уровня.
Что такое НИПТ и почему об этом исследовании столько говорят в последнее время? Какие преимущества у данных тестов? Кому они показаны и существуют ли ограничения? Сегодня мы найдём ответы на эти и другие актуальные вопросы.
Биохимические скрининговые программы не обладают высокой точностью, они основаны на cовокупности данных статистики, уровня гормонов и размеров плода по УЗИ. Амниоцентез – самый точный метод, но он инвазивный (нужно сделать прокол плодного пузыря, чтобы получить для исследования клетки, принадлежащие плоду) и угрожает развитием осложнений и прерыванием беременности.
Медицинская наука не прекращала поиски новых тестов для скрининга, которые были бы более точны и не зависели от расчётных показателей. В качестве скрининговых тестов в последнее время хорошо себя зарекомендовали НИПТ (неинвазивные пренатальные тесты) как надёжные, удобные и не мешающие нормальному протеканию беременности. Точность метода достигает 99,9%, так как исследуется генетический материал плода (его ДНК) в венозной крови будущей матери.
Как это возможно? Учёные выяснили, что начиная примерно с 10 недели беременности в крови женщины свободно циркулирует ДНК плода. Благодаря современным технологиям врачи научились выделять её и исследовать, выявляя самые распространенные изменения хромосом.
Таким образом, почти каждая женщина может сдать венозную кровь, дождавшись срока 10 недель беременности, и определить генетическое здоровье будущего малыша.
В каких случаях исследование с применением НИПТ будет наиболее полезно?
В спектре лаборатории KDL представлено несколько комплексов НИПТ. Они отличаются объёмом исследования, показаниями и ограничениями. Важно чтобы понять, какой тест подходит именно Вам.
В каких случаях выполнение НИПТ невозможно?
Итак, выполнение неинвазивных пренатальных тестов возможно при одноплодной и двуплодной беременности. Если беременность одноплодная естественная или наступила после ЭКО с использованием собственной яйцеклетки, то доступны все исследования НИПТ. В остальных случаях существуют ограничения.
В чем отличия разных тестов линейки НИПТ?
НИПС Т21 (Геномед)- диагностика только синдрома Дауна. В исследовании выявляется дополнительная 21 хромосома, если она есть у плода. Синдром Дауна считается одной из самых частых хромосомных аномалий и его частота растёт с увеличением возраста женщины. Выполняется при беременности вследствие естественного зачатия, при ЭКО с собственной яйцеклеткой или при использовании донорской яйцеклетки; при беременности одним плодом и двойней, а также при суррогатном материнстве и если произошла редукция одного эмбриона в двойне.
НИПС 5 – ДНК тест на 5 синдромов (Геномед) – неинвазивный тест на 5 синдромов, можно определить аномалии 13, 18, 21 и в большинстве исследований выявить аномалии половых хромосом X и Y.
НИПС 5 универсальный, его выполнение возможно как при одноплодной естественной беременности, так и при беременности двойней, при носительстве донорской яйцеклетки, суррогатным матерям и в том случае, когда один плод в двойне редуцирован.
3 тестовые базовые панели:
Базовые панели позволяют выявить хромосомные аномалии 13,18, 21, Х и Y хромосом плода, а также триплоидии.
НИПС (Геномед) – включает определение вышеперечисленных синдромов (скрининг 13, 18, 21, Х, Y хромосом плода) и определение носительства у матери частых мутаций, которые могут привести к наследственным болезням, если ребенок унаследует два дефектных рецессивных гена от обоих родителей или один доминантный ген. Данные мутации выявляются в крови без выделения ДНК плода, т.е. оценивается не хромосомная мутация плода, а наличие аномальных вариантов генов у матери.
Генетические заболевания, связанные в тестируемыми в этом исследовании вариантами генов:
НИПС уникален не только клинической значимостью, но и доступностью. Одноплодная беременность, беременность двойней (с определением зиготности), в том числе при редукции одного из эмбрионов в двойне. При ЭКО с донорской яйцеклеткой и суррогатном материнстве этот тест нецелесообразен, так как определять мутации, связанные с генетическими заболеваниями нужно по крови той женщины, чья яйцеклетка дала начало эмбриону.
Следующие 2 панели включают микроделеционные синдромы:
Микроделеции – это поломки сегмента хромосом, которые являются менее распространенными, но не менее опасными, и их невозможно заподозрить на УЗИ.
НИПТ Panorama, расширенная панель (Natera) – исследуются и стандартные аномалии хромосом (13,18,21, Х, Y, триплоидии) и микроделеционные синдромы. Если у Вас беременность одноплодная естественная или в результате ЭКО с собственной яйцеклеткой, то выполнение данных панелей возможно.
При наличии двух плодов, ЭКО с донорской яйцеклеткой и суррогатном материнстве определить сегментарные нарушения технически невозможно.
Можно ли определить пол плода и в каких случаях?
Да, по желанию женщины любой НИПТ определяет пол плода и это доступно как при одноплодной, так и при двуплодной беременности.
Обращаем Ваше внимание, что получение результатов, указывающих на риски развития патологических синдромов, требует консультации генетика и дополнительной инвазивной диагностики.
Неинвазивное пренатальное тестирование: революция в пренатальном скрининге

Выявление циркулирующих клеток плода в кровотоке матери: на этапе революции генетической диагностики
Экскурс в историю
В 1959 году Lejeune и его коллеги впервые продемонстрировали, что в основе формирования синдрома Дауна лежит образование дополнительной копии 21 хромосомы (трисомия 21). Это открытие вызвало настоящий переворот в медицине. Позднее были установлены причины синдромов Патау и Эдвардса — трисомии по 13 и 18 хромосомам. Ученые со всего мира потратили десятки лет на изобретение технологий, позволяющих диагностировать хромосомные аномалии у плода еще на ранних сроках беременности. В настоящее время все беременные женщины проходят неинвазивный комбинированный скрининг I триместра, состоящий из биохимического анализа крови и ультразвукового исследования, который позволяет выявить группу пациентов высокого риска. Чувствительность этого подхода составляет 75−95% с частотой ложноположительных результатов 5−10%. Таким образом, врачи вынуждены направлять до 30% беременных женщин на проведение инвазивной диагностики, которая помимо высокой чувствительности всегда ассоциирована с риском невынашивания беременности.
В 1997 году Lo et al. выявили, что в крови матери, начиная с 4-ой недели беременности и до рождения ребенка, помимо материнской свободная внеклеточная ДНК, циркулирует еще и фрагменты ДНК плода. Концентрация этой ДНК медленно увеличивается на протяжении всей беременности, в среднем составляя от 11% до 13,4% от всей свободноциркулирующей ДНК в крови женщины. Это открытие произвело настоящую революцию в медицине и привело к разработке и внедрению в клиническую практику НИПТ.
В 1969 году исследователи сделали настоящее открытие: они впервые заявили о том, что в крови матери циркулируют клетки плода, которые теоретически можно выделить и проанализировать на наличие хромосомных патологий [7]. Новых подход произвел настоящую революцию в генетической диагностике. В крови матери было выделено несколько типов клеток плода, включая трофобласт, лимфоциты, гранулоциты, ядерные эритроциты и тромбоциты.
Первые попытки определения анеуплодий и трисомий путем выделения из крови матери и анализа клеток плода были проведены методом флуоресцентной гибридизации in situ [8]. Однако, данный метод имел свои ограничения и не позволял проводить точный анализ при наличии небольшого количества выделенных фетальных клеток. На смену этому методу пришел более новый: Lo et al. (1997) выявили, что в крови матери возможно определение внеклеточной ДНК плода, концентрация которой достигает поразительно высоких значений в 3,4−6,2%, что в 20−25 раз выше концентрации клеточных фракций плода в крови матери [9,10]. Кроме того, обнаружить фетальную ДНК возможно в даже небольшом объеме крови матери: достаточно образца объемом всего 10 мл [10]. Данное открытие произвело настоящую революцию в медицине и привело к открытию и массовому использованию новейшего, уникального диагностического метода — неинвазивного пренатального тестирования.
НИПТ — прорыв в области диагностики хромосомных аномалий плода
В период с марта 2012 года по апрель 2013 года проведено масштабное международное исследование, в котором проанализировали образцы крови у 15 841 беременной женщины в возрасте от 18 до 48 лет со сроком гестации от 10 до 14 недель. Всем пациентам выполнили стандартный комбинированный скрининг и НИПТ с целью обнаружения риска трисомии по 21, 18 и 13 хромосомам. Кроме того, авторы изучили чувствительность НИПТ для пациенток в возрасте до 35 лет, а также для пациенток из этой возрастной группы, которые по результатам скрининга I триместра имели риск трисомии 21 хромосомы менее 1:270 (группа низкого риска).
В 68 случаях был выявлен высокий риск хромосомной аномалии (т.е., в 1 беременности из 236). Из них: 38 случаев указывали на риск синдрома Дауна, 10 — синдром Эвардса, 6 — синдром Патау, 3 случая — сидром Шерешевского-Тернера (моносомия Х).
| Переменная | Стандартный скрининг | НИПТ | ||
|---|---|---|---|---|
| Все пациенты (n = 15 841) | Все пациенты (n = 15 841) | Пациенты в возрасте до 35 лет (n = 11 994) | Пациенты низкой группы риска (n = 14 957) | |
| Истинно положительный результат | 30 | 38 | 19 | 8 |
| Истинно отрицательный результат | 14 949 | 15 794 | 11 969 | 14 941 |
| Ложно положительный результат | 854 | 9 | 6 | 8 |
| Ложно отрицательный результат | 8 | 0 | 0 | 0 |
| Чувствительность (95% ДИ), % | 78,9 (62,7−90,4) | 100 (90,4−100) | 100 (82,4−100) | 100 (63,1−100) |
| Специфичность (95% ДИ), % | 94,6 (94,2−94,9) | 99,9 (99,9−100)* | 99,9 (99,9−100) | 99,9 (99,9−100) |
| Прогностическая ценность положительного результата (95% ДИ), % | 3,4 (2,3−4,8) | 80,9 (66,7−90,9)* | 76,0 (54,9−90,6) | 50 (24,7−75,3) |
| Прогностическая ценность отрицательного результата (95% ДИ), % | 99,9 (99,9−100) | 100 (99,9−100)† | 100 (99,9−100) | 100 (99,9−100) |
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.