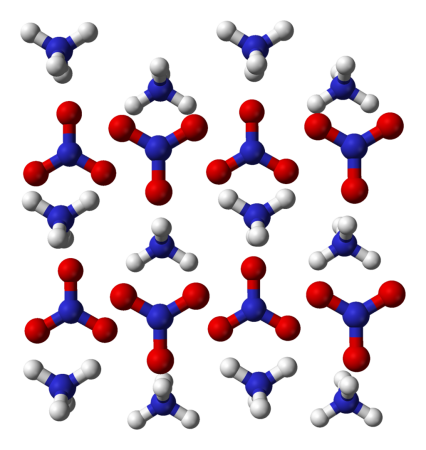
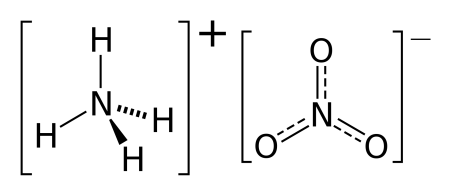Нитрат аммония
| Нитрат аммония | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитрат аммония |
| Химическая формула | NH4NO3 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдый |
| Отн. молек. масса | 80,04 а. е. м. |
| Молярная масса | 80,04 г/моль |
| Плотность | 1,725 (IV модификация) г/см³ |
| Термические свойства | |
| Температура плавления | 169,6 °C |
| Температура кипения | 235 °C |
| Температура разложения | |
| Химические свойства | |
| Растворимость в воде | 20 °C — 190 г/100 мл |
| Классификация | |
| Рег. номер CAS | 6484-52-2 |
Нитра́т аммо́ния (аммонийная (аммиачная) селитра) — химическое соединение NH4NO3, соль азотной кислоты. Впервые получена Глаубером в 1659 году.
Содержание
Физические свойства
Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение вещества, а при температуре 210 °C происходит полное разложение. Температура кипения при повышенном давлении — 235 °C. Молекулярная масса 80,04 а. е. м.. Скорость детонации 2570 м/с.
Растворимость
| Температура, °C | Растворимость, г/100мл |
|---|---|
| 0 | 119 |
| 25 | 212 |
| 50 | 346 |
| 100 | 1024 |
При растворении происходит сильное поглощение тепла (аналогично нитрату калия), что значительно замедляет растворение. Поэтому для приготовления насыщенных растворов нитрата аммония применяется нагревание, при этом твёрдое вещество засыпается небольшими порциями.
Состав
Содержание элементов в нитрате аммония в массовых процентах:
Методы получения
Основной метод
В промышленном производстве используется безводный аммиак и концентрированная азотная кислота:
Реакция протекает бурно с выделением большого количества тепла. Проведение такого процесса в кустарных условиях крайне опасно (хотя в условиях большого разбавления водой нитрат аммония может быть легко получен). После образования раствора, обычно с концентрацией 83 %, лишняя вода выпаривается до состояния расплава, в котором содержание нитрата аммония составляет 95—99,5 % в зависимости от сорта готового продукта. Для использования в качестве удобрения расплав гранулируется в распылительных аппаратах, сушится, охлаждается и покрывается составами для предотвращения слёживания. Цвет гранул варьируется от белого до бесцветного. Нитрат аммония для применения в химии обычно обезвоживается, так как он очень гигроскопичен и процентное количество воды в нём (
Метод Габера
По способу Габера из азота и водорода синтезируется аммиак, часть которого окисляется до азотной кислоты и реагирует с аммиаком, в результате чего образуется нитрат аммония:
Нитрофосфатный метод
Этот способ также известен как способ Одда, названный так в честь норвежского города, в котором был разработан этот процесс. Он применяется непосредственно для получения азотных и азотно-фосфорных удобрений из широко доступного природного сырья. При этом протекают следующие процессы:
А также амфотерный метод.
Химические свойства
Реакции разложения
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
Кристаллические состояния нитрата аммония
Изменения кристаллического состояния нитрата аммония под воздействием температуры и давления меняют его физические свойства. Обычно различают следующие состояния:
| Система | Диапазон температур (°C) | Состояние | Изменение объёма (%) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| — | > 169.6 | жидкость | |||||||||||
| I | 169.6 — 125.2 | кубическая | +2.1 | ||||||||||
| II | 125.5 — 84.2 | тетрагональная | −1.3 | ||||||||||
| III | 84.2 — 32.3 | α-ромбическая | +3.6 | ||||||||||
| IV | 32.3 — −16.8 | β-ромбическая | −2.9 | ||||||||||
| V | Применение Взрывчатые веществаНаиболее широко в промышленности и горном деле применяются смеси аммиачной селитры с различными видами углеводородных горючих материалов, других взрывчатых веществ, а также многокомпонентные смеси: УдобренияБо́льшая часть нитрата аммония используется либо непосредственно как хорошее азотное удобрение, либо как полупродукт для получения прочих удобрений. Аварии и взрывыДополнительная информацияМировое производство аммиачной селитры на 1980 год составляло 14 млн т, в пересчёте на азот. В весенний период подкормка из азотного аммония — идеальный вариант, так как растения на начальном этапе роста потребляют азот в огромных количествах. Рассмотрим нюансы применения в качестве минеральной подкормки аммиачной селитры. Что это такое?
Формула: NH4+. Химический состав: нитраты, металлы, аммоний с положительным зарядом ионов. Виды | ||||||||||||
| Нормы расхода аммиачной селитры | ||
| Овощи | 5-10 г на 1 кв.м | Вносить дважды за сезон: в июне (до цветения) и июле (после того, как завяжутся плоды). Не рекомендуется применять для подкормки кабачков, тыквы и патиссонов (из-за риска накопления нитратов). |
| Корнеплоды | 5-7 г на 1 кв.м | Вносить спустя 3 недели после появления всходов в бороздки между рядами, заделывая в почву на глубину 2-3 см. |
| Плодовые деревья | 15-20 г на 1 кв.м | Можно вносить в сухом виде однократно в начале сезона (с появлением листьев) – 15-20 г на 1 кв.м. Предпочтительнее – в виде раствора (25-30 г на 10 л воды) под корень трижды за лето. |
Для удобства расчета возьмите на заметку: в 1 ст.л. помещается 17 г аммиачной селитры, в 1 стакане – приблизительно 170 г гранул.
При высадке рассады томатов, дынь и перцев в почву вносят аммиачную селитру из расчета 3-4 г на лунку или 4-6 г на погонный метр. А вот полив аммиачной селитрой восполнит недостаток азота у растений в период вегетации (для приготовления раствора аммиачной селитры 30-40 г удобрения растворяют в 10 л воды).
Внекорневая подкормка аммиачной селитрой опасна для растений, поскольку высокая концентрация азота в удобрении может стать причиной ожога листьев. Если размышляете над тем, чем заменить аммиачную селитру, то вот совет: для опрыскивания по листу подойдет 1%-ный раствор мочевины (100 г удобрения на 10 л воды).
Что подкармливают аммиачной селитрой?
Аммиачную селитру используют для подкормки рассады, выращивания культур в открытом и закрытом грунте. Нитрат аммония можно применять также во время активного роста растения.
Подкормка рассады аммиачной селитрой способствует укреплению здоровья сеянцев, их росту. Подробнее о том, как развести аммиачную селитру для подкормки рассады томатов:
Удобрение вносят под корень после полива рассады, используя раствор в объеме, равном количеству воды при поливе. Нельзя допускать попадания удобрения на листья растения, а при необходимости промывать их водой.
Огурцы можно подкармливать аммиачной селитрой в комплексе с другими удобрениями:
первая подкормка (спустя 2 недели после посадки): 10 г аммиачной селитры, 10 г калийной соли и 10 г супeрфосфата нa 10 л вoды;
вторая подкормка (в начале цветения): 30 г аммиачной селитры, 20 г калийной селитры и 40 г суперфосфата на 10 л воды.
Подкормка картофеля аммиачной селитрой весной – необходимая мера для полноценного питания этой культуры. Перед посадкой в перекопанную почву из расчета на 1 кв.м вносят смесь удобрений: 20 г аммиачной селитры и 20 г сульфата калия (их можно заделать в почву вместе с сидератами). Полезна и междурядная подкормка такой же смесью либо раствором аммиачной селитры (20 г гранул на 10 л воды) перед первым окучиванием. Почву слегка рыхлят, а после внесения удобрения обильно поливают.
В первый год после посадки клубнику не удобряют аммиачной селитрой, чтобы не допустить переизбытка азота.

На второй год клубнику подкармливают из расчета 10 г на 1 кв.м, внося гранулы в бороздки глубиной 10 см, сделанные в междурядьях, и засыпают землей. На третий год вносят смесь: 15 г аммиачной селитры, 10 г хлористого калия, 10 г суперфосфата на 1 кв.м.
Ранней весной, когда сойдет снег, почву на участке, где планируется посадка чеснока, перекапывают и вносят аммиачную селитру (10-12 г на 1 кв.м). Озимый чеснок подкармливают смесью удобрений: 6 г аммиачной селитры, 5-6 г сульфата калия, 9-10 г суперфосфата на 1 кв.м. Через месяц подкормку повторяют.
При высадке севка в почву вносят смесь удобрений: 7 г аммиачной селитры, 5 г хлористого калия и 7 г суперфосфата на 1 кв.м. В дальнейшем за сезон проводят еще 2 подкормки аммиачной селитрой:
Хранение аммиачной селитры
Чтобы азот не улетучился, аммиачную селитру хранят в сухом темном закрытом, но хорошо вентилируемом помещении при температуре не выше 30°С. Это вещество взрывоопасно, поэтому нельзя допускать перегрева удобрения.
В регионах с нормальной влажностью это удобрение рекомендуется применять весной и в первой половине лета, а в регионах с высоким уровнем влажности – еще и осенью.
Нитрат аммония
наименование
210 °C
Нитрат аммония (аммонийная (аммиачная) селитра) — химическое соединение NH4NO3, соль азотной кислоты. Впервые получена Глаубером в 1659 году. Используется в качестве компонента взрывчатых веществ и как азотное удобрение.
Содержание
Физические свойства
Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение вещества, а при температуре 210 °C происходит полное разложение. Температура кипения при пониженном давлении — 235 °C. Молекулярная масса 80,04 а. е.м. Скорость детонации 2570 м/с.
Растворимость
Растворимость в воде:
| Температура, °C | Растворимость, г/100мл |
|---|---|
| 0 | 119 |
| 10 | 150 |
| 25 | 212 |
| 50 | 346 |
| 80 | 599 |
| 100 | 1024 |
При растворении происходит сильное поглощение тепла (аналогично нитрату калия), что значительно замедляет растворение. Поэтому для приготовления насыщенных растворов нитрата аммония применяется нагревание, при этом твёрдое вещество засыпается небольшими порциями.
Также соль растворима в аммиаке, пиридине, метаноле, этаноле.
Состав
Содержание элементов в нитрате аммония в массовых процентах:
Методы получения
Основной метод
В промышленном производстве используется безводный аммиак и концентрированная азотная кислота:
Реакция протекает бурно с выделением большого количества тепла. Проведение такого процесса в кустарных условиях крайне опасно (хотя в условиях большого разбавления водой нитрат аммония может быть легко получен). После образования раствора, обычно с концентрацией 83 %, лишняя вода выпаривается до состояния расплава, в котором содержание нитрата аммония составляет 95—99,5 % в зависимости от сорта готового продукта. Для использования в качестве удобрения расплав гранулируется в распылительных аппаратах, сушится, охлаждается и покрывается составами для предотвращения слёживания. Цвет гранул варьируется от белого до бесцветного. Нитрат аммония для применения в химии обычно обезвоживается, так как он очень гигроскопичен и процентное количество воды в нём получить практически невозможно.
Метод Габера
По способу Габера из азота и водорода синтезируется аммиак, часть которого окисляется до азотной кислоты и реагирует с аммиаком, в результате чего образуется нитрат аммония:
Нитрофосфатный метод
Этот способ также известен как способ Одда, названный так в честь норвежского города, в котором был разработан этот процесс. Он применяется непосредственно для получения азотных и азотно-фосфорных удобрений из широко доступного природного сырья. При этом протекают следующие процессы:
А также амфотерный метод.
Химические свойства
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
Кристаллические состояния нитрата аммония
Изменения кристаллического состояния нитрата аммония под воздействием температуры и давления меняют его физические свойства. Обычно различают следующие состояния:
| Система | Диапазон температур (°C) | Состояние | Изменение объёма (%) | |
|---|---|---|---|---|
| — | > 169.6 | жидкость | ||
| I | 169.6 — 125.2 | кубическая | −2.13 | |
| II | 125.5 — 84.2 | тетрагональная | −1.33 | |
| III | 84.2 — 32.3 | α-ромбическая | +0.8 | |
| IV | 32.3 — −16.8 | β-ромбическая | −3.3 | |
| V | −50 — −16.8 | тетрагональная | +1.65 | |
| VI | существует при высоких давлениях | |||
| VII | 170 | |||
| VIII | существует при высоких давлениях | |||
| IX | существует при высоких давлениях |
Фазовый переход от IV к III при 32,3 °C приносит неприятности производителям удобрений, потому как изменения плотности приводят к разрушению частиц при хранении и применении. Это особенно важно в тропических странах, где нитрат аммония испытывает циклические изменения, приводящие к разрушению гранул, слёживанию, повышенному пылению и риску возникновения взрыва.
Применение
Удобрения
Бо́льшая часть нитрата аммония используется либо непосредственно как хорошее азотное удобрение, либо как полупродукт для получения прочих удобрений. Для предотвращения создания взрывчатых веществ на основе нитрата аммония в удобрения, доступные в широкой продаже, добавляют компоненты, снижающие взрывоопасность и детонационные свойства чистого нитрата аммония, такие как мел (карбонат кальция).
В Австралии, Китае, Афганистане, Ирландии и некоторых других странах свободная продажа нитрата аммония даже в виде удобрений запрещена или ограничена. После террористического акта в Оклахома-Сити ограничения на продажу и хранение нитрата аммония были введены в некоторых штатах США.
Взрывчатые вещества
Наиболее широко в промышленности и горном деле применяются смеси аммиачной селитры с различными видами углеводородных горючих материалов, других взрывчатых веществ, а также многокомпонентные смеси:
Безопасный состав
Дополнительная информация
Мировое производство аммиачной селитры на 1980 год составляло 14 млн т, в пересчёте на азот.

 Чтобы получить аммиачную селитру, используется концентрированная азотная кислота и аммиак.
Чтобы получить аммиачную селитру, используется концентрированная азотная кислота и аммиак.