Нитрат ртути I
| Нитрат ртути I | |
|---|---|
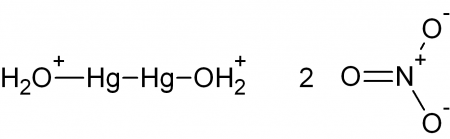 | |
| Систематическое наименование | Нитрат ртути I |
| Хим. формула | Hg2(NO3)2 |
| Состояние | бесцветные кристаллы |
| Молярная масса | 525.2 г/моль |
| Плотность | 4,79 г/см³ |
| Температура | |
| • плавления | 70 °C |
| Энтальпия | |
| • образования | -868 кДж/моль |
| Рег. номер CAS | [7782-86-7] |
| PubChem | 51346573 |
| Рег. номер EINECS | 233-886-4 |
| SMILES | |
| ChemSpider | 9493944 и 21493988 |
| Токсичность | Чрезвычайно токсичен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Синонимы: динитрат диртути, ртуть азотнокислая закисная.
Содержание
Физические и химические свойства
В чистом виде — бесцветные кристаллы, в воде гидролизуются, растворимы в сероуглероде и азотной кислоте. Растворы обладают сильными восстановительными свойствами. Для предотвращения частичного окисления кислородом воздуха, в растворы нитрата ртути добавляют свободную ртуть.
Образует кристаллогидрат Hg2(NO3)2•2H2O. На воздухе теряет кристаллогидратную воду.
Неустойчив, при добавлении щелочи к раствору соли образуется чёрный осадок:
Разлагается при температуре 70-150°C:
Концентрированный раствор соли гидролизуется водой с образованием осадка основной соли:
Реагирует с разбавленной хлороводородной кислотой:
Окисляется горячей концентрированной азотной кислотой:
Может также окислиться разбавленной азотной кислотой в присутствии кислорода:
Выпадение желтого осадка ртути при реакции с медью:
Hg2(NO3)2 + C u → 2 H g ↓ + C u ( N O 3 ) 2
Реагирует с насыщенным раствором сероводорода:
Выпадает осадок дийодида диртути при добавлении йодида калия:
На холоду реагирует с гидрокарбонатом калия:
Получение
Соль может быть получена из металлической ртути при действии разбавленной азотной кислоты на холоду:
А также при добавлении жидкой ртути к нитрату ртути:
Производство
В СССР выпускался химический реактив Ртуть I азотнокислая 2-водная нескольких квалификаций по ГОСТ 4521-78.
Применение
Токсикология и физиологические свойства
Нитрат ртути(II)
| Нитрат ртути(II) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Общие | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Систематическое наименование | Нитрат ртути(II) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Традиционные названия | Азотнокислая ртуть | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Химическая формула | Hg(NO3)2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная масса | 324,30 г/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность | гидр. 4,30 г/см³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Термические свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 79 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Классификация | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рег. номер CAS | 10045-94-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Регистрационный номер EC | 233-152-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| RTECS | OW8225000 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер ООН | 1625 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Безопасность | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Нитрат ртути(II)» в других словарях:
Нитрат ртути — Нитрат ртути: Нитрат ртути(I) Нитрат ртути(II) Список значений слова или словосочетания со ссылкам … Википедия
нитрат ртути — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN silver nitrate … Справочник технического переводчика
Нитрат ртути(I) — У этого термина существуют и другие значения, см. Нитрат ртути. Нитрат ртути(I) … Википедия
Нитрат аммония — Нитрат аммония … Википедия
Нитрат меди(II) — Нитрат меди(II) … Википедия
Нитрат калия — Нитрат калия … Википедия
Нитрат натрия — Нитрат натрия … Википедия
Нитрат бария — Нитрат бария … Википедия
Нитрат лития — Нитрат лития … Википедия
Нитрат стронция — Общие … Википедия
Нитрат ртути(I)
| Нитрат ртути(I) | |
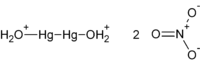 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитрат ртути(I) |
| Химическая формула | Hg2(NO3)2 |
| Физические свойства | |
| Состояние (ст. усл.) | бесцветные кристаллы |
| Отн. молек. масса | 525.2 а. е. м. |
| Молярная масса | 525.2 г/моль |
| Плотность | 4,79 (для гидрата при 4 °C), г/см³ |
| Термические свойства | |
| Температура плавления | 70 (для гидрата) °C |
| Классификация | |
| Рег. номер CAS | [7782-86-7] |
Нитрат ртути(I) — химическое соединение, существует только в виде димера Hg2(NO3)2.
Синонимы: динитрат диртути, ртуть азотнокислая закисная.
Содержание
Свойства
В чистом виде — бесцветные кристаллы, в воде гидролизуются, растворимы в сероуглероде и азотной кислоте. Растворы обладают сильными восстановительными свойствами. Для предотвращения частичного окисления кислородом воздуха, в растворы нитрата ртути добавляют свободную ртуть.
Образует кристаллогидрат Hg2(NO3)2·2H2O. На воздухе теряет кристаллогидратную воду.
При разбавлении нитрата ртути водой на холоде медленно, а при нагревании быстрее, выпадает лимонно-желтый осадок основной соли Hg2OH(NO3).
Неустойчив, при добавлении щелочи к раствору соли образуется черный осадок:
Получение
Может быть получена по реакциям обмена или из металлической ртути при действии азотной кислоты и нагревании не выше 45 °C.
Производство
В СССР выпускался химический реактив Ртуть (I) азотнокислая 2-водная нескольких квалификаций по ГОСТ 4521-78.
Применение
Безопасность обращения
См. также
Литература
Нитрат ртути II
| Нитрат ртути II | |
|---|---|
 | |
| Систематическое наименование | Нитрат ртути II |
| Традиционные названия | Азотнокислая ртуть |
| Хим. формула | Hg(NO3)2 |
| Молярная масса | 324,30 г/моль |
| Плотность | гидр. 4,30 г/см³ |
| Температура | |
| • плавления | 79 °C |
| Рег. номер CAS | 10045-94-0 |
| PubChem | 16683796 |
| Рег. номер EINECS | 233-152-3 |
| SMILES | |
| RTECS | OW8225000 |
| Номер ООН | 1625 |
| ChemSpider | 23247 и 48056839 |
| Токсичность | токсично |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрат ртути II — неорганическое соединение, соль металла ртути и азотной кислоты с формулой Hg(NO3)2, бесцветные кристаллы, растворимые в кислых водных растворах, токсичен, гидролизуется горячей водой, образует кристаллогидраты.
Содержание
Получение
Физические свойства
Нитрат ртути II образует бесцветные кристаллы.
Растворим в подкисленной холодной воде, гидролизуется в горячей воде. Растворяется в ацетоне.
Образует кристаллогидраты состава Hg(NO3)2•n H2O, где n = ½, 1, 2, 8.
Ртуть (ІІ) азотнокислая – это. Что такое нитрат ртути (IІ)?
Если вы не понаслышке знаете, что такое химический анализ и органический синтез, вам обязательно нужно обладать информацией о таком веществе, как азотнокислая ртуть (ІІ). И не просто обладать, а уметь применять эти сведения на практике, знать, что собой представляет данный материал и в каких случаях он готов прийти вам на помощь.
Ртуть (ІІ) азотнокислая (нитрат ртути (ІІ)) – это соединение неорганической природы, являющееся, по своей сути, солью металлической ртути и HNO3. Это лишенная окраса прозрачная кристаллическая масса с массовой долей основного вещества не менее 99 %. Характеризуется токсичностью, на что не менее важно обращать внимание.
Растворению поддается в таких средах, как диметилкетон, углерода (IV) сульфид, азотная кислота и холодные кислые водные растворы. Формирует кристаллогидраты. Гидролиз можно наблюдать при воздействии горячей воды. Растворам характерны значительные восстановительные качества. При контакте с воздушными массами происходит потеря кристаллогидратной воды. Чтобы предотвратить частичное окисление кислородом воздуха в растворы вводят свободную ртуть.
Если разбавить нитрат ртути водой, выпадет осадок светло-желтого цвета. Это сформируется основная соль Hg2(OH)NO3. Причем на холоде реакция будет протекать более медленно, а при нагреве – оперативнее.
Из химических свойств стоит отметить следующие:
— разложение при нагреве до 360 °С на оксид ртути, диоксид азота и кислород, а при t более 400 °С – на ртуть, диоксид азота и кислород;
— вступление в обменные реакции;
— реагирование со ртутью в разбавленной нитратной кислоте.
Молярная масса – 324,3 г/моль, плотность гидр. – 4,3 г/см³. Термосвойства: t плавления – 79 °С. Формула: Hg(NO3)2.
Получение
Синтез данного вещества возможен разными способами:
— растворение Hg в нагретой до 90 °С HNO3 высокой концентрации;
— растворение HgO в разбавленной HNO3;
— окисление ртути азотнокислой закисной с помощью нагретой до 90 °С концентрированной HNO3 или кислородом в разбавленной кислоте;
— реагирование Hg и оксида азота.
Для получения безводной соли кристаллогидрат поддают сушению в условиях вакуума при 20-30 °С.
Применение
Ртуть (ІІ) азотнокислая – это индивидуальный химический препарат, предназначение которого заключается в химическом анализе научно-исследовательских и всяческих лабораторных работ. Соответственно, основные направления, в которых нитрат ртути (ІІ) находит применение – это химический анализ и органический синтез в условиях лаборатории. Здесь данное соединение известно в качестве важного реактива. В частности задействуется в меркуриметрических методах объемного анализа.
Среди других процессов, при выполнении которых часто не обходятся без Hg(NO3)2:
— нанесение покрытий из золота и бронзы;
— роспись изделий из фарфора;
— изготовление пестицидов и составов для семенеобработки;
— создание лечебных мазей для медицинских нужд;
Токсичность
Нитрат ртути (ІІ) – это токсичный химический продукт, как впрочем и сама ртуть и иные ее соединения (его токсичность примерно равна ядовитому воздействию хлорида ртути (II)). Принадлежит к первому классу опасности, то есть является сильно действующим на человеческий организм ядом. Перевозка и хранение должны производится с учетом принадлежности в этом плане к 6-му классу опасности хим. веществ.
Ввиду того, что рассматриваемое соединение является неорганическим, оно действует менее токсично, по сравнению с субстанциями органической этимологии. Но, так как на токсичность непосредственно влияет степень водорастворения, его отрицательное воздействие больше, если сопоставлять с хлоридом или сульфидом ртути.
Проникновение этой соли в организм возможно и вредно следующими способами: через дыхательные пути, ЖКТ, кожу и слизистые. После попадания оно не просто надолго задерживается в органах и системах, оно аккумулируется. Выведение, в основном, происходит, благодаря почкам, а также частично с помощью слюнных, молочных и некоторых других желез.
Техника безопасности
Чтобы избежать вышеупомянутых негативов при работе с этим реактивом, важно соблюдать ряд, в целом, несложных, но, как сами понимаете, жизненно важных требований. Во-первых, позаботьтесь о том, чтобы лаборатория была оборудована общей приточно-вытяжной вентиляцией. Во-вторых, всегда используйте СИЗ (респиратор, перчатки из резины и защитные очки) и не пренебрегайте мероприятиями личной гигиены. В-третьих, любые анализы с задействованием данного вещества проводите в лабораторном вытяжном шкафу.
Помните: чем более автоматизированными будут действия, осуществляемые с указанным реагентом, чем минимизированнее работа вручную, тем лучше и безопаснее для вас.
И следите, чтобы ПДК в воздушной среде рабочего пространства не превышала допустимых значений, а именно 0,2 мг/м³ или в среднем за смену 0,05 мг/м³.
Хранить этот продукт необходимо в крытых складах в герметичной таре производителя, исключая воздействие прямого солнечного излучения, не больше срока годности (полгода со дня изготовления). Если имеет место использование по истечении шестимесячного периода, результаты исследований могут подвергаться сомнениям. Кстати, герметичности требует и технологическое оборудование. Перевозка допустима любыми ТС с соблюдением правил, касающихся каждого из них.
Теперь вы не только знаете, что такое ртуть (ІІ) азотнокислая, но и обладаете всеми необходимыми сведениями о том, как правильно обращаться с данным веществом, дабы исключить любые негативные проявления. Будьте бдительны, берегите себя – и рассмотренный материал будет ассоциироваться у вас исключительно с важностью и ценностью применения, а не с опасностью и вредом.









