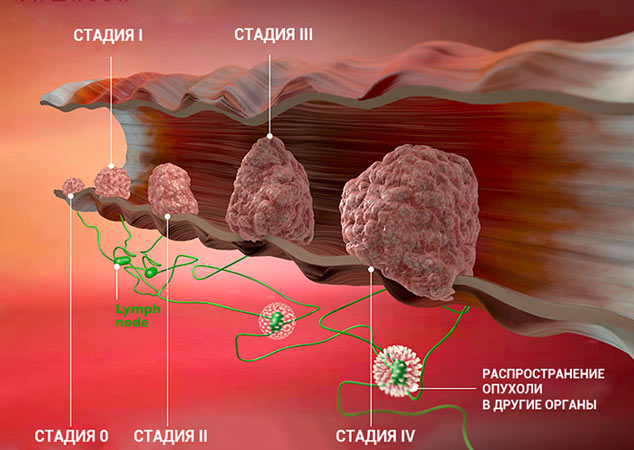
Стадии рака
Все опухоли (или, на языке врачей — новообразования) делят на две большие группы: доброкачественные и злокачественные. Первые обычно не опасны для жизни, а вторые, если человек не получает лечения, приводят к гибели. В 2015 году от рака во всем мире умерло почти 9 миллионов человек.
Фатальность злокачественных опухолей связана с двумя их главными свойствами, которые, собственно, и отличают их от доброкачественных новообразований:
Для врача важно понимать, насколько сильно рак успел распространиться в организме пациента. Ведь от этого зависит лечение и прогноз. Для того чтобы упростить эту задачу и внести четкость, в течении каждого онкологического заболевания принято выделять определенные стадии.
Классификация TNM
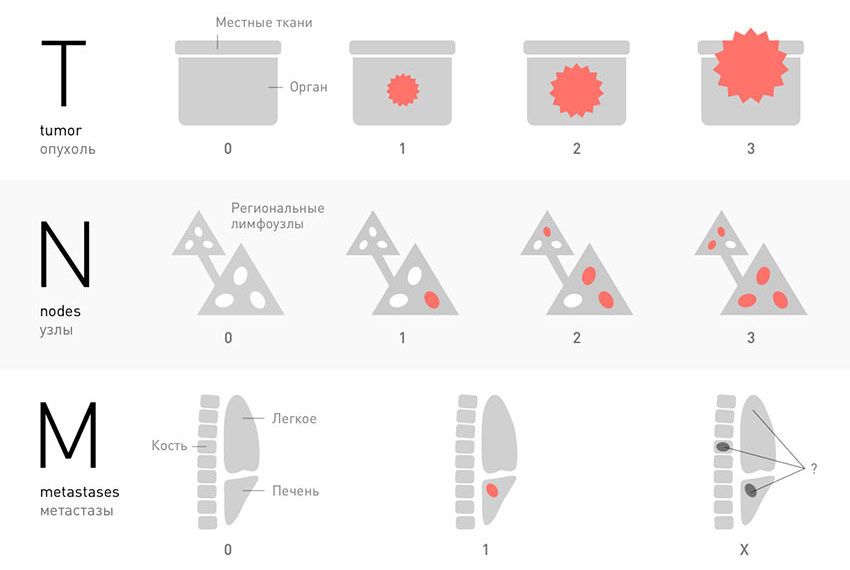
В большинстве случаев, для того чтобы установить стадию рака, ориентируются на три характеристики злокачественной опухоли, которые соответствуют трем буквам аббревиатуры TNM. К каждой букве приписывают индекс в виде цифры или специального обозначения.
T — tumor. Эта буква обозначает первичную опухоль, ее размеры, прорастание в стенку органа, соседние ткани:
N — nodus. Когда раковые клетки отрываются от первичной опухоли и мигрируют с током лимфы, в первую очередь они попадают в близлежащие (регионарные) лимфатические узлы. Можно сказать, что это первые баррикады на пути распространения рака в организме. В зависимости от того, обнаружены ли опухолевые клетки в регионарных лимфатических узлах, N может принимать значения:
M — metastasis. Эта буква показывает, обнаружены ли в теле больного отдаленные метастазы — вторичные очаги в различных органах:
Классификация TNM применима для большинства видов рака. Она позволяет очень подробно описывать злокачественные опухоли. В пределах основных групп выделяют подгруппы, их обозначают с помощью букв, например: T1a, T1b, T1c.
Однако, зачастую система TNM оказывается слишком громоздкой и не совсем удобной. Существует ее упрощенный вариант, когда возможные сочетания значений T, N и M сводят к пяти стадиям.
Стадии злокачественной опухоли
Часто онкологи обозначают стадию рака римской цифрой от I до IV. Эта классификация основана на TNM, но она проще и зачастую удобнее:
Это очень приблизительное описание стадий. Деление зависит от типа рака, от того, в каком органе он находится. Для того чтобы обозначить подстадию, к букве приписывают цифру. Например, стадия I может делиться на подстадии IA и IB.
Сторожевой лимфатический узел
Когда хирург оперирует онкологического пациента, зачастую ему приходится решать сложную задачу: стоит ли удалять регионарные лимфатические узлы? Если в них есть раковые клетки, и они будут оставлены в организме больного, произойдет рецидив. Если же удалить «чистые» лимфоузлы, это чревато осложнением в виде лимфедемы — отека на руке или ноге из-за нарушения оттока лимфы.
Раньше врачи нередко предпочитали меньшее из зол и удаляли лимфатические узлы «на всякий случай». Современные хирурги уже не действуют вслепую и могут более точно определить показания к лимфодиссекции. Это стало возможно благодаря появлению сентинель-биопсии или биопсии сторожевого лимфатического узла.
Сторожевым называется лимфатический узел (или группа лимфатических узлов), который первым принимает лимфу, оттекающую от злокачественной опухоли. Его можно обнаружить во время операции: для этого нужно ввести в опухоль флуоресцентный краситель или препарат с радиоактивной меткой. Препарат проникает в лимфатические сосуды, затем в сигнальный лимфоузел и «прокрашивает» его. Лимфатический узел удаляют и проверяют, нет ли в нем раковых клеток.
Для обозначения состояния сигнального лимфоузла используют специальную классификацию:
Если в сигнальном лимфоузле обнаружена опухолевая ткань — это показание к удалению регионарных лимфоузлов.
Степень злокачественности
Злокачественность и степень дифференцировки — два показателя, которые тесно взаимосвязаны. Они описывают внешний вид раковых клеток под микроскопом. Степень дифференцировки показывает, насколько раковая клетка отличается от здоровой. Если она высокая — опухолевая ткань похожа на здоровую. Низкодифференцированные раковые клетки полностью теряют сходство с нормальными.
Чем ниже степень дифференцировки и выше злокачественность, тем агрессивнее ведет себя рак и быстрее распространяется в организме. Для оценки используют гистологическую классификацию:
Шкала Глисона при раке простаты
Для того чтобы оценить степень злокачественности и агрессивности рака предстательной железы, используют шкалу Глисона, разработанную в 1960-х годах. В зависимости от того, как опухолевая ткань выглядит под микроскопом, ей присваивают оценку от 1 до 5. Чем ниже оценка, тем более высокодифференцированными и менее злокачественными являются клетки. Патологоанатом должен выявить два преобладающих типа ткани и выставить две оценки. Итоговая сумма баллов может колебаться от 2 до 10. Чем она больше, тем агрессивнее ведет себя опухоль, и выше риски.
Классификации рака печени
Классификация TNM не очень хорошо отражает течение злокачественных опухолей печени, поэтому в разных странах были созданы специальные классификации печеночно-клеточного рака. Например, многие врачи используют Барселонскую клиническую классификацию. В ее рамках выделяют следующие стадии рака печени:
В некоторых странах практикуется классификация итальянской программы по изучению рака печени (CLIP). В ней учитывается четыре фактора: состояние функции печени, распространение опухолевых очагов (больше или меньше половины печени), уровень альфа-фетопротеина (опухолевый маркер) и наличие тромбоза портальной вены. По каждому показателю врач выставляет оценку 0, 1 или 2 балла. Выживаемость пациентов зависит от суммы баллов:
В соответствии с системой CLIP, всех больных печеночно-клеточным раком можно поделить на две группы: 0–2 балла — значительно более благоприятный прогноз; более 2 баллов — значительно менее благоприятный прогноз.
В 1985 году была предложена классификация Okuda, в которой учитываются: степень поражения печени, наличие асцита (скопления жидкости в брюшной полости), изменение уровня альбумина и билирубина в крови. В соответствии с классификацией Okuda, выделяют три стадии рака печени:
Почему важно установить стадию злокачественной опухоли?
Знание стадии рака по TNM и другим системам помогает онкологу решать важные задачи:
Единые классификации помогают врачам из разных клиник и стран «разговаривать на одном языке». Видя стадию опухоли, диагностированную в другой клинике, онколог четко понимает, что это значит, и как дальше работать с пациентом.
Степени рака мочевого пузыря
Что такое степень рака?
Степень опухоли определяется тем, как раковые клетки выглядят под микроскопом. Врач сравнивает насколько опухолевая клетка отличается от нормальной.
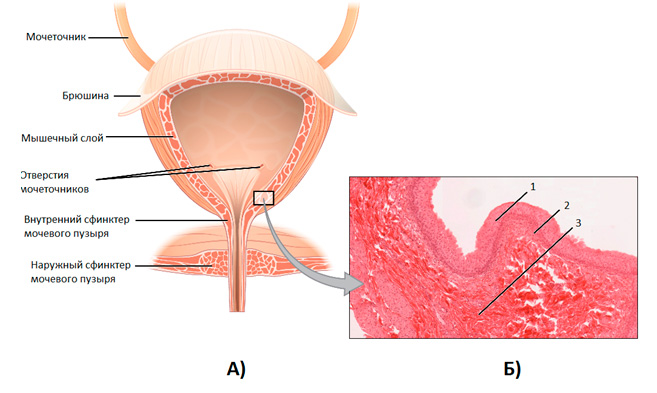
Рисунок. А – мочевой пузырь. Б – вид под микроскопом: 1 – слизистая оболочка, 2 – собственная пластинка, 3 – подслизистая оболочка.
В настоящее время распространены две системы классификации злокачественных поражений мочевого пузыря.
Классификация рака Всемирной организации здравоохранения (ВОЗ) от 1973 года
Низкая степень рака мочевого пузыря (1)
Здоровая ткань состоит из множества клеток разного вида, сгруппированных вместе. Если опухоль по строению напоминает здоровую ткань и ее клетки похожи на нормальные, она называется высокодифференцированной или низкой степени злокачественности. Такая опухоль растет медленно, не склонна к инвазии и имеет низкий риск метастазов. Хорошо лечится, вероятность рецидива невысока.
Средняя степень рака мочевого пузыря (2)
Раковые клетки выглядят более атипично, т.е. значительно отличаются от здоровых. Опухоль растет быстрее, имеет тенденцию к инвазивному росту, характеризуется более высокой вероятностью развития метастазов. Такая опухоль называется умеренно дифференцированной.
Высокая степень рака мочевого пузыря (3)
Такая опухоль наиболее злокачественна и опасна. Ее клетки и структура ткани абсолютно не похожи на здоровые, она быстро растет, распространяется на все слои мочевого пузыря и за его пределы, высока вероятность метастазирования. Опухоль называется низко дифференцированной. После лечения высок риск рецидива.
Классификация рака ВОЗ от 2004 года
Кроме злокачественных поражений мочевого пузыря существуют и доброкачественные опухоли, а также предраковые состояния. Классификация ВОЗ от 2004 года учитывает эти состояния и дает более детальную морфологическую оценку новообразований мочевого пузыря.
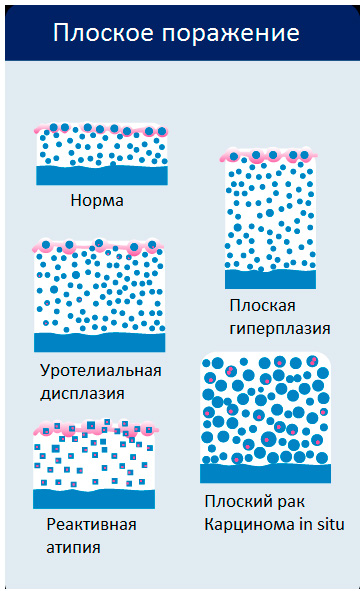
Плоские новообразования
Атипия – аномальное, отличающееся от нормального, строение клеток.
Рисунок. Плоские новообразования
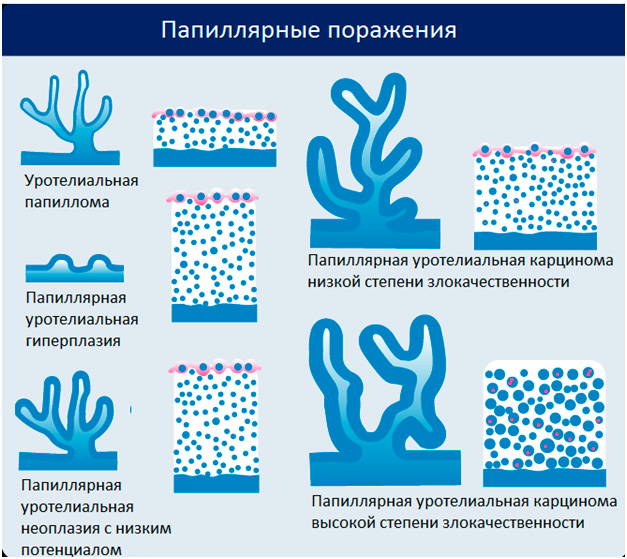
Папиллярные новообразования
Рисунок. Папиллярные новообразования.
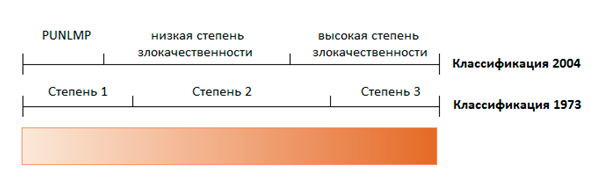
Соответствие двух классификаций
Классификация 2004 года
Классификация 1973 года
Папиллярная уротелиальная неоплазия с низким потенциалом
Папиллярная уротелиальная карцинома низкой степени злокачественности
Папиллярная уротелиальная карцинома высокой степени злокачественности
Рисунок. Соотношение классификаций
Кешишев Николай Георгиевич
Статьи по данной теме
Врачи направления
Видеоотзывы пациентов
Аденома простаты. ТУР простаты (Трансуретральная резекция) 4 года назад
Рак простаты с метастазами: 8 лет борьбы за жизнь
Коралловидный камень почки. Чрескожная нефролитотрипсия 10 дней назад
Низкий потенциал злокачественности что это
Лейомиоматозы — гетерогенная группа гладкомышечных опухолей с неопределенным потенциалом злокачественности. Она включает диффузный лейомиоматоз, агрессивный лейомиоматоз, интравенозный (внутрисосудистый) лейомиоматоз, доброкачественную метастазирующую лейомиому, перитонеальный лейомиоматоз (паразитирующая лейомиома), диссеминирующий перитонеальный лейомиоматоз. Для нозологий данной категории характерно формирование гладкомышечных опухолей с доброкачественными морфологическими характеристиками, но с нетипичной клинической картиной: внутрисосудистым распространением, формированием отдаленных метастазов, диссеминацией по брюшине, массивным вовлечением мягких тканей. Заболевания описаны преимущественно у женщин детородного возраста и являются гормонозависимыми. Самая частая локализация первичной опухоли — тело матки (см. таблицу). 
Материал и методы
В рамках данного исследования была сформирована группа из 26 пациенток с лейомиоматозом в возрасте 30—63 лет (средний возраст 37 лет). Интравенозный лейомиоматоз (8890/1) на основании клинико-морфологических данных диагностирован в 20 наблюдениях. В остальных случаях выявлены другие варианты гладкомышечных опухолей: метастазирующая лейомиома (8898/1) — 2 наблюдения, диссеминированный перитонеальный лейомиоматоз (8898/1) — 3 наблюдения, гладкомышечная опухоль с неопределенным потенциалом злокачественности (8897/1) —1 случай.
Жалобы пациенток как при первичных, так и при повторных обращениях неспецифичны: боли в животе (n=9, 34,5%), слабость (n=9, 34,5%), одышка (n=7, 26,9%), увеличение живота в объеме (n=5, 19,2%), обильные менструальные кровотечения (n=5, 19,2%), перебои в работе сердца (n=4, 15,3%), отек одной (n=2, 7,7%) или обеих (n=2, 7,7%) ног. В 6 (23,0%) случаях заболевание протекало бессимптомно и выявлено случайно при плановом осмотре. В анамнезе у большинства пациенток диагностирована лейомиома тела матки (n=21, 81,2%). На момент обращения 14 (53%) пациенток имели хирургический анамнез: консервативную миомэктомию в 8 случаях (в 1 случае после миомэктомии выполнена экстирпация матки с придатками), надвлагалищную ампутацию матки без придатков в 2, надвлагалищную ампутацию матки с левыми придатками, удаление опухоли малого таза в отложенном периоде (20 мес после первичной операции) в 1, биопсию опухоли малого таза в 2, удаление забрюшинной опухоли в 1. При этом 11% (n=3) пациенток перенесли неоднократные хирургические вмешательства.
Иммуногистохимическое исследование с антителами к гладкомышечному актину (1А4), десмину (D33), кальдесмону (h-CD), CD99 (12E7), Ki-67 (MIB1), CD10 (56C6), кальретинину (DAK-Calret1) проводили по стандартной методике с использованием системы визуализации EnVision Flex («Dako») на автостейнере Avtosteiner Link48 («Dako»).
Для молекулярно-генетического исследования отобрали парные парафиновые блоки: образцы опухолевой ткани (более 70% опухолевых клеток, подтвержденных морфологическим контролем по микропрепарату) и образцы нормальной ткани без опухолевых изменений. Исследование микросателлитной нестабильности проводили методом фрагментного анализа на генетическом анализаторе с использованием тест-системы из шести маркеров, изменения в которых ассоциированы с развитием лейомиосаркомы [4]. Тестирование осуществляли в лабораториях ЛМГД-2, эпигенетики ФГБНУ «Медико-генетический научный центр».
В полученных парных образцах (норма/опухоль) тестировали генетические изменения по 6 микросателлитным маркерам: D10S1146, D10S218, D10S24, D10S1213, D3S1295, D9S942. Анализ проводили методом полимеразной цепной реакции (ПЦР) с использованием специфических меченых праймеров с последующим фрагментным анализом на генетическом анализаторе ABIPrism 3500 («Applied Biosystems»).
Выделение ДНК из операционного материала (парафиновых блоков) проводили с помощью коммерческих наборов ДНК-СорбВ («ИнтерЛабСервис», Россия) и/или набора QIAamp DNA FFPE Tissue kit («QIAGEN», Германия) в соответствии с рекомендациями фирм-производителей. Предварительную депарафинизацию материала осуществляли по стандартной схеме путем последовательной обработки ксилолом и этанолом (96%).
Молекулярно-генетические изменения — потерю гетерозиготности и/или микросателлитную нестабильность маркеров D10S1213, D10S1146, D10S218, D10S24, D9S942 и D3S1295 в парных образцах опухолевой и нормальной ткани тестировали путем ПЦР с использованием специфических праймеров, меченных флюоресцентной меткой FAM. Подбор олигонуклеотидных праймеров проводили с помощью программ Primer-blast-ncbi, PrimerExpress. Праймеры синтезированы в компаниях «Литех», «Синтол» (Россия).
Далее проводили вертикальный электрофорез в полиакриламидном геле (8% ПААГ) с целью определения специфичности и качества прохождения ПЦР с последующей визуализацией результатов методом окрашивания нитратом серебра. Полученные продукты амплификации тестировали с использованием сравнительного фрагментного анализа с последующей обработкой полученных результатов (программа Gene Mapper).
Результаты
Всем пациенткам выполнена операция по удалению первичной/рецидивной или остаточной опухоли с результатом R0 (18 наблюдений с учетом повторных операций) и R2 (7 наблюдений). Одна пациентка умерла до операции, в данном случае распространенность опухоли оценена по результатам патологоанатомического вскрытия. У 12 из 20 больных с интравенозным лейомиоматозом выявлено интракардиальное распространение опухоли: у 7 пациенток верхушка тромба достигала правого предсердия, у 5 — правого желудочка, у 3 — тромбоз был правосторонним, у 5 — левосторонним, у 3 — двусторонним. В 4 случаях опухолевый тромбоз распространялся из малого таза по яичниковым венам, в 4 — по подвздошным, в 3 — по яичниковым и подвздошным. Поражение легких отмечено у 5 пациенток: у 3 с интравенозным лейомиоматозом, у 2 с метастазирующей лейомиомой. Диссеминация по брюшине выявлена у 5 пациенток (в 3 случаях диссеминированный перитонеальный лейомиоматоз, в 1 интравенозный лейомиоматоз, в 1 гладкомышечная опухоль с неопределенным потенциалом злокачественности).
Учитывая особенности гормонального статуса опухоли, 15 (57,6%) пациенткам после операции назначена антиэстрогеновая терапия: 5 (19,2%) — в связи с множественными метастазами в легких, 5 (19,2%) для профилактики рецидива, 3 (11,5%) из-за наличия остаточной опухоли, 2 (7,6%) — вследствие продолженного роста после нерадикальной операции [5]. Стабилизация или уменьшение очагов опухоли на фоне лечения отмечены в 4 (26,6%) случаях, прогрессирование заболевания — в 6 (40%), у 5 пациенток оценить эффект от проводимой гормональной терапии не удалось.
При перитонеальном лейомиоматозе выявляли множественные плотные округлые миоматозные узлы по поверхности висцеральной брюшины (рис. 1, а). 

Анализ результатов фрагментного анализа проводили для каждого исследуемого локуса. Размеры и количество аллелей тестируемого микросателлитного маркера сравнивали между ПЦР-продуктами нормальной и опухолевой ткани. При определении на хроматограмме новых сигналов в образцах опухолевой ткани по сравнению с аллелями из образцов нормальной ткани пациентки результат рассматривали как микросателлитную нестабильность (рис. 3). 

Изменения микросателлитных повторов, характерные для лейомиосарком (потеря гетерозиготности хотя бы по одному исследованному локусу), выявлены у 6 пациенток, все с клинико-морфологическим диагнозом интравенозного лейомиоматоза. В 3 из этих 6 случаев лейомиоматоз сопровождался метастазами в легких и распространением по брюшине, в 2 отмечено поражение сердца (интракардиальная форма). Проведенный анализ данных не позволил выявить каких-либо значимых клинико-морфологических критериев для этой группы. Заболевание протекало как типичная лейомиома у 1 пациентки, у 2 манифестировало с внутрисосудистого поражения сердца и соответствующей клинической картины, у 2 — с метастазов в легких, у 1 — с поражения брюшины. Размер опухоли в матке по клиническим данным варьировал от 2 до 8 см, в 1 случае отмечены множественные интрамуральные и субсерозные опухолевые узлы, прослеживались тромбы в сосудах.
В некоторых случаях при наличии гомозигот в норме и опухоли по 3 микросателлитным маркерам и более результат может быть трактован как «неинформативный» (рис. 5). 
Таким образом, в результате проведенного молекулярно-генетического исследования нозологическая группа, однородная по клинико-морфологическим параметрам, может быть разделена на три условные категории: доброкачественные лейомиоматозы (опухоли, в которых не выявлено изменений, характерных для лейомиосаркомы) — 15 наблюдений, опухоли с потенциально агрессивным течением, содержащие изменения, характерные для лейомиосаркомы (6 наблюдений) и наконец опухоли неуточненного потенциала злокачественности (5 недостаточно информативных наблюдений).
Таким образом, лейомиоматозы не являются «переходной формой» от доброкачественной лейомиомы к лейомиосаркоме, что подтверждается статусом исследованных молекулярных маркеров [3, 4, 6]. Несмотря на различия в генотипе опухолей исследованной группы, клинико-морфологическая картина сходная: даже при наличии изменений, характерных для лейомиосаркомы, морфологическая картина не соответствовала злокачественной опухоли. С другой стороны, отсутствие изменений микросателлитных повторов вовсе не свидетельствует о доброкачественном течении данной группы опухолей. Также стоит признать, что анализ молекулярно-генетических изменений ДНК в образцах опухолевой ткани не позволяет категорически уточнить характер заболевания путем выявления признаков генетической нестабильности, однако требуется дальнейшее накопление опыта в изучении опухолей этой группы и выявлении возможной связи с прогнозом заболевания. Следует также отметить, что консервативная миомэктомия у пациенток с гладкомышечными опухолями с неопределенным злокачественным потенциалом связана с неоправданно высоким риском рецидива заболевания. При наличии рецидивирующей лейомиомы целесообразно провести расширенное исследование материала и пересмотреть тактику лечения пациентки, учитывая, что «золотым стандартом» хирургического лечения признана гистерэктомия в сочетании с двусторонним удалением придатков [7]. Кроме того, рецидивы, внутрисосудистое распространение и метастазы этих опухолей не следует расценивать как лейомиосаркому.
Концепция и дизайн исследования — Ю.Ю.А., Г. А.Ф., Ю.Г.П., М.М.Д.
Сбор и обработка материала — О.В.Б., А.И.Ж., Т.В.К., И.О.К., Ю.Л.П.
Статистическая обработка — Л.В.М., О.В.Б., Ю.Г.П., И.О.К.
Написание текста — Л.В.М., Ю.Ю.А., И.О.К.
Редактирование — Г. А.Ф., Т.В.К., И.С.С., Л.Э.З.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.