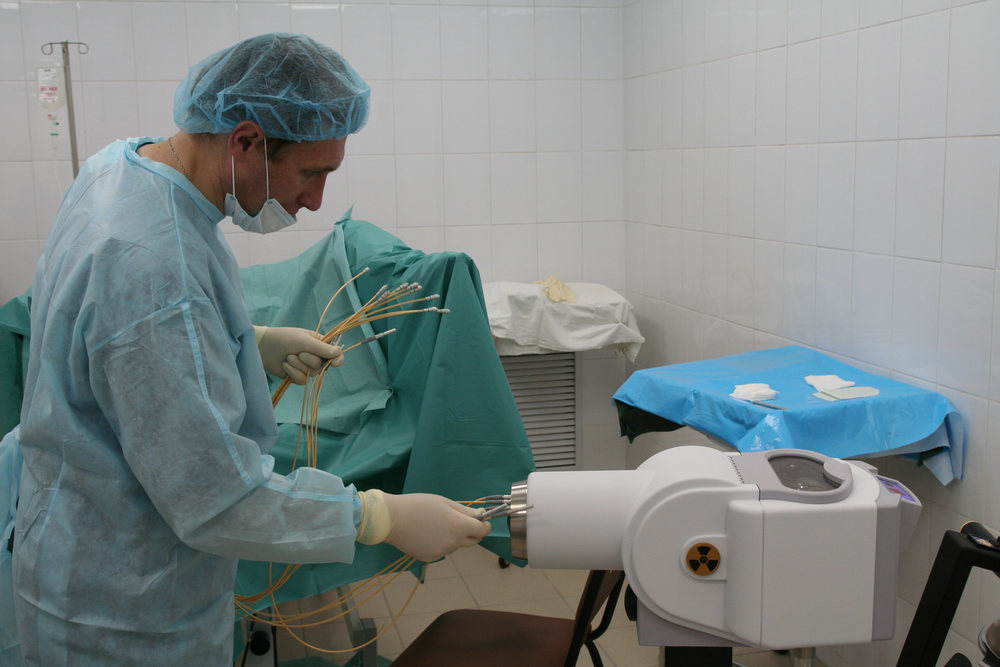
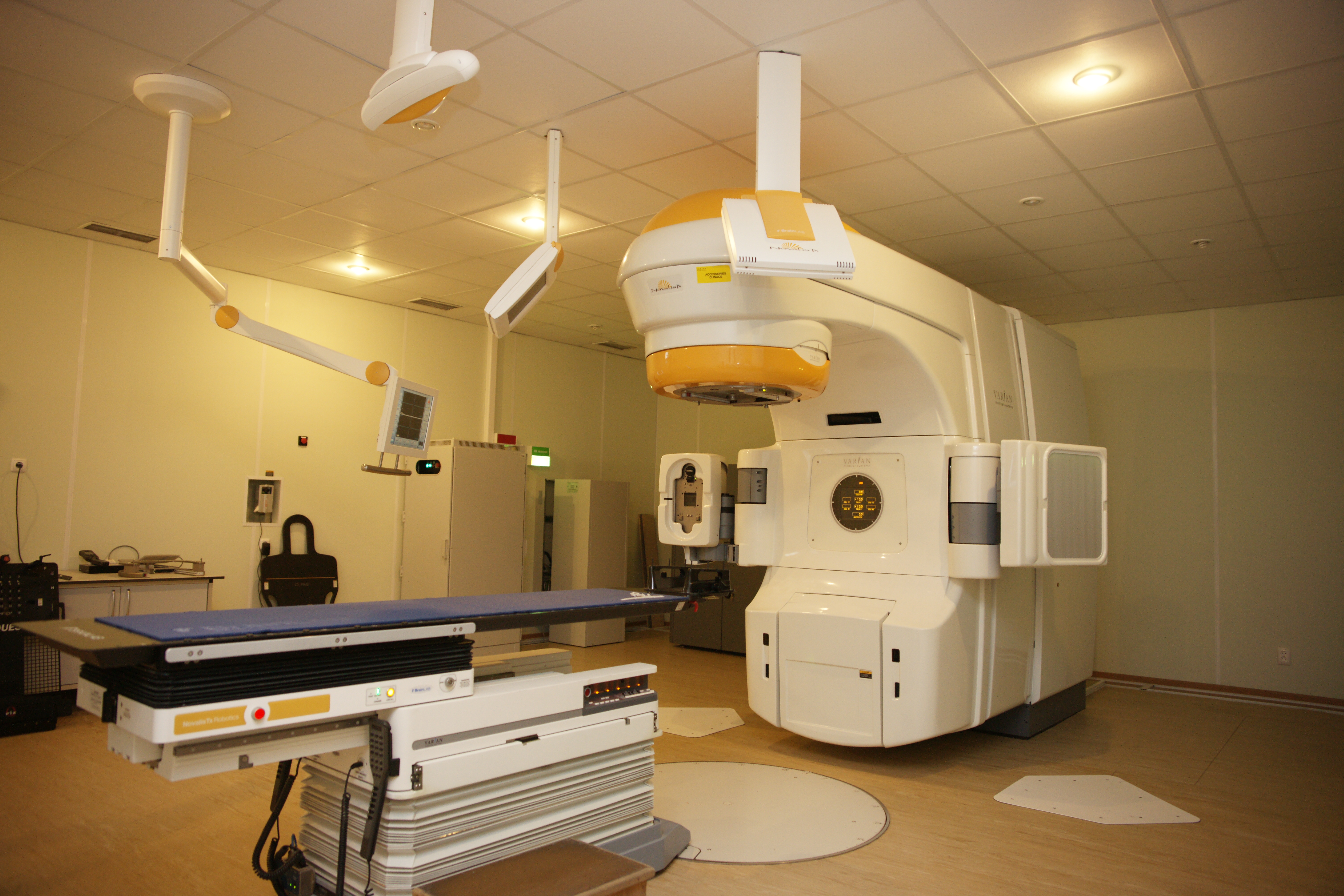
Ошибки диагностики и стадирования рака предстательной железы
С. Х. Аль-Шукри, С. Ю. Боровец, М. А. Рыбалов
Кафедра урологии Санкт-Петербургского государственного медицинского университета имени акад. И. П. Павлова
В данном обзоре оцениваются преимущества и недостатки основных методов диагностики и стадирования рака предстательной железы, приводятся сведения о современных высокотехнологичных методах стадирования и номограммах. Рассматриваются причины ошибок, возникающих при диагностике и стадировании рака предстательной железы.
Ключевые слова: рак предстательной железы; диагностика; стадирование.
Введение
Повышение эффективности лечения рака предстательной железы (РПЖ) является одной из наиболее актуальных проблем современной урологии. В мире РПЖ занимает 3–4 место в структуре заболеваемости злокачественными новообразованиями. В России заболеваемость РПЖ в 2004 году составляла 6,9 %, а в 2009 году — уже 10,7 % [1]. При этом за последние три десятилетия возросло число мужчин, умерших от этого заболевания [2].
I. МЕТОДЫ ДИАГНОСТИКИ РПЖ
Методы диагностики рпж — включают оценку результатов пальцевого ректального исследования (ПРИ), определении уровня ПСА в плазме крови. Окончательный диагноз РПЖ может быть установлен только по результатам биопсии предстательной железы, которую целесообразно выполнять под ТРУЗ-контролем. При клиническом стадировании для уточнения границ местного распространения новообразования предстательной железы и для выявления местных и отдаленных метастазов в дополнение используют различные методы, позволяющие получить изображение: компьютерную томографию (КТ), магнитно-резонансную томографию (МРТ), сцинтиграфию костей скелета и др. Однако результаты этих методов могут быть интерпретированы ошибочно как в пользу гипо, так и гипердиагностики. Работы многих исследователей посвящены оптимизации скрининга и ранней диагностики РПЖ [3–5].
1.1. ПРИ. До внедрения в широкую клиническую практику ПСА, ПРИ было единственным методом диагностики РПЖ. Большинство злокачественных новообразований РПЖ располагаются в периферической зоне простаты и могут быть выявлены с помощью ПРИ, если их объем превышает 0,2 см 3. Положительная прогностическая ценность ПРИ варьирует от 4 % до 11 % у мужчин с уровнем ПСА от 0 до 2,9 нг/мл, и от 33 % до 83 % — от 3 до 9,9 нг/мл и выше [6]. В связи с тем, что оба этих метода имеют независимую друг от друга диагностическую ценность, рекомендовано применять их комбинацию.
1.2. ПСА и его производные. Несмотря на то, что уровень ПСА в плазме крови повышается при различных заболеваниях предстательной железы — РПЖ, доброкачественной гиперплазии предстательной железы (ДГПЖ) и простатите, ПСА остается практически единственным маркером, применяемым в целях ранней диагностики РПЖ. Однако единых общепринятых международных стандартов в отношении пороговых значений ПСА, которые могли бы использоваться для диагностики РПЖ, не существует [7]. Результаты недавнего исследования по профилактике РПЖ, проведенного в США, подтвердили, что у многих мужчин РПЖ может присутствовать, несмотря на низкий уровень ПСА крови [8] (см. табл. 1).
При использовании более высоких условных границ уровня ПСА (>4 нг/мл) для принятия решения о целесообразности проведении биопсии простаты повышается и риск пропустить клинически значимый РПЖ; в тоже время при снижении этого показателя ( 10 частота выявляемости РПЖ на превышает 8 % [12].
1.3. PCA3. Относительно новый и интенсивно исследуемый в настоящее время маркер — PCA3 (простатоспецифический некодирующий мРНК), который определяют в осадке мочи после массажа простаты. Этот маркер имеет более высокую чувствительность и специфичность по сравнению с ПСА, не зависит от объема простаты и наличия простатита у больного [13]. Сравнительно небольшое число опубликованных работ по анализу диагностической ценности этого маркера не позволяет рекомендовать его для широкого использования в клинической практике. В связи с этим в настоящее время этот маркер можно рассматривать как экспериментальный метод диагностики РПЖ.
1.4. ТРУЗИ. Классическая картина гипоэхогенного образования, расположенного в периферической зоне простаты, встречается не всегда, поэтому ТРУЗИне относят к методам, позволяющим достоверно определять наличие РПЖ. ТРУЗ-контроль получил широкое распространение при выполнении биопсии простаты.
1.5. Биопсия простаты. Биопсия предстательной железы является достоверным методом верификации диагноза РПЖ. Многими авторами были предложены различные методики выполнения этого исследования, отличающиеся по количеству и участкам расположения биопсийных вколов. При объёме ПЖ 30–40 см3 необходимо проводить биопсию не менее чем из 8 точек. С увеличением количества точек более 12, точность анализа существенно не изменяется [14]. На основании результатов Британского исследования по диагностике и лечению РПЖ была рекомендована биопсия из 10 точек [15].
II. МЕТОДЫ СТАДИРОВАНИЯ РПЖ
2.1. ПРИ. Принято выделять клиническое стадирование, основанное на данных ПРИ, определении уровня ПСА, рентгенологических, радиоизотопных и других клинических методах исследования, а также патологоанатомическое стадирование, которое становится возможным после морфологического анализа удаленной предстательной железы, семенных пузырьков и лимфатических узлов. Патологоанатомическое стадирование более точно позволяет оценить распространение болезни и судить о ее прогнозе. Наиболее важными патологоанатомическими прогностическим факторами после радикальной простатэктомии являются степень дифференцировки новообразования, позитивный хирургический край, экстракапсулярное распространение опухоли, ее инвазия в семенные пузырьки и метастазирование в тазовые лимфатические узлы. Сведения об ошибках патологоанатомического стадирования не включены в настоящий обзор литературы.
ПРИ позволяет определить не только наличие РПЖ, но и степень его местного распространения. Пальпируемая опухоль в простате — это признак, характерный для низкодифференцированного РПЖ (степень злокачественности по Gleason — 8–10 баллов). Чувствительность и воспроизводимость ПРИ весьма низкие, что приводит как к недооценке, так и к переоценке степени распространения РПЖ. Чувствительность метода при определении клинической стадии РПЖ не превышает 30 % [16]. Стадия рака простаты правильно диагностируется с помощью данного исследования менее чем в 50 % случаев [17].
2.2. ПСА. Более высокий уровень ПСА в плазме крови косвенно указывает на большую степень распространения РПЖ, но не позволяет достоверно предсказать ни клиническую, ни патоморфологическую его стадию [18, 19].
2.3. ТРУЗИ позволяет выявить только 60 % опухолей простаты, остальные не распознаются из-за эхогенности, сходной с таковой у окружающих здоровых тканях. При этом остаются недиагностированными более 60 % РПЖ на стадии рТ3 [20]. ТРУЗИ в комбинации с цветной допплерографией позволяет визуализировать проходящие через капсулу кровеносные сосуды, что типично при экстракапсулярном распространении новообразования [21, 22]. Однако эта методика имеет низкую воспроизводимость, в связи с чем ее относят к категории вспомогательных.
2.4. Биопсия простаты. По результатам биопсии простаты можно оценить степень местного распространения РПЖ, а также степень злокачественности новообразования в баллах по шкале Gleason. Процент пораженной ткани — наиболее надежный прогностический фактор риска инвазии опухоли в семенные пузырьки и экстракапсулярного распространения новообразования.
2.5. КТ и МРТ недостаточно надежно позволяют судить о степени распространения РПЖ, чтобы рекомендовать их как обязательные методы обследования. МРТ с эндоректальной катушкой позволяет более точно определить стадию РПЖ и прорастание опухоли в семенные пузырьки. Однако на фоне геморроидальных и воспалительных изменений ПЖ или после ее биопсии интерпретация данных может быть затруднена [9]. Сочетание контрастной МРТ и МРТ в Т2‑режиме усиления и применение МРТспектроскопии позволяет лучше верифицировать опухолевую ткань и диагностировать экстракапсулярное распространение опухоли [23].
Недостатки методов визуализации при РПЖ:
2.6. Высокотехнологичные методы стадирования РПЖ. К новым перспективным методам, позволяющим получить изображение, можно отнести ПЭТ, при помощи которого диагностируют около 70 % РПЖ на стадии рТ2 и pT3a‑4 [9]. При этом очаг рака и микрометастазы 100 нг/мл практически у всех больных имеют место отдаленные метастазы РПЖ [29].
III. Причины ошибок при диагностике и стадировании РПЖ
Среди причин, приводящих к ошибкам при диагностике и стадировании РПЖ можно выделить субъективные и объективные.
В заключении следует отметить, что в последние годы предпринимаются попытки совершенствования методов ранней диагностики и стадирования РПЖ.
Однако существует потребность в создании новых, более точных методов, позволяющих выявлять клинически значимый РПЖ. К перспективным методам, позволяющим оптимизировать процессы диагностики и стадирования, можно отнести ПЭТ/КТ, диффузионную МРТ, МР-спектроскопию, динамическую МРТ с повышением контраста. Необходима дальнейшая разработка специфичных для РПЖ радиофармпрепаратов. Кроме того, важна унификация при интерпретации полученных данных — использование рекомендаций Европейской ассоциации урологов.
Список литературы
Рак предстательной железы: почему возникает, симптоматика, методы диагностики и лечения
Введение
Согласно данным множества исследований, отмечается неуклонный рост случаев обнаружения первичного рака предстательной железы (РПЖ). В России это заболевание находится на 4-м месте среди всей онкологии, выявляемой во время профосмотров. Опережает его рак шейки матки, молочной железы и губы. В западных странах рак простаты составляет 25% от всех онкологических заболеваний.
Что такое рак простаты?
РПЖ представляет собой злокачественное новообразование, которое развивается из тканей предстательной железы.
Предстательная железа, или простата, – мужской репродуктивный орган, по размерам схожий с каштаном. Он находится под мочевым пузырем и охватывает передний отдел мочеиспускательного канала.
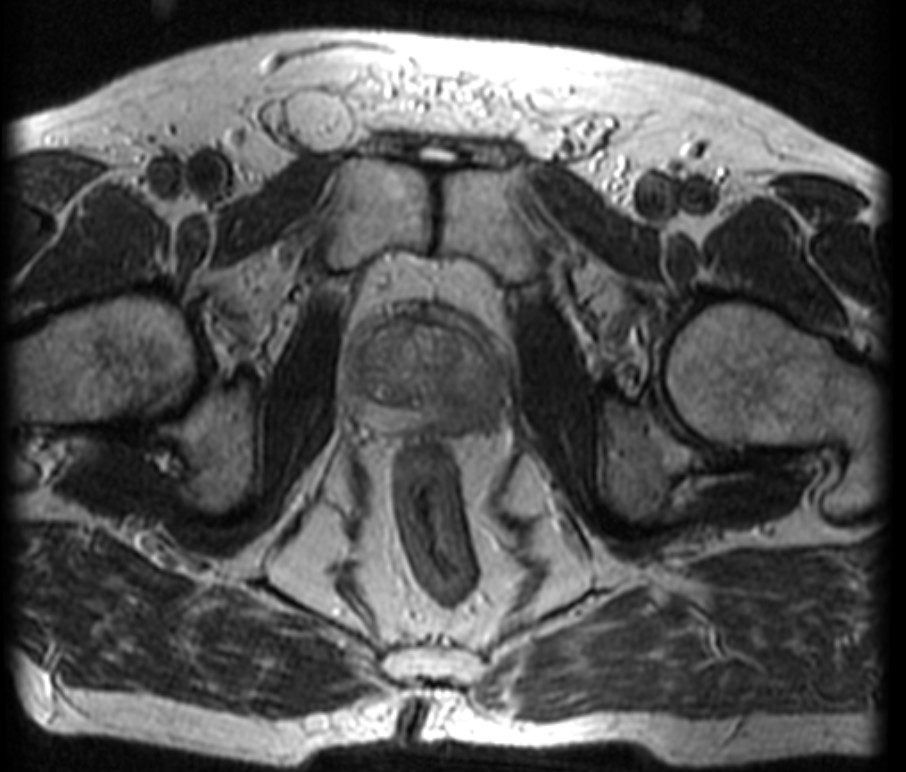
Рис. 1. МРТ (Т2-взвешенные изображения) картина поражения левой доли предстательной железы.
Разновидности рака предстательной железы
В 95% случаев РПЖ развивается из эпителиальных клеток собственных желез (их называют «ацинусы»), из которых сформирована периферическая часть предстательной железы. Эта форма болезни называется «ацинарная аденокарцинома». В остальных 5% случаев диагностируется интрдуктальная разновидность, для которой характерно более агрессивное течение.
Важная характеристика аденокарциномы – степень ее дифференцировки, которая выявляется при гистологическом исследовании биоптата или биоматериала, полученного в ходе операции. Дифференцировка сегодня выражается шкалой Глисона (Gleason), в соответствии с которой присваивается сумма баллов: от 6 (самый благоприятный прогноз) до 10 (самый неблагоприятный вариант).
Характерные признаки заболевания
Риск развития РПЖ растет с возрастом: средний показатель в этой категории заболевших – 68 лет. Существуют также факторы риска, то есть то, что повышает шанс появления онкологического заболевания. Современной медициной не выявлены достоверные факторы, которые приводят к повышению риска развития РПЖ (какие-либо препараты, характер рациона, вредные привычки, плохая экология и др.). Поэтому основным фактором остается возраста, а также возрастной гормональный дисбаланс (между эстрогенами и андрогенами).
Симптоматика, первые признаки
На ранних стадиях злокачественная опухоль обычно не проявляет себя. Кроме аденокарциномы, у людей с повышенным риском развития РПЖ почти всегда присутствуют сопутствующие патологии (простатит, аденома простаты), и они могут давать симптоматику. Чаще всего встречаются следующие симптомы:
Таким образом, чем выше стадия, тем больше вероятность проявления симптоматики. Чаще всего РПЖ обнаруживается во время профилактического обследования (оно рекомендовано всем мужчинам старше 40-ка лет). Такое обследование включает в себя:
ПСА – это маркер, используемый для раннего выявления РПЖ. Он достаточно чувствителен и специфичен, чтобы заподозрить наличие рака на начальной стадии. Кроме ПСА, анализу могут подвергаться его производные – индекс здоровья простаты, плотность ПСА, соотношение свободного ПСА и общего.
Методы диагностики
Основа диагностики РПЖ – биопсия предстательной железы, иными словами, морфологическая верификация.
Показания к биопсии:
Важно! Если уровень ПСА ниже верхней допустимой границы, это не всегда говорит о том, что РПЖ отсутствует. Примерно 25% случаев заболеваемости отмечаются на фоне нормальных значений этого показателя. Поэтому решение о необходимости проведения биопсии должно приниматься после комплексного обследования, которое включает все виды диагностики.
Варианты биопсии простаты:
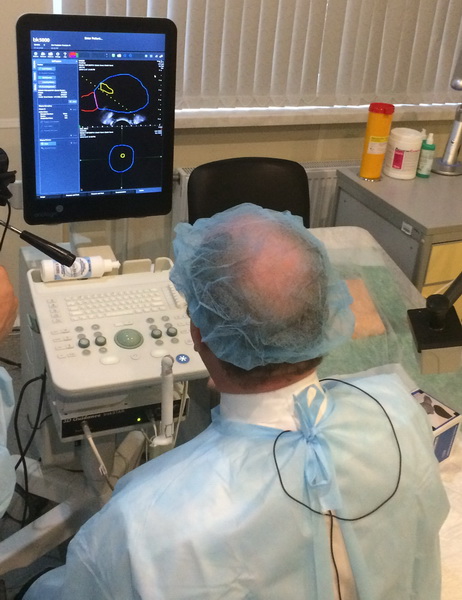
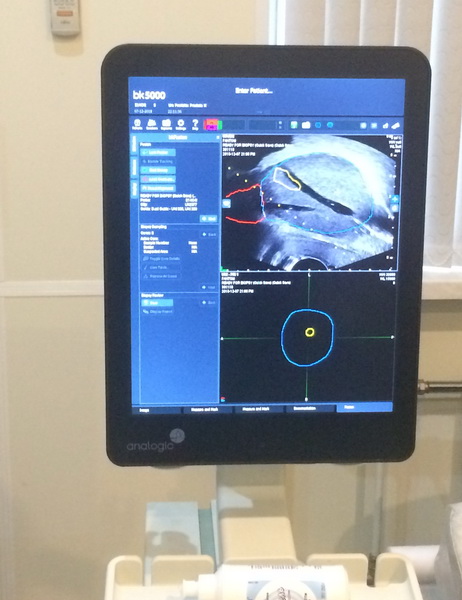
Рис. 2 А., 2 Б. Фьюжн-биопсия. Мастер-класс в НМИЦ онкологии им. Н.Н. Петрова
Стадии рака предстательной железы
Стадирование РПЖ и определение группы риска рецидивирования после возможной терапии производятся после гистологической верификации заболевания.
Стадирование при стандартном подходе подразумевает остеосцинтиграфию и МРТ органов малого таза. Магнитно-резонансная томография нужна, чтобы выявить степень локального распространения процесса в зоне простаты (прорастание в семенные пузырьки, выход новообразования за капсулу железы), а также определить, есть ли поражение регионарных лимфоузлов.
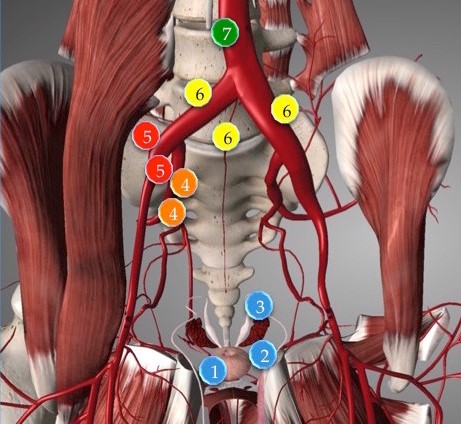
Рис. 3. Пути распространения рака предстательной железы в лимфоузлы таза.
В случае необходимости дополнительно проводится КТ органов груди или брюшной полости.
Цель проведения остеосцинтиграфии – выявление возможного поражения опухолью костей скелета.
Могут назначиться дополнительные исследования – рентгенография (прицельная), УЗИ, урофлоуметрия.
Группа риска определяется, исходя из уровня ПСА на момент до начала терапии, суммы Глисона, согласно данным биопсии, и клинической стадии болезни. Группа риска может быть низкой, промежуточной и высокой. Ее определение крайне важно, чтобы выбрать оптимальный метод лечения.
ПСА от 10 до 20 нг/мл
Методики лечения
В соответствии с результатами многоцентрового проспективного рандомизированного исследования ProtecT (2016) лучевая терапия и хирургическое лечения демонстрируют раную противоопухолевую эффективность и обеспечивают надежный контроль над заболеванием у большинства (более 90%) больных раком предстательной железы с низким и промежуточным риском рецидива заболевания. В настоящее время решающим фактором при выборе противоопухолевого лечения у этой категории больных является безопасность терапии и снижение риска осложнений.
Рассмотрим основные виды терапии: хирургическое лечение, брахитерапия, стереотаксическое облучение, сочетанная лучевая терапия.
Хирургическое вмешательство
РПЭ, или радикальная простатэктомия, представляет собой хирургическое вмешательство по удалению предстательной железы, а также окружающей клетчатки и лимфоузлов. При такой операции с железой единым блоком удаляют семенные пузырьки и участок канала уретры.
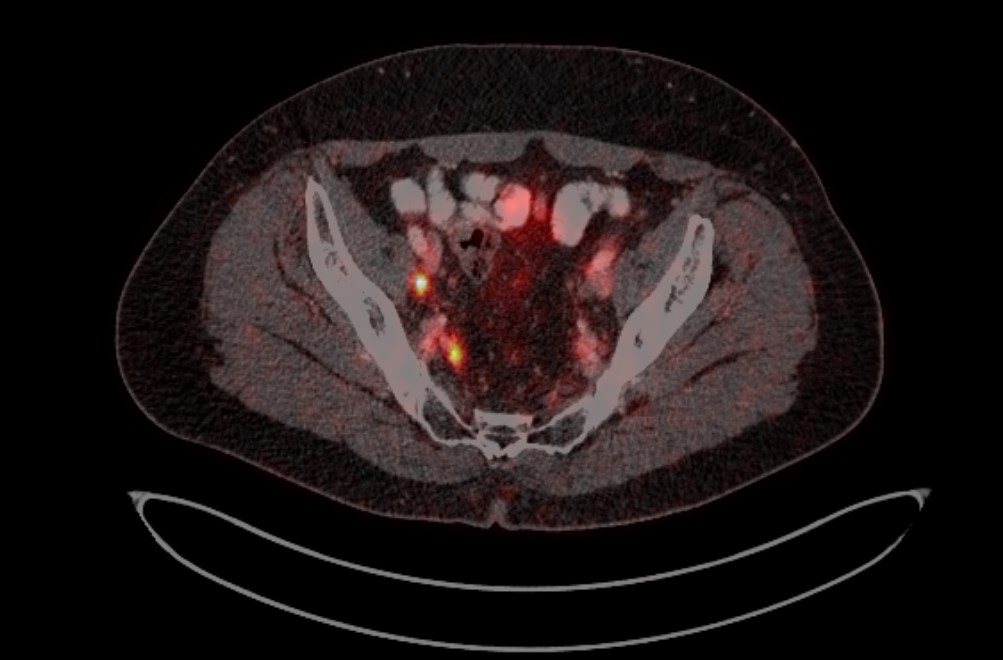
Рис. 4. ПЭТ-КТ изображения больного М. с поражением тазовых лимфоузлов
РПЭ различается по виду доступа и степени инвазивности:
Позадилонный доступ предполагает разрез в нижней части живота, через который удаляется простата и местные ткани.
Промежностная методика – это открытый способ, при котором небольшой надрез делается в зоне между анусом и кожно-мышечным мешком, то есть мошонкой. Методика позволяет удалить простату, но при ее применении нельзя также удалить неблагоприятные ткани и узлы, расположенные около железы. Если после проведения промежностной операции в органах малого таза обнаружатся раковые клетки, нужно будет дополнительно делать лимфаденэктомию. Сейчас промежностная методика применяется крайне редко.
Лапароскопическая методика – наиболее щадящая. Врач имеет доступ к пораженному органу через маленький разрез внизу живота. В него вводится камера и все нужные хирургу инструменты. Камера подает на экран изображение органов малого таза, благодаря чему врач полностью контролирует процесс, а пациент получает минимум вреда. При таком способе минимизированы кровопотери, посторонние органы почти не травмируются, эректильная функция сохраняется частично или полностью и т. д.
Рассмотрим также наиболее распространенные осложнения, которые могут возникнуть после операции на простате:
Брахитерапия
Брахитерапия представляет собой введение в ткани источников излучения. Эта методика – самая «молодая» среди способов лечения РПЖ. Сегодня это один из наиболее востребованных методов облучения простаты, обеспечивающий очень высокую избирательность подведения дозы. Основная особенность брахитерапии заключается в том, что простата облучается изнутри – источник облучения вводится непосредственно в нее. Такой метод дает возможность применять высокие дозы (100-140 Гр и более), при этом избегая высокого риска лучевого поражения не подверженных раку тканей.
Стремительный рост клинического применении брахитерапии, по сравнению с хирургическими вмешательствами, обуславливается высокой эффективностью, которая сопоставима с простатэктомией, при гораздо более низкой частоте возникновения осложнений.
Различают 2 вида брахитерапии, в зависимости от способа введения источника излучения в железу и его мощности:
При проведении низкомощностной брахитерапии в ткани простаты вживляется источник излучения и остается в них до полного распада. Долгое время при РПЖ именно этот вид брахитерапии применялся чаще всего. Наиболее часто для выполнения терапии используется изотоп радиоактивного йода, то есть I125.
Согласно многочисленным исследованиям, брахитерапия низкой мощности обеспечивает не очень высокую точность облучения. Это объясняется смещением источника излучения, изменением формы и размеров простаты, затрагиванием прилежащих здоровых органов. Ввиду этого низкомощностная методика показана в основном пациентам с самыми начальными стадиями, когда опухоль небольшая и не выходит за пределы железы. Такая брахитерапия имеет и другие существенные недостатки. Первый – это высокая частота осложнений, возникающих со стороны мочевыводящих путей, может даже возникнуть острая задержка мочи и необходимость эпицистостомы, то есть формирования надлобкового мочепузырного свища, на долгий срок. В основе осложнений – отек предстательной железы из-за того, что в ней остается несколько сотен зерен (инородных тел). Кроме того, радиоактивные зерна, если они долго находятся в организме, представляют собой источники излучения, представляющие определенную опасность для других людей. Из-за этого контакт пациента с родными ограничен (нельзя близко общаться с маленькими детьми).
Рис. 5. Высокомощностная (высокодозная) брахитерапия
Самая современная методика внутритканевой терапии – высокомощностная брахитерапия. Источники излучения автоматически загружаются и извлекаются. Эта лучевая терапия обладает принципиальным плюсов – высокой точностью облучения, достигаемой путем введения игл под контролем специального УЗ-аппарата. Одновременно в автоматическом режиме рассчитываются дозы и возможность быстрой корректировки плана лучевого лечения. Источник излучения находится в организме пациента временно, поэтому уровень осложнений – самый низкий, по сравнению со всеми радикальными методиками терапии РПЖ, включая низкодозную разновидность брахитерапии.
Технологические особенности методики позволяют предлагать ее большинству больных, вне зависимости от размеров злокачественного новообразования и его распространенности за пределы простаты. Кроме того, высокомощностная брахитерапия – это «золотой стандарт» при комбинированном лечении, то есть одновременном использовании с дистанционным облучением у больных с неблагоприятными характеристиками новообразования.
Самый большой недостаток высокомощностной методики – высокие требования, касающиеся квалификации медицинского персонала, а также необходимость использования высокотехнологичного оборудования. Этим объясняется малая распространенность метода в России.
Противопоказания к брахитерапии подразделяются на общие и урологические. Самые частые урологические противопоказания – это серьезные нарушения процесса мочеиспускания:
Нужно отметить, что большой объем простаты, который имеет значение для низкодозной брахитерапии (50-60 см 3 ), почти не ограничивает возможности лечения в режиме высокомощностной методики.
Данные противопоказания относятся не только к брахитерапии, но и к другим методикам лучевой терапии РПЖ.
Стереотаксическое облучение
СТЛТ (стереотаксическая лучевая терапия) – высокоточная методика лечения очага РПЖ высокими дозами ионизирующего излучения.
Рис. 6. Стереотаксический лучевой ускоритель
Сегодня СТЛТ при раке простаты реализуется несколькими основными методами, каждый из которых обладает своими особенностями, плюсами и минусами:
Сравнительная характеристика техник СТЛТ простаты
Низкий риск рпж что это
Синонимы английские
[-2]pro-prostate specific antigen and prostate health index (PHI), Proenzyme PSA, p2ПСА, Isoform p2PSA, Truncated [-2]pPSA.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Для ранней диагностики рака предстательной железы (РПЖ) широко применяются несколько клинико-лабораторных маркеров: простатспецифический антиген (ПСА), свободный ПСА (fПСА), соотношение fПСА / общий ПСА и другие. Эти показатели, однако, не являются специфическими, не обладают необходимым уровнем чувствительности в отношении РПЖ и не могут быть использованы в качестве однозначных критериев отбора пациентов для проведения биопсии простаты, что объясняет необходимость поиска новых методов ранней диагностики РПЖ. В последнее время в клиническую практику внедряется новый расчетный показатель риска РПЖ – индекс здоровья простаты, phi (от англ. Prostate Health Index).
При расчете phi принимаются во внимание три показателя: общий ПСА, свободный ПСА и [-2] proПСА. Общий ПСА – это сериновая протеаза, секретируемая эпителием простаты в семенную жидкость и в небольшом количестве попадающая в кровь. Повышение уровня общего ПСА выше порогового значения (4 нг/мл) позволяет подозревать РПЖ, но также может наблюдаться при других состояниях (доброкачественная гиперплазия предстательной железы, простатит, после массажа и биопсии простаты и др.). Основное количество ПСА присутствует в крови в связанном с ингибиторами протеаз виде. До 35 % от общего ПСА приходится на долю не связанного с белками, свободного ПСА. Показано, что у пациентов с РПЖ нормальное соотношение связанного и свободного ПСА изменяется, при этом доля fПСА уменьшается. Несмотря на то что исследование fПСА помогает в дифференциальной диагностике РПЖ и доброкачественных заболеваний, этот маркер также не является специфическим для рака простаты. Свободный ПСА – это комплекс белков, состоящий из различных изоформ фермента, характерных как для РПЖ, так и для доброкачественной гиперплазии простаты. В качестве третьего показателя при расчете phi используется [-2] proПСА. В отличие от общего и свободного ПСА, он является онкомаркером, характерным именно для РПЖ и нетипичным для доброкачественной гиперплазии предстательной железы.
Различные зоны предстательной железы характеризуются разной степенью секреции изоформ профермента сериновой протеазы (proПСА). [-2] proПСА представляет собой одну из изоформ proПСА, которая преобладает в периферических отделах простаты и является основной изоформой, обнаруживаемой при РПЖ. Это гликопротеин, который образуется из proПСА путем отщепления короткой последовательности аминокислот. Особенностью [-2] proПСА является его устойчивость к воздействию трипсина и калликреина-2. Клиническое значение других изоформ proПСА, обнаруживаемых в крови пациентов с РПЖ ([-1], [-4], [-5] [-7] pПСА), неясно.
Исследование [-2] proПСА применяется в дифференциальной диагностике РПЖ и доброкачественных заболеваний. Его уровень может быть использован как дополнительный диагностический критерий при обследовании мужчин с результатом ПСА в пределах 2,0-10,0 нг/мл и нормальным результатом пальцевого ректального обследования. Однако наибольшая польза для диагностики достигается при объединении показателей [-2] proПСА, а также общего и свободного ПСА в индекс phi.
Существует прямая зависимость между значением phi и риском РПЖ. Так, вероятность рака простаты у пациентов с phi менее 25,0 составляет 11 %, а с phi – более 55-52,1 %. Эта зависимость продемонстрирована во всех возрастных группах и не зависит от объема простаты. Специфичность phi в отношении РПЖ превосходит специфичность общего ПСА, свободного ПСА и соотношения fПСА / общий ПСА. Кроме того, есть взаимосвязь phi и агрессивности РПЖ: большие значения phi соответствуют шкале Глисона 7 и более. На основании выявленных закономерностей был сделан вывод, что индекс phi может быть использован в качестве скринингового метода диагностики РПЖ в группе пациентов в возрасте старше 50 лет, у которых ПСА в пределах 2-10 нг/мл и нормальный результат пальцевого ректального обследования. Результат phi следует интерпретировать с учетом дополнительных клинических, лабораторных и инструментальных данных.
Важно отметить, что при расчете phi используются три параметра, каждый из которых должен быть получен в одной и той же лаборатории. Концентрации [-2] proПСА, ПСА и fПСА зависят от того, какие стандарты использовались для калибровки тестов, а значения, полученные при выполнении тестов от разных изготовителей, не являются взаимозаменяемыми. В данном исследовании используются оригинальные калибраторы Hybritech Tandem™-R.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
ПСА свободный / ПСА общий
Интерпретация при уровне общего ПСА 4-10 нг/мл и отрицательном результате ПРИ (пальцевого ректального исследования):
(В соответствии с документом Guidelines on Prostate Cancer. European Association of Urology 2015).
Индекс здоровья простаты (phi)
Интерпретация при уровне общего ПСА 2-10 нг/мл:
Что может влиять на результат?
Кто назначает исследование?
Уролог, дерматовенеролог, врач общей практики.