Низкий уровень мозаицизма по отдельным хромосомам что это значит
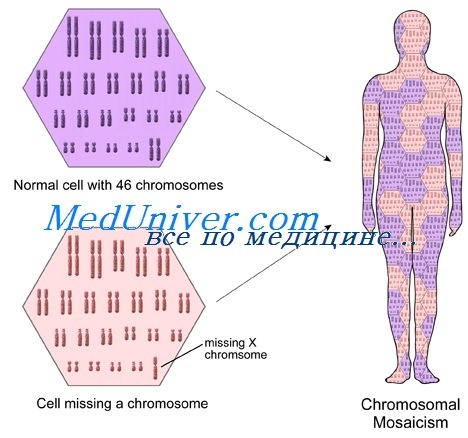
Когда человек имеет хромосомную аномалию, она обычно присутствует во всех его клетках. Тем не менее иногда у одного и того же индивидуума одновременно присутствуют клетки с двумя или более различными хромосомными наборами; эта ситуация называется мозаицизмом. Мозаицизм может быть числовой или, реже, структурный. Мозаицизм обычно обнаруживают стандартным кариотипированием, но он может быть заподозрен на основе FISH или CGH-матричного анализа интерфазы.
Частая причина мозаицизма — нерасхождение хромосом в ранних постзиготических митотических делениях. Например, зигота с дополнительной хромосомой 21 может потерять дополнительную хромосому в одном из митотических делений и продолжить развитие как мозаик 46/47,+21.
Часто бывает трудно оценить значимость обнаружения мозаицизма, особенно если его выявляют пренатально. Влияние мозаицизма на развитие изменяется в зависимости от срока нерасхождения, природы хромосомной аномалии, пропорции различных имеющихся хромосомных наборов и затронутой ткани.
Дополнительная проблема в том, что соотношение различных хромосомных наборов, обнаруженное в проанализированных клетках, (например, амниоцитах или лимфоцитах), не обязательно отражает истинное соотношение в других тканях или в плоде на стадиях эмбриогенеза. В лабораторных исследованиях цитогенетики пытаются отличить истинный мозаицизм от псевдомозаицизма, когда мозаицизм возникает в культуре клеток, после того как они были забраны. Достоверно различить эти типы не всегда легко. В частности, мозаицизм сравнительно часто возникает в цитогенетических исследованиях культур ворсин хориона и может вести к трудностям в интерпретации пренатального диагноза.
Клинические исследования фенотипических эффектов мозаицизма имеют две слабые стороны. Во-первых, поскольку людей почти никогда не кариотипируют без каких-либо клинических показаний, клинически нормальных лиц с мозаицизмом выявляют редко; во-вторых, имеется лишь несколько катамнестических исследований пренатально выявленного мозаицизма.
Тем не менее принято считать, что индивидуумы, мозаичные по той или иной трисомии, например мозаичный синдром Дауна или Тернера, менее поражены, чем немозаичные.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Особенности мозаицизма у эмбрионов человека в программах лечения бесплодия методами вспомогательных репродуктивных технологий
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России, Москва, Россия
Актуальность. На сегодняшний день, несмотря на широкое применение преимплантационного генетического тестирования на анеуплоидии (ПГТ-А), правильная оценка полученных результатов крайне важна. Наличие мозаицизма является одной из причин ошибочной интерпретации данных о генетическом статусе эмбриона при проведении ПГТ-А.
Материалы и методы. Проведено исследование, включающее анализ трофэктодермы 17 эмбрионов с помощью метода высокопроизводительного секвенирования (NGS). Все эмбрионы были анеуплоидными. Анеуплоидные эмбрионы были разделены на три части: клетки внутренней клеточной массы (ВКМ), трофэктодермы №1 и трофэктодермы №2.
Результаты. При анализе образцов клеток из разных частей эмбриона были обнаружены дополнительные хромосомные аномалии. У эмбриона №1 в клетках ВКМ были обнаружены делеция и дупликация по одной из хромосом, а в образце трофэктодермы №2 получена моносомия. Результат анализа клеток ВКМ эмбриона №2 показал дупликацию.
Заключение. Полученные данные подтверждают, что биопсия части трофэктодермы может быть нерепрезентативной относительно всех клеток трофэктодермы и ВКМ. Таким образом, стоит подчеркнуть, что в программах вспомогательных репродуктивных технологий (ВРТ) рекомендовано обязательное проведение скрининга I триместра на сроке 11–13 недель гестации.
У эмбрионов человека хромосомный мозаицизм определяется как две или более отдельных клеточных линий внутри одного эмбриона и является достаточно частым явлением, которое широко обсуждается в области вспомогательных репродуктивных технологий (ВРТ) [1]. Мозаицизм может возникать в результате митотического кроссинговера, соматических мутаций в зиготе или на ранних стадиях дробления, ошибок сегрегации при делении клеточного ядра и генотерапии [2]. Традиционно считалось, что только генетические нарушения в ооцитах или сперматозоидах ответственны за возникновение аномальных эмбрионов. Тем не менее в настоящее время доказано, что мозаицизм также возникает во время первых митотических делений [3]. Во время преимплантационного периода мозацизм является относительно частым явлением, однако на различных стадиях развития эмбриона степень мозаицизма колеблется. Считается, что степень мозаицизма максимальна на 2–3-и сутки развития и уменьшается к 5–6-му дню после оплодотворения. Способность эмбрионов самостоятельно компенсировать мозацизм по мере своего развития отражает возможный физиологичный характер данного явления и необходимость более тщательной интерпретации результатов преимплантационного генетического тестирования (ПГТ) [4].
В литературе описано несколько моделей, объясняющих, почему происходит уменьшение уровня мозаицизма эмбриона на стадии бластоцисты. Естественный отбор чаще работает против мозаичных эмбрионов – in vivo может происходить элиминация эмбриона на основании доли анеуплоидных клеток в нем на разных этапах развития. Другая модель – это модель «клонального истощения», которая описывает апоптотические изменения клеток эмбриона и элиминацию анеуплоидных клеток у эмбрионов с мозаицизмом. И третья модель описывает коррекции анеуплоидий, которые позволяют клеткам с моносомией или трисомией разделяться на клетки с эуплоидным количеством хромосом [5, 6].
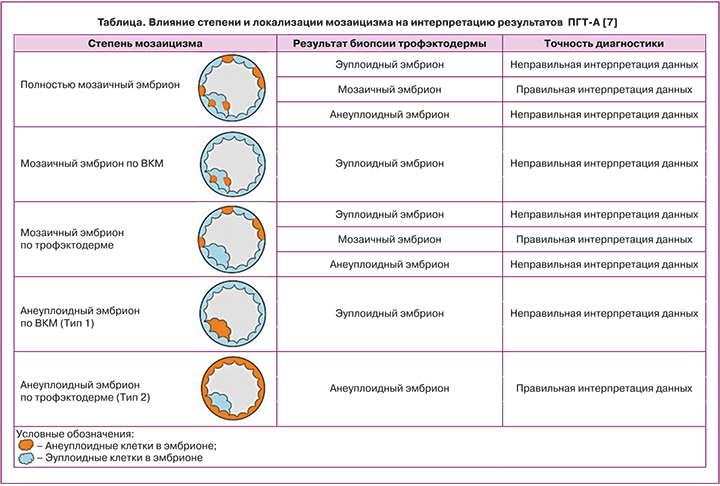
При биопсии трофэктодермы уровень мозаицизма, по разным данным, составляет от 4 до 32%. С введением высокопроизводительного секвенирования следующего поколения (NGS) теперь возможно диагностировать хромосомный мозаицизм на уровне от 20 до 80% [7]. Тем не менее в зависимости от степени выраженности мозаицизма и его локализации результат биопсии трофэктодермы эмбриона и последующая интерпретация данных ПГТ-А (преимплантационное генетическое тестирование на анеуплоидии) не всегда соответствует истинным показателям. Мозаицизм может затрагивать как весь эмбрион, так и отдельные его части: трофэктодерму, из которой образуется плацента, или внутриклеточную массу (ВКМ), которая дает начало эмбриону. Если мозаицизм затрагивает только ВКМ, то результат биопсии трофэктодермы у такого эмбриона будет соответствовать эуплоидному эмбриону. Если биопсия трофэктодермы была произведена у эмбриона, мозаичного по клеткам трофэктодермы, но в исследуемый образец попали эуплоидные клетки, результат ПГТ-А будет интерпретирован в пользу эуплоидного эмбриона. В таблице представлены точность диагностики различной степени и локализации мозаицизма у анализируемого эмбриона и возможные варианты диагностических ошибок. Представленные данные подтверждают, что процент мозаицизма в образце биопсии не всегда может быть прямым показателем процента мозаицизма во всем эмбрионе [8].
Несмотря на отсутствие определенного ограничения для определения мозаицизма, Международное общество преимплантационной генетической диагностики (PGDIS, 2019) предлагает эмбрион с более чем 20% анеуплоидных клеток считать мозаичным. Это означает, что эмбрионы с более низким уровнем мозаицизма следует рассматривать как нормальные (эуплоидные). Мозаичные эмбрионы отличаются по степени (низкая, средняя или высокая) и типу мозаицизма (сегментарный, одиночная хромосома, двойная хромосома или сложный мозаицизм) [9]. Результаты нескольких крупных исследований показали, что мозаичные эмбрионы могут имплантироваться и приводить к рождению здоровых детей в программах ВРТ [10]. В исследовании Spinella F. et al., опубликованном в 2017 г., было показано, что исход беременности при переносе мозаичного эмбриона зависит от степени мозаицизма и типа анеуплоидии [11].
Существуют предположения, что в случае соматических клеток мозаицизм обладает благотворным влиянием на организм. Например, в нейронах мозаицизм встречается очень часто, что позволяет разнообразить их функциональный статус [12–14]. Однако чаще всего мозаицизм связывают с очевидно отрицательными последствиями, например, с повышенной частотой прерывания беременности, появлением врожденных дефектов, задержками и расстройствами развития. Чем выше уровень мозаицизма эмбриона, тем ниже вероятность имплантации и выше риск выкидыша. В научной литературе сообщается о статистически значимом снижении частоты наступления клинической беременности, имплантации и живорождении при переносе эмбрионов с высоким уровнем мозаици.
Низкий уровень мозаицизма по отдельным хромосомам что это значит
Информационное письмо Международного общества ПГД от 27 мая 2019 г.
Журнал: Проблемы репродукции. 2019;25(4): 8-12
Информационное письмо Международного общества ПГД от 27 мая 2019 г.. Проблемы репродукции. 2019;25(4):8-12.
PGDIS Newsletter, May 27, 2019. Russian Journal of Human Reproduction. 2019;25(4):8-12.
https://doi.org/10.17116/repro2019250418
В предыдущем заявлении о позиции Международного общества преимплантационной генетической диагностики (МО-ПГД) от 2016 г. (www.pgdis.org) не представлены классификация мозаицизма и рекомендации для переноса эмбрионов с мозаицизмом [1].
Цель данного документа — оценка накопленной информации о переносе эмбрионов с мозаицизмом.
Введение
Основной задачей преимплантационной генетической диагностики на анеуплоидию (ПГТ-А) является повышение эффективности переносов в программе экстракорпорального оплодотворения (ЭКО) путем отбора эмбрионов без анеуплоидии. Доказано, что перенос эуплоидных эмбрионов повышает частоту имплантации, наступления беременности, живорождения. В последние годы в клиническую практику внедрены новые молекулярно-генетические методы исследования бластоцист на хромосомную патологию — анеуплоидию, такие как aCGH, SNP и NGS.
В настоящее время большинство лабораторий ЭКО культивируют эмбрионы до стадии бластоцисты с целью выявления жизнеспособных эмбрионов, а затем проводят биопсию небольшого числа клеток трофэктодермы для исследования на анеуплоидию. Анализ многоклеточных биоптатов дает возможность получить даже промежуточные результаты, определить состояние между полной анеуплоидией и эуплоидией (частично мозаичные эмбрионы).
Под хромосомным мозаицизмом принято понимать наличие в единичной пробе двух клеток или более с разным хромосомным набором, что иногда наблюдается и у незначительного количества здоровых эмбрионов на всех стадиях преимплантационного развития. При применении высокочувствительных методов исследования, таких как матричная CGH и NGS, основанных на методике подсчета числа копий, можно дифференцировать простую равномерную анеуплоидию, затрагивающую все клетки в биоптате, от частичной (мозаичной) анеуплоидии, затрагивающей только часть клеток в биоптате, а также подсчитать степень изменений количества копий [2]. При использовании высокоразрешающих методов NGS также можно выявить сегментарный мозаицизм и благодаря этому идентифицировать небольшие делеции или дупликации хромосом (обычно более 10 Мб).
Обзор новых данных
Частота эмбрионов с мозаицизмом
На стадии бластоцисты частота мозаицизма, установленная методами NGS, очень различается по данным разных клинических учреждений, варьирует от наименьшей — 2% и доходит до 40%. Тем не менее большинство клиник сообщают о частоте эмбрионов с мозаицизмом 5—10% среди всех протестированных эмбрионов [2—4]. Стабильная высокая частота мозаичных эмбрионов в некоторых клиниках может быть результатом методов лечения, особенностей культивирования, подходов к диагностике; имеет значение и контингент пациентов [4]. В таких случаях необходимо провести аудит клинической и лабораторной работы. Все клиники, которые отправляют эмбрионы в лаборатории для исследования на ПГТ-А, имеют право запросить у лаборатории информацию о частоте выявления мозаицизма и показателях пороговых данных.
Результаты переноса эмбрионов с мозаицизмом
В первом опубликованном исследовании метода матричной CGH на ПГТ-А сообщено о рождении здоровых детей после переноса заведомо мозаичного эмбриона [5]. После этого сообщения проведено несколько других исследований переноса большого количества эмбрионов с мозаицизмом [6—9]. В результате переноса мозаичных или частично мозаичных эмбрионов может наступить нормальная беременность, но по сравнению с переносом эуплоидных эмбрионов отмечается снижение частоты имплантации и повышение частоты самопроизвольного патологического прерывания беременности. В целом хорошие результаты получены при переносе эмбрионов с менее 40% мозаицизма, тогда как при мозаицизме 40—80% наступление жизнеспособной беременности маловероятно. Результаты хуже при переносе эмбрионов со сложным мозаицизмом, в который вовлечено более 1 хромосомы. Хотя опыт включает перенос менее 500 эмбрионов с мозаицизмом, все же понятно, что большое число эмбрионов с мозаицизмом обладает некоторой способностью к развитию. Важно, что после последующей пренатальной диагностики беременности методом амниоцентеза обнаружены нормальные эуплоидные плоды; это означает, что мозаицизм трофэктодермы в бластоцисте, вероятно, мог исчезнуть самопроизвольно. Все рожденные дети в настоящее время здоровы, не имеют признаков хромосомных заболеваний. Кроме того, в исследованиях показано, что результаты в целом не зависели от вовлеченных в начальный мозаицизм хромосом.
Генетический анализ бластоцист с мозаицизмом
В исследованиях, в которых проведен повторный анализ непригодных бластоцист после NGS, продемонстрировано соответствие (более 95%) начальным результатам анеуплоидии при исследовании других участков эмбрионов, включая внутреннюю клеточную массу (ВКМ) и другие участки трофэктодермы [7, 10, 11]. С недавних пор в результате исследований эмбрионов с мозаицизмом стала более понятной хромосомная организация бластоцист с мозаицизмом [12]. В целом, если уровень мозаицизма при начальной биопсии был высоким (более 40—80%), при последующей биопсии трофэктодермы и анализе ВКМ также обнаруживали некоторый уровень мозаицизма. Однако если уровень мозаицизма изначально был низким (менее 40%), то при последующем анализе трофэктодермы и ВКМ также обнаруживали его снижение, при этом некоторые эмбрионы были равномерно эуплоидными.
Технические вопросы
В процессе проведения ПГТ-А появляются косвенные доказательства того, что NGS и конвейер анализа данных для измерения количества копий хромосом могут неправильно указывать на мозаицизм в некоторых эмбрионах как следствие влияния различных методик [4]. Вероятные причины подобных артефактов следующие:
— методика проведения биопсии: некачественная техника биопсии, при которой получены клетки в малом количестве, с повреждениями или частичным разрушением и потерей клеточной ДНК, что влияет на хромосомный профиль;
— анализ: алгоритмы нормализации ячеек картирования хромосом также могут потенциально искажать результат, особенно если количество ячеек, используемое для нормализации профилей, является переменным или низким. Кроме того, искажения в построении библиотеки из-за исходной ДНК худшего качества (включая нарушения амплификации целого генома) могут привести к недооценке или избыточному накоплению хромосом (мозаицизм целых хромосом) или субхромосомных областей (сегментарный мозаицизм). При NIPT-анализе свободно-клеточной ДНК, при котором используется похожая методика NGS, выдвинуто предположение, что искажения могут возникать на этапе подготовки библиотеки, что приводит к неправильному копированию участков, особенно для хромосомных сегментов.
Как это влияет на исследование анеуплоидии в клинической практике?
Большинство (более 90%) результатов биопсии трофэктодермы показывает неравномерную эуплоидию для всех хромосом или полную анеуплоидию, включая одну хромосому или более. Тем не менее у небольшого количества эмбрионов может быть промежуточное количество изменений в одной или нескольких хромосомах, что свидетельствует о возможном мозаицизме. Иногда это могут быть единственные эмбрионы, доступные для переноса. Мозаицизм в биоптатах трофэктодермы теоретически может оказывать клиническое влияние на беременность, в том числе на функцию плаценты или на развитие синдромов заболеваний новорожденных, поэтому перенос подобных эмбрионов может проводиться только с согласия пациентов и после рассмотрения всех других вариантов.
Рекомендации для лаборатории
1. Следует понимать, какое влияние на последующий результат может оказывать плохая техника биопсии. В идеале для биопсии нужно брать 5 клеток и более, чтобы провести точную и сбалансированную амплификацию. Количество клеток менее 5 может влиять на профиль амплификации (шум) и степень диагностики мозаицизма. Рекомендуется проводить биопсию не более 10 клеток, чтобы свести к минимуму влияние самой процедуры на оставшийся эмбрион. Необходимо уменьшить вероятность повреждения клеток, чтобы снизить отклонения в амплификации и получить ДНК, соответствующую оригиналу в клетке. Если для биопсии используется лазер, то точки контакта должны быть минимальными и предпочтительно располагаться в местах соединения клеток. Если у когорты эмбрионов выявляется достаточно высокая частота мозаицизма, то необходимо провести оценку эмбриологических протоколов и методики проведения ПГТ-А для выяснения причины такого явления.
2. По техническим причинам при отчете об уровне мозаицизма в образце биопсии следует использовать только аналитическое оборудование, которое способно воспроизводимо измерять количество копий. Различное аналитическое оборудование может обладать меньшим (или большим) диагностическим и количественным потенциалом для диагностики мозаицизма, а также внутренним шумовым уровнем. Сервисные лаборатории могут проводить собственные контрольные эксперименты как для эуплоидных, так и для анеуплоидных продуктов WGA из различного набора проб. Значения, лежащие вне этого эуплоидного или анеуплоидного разброса, считаются мозаичными. Диагностику и количественное определение уровня мозаицизма можно при необходимости осуществлять в экспериментах по перемешиванию клеток. Эксперименты по смешиванию небольшого количества ДНК могут быть не такими информативными из-за теоретических проблем с отбором небольшого количества копий, приводящих к смещению относительного хромосомного соотношения. Эмбрионы в избранном низшем значении могут быть определены как эуплоидные, тогда как эмбрионы над верхней установленной границей могут считаться анеуплоидными. Типичный нижний предел в ряде публикаций установлен как 20%, тогда как верхний — 80% [13—17]. На эти предельные значения от референсной группы должна опираться сервисная группа. Рекомендуется, чтобы любая клиника, использующая коммерческие наборы для ПГТ-А, учитывала эти референсные показатели для четкой диагностики мозаицизма и консультирования пациентов.
3. Принимая во внимание биологию и развитие мозаицизма, следует учитывать, что любой биопсированный фрагмент, расцененный как мозаичный, может четко не отображать состояние окружающей трофэктодермы в остальной части эмбриона. В связи с широким разбросом данных полученные значения нужно рассматривать только как ориентир для консультирования пар относительно переноса (или уничтожения) эмбриона с подозрением на мозаицизм. Мы предлагаем рассматривать мозаичный спектр как непрерывный градиент риска неблагоприятного результата — от относительно низкого уровня (20%) до высокого риска, когда показатель приближается к 80% (см. рисунок). 
4. В формат лабораторной отчетности необходимо включать отчет о мозаицизме, референсные показатели для мозаицизма и описание природы выявленной хромосомной аномалии.
Рекомендации для клиницистов
1. Пациентам следует сообщать, что любой генетический анализ, проводимый на выборке из одной или небольшого числа клеток из биоптата преимплантационного эмбриона, не может иметь стопроцентной точности по причине технических и биологических факторов, включая хромосомный мозаицизм.
2. Консультирование пациентов и информированное согласие на исследование анеуплоидии (если проводится) должны затрагивать вопросы влияния мозаицизма на исходы переноса и имплантации. Это должен объяснять пациенту врач, который рекомендует ПГТ-А.
3. Переносу бластоцист с нормальным эуплоидным набором должно отдаваться предпочтение перед переносом мозаичного эмбриона.
4. При рассмотрении вопроса о переносе бластоцисты с мозаицизмом необходимо обсудить с пациентом следующие возможности:
— возобновление дальнейших циклов ПГТ-А для повышения шанса получения эуплоидной бластоцисты для переноса;
— перенос бластоцисты с более низким уровнем мозаицизма после соответствующего консультирования.
Настоятельно рекомендуется проведение пренатальной диагностики плода и плаценты при любой беременности после ПГТ, особенно это касается случаев после переноса эмбриона с мозаицизмом. Амниоцентез с 14-й недели в настоящее время считается наиболее информативным для генетической диагностики плода. Для более раннего исследования плаценты (с 10-й недели) можно рассмотреть методику NIPT, позволяющую анализировать плацентарные копии всех 24 хромосом. Простое NIPT-исследование 5 хромосом (21-й, 18-й, 13-й, Х и Y) может быть недостаточно информативным. Для диагностики аномалий плода можно использовать ультразвуковое исследование, а для диагностики нарушения функции плаценты — допплеровское исследование и скрининг PAPP-A.
Рекомендации по очередности переноса мозаичных эмбрионов
Основываясь на наших текущих знаниях о репродуктивных исходах для плода и плацентарном мозаицизме при пренатальной диагностике и на новой информации, полученной в результате недавних исследований по анализу и переносу эмбрионов, предлагаем клиницистам (или генетическим консультантам, если таковые имеются) руководствоваться следующими положениями:
1. Эмбрионы с низким уровнем мозаицизма (низкий риск неблагоприятного результата переноса эмбриона) предпочтительнее эмбрионов с высоким риском мозаицизма, который в свою очередь может обусловливать дальнейший неблагоприятный исход. Относительный процент мозаицизма является более благоприятным прогностическим фактором, нежели вовлечение конкретной хромосомы (хромосом). Конкретные хромосомы связаны с конкретными синдромами, и это должно обсуждаться при консультировании. Эмбрионы с высоким риском мозаицизма нужно переносить с осторожностью и только после соответствующей генетической консультации.
2. Если принято решение о переносе эмбриона с мозаицизмом по одной хромосоме, то в первую очередь нужно делать выбор на основании уровня мозаицизма, а затем — конкретно задействованной хромосомы. Выбор в отношении мозаичного эмбриона должен основываться на информации о хромосомных синдромах, а также на уровне мозаицизма в биопсийной пробе. Если есть выбор между переносом 2 эмбрионов с мозаицизмом одинакового уровня, то наименьший приоритет отдается эмбрионам с мозаицизмом по хромосомам, связанным с непарной дисомией, тяжелой задержкой внутриматочного развития или жизнеспособными синдромами. Для получения более подробной информации о специфических осложнениях развития плаценты и о синдромах плода, а также о вероятной связи хромосом с различными аномалиями можно обратиться к обзору F. Grati и соавт. [18]. Для справки по вопросам переноса эмбрионов с мозаицизмом можно использовать последние рекомендации Американского общества репродуктивной медицины (American Society for Reproductive Medicine — ASRM) [19].
Заключение
Развитие геномных технологий для преимплантационной генетической диагностики произвело революцию в нашей способности обнаруживать на уровне отдельных клеток или небольшого количества клеток генетические аномалии различных типов. Повышение чувствительности и разрешающей способности этих методов позволит также идентифицировать более полный спектр хромосомных аномалий, включая хромосомный и сегментарный мозаицизм — область, в которой наши знания неполны и все еще развиваются. Предыдущие результаты экстракорпорального оплодотворения указывают на отсутствие повышенного риска хромосомных аномалий по сравнению с естественной беременностью, и поэтому, исходя из имеющихся данных преимплантационной генетической диагностики на анеуплоидию, перенос эмбрионов с мозаицизмом представляется относительно безопасным вариантом для пар с низким или минимальным риском неблагоприятных исходов беременности. Тем не менее вопрос о переносе бластоцисты после определения в ней различной степени анеуплоидии должен решаться только на основании тщательного консультирования пациентов, в том числе генетического. Необходимо принимать во внимание лабораторные рекомендации при консультировании пациентов о риске неблагоприятного результата, связанном с переносом эмбриона с мозаицизмом. Пациент должен быть информирован о необходимости последующего наблюдения за течением беременности и проведения неинвазивной пренатальной диагностики или инвазивных исследований, таких как амниоцентез, при которых может быть выявлен мозаицизм. Чтобы лучше понять последствия переноса эмбрионов с мозаицизмом и представить ценную информацию для улучшения генетического консультирования пациентов, рассматривающих такую возможность, необходимо проводить долгосрочные исследования всех предполагаемых переносов эмбрионов с мозаицизмом. С широким внедрением неинвазивной пренатальной диагностики и появлением более точных технологий неинвазивного скрининга анеуплоидий можно легко наблюдать за развитием беременности после переноса эмбриона с мозаицизмом. Более того, поскольку показано, что неинвазивная диагностика дает возможность обнаруживать мозаицизм плода даже с вовлечением редких трисомий [20], теперь есть возможность проследить за конечным результатом исходного мозаицизма трофэктодермы. Получение этих данных, а также исследование плацентарной ткани при рождении помогут лучше понять, насколько безопасен перенос эмбриона с мозаицизмом. Что касается исследований, то генетический анализ методом NGS непригодных для переноса эмбрионов с мозаицизмом, переданных для исследований, поможет лучше понять значение оценки начальной биопсии и предоставить ценную информацию об их генетическом строении.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.
Автор, ответственный за переписку: Ярмолинская М.И. —
e-mail: yarmolinskaya@gmail.com
* DS Cram, D Leigh, A Handyside, L Rechitsky, K Xu, G Harton, J Grifo, C Rubio, E Fragouli, S Kahraman, E Forman, M Katz-Jaffe, H Tempest, A Thornhill, C Strom, T Escudero, Q Jie, S Munne, JL Simpson, A Kuliev