Мультилокулярная кистозная почечная неоплазия низкого злокачественного потенциала: опыт НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина
Полный текст:
Аннотация
Введение. Мультилокулярная кистозная почечная неоплазия низкого злокачественного потенциала (МКПННЗП), или мультилокулярный кистозный почечно-клеточный рак (ПКР), в настоящее время выделена в отдельную нозологическую единицу. В литературе не опубликованы результаты крупных исследований, основанных на большом количестве наблюдений.
Цель исследования – систематизация клинических и патоморфологических характеристик МКПННЗП.
Материалы и методы. В период с января 2011 г. по декабрь 2015 г. в клинике НИИ урологии и интервенционной радиологии им. Н. А. Лопаткина среди 588 больных ПКР диагностированы 32 случая МКПННЗП. Нами были изучены и продемонстрированы клинико-морфологические характеристики данного заболевания, хирургические подходы к его лечению и отдаленные результаты.
Результаты. МКПННЗП составила 5,44 % случаев среди всех гистологических форм ПКР. Большинство (75 %) больных не имели клинических проявлений заболевания. Стадия опухолевого процесса Т1а соответствовала 65,6 % опухолей, стадия Т1b – 28,1 % и стадия Т2 – только 6,2 %. Во всех случаях неоплазия характеризовалась средней и умеренной дифференцировкой (G1–2) ядерной градации Интернационального общества урологических патологов (International Society of Urological Pathology, ISUP). Отмечено, что только 25 % больных имели нормальный показатель индекса массы тела. У 31 из 32 пациентов прослежены отдаленные результаты. Медиана наблюдения составила 29 (14–66) мес. Ни у одного пациента не выявлено признаков прогрессирования заболевания.
Заключение. Больные МКПННЗП обладают наилучшим онкологическим прогнозом среди пациентов с ПКР. Необходимость классификации этой опухоли по системе TNM в настоящее время является сомнительной. В качестве хирургического лечения следует использовать только органосохраняющие операции. В случае МКПННЗП рекомендуется увеличить периоды между контрольными обследованиями, предложенные для больных ПКР, а комплекс диагностических манипуляций должен быть сведен до минимума.
Ключевые слова
Об авторах
Заведующий отделом «Патологический анатомии с группой молекулярной генетики»
Россия, 105425 Москва, ул. 3-я Парковая, 51, стр. 1
Конфликт интересов: Встатье нет конфликта интересов
Список литературы
1. Злокачественные новообразования в России в 2015 году (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИРЦ» Минздрава России, 2016. 250 с. [Malignant tumors in Russia in 2015 (morbidity and fatality). Eds.: А.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: MNIOI im. P.A. Gertsena – filial FGBU “NMIRTS” Minzdrava Rossii, 2016. 250 p. (In Russ.)].
2. Ferlay J., Steliarova-Foucher E., Lortet-Tieulent J. et al. Cancer incidence and mortality patterns in Europe: estimates for 40 countries in 2012. Eur J Cancer 2013;49(6):1374–403. DOI: 10.1016/j.ejca.2012.12.027. PMID: 23485231.
3. Lopez-Beltran A., Scarpelli M., Montironi R., Kirkali Z. 2004 WHO classification of the renal tumors of the adults. Eur Urol 2006;49(5):798–805. DOI: 10.1016/j.eururo.2005.11.035. PMID: 16442207.
4. Bhatt J.R., Jewett M.A., Richard P.O. et al. Multilocular cystic renal cell carcinoma: pathological T staging makes no difference to favorable outcomes and should be reclassified. J Urol 2016;196(5):1350–5. DOI: 10.1016/j.juro.2016.05.118. PMID: 27341751.
5. Li T., Chen J., Jiang Y. et al. Multilocular cystic renal cell neoplasm of low malignant potential: a series of 76 cases. Clin Genitourin Cancer 2016;14(6):553–7. DOI: 10.1016/j.clgc.2016.03.017. PMID: 27108004.
6. Mazzucchelli R., Scarpelli M., Montironi R. et al. Multilocular cystic renal cell neoplasms of low malignant potential. Anal Quant Cytopathol Histpathol 2012;34(5):235–8. PMID: 23301382.
7. Srigley J.R., Delahunt B., Eble J.N. et al. The International Society of Urological Pathology (ISUP) vancouver classification of renal neoplasia. Am J Surg Pathol 2013;37(10):1469–89. DOI: 10.1097/PAS.0b013e318299f2d1. PMID: 24025519.
8. Montironi R., Lopez-Beltran A., Cheng L., Scarpelli M. Multilocular cystic renal cell carcinoma with focus on clinical and pathobiological aspects. Eur Urol 2013;63:400–1.
9. Kuroda N., Ohe C., Mikami S. et al. Multilocular cystic renal cell carcinoma with focus on clinical and pathobiological aspects. Histol Histopathol 2012;27(8):969–74. DOI: 10.14670/HH-27.969. PMID: 22763870.
10. You D., Shim M., Jeong I.G. et al. Multilocular cystic renal cell carcinoma: clinicopathological features and preoperative prediction using multiphase computed tomography. BJU Int 2011;108(9):1444–4. DOI: 10.1111/j.1464-410X.2011.10247.x. PMID: 21722289.
11. Israel G.M., Hindman N., Bosniak M.A. et al. Evaluation of cystic renal masses:
12. comparison of CT and MR imaging by using the Bosniak classification system. Radiology 2004;231(2):365–71. DOI: 10.1148/radiol.2312031025. PMID: 15128983.
13. Pedersen J.F., Emamian S.A., Nielsen M.B. Simple renal cyst: relations to age and arterial blood pressure. Br J Radiol 1993;66(787):581–4. DOI: 10.1259/0007-1285-66-787-581. PMID: 8374720.
14. Gong K., Zhang N., He Z. et al. Multilocular cystic renal cell carcinoma: an experience of clinical management for 31 cases. J Cancer Res Clin Oncol 2008;134(4):433–7. DOI: 10.1007/s00432-007-0302-1. PMID: 17846788.
15. Halat S., Eble J.N., Grignon D.J. et al. Multilocular cystic renal cell carcinoma is a subtype of clear cell renal cell carcinoma. Mod Pathol 2010;23(7):931–6. DOI: 10.1038/modpathol.2010.78. PMID: 20348877.
16. Jhaveri K., Gupta P., Elmi A. et al. Cystic renal cell carcinomas: do they grow, metastasize, or recur? AJR Am J Roentgenol 2013;201(2): 292–6. DOI: 10.2214/AJR.12.9414. PMID: 23883243.
17. Webster W.S., Thompson R.H., Cheville J.C. et al. Surgical resection provides excellent outcomes for patients with cystic clear cell renal cell carcinoma. Urology 2007;70(5):900–4. DOI: 10.1016/j.urology.2007.05.029. PMID: 18068445.
18. Koga S., Nishikida M., Hayashi T. et al. Outcome of surgery in cystic renal cell carcinoma. Urology 2000;56(1):67–70. PMID: 10869626.
Для цитирования:
Алексеев Б.Я., Шевчук И.М., Ефремов Г.Д., Самойлова С.И. Мультилокулярная кистозная почечная неоплазия низкого злокачественного потенциала: опыт НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина. Онкоурология. 2017;13(3):34-38. https://doi.org/10.17650/1726-9776-2017-13-3-34-38
For citation:
Alekseev B.Y., Shevchuk I.M., Efremov G.D., Samoylova S.I. Multilocular cystic renal neoplasm of low malignant potential: experience of N.N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology. Cancer Urology. 2017;13(3):34-38. (In Russ.) https://doi.org/10.17650/1726-9776-2017-13-3-34-38
Клиническая постановка, лечение и прогноз уротелиальной карциномы
Международное общество урологической патологии разработало классификационную схему классификации карциномы переходных клеток. Этими четырьмя классами являются уротелиальная папиллома, уротелиальные новообразования с низким злокачественным потенциалом, уротелиальная карцинома и полноценная карцинома. Папиллома обычно наблюдается у более молодых пациентов и встречается редко. Новообразования с низким злокачественным потенциалом иногда трудно отличить от уротелиальных карцином. Эти опухоли редко становятся инвазивными к соседней ткани.
Уротелиальная карцинома также проявляется в виде папиллом. Эти опухоли могут вторгаться в близлежащие ткани, но обычно не прогрессируют. Карциномы бывают плоскими, папиллярными или и теми, и другими. Эти опухоли больше склонны вторгаться в близлежащую мышечную ткань. Наиболее распространенным средством лечения папиллярной карциномы в мочевом пузыре является хирургическое вмешательство. Когда эти опухоли классифицируются, их обычно можно полностью удалить.
К сожалению, эти карциномы рецидивируют от 50% до 70% времени. Из-за этой высокой частоты рецидивов рака пациентам с карциномой следует тщательно контролировать после операции с цистоскопией и регулярным анализом мочи. Другие виды терапии, называемые иммунологической терапией (иммунотерапия) и химиотерапией, часто используются при лечении карциномы мочевого пузыря. Эти методы используют агенты, которые непосредственно применяются к мочевому пузырю. Когда агент помещается в мочевой пузырь, организм начинает иммунный ответ, который иногда разрушает опухоль.
Пациенты обычно получают одно лечение в неделю в течение шести недель. После этого периода используется программа обслуживания, включающая трехнедельные курсы лечения на срок до двух лет. Наиболее распространенной химиотерапией, используемой для транзиторной клеточной карциномы в прошлом, является комбинация препаратов цисплатин, адриамицин, винбластин и метотрексат. Более новые и менее токсичные препараты, такие как целекоксиб, бортезомиб, иксабепилон и мальтолат галлия, проверяются на замену этих более старых агентов. Комбинированный режим химиотерапии и излучения рассматривается как терапия, когда карцинома вторгается в мышцу, окружающую мочевой пузырь. Эффективность этого метода еще не изучена в исследованиях. Только лучевая терапия не является эффективным лечением. Карциному в верхних мочевых путях также лечат хирургическими процедурами.
Пострадавшие районы в этом регионе, включая почку, иногда удаляются. Часть или весь мочеточник и части мочевого пузыря также удаляются, в некоторых случаях. Неинвазивная папиллома редко повторяется после удаления. Если уротелиальные новообразования с низким злокачественным потенциалом повторяются, они обычно являются доброкачественными опухолями. Однако примерно в 3% — 5% случаев эти рецидивы имеют более высокий класс. Эти карциномы редко становятся инвазивными, и пациенты с ними имеют годичную выживаемость от 95% до 98%. Уротелиальные карциномы часто проявляют признаки инвазии во время диагностики, но не связаны с высоким риском развития злокачественных новообразований.
Степени рака мочевого пузыря
Что такое степень рака?
Степень опухоли определяется тем, как раковые клетки выглядят под микроскопом. Врач сравнивает насколько опухолевая клетка отличается от нормальной.
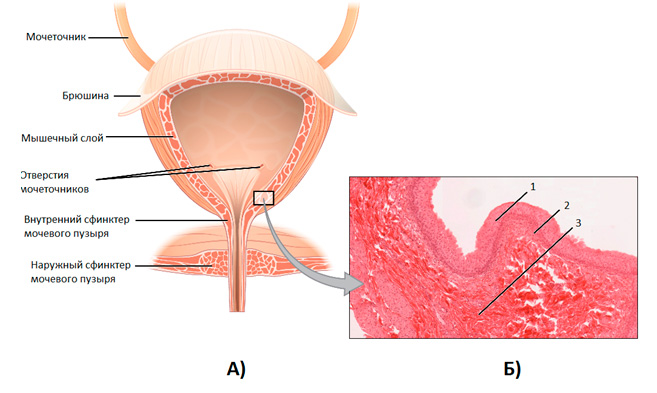
Рисунок. А – мочевой пузырь. Б – вид под микроскопом: 1 – слизистая оболочка, 2 – собственная пластинка, 3 – подслизистая оболочка.
В настоящее время распространены две системы классификации злокачественных поражений мочевого пузыря.
Классификация рака Всемирной организации здравоохранения (ВОЗ) от 1973 года
Низкая степень рака мочевого пузыря (1)
Здоровая ткань состоит из множества клеток разного вида, сгруппированных вместе. Если опухоль по строению напоминает здоровую ткань и ее клетки похожи на нормальные, она называется высокодифференцированной или низкой степени злокачественности. Такая опухоль растет медленно, не склонна к инвазии и имеет низкий риск метастазов. Хорошо лечится, вероятность рецидива невысока.
Средняя степень рака мочевого пузыря (2)
Раковые клетки выглядят более атипично, т.е. значительно отличаются от здоровых. Опухоль растет быстрее, имеет тенденцию к инвазивному росту, характеризуется более высокой вероятностью развития метастазов. Такая опухоль называется умеренно дифференцированной.
Высокая степень рака мочевого пузыря (3)
Такая опухоль наиболее злокачественна и опасна. Ее клетки и структура ткани абсолютно не похожи на здоровые, она быстро растет, распространяется на все слои мочевого пузыря и за его пределы, высока вероятность метастазирования. Опухоль называется низко дифференцированной. После лечения высок риск рецидива.
Классификация рака ВОЗ от 2004 года
Кроме злокачественных поражений мочевого пузыря существуют и доброкачественные опухоли, а также предраковые состояния. Классификация ВОЗ от 2004 года учитывает эти состояния и дает более детальную морфологическую оценку новообразований мочевого пузыря.
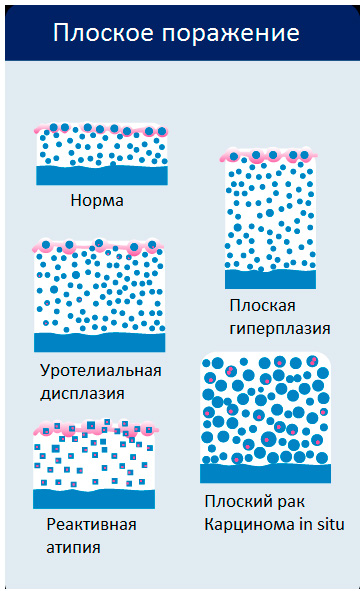
Плоские новообразования
Атипия – аномальное, отличающееся от нормального, строение клеток.
Рисунок. Плоские новообразования
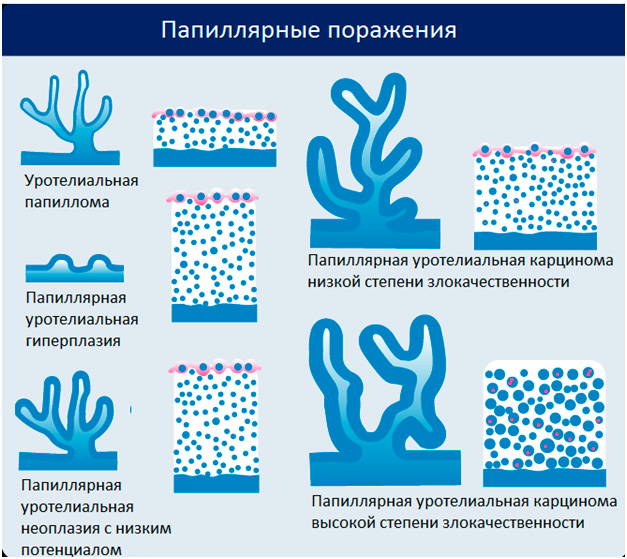
Папиллярные новообразования
Рисунок. Папиллярные новообразования.
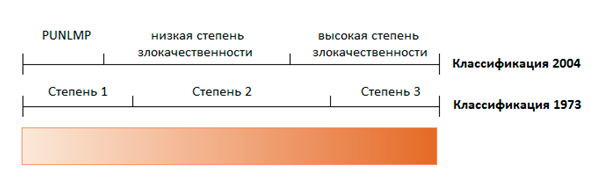
Соответствие двух классификаций
Классификация 2004 года
Классификация 1973 года
Папиллярная уротелиальная неоплазия с низким потенциалом
Папиллярная уротелиальная карцинома низкой степени злокачественности
Папиллярная уротелиальная карцинома высокой степени злокачественности
Рисунок. Соотношение классификаций
Кешишев Николай Георгиевич
Статьи по данной теме
Врачи направления
Видеоотзывы пациентов
Аденома простаты. ТУР простаты (Трансуретральная резекция) 4 года назад
Рак простаты с метастазами: 8 лет борьбы за жизнь
Коралловидный камень почки. Чрескожная нефролитотрипсия 10 дней назад
Низкий злокачественный потенциал что это
ФГУ Эндокринологический научный центр, Москва
Новая международная гистологическая классификация опухолей щитовидной железы
Журнал: Архив патологии. 2018;80(1): 37-45
Абросимов А. Ю. Новая международная гистологическая классификация опухолей щитовидной железы. Архив патологии. 2018;80(1):37-45.
Abrosimov A Iu. The new international histological classification of thyroid tumors. Arkhiv Patologii. 2018;80(1):37-45.
https://doi.org/10.17116/patol201880137-45
ФГУ Эндокринологический научный центр, Москва
В 2017 г. Международное агентство по изучению рака (МАИР) выпустило в свет новое 4-е издание Классификации ВОЗ опухолей эндокринных органов. Как и в предыдущем издании 2004 г., в новой классификации значительное внимание уделено новообразованиям щитовидной железы (ЩЖ). В номенклатуре опухолей ЩЖ произошли изменения, основанные на полученных за истекший период результатах клинических морфологических и молекулярно-генетических, исследований и соответствующих новых взглядах на злокачественный потенциал и прогноз ряда новообразований, которые следует учитывать патологоанатомам в повседневной диагностической практике. Целью настоящей публикации является представление новой классификации опухолей ЩЖ с акцентом на внесенные изменения.
ФГУ Эндокринологический научный центр, Москва
Новое издание Классификации ВОЗ опухолей эндокринных органов [1] отражает согласованное мнение 166 экспертов международной рабочей группы, принятое на заседании редакции МАИР в Лионе, Франция, 26—28 апреля 2016 г. Редакторами издания являются R.V. Lloyd, R.Y. Osamura, G. Klöppel, J. Rosai. В предисловии к главе, посвященной опухолям щитовидной железы (ЩЖ), J. Rosai процитировал всемирно известного патолога P. Masson [2], написавшего в своем научном труде «Human tumors», что «Нет более трудной задачи, чем разработка классификации карцином щитовидной железы…», и «…из всех карцином они (карциномы щитовидной железы), вероятно, преподносят гистопатологам самые большие уроки…».
Выход в свет нового издания классификации обусловлен научными достижениями последних лет по ряду направлений исследования тиреоидного канцерогенеза, главным из которых является раскрытие молекулярно-генетических особенностей высокодифференцированных опухолей ЩЖ, имеющих фолликулярное строение и развивающихся из фолликулярного эпителия. Понимание молекулярных механизмов опухолевого роста позволило пролить свет на различия, дающие теоретические и практические основания для выделения классификационных категорий папиллярного и фолликулярного, доброкачественного и злокачественного типов новообразований. Вместе с тем остаются дискуссионными вопросы относительной диагностической значимости формирования опухолью сосочковых структур и установления особых изменений ядер опухолевых клеток, характеризующих папиллярную карциному. Для высокодифференцированных инкапсулированных опухолей фолликулярного строения капсулярная и/или сосудистая инвазия остается главным диагностическим критерием злокачественности. Камнем преткновения прошлого издания классификации стали категории инкапсулированных опухолей фолликулярного строения, занимающих промежуточное положение между фолликулярными аденомами и фолликулярными карциномами («фолликулярные новообразования неопределенного злокачественного потенциала»), фолликулярными аденомами и фолликулярным вариантом папиллярного рака («высокодифференцированные новообразования неопределенного злокачественного потенциала»), которые были лишь упомянуты, но не рекомендованы в качестве категорий для широкого использования [3]. Напротив, эксперты ВОЗ справедливо рекомендовали проводить тщательное гистологическое исследование адекватного количества образцов опухолевой ткани, особенно периферических отделов инкапсулированных новообразований фолликулярного строения, с целью получения оснований для более категоричного заключения о доброкачественном и злокачественном характере опухоли. Вместе с тем категории пограничных опухолей («серой зоны», или опухолей неопределенного злокачественного потенциала) используют в классификациях новообразований других органов. В новой классификации опухолей ЩЖ принципиальный вопрос о том, являются ли пограничные опухоли отдельными категориями (должны ли быть классифицированы как карциномы или как новообразования с низким злокачественным потенциалом), получил свое дальнейшее развитие. В разделе классификации, озаглавленном «другие инкапсулированные опухоли щитовидной железы фолликулярного строения», после соответствующего предисловия, сделанного J.K.C. Chan, Y.E. Nikiforov, G. Tallini, выделены две категории опухолей неопределенного злокачественного потенциала («фолликулярная опухоль неопределенного злокачественного потенциала» и «высокодифференцированная опухоль неопределенного злокачественного потенциала») и одна новая категория пограничных опухолей, названная «неинвазивная фолликулярная опухоль с изменениями ядер опухолевых клеток папиллярного типа» (non-invasive follicular thyroid neoplasm with papillary-like nuclear features). Последней из перечисленных категорий в предыдущей гистологической классификации не было, в новой номенклатуре опухолей ей присвоен код 8349/1. Следует заметить также, что ранее гиалинизирующая трабекулярная опухоль была отнесена в группу аденом и аналогичных им опухолей с гистологическим кодом 8336/0, что означало доброкачественность новообразования. В новой классификации «гиалинизирующая трабекулярная опухоль» поименована отдельно после фолликулярной аденомы и имеет код 8336/1, что означает неуточненный, неопределенный злокачественный потенциал или пограничную опухоль. В табл. 1 представлена

Кроме выделения группы «другие инкапсулированные опухоли фолликулярного строения», состоящей из трех категорий с соответствующими классификационными кодами, а также изменения гистологического кода «гиалинизирующая трабекулярная опухоль», выделен ряд гистологических вариантов папиллярного, фолликулярного рака и отдельно онкоцитарных (Гюртле-клеточных) опухолей.
Представляется целесообразным остановиться подробнее на наиболее распространенных диагностических категориях, интерпретация которых претерпела изменения по сравнению с предыдущим изданием классификации.
Фолликулярная аденома определена как доброкачественная инкапсулированная неинвазивная опухоль, демонстрирующая признаки фолликулярно-клеточной дифференцировки при отсутствии изменений ядер опухолевых клеток, характерных для папиллярной карциномы. В отличие от гиперпластического неопухолевого узлового поражения фолликулярная аденома характеризуется моноклональным клеточным составом. В связи с тем что без молекулярно-генетического исследования установить клональность затруднительно, возникают трудности дифференциальной диагностики аденомы и гиперпластических неопухолевых узловых образований. Многие патологоанатомы при многоузловом поражении ЩЖ не ставят диагноз аденомы, а лишь констатируют наличие гиперпластического процесса и отсутствие признаков злокачественности. Гистологическое исследование позволяет установить опухоль, окруженную собственной фиброзной капсулой. Строение аденом широко варьирует: нормо-, макро-, микрофолликулярное, солидное и трабекулярное. В одной опухоли могут быть представлены несколько структурных компонентов. Редко аденомы имеют сосочковое и инсулярное строение. В пояснительном тексте новой классификации упомянуты следующие варианты аденом: гиперфункционирующая (токсическая или горячая) аденома, аденома с сосочковой гиперплазией, липоаденома (аденолипома), аденома с уродливыми ядрами, перстневидно-клеточная аденома, светлоклеточная аденома, веретеноклеточная аденома, черная фолликулярная аденома (у пациентов, получавших лечение миноциклином). В новой классификации нет упоминания о ранее использовавшемся и вводившем в заблуждение клиницистов термине «атипическая аденома». Онкоцитарные (Гюртле-клеточные) аденомы выделены в отдельную категорию Гюртле-клеточных опухолей (Гюртле-клеточная аденома и Гюртле-клеточная карцинома). При иммуногистохимическом исследовании опухолевые клетки иммунореактивны с антителами к цитокератинам, тиреоглобулину, TTF-1, PAX8, но негативны с антителами к кальцитонину, CEA, нейроэндокринным маркерам. Индекс мечения пролиферирующих клеток Ki-67 обычно составляет менее 5%. Реакции с антителами к галектину-3, HBME-1 и CITED редко бывают позитивными. Молекулярно-генетический профиль 30% аденом характеризуется соматическими мутациями генов семейства RAS. «Горячей точкой» мутаций NRAS и HRAS является кодон 61, менее часты соматические мутации гена KRAS. В отличие от фолликулярных карцином клетки аденом реже имеют структурные перестройки PAX8/PPARG. Мутации TSHR и GNAS обнаружены в клетках фолликулярных аденом с признаками повышенной функциональной активности.
Гиалинизирующая трабекулярная опухоль — новообразование, развивающееся из фолликулярного эпителия и состоящее из трабекулярных структур, образованных полигональными и вытянутой формы клетками. Трабекулы перемежаются с интра- и межтрабекулярно расположенным гиалиновым материалом, имеющим разную степень выраженности. В новой классификации опухоль отнесена к группе пограничных новообразований низкого или неопределенного злокачественного потенциала. Средний возраст пациентов составляет 50 лет, хотя описаны наблюдения у лиц 28—30-летнего возраста, при этом преобладают пациенты женского пола. Гиалинизирующая трабекулярная опухоль может возникать на фоне хронического тиреоидита, иногда встречается вместе с папиллярным раком, многоузловым зобом. Гистологическое исследование выявляет однотипное трабекулярно-альвеолярное строение опухоли, которая состоит из клеток вытянутой формы, среднего и крупного размера, с мелкогранулярной, ацидофильной или амфофильной цитоплазмой с наличием внеклеточного эозинофильного вещества (гиалина), характеризующегося положительной ШИК-реакцией. Ядра опухолевых клеток с узурами, псевдовключениями и мелкими ядрышками (похожи на ядра клеток папиллярного рака), митозы редки. Опухолевые трабекулы окружены нежной фиброваскулярной стромой. Окраска на амилоид отрицательная. Клетки опухоли экспрессируют тиреоглобулин, TTF-1, но не экспрессируют кальцитонин. Экспрессия маркеров, используемых для оценки злокачественного потенциала (галектин-3, цитокератин-19 и HBME-1), может наблюдаться в клетках до 50% опухолей. Характерной для гиалинизирующей трабекулярной опухоли является мембранная экспрессия MIB1 (Ki-67) в отличие от ядерной, обычно используемой для оценки индекса пролиферативной активности. Следует заметить, что мембранная экспрессия Ki-67 отмечена лишь при отсутствии высокотемпературной демаскирующей обработки срезов, применяемой с целью восстановления антигенных детерминант после воздействия фиксирующих растворов. Молекулярно-генетические исследования, установившие наличие структурных перестроек хромосом с формированием химерных генов RET/PTC1 в половине наблюдений гиалинизирующих трабекулярных опухолей, позволили высказать предположение о возможной связи с аналогичными молекулярными механизмами развития папиллярного рака, однако не было получено дальнейшего подтверждения указанной гипотезы, равно как пока не зарегистрировано мутаций BRAF или RAS в клетках гиалинизирующей трабекулярной опухоли. Несмотря на благоприятный прогноз у большинства пациентов после хирургического лечения, в англоязычной литературе представлены очень редкие описания метастазирования опухоли в регионарные лимфатические узлы и лишь одно наблюдение метастазов в ткань легкого [4].
Другие инкапсулированные опухоли фолликулярного строения (рис. 1).



Папиллярная карцинома — это злокачественная эпителиальная опухоль, демонстрирующая фолликулярно-клеточную дифференцировку и ряд признаков, касающихся изменений ядер опухолевых клеток (рис. 3).
Папиллярная карцинома с фиброматозом (фасциитоподобной стромой) отличается обильно развитым стромальным компонентом, настолько выраженным, что опухоль напоминает узловатый фасциит, фиброматоз и другие пролиферативные миофибробластические процессы. Солидно-трабекулярный вариант не является необычным для папиллярной карциномы, демонстрирует солидную и/или трабекулярную картину роста, чаще встречающуюся в опухолях детской возрастной группы. Термин «солидный вариант» должен быть использован, если вся или часть опухоли не относится к другим вариантам, имеющим солидную, трабекулярную или инсулярную картину роста. Солидный вариант составляет всего 1—3% папиллярного рака у взрослых лиц по сравнению с более высокими показателями распространенности среди карцином у детей, особенно подвергшихся действию радиации. Эти опухоли чаще ассоциированы с хромосомными аберрациями, приводящими к перестройкам типа RET/PTC3 в детских и облученных популяциях. Этот вариант должен быть отличим патологоанатомами от низкодифференцированной карциномы, которая имеет аналогичный тип роста, но характер клеток иной (отсутствуют признаки папиллярной карциномы), присутствуют некроз и высокая митотическая активность.
Веретеноклеточный вариант папиллярной карциномы. Изредка папиллярная карцинома демонстрирует наличие очагов веретеноклеточной метаплазии. Эпителиальная природа этих клеток подтверждается иммуноэкспрессией цитокератинов и TTF-1. Веретенообразные клетки не связаны с кровоизлиянием или гемосидерином, и форма зоны опухолевого роста не имеет географически четкой конфигурации, что отличает истинные веретеноклеточные участки папиллярных карцином от реактивных изменений после тонкоигольных биопсий. В отличие от недифференцированного рака при веретеноклеточном варианте клетки выглядят менее злокачественно, отсутствуют некроз и фигуры митоза.
Светлоклеточный вариант — очень необычный, часто сочетается с оксифильно-клеточным. Этот вариант следует дифференцировать от светлоклеточного варианта медуллярной (С-клеточной) карциномы, интратиреоидной локализации гиперпластических процессов околощитовидной железы, метастазов светлоклеточного почечно-клеточного рака. Полезными иммуногистохимическими маркерами дифференциальной диагностики являются TTF-1, хромогранин А, синаптофизин, гормон околощитовидной железы, эпителиальный мембранный антиген, RCC. Уортино-подобный вариант папиллярной карциномы отличается увеличенными в размере клетками с эозинофильной цитоплазмой и выраженной лимфоидной инфильтрацией стромы. Опухоль возникает в ЩЖ с тиреоидитом Хашимото. Строение напоминает одноименную опухоль слюнной железы. Прогноз не отличается от такового при обычном классическом папиллярном раке с аналогичным размером опухоли и стадией опухолевого роста.
Фолликулярная карцинома — это злокачественная опухоль, возникающая из фолликулярного эпителия, в которой отсутствуют признаки изменений ядер опухолевых клеток, характерные для папиллярной карциномы. Опухоль обычно инкапсулирована и имеет признаки инвазивного роста. Онкоцитарные карциномы классифицируются отдельно. Выделены следующие категории фолликулярных карцином: минимально инвазивная; инкапсулированная ангиоинвазивная; и широкоинвазивная, которая имеет аналогичный с фолликулярной карциномой без дополнительного уточнения (БДУ) гистологический код. Непременным признаком фолликулярной карциномы является инвазивный рост. Для минимально инвазивной карциномы характерна лишь капсулярная инвазия. Большинство авторов капсулярной инвазией считают лишь пенетрацию опухоли сквозь всю толщу собственной капсулы. Неровные контуры внутренней границы капсулы, выпячивание структур опухоли в сторону собственной капсулы или наличие опухолевых гнезд среди волокон фиброзной капсулы не могут служить достаточными признаками инвазивного роста. Разрыв капсулы вследствие хирургических манипуляций, предоперационной тонкоигольной биопсии и/или перекручивание края опухоли по периферии гистологического среза не равнозначны инвазивному росту. Минимальная капсулярная инвазия, как правило, имеет грибовидную форму. Для инкапсулированной ангиоинвазивной карциномы должна быть установлена сосудистая инвазия, т. е. бесспорная инвазия с наличием связи опухолевых структур с сосудистой стенкой, присутствием эндотелиальных клеток на периферии опухолевых тромбов в просветах сосудов собственной капсулы или за ее пределами. Наличие свободно расположенных опухолевых клеток в просветах тонкостенных сосудов в толще опухоли не является признаком сосудистой инвазии и злокачественного потенциала. Полагают, что наличие в опухоли менее 4 очагов сосудистой инвазии ассоциировано с лучшим прогнозом по сравнению с опухолями, имеющими более распространенную сосудистую инвазию. Широкоинвазивные карциномы демонстрируют распространенную инвазию в окружающую ткань ЩЖ и экстратиреоидный рост в прилежащие мягкие ткани. Широкоинвазивные карциномы, особенно с солидным и трабекулярным типами роста, по сравнению с инкапсулированными ангиоинвазивными имеют менее благоприятный прогноз. Тем не менее следует отличать этот вариант от низкодифференцированных карцином, равно как от солидно-трабекулярного варианта папиллярной карциномы. В новой классификации фолликулярных карцином выделен светлоклеточный вариант (с наличием более 50% светлых клеток). Появление светлых клеток в опухоли связывают с накоплением в их цитоплазме гликогена, липидов, муцина, тиреоглобулина или с расширением и гипертрофией митохондрий и комплекса Гольджи. К другим вариантам отнесены перстневидно-клеточный вариант, фолликулярная карцинома с гломерулярным типом роста, веретеноклеточный вариант.
Гюртле-клеточные (онкоцитарные) опухоли — опухоли (обычно инкапсулированные) состоят из онкоцитов. Неинвазивные онкоцитарные опухоли классифицируют как Гюртле-клеточные аденомы, а при наличии капсулярной и/или сосудистой инвазии — как Гюртле-клеточные карциномы.
Низкодифференцированная карцинома — фолликулярно-клеточная опухоль, занимающая морфологически и по своим биологическим особенностям промежуточное положение между дифференцированным (фолликулярным и папиллярным) и недифференцированным (анапластическим) раком. Алгоритм диагностики низкодифференцированной карциномы предложен на международном рабочем совещании патологов в Турине, Италия, в 2007 г. Кратко он состоит в том, что злокачественные опухоли ЩЖ из фолликулярного эпителия, имеющие солидное, трабекулярное или инсуляр