Роль допплеровских методов в дифференциальной диагностике опухолей матки и яичников
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
С внедрением в клиническую практику новых неинвазивных методов исследования, в том числе цветового допплеровского картирования (ЦДК), стало возможным более раннее выявление опухолей 6. Этот метод является простым, доступным, высокоинформативным, позволяющим провести эхографическую дифференциальную диагностику опухолей и опухолевидных образований яичников, а также различных видов онкопатологии матки 9.
A. Kurjak [11], Т. Bourne [12] одними из первых сообщили, что при проведении трансвагинальной цветовой допплерографии была обнаружена выраженная разница допплерометрических показателей в доброкачественных и злокачественных новообразованиях. Данные об информативности пороговых значений индексов при проведении дифференциального диагноза доброкачественного и злокачественного новообразования остаются противоречивыми. Одни авторы [5, 10, 11] высоко оценивают их диагностические возможности, не признавая эффективности показателей скорости, другие предлагают все делать наоборот [12]. Большая группа исследователей склоняется к тому, что только комплексное использование анамнестических данных, различных ультразвуковых методов, а также биохимических онкомаркеров и маркеров ангиогенеза приводит к реальному повышению точности диагностики [7-10, 13, 14]. Тем не менее исследование кровотока в сосудах новообразований имеет свои характерные особенности, что позволяет считать метод ЦДК важным в дифференциальной диагностике доброкачественных и злокачественных опухолей [15].
ЦДК позволяет оценить три параметра кровотока одновременно: направление, скорость и характер потока (однородность и турбулентность). Высокая разрешающая способность современных аппаратов дает возможность в режиме энергетического допплера визуализировать кровоток в мельчайших сосудах вплоть до системы микроциркуляторного русла, невидимых при сканировании в В-режиме [4, 8, 9]. Исследование характера васкуляризации опухолей внутренних половых органов допплеровскими методами открывает большую перспективу в их неинвазивной дифференциальной диагностике по степени злокачественности, а также в прогнозировании быстроты роста опухоли [9, 10, 14].
Материалы и методы
Основными клиническими проявлениями заболевания были болевой синдром у 41 (20,5%) женщины, нарушение менструальной функции у 38 (19,0%), нарушение функции соседних органов у 5 (2,5%), и бесплодие у 8 (4%) пациенток.
Результаты исследования
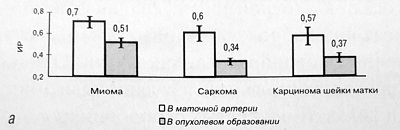
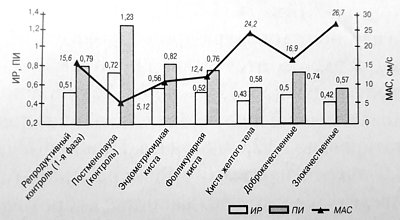
Рис. 1. Значения ИР (а) и МАС, см/с (б), в маточной артерии и внутриопухолевом образовании при миоме, саркоме и карциноме шейки матки.
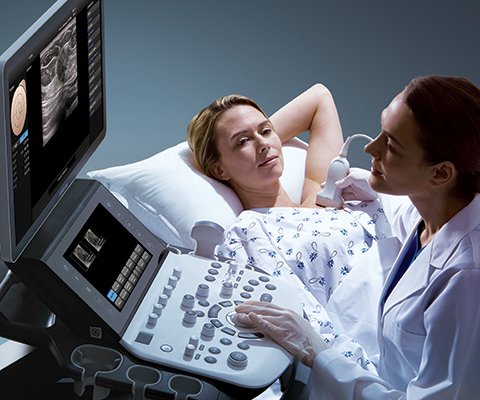
Дифференциальным диагностическим критерием между саркомой и миомой матки в режиме ЦДК является визуализация нерегулярных, тонких, хаотично разбросанных сигналов от сосудов с показателями низкой резистентности как внутри, так и вокруг опухоли. Предлагается использовать пороговое значение ИР внутриопухолевого кровотока, равное 0,4, а максимальная систолическая скорость более 45 см/с.
Как и при саркоме матки у больных с раком шейки матки значения ИР в ветви маточной артерии и внутри опухоли были достоверно ниже (0,57 ± 0,14 и 0,37 ± 0,05 соответственно) как по отношению к контролю, так и к значениям, полученным при миоме матки. Скорость кровотока внутри опухоли недостоверно превышала скорость в маточной артерии (58,8 ± 8,64 против 51,9 ± 7,17 и см/с).
Сравнительная характеристика резистентности и скорости кровотока у больных с доброкачественными и злокачественными новообразованиями на уровне эндометрия представлена на рис. 2а,б. Рак эндометрия является довольно частой патологией и занимает второе место среди всех злокачественных заболеваний женских половых органов [2]. Многочисленные исследования свидетельствуют о том, что основное внимание при диагностике рака эндометрия отводится определению толщины М-эхо [6].
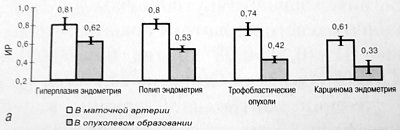
Рис. 2. Значения ИР (а) и МАС, см/с (б), в маточной артерии и внутриопухолевом образовании при гиперплазии, полипе и карциноме эндометрия, а также в трофобластических опухолях.
В менопаузе этот показатель, превышающий 5 мм, рассматривается как ведущий эхографический признак данной патологии, что требует комплексного обследования для уточнения диагноза.
Таким образом, применение допплеровских методов позволяет выявить вполне отчетливую зависимость опухолевого кровотока от клеточной пролиферации и ангиогенеза при доброкачественных и злокачественных новообразованиях матки. Однако требуется дальнейшее изучение зависимости показателей кривых скоростей кровотока от гистологического строения и степени дифференцировки опухолей.
При допплерографической оценке патологических состояний яичников имеют большое значение такие особенности нормального интраовариального кровотока в репродуктивном возрасте, как значительное повышение скорости и снижение резистентности в фазу расцвета желтого тела [8].
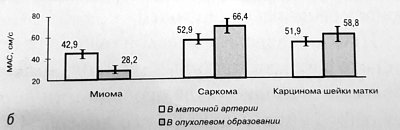
Рис. 3. Допплерометрические показатели (ИР, ПИ, МАС) внутриопухолевого кровотока в опухолевидных образованиях, доброкачественных и злокачественных опухолях яичников.
У женщин с фолликулярными кистами (15 наблюдений) визуализировался достаточно бедный сосудистый рисунок в стенках кисты, напоминающий интраовариальный кровоток в среднюю и позднюю фолликулярную фазу менструального цикла. Полученные значения MAC, ПИ и ИР составили 12,4 ± 3,67 см/с, 0,76 ± 0,07 и 0,52 ± 0,04 соответственно. Надежных эхографических дифференциальнодиагностических критериев между фолликулярными кистами и однокамерными гладкостенными цистаденомами при помощи допплеровских методов получено не было.
Значение допплерографии в дифференциации эндометриоидных кист или кист желтого тела и злокачественных новообразований яичников очевидно.
Эхографически опухоли представляли собой кистозно-солидные образования с множественными перегородками различной толщины и плотным компонентом средней или повышенной эхогенности (папиллярные разрастания по внутренней поверхности опухоли и на ее перегородках). Во всех наблюдениях образования содержали мелкодисперсную взвесь.
Миома матки: возможности лечения и профилактики
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
ММА имени И.М. Сеченова
М иома матки является истинной доброкачественной опухолью матки, которая в свою очередь относится к гормонально зависимым органам. Развивается миома матки из мышечной ткани и в своей структуре содержит миоциты, соединительнотканые компоненты, кровеносные сосуды, перициты, плазматические и тучные клетки.
В зависимости от соотношения паренхимы и стромы эта опухоль ранее имела различные названия: миома, фиброма, фибромиома. Однако принимая во внимание, что узлы миомы чаще развиваются именно из мышечной клетки, т.е. имеет моноклональное происхождение, большинство авторов считают более правильным термин – лейомиома (миома).
Миома матки имеет свои характерные особенности:
– Это самая распространенная опухоль матки у женщин позднего репродуктивного (35–45 лет) и пременопаузального (46–55 лет) возраста.
– Способна к росту, регрессии и даже полному исчезновению в менопаузу. Однако у 10–15% больных в первые 10 лет постменопаузального периода миома матки может увеличиваться, сочетаясь с гиперпластическими процессами эндометрия, пролиферативными заболеваниями яичников.
– Миома матки небольших размеров (до 10 недель беременности) может долго сохранять стабильное состояние, но при воздействии провоцирующих факторов (воспалительный процесс матки и придатков, выскабливание матки, длительное венозное полнокровие органов малого таза) увеличивается быстро и очень быстро (так называемый «скачок роста»).
– Характерно многообразие клинических вариантов (малосимптомная, симптомная), зависящих от локализации (подбрюшинная, межмышечная, подслизистая и промежуточные варианты), размеров (небольшие, средние, большие), расположения (дно, тело, перешеек, шейка матки) и характера роста (истинный, ложный).
– По морфологическим особенностям миома матки может быть простая (преобладание соединительнотканного компонента) и пролиферирующая (клеточная, отличающаяся опухолевой прогрессией).
– В зависимости от клетки–родоначальницы миома матки может быть сосудистой, эпителиоидной, аденоматозной, интравенозной. Наблюдается большое морфологическое разнообразие миоматозных узлов, что объясняется ее мезенхимальным происхождением (из полового бугорка), а также из целомического эпителия Мюллерова протока. Из этих клеток дифференцируются миобласты, клетки стромы, перициты, фибробласты, тучные и плазматические клетки.
– В большинстве клинических наблюдений в миометрии вокруг тонкостенного венозного сосуда сразу закладываются несколько зачатков роста, но дальнейший рост и развитие в микроскопический и макроскопический узел происходят с разной скоростью и не всегда в одно и то же время.
– Миома матки имеет автономный рост (аутокринный и паракринный), обусловленный воздействием ростовых факторов и образованием гормонально чувствительных и ростовых рецепторов.
– Как у всякой опухоли, процесс роста и развития миомы матки сопровождается образованием новых сосудов (неоангиогенез), но сосуды миомы отличаются от нормальных, т.к. имеют синусоидный характер с низкорезистентным кровотоком.
– Для пролиферирующих быстро растущих миом характерна повышенная клеточность, крупное гиперхромное ядро, содержащее повышенное количество ДНК.
– Хотя митотическая активность миом матки, как правило, низкая, клетки миомы экспрессируют онкобелки пролиферации (Ki–67) и онкобелки, снижающие процесс апоптоза (bcl–2, bax).
Развитие опухоли от «зачатка роста» и микроскопического узелка без признаков клеточной дифференцировки до макроскопического узла, определяемого при бимануальном исследовании или с помощью УЗИ, занимает в среднем 5 лет.
Начало возникновения узлов миомы матки приходится на 30 лет, когда у женщин накапливаются соматические, гинекологические заболевания и нейроэндокринные нарушения. Суммирование патологических факторов в этом возрасте вызывает соматическую мутацию клеток в органах репродуктивной системы, что, вероятно, играет ведущую роль на стадии формирования пролиферативного компонента при процессах регенерации поврежденных клеток миометрия.
Для последующего роста узлов опухоли требуется дальнейшее накопление неблагоприятных факторов, вызывающих опухолевую прогрессию:
На возраст 44–45 лет приходится самая высокая частота оперативных вмешательств (чаще всего это удаление матки), показанием к которым является быстрый рост миомы матки, ее большие размеры, сочетание миомы матки с патологией эндометрия (гиперплазия, атипическая гиперплазия) и яичников (доброкачественные и злокачественные опухоли).
Таким образом, рост опухоли усиливается в возрасте 35–45 лет, когда снижается функциональная активность яичников и их чувствительность к гонадотропной стимуляции, синхронно возрастает продукция гонадотропных гормонов, возникает хроническое функциональное напряжение систем регуляции (нейроэндокринной, гормональной, иммунной) и чаще всего нарушается гемостаз и гомеостаз.
Фоном для усиленного роста миоматозных узлов в пременопаузальном возрасте является не постепенный, достаточно медленный переход к окончанию гормональной функции яичников, а скачкообразный, слишком быстрый и ранний климакс или чрезмерно замедленный переход к менопаузе (поздняя менопауза – 53–55 лет). Отрицательную роль играют длительно существующие нейроэндокринные нарушения, патологический климакс, действие факторов, стимулирующих гиперпластические и пролиферативные процессы в организме (ожирение, нарушение углеводного и липидного обмена, эндометриоз, аденомиоз).
Лечение миомы матки
Лечение миомы матки – очень непростая проблема, т.к. несмотря на гормональную зависимость, эта опухоль весьма гетерогенна.
Первоначально следует выявить безусловные показания к хирургическому лечению:
Объем хирургического вмешательства во многом определяется возрастом пациентки.
До 40 лет при наличии показаний к хирургическому лечению, если позволяют технические возможности, производят консервативную миомэктомию. Особенно целесообразно удалять макроскопические миоматозные узлы средних размеров (в диаметре от 2 до 5 см), пока не произошло их интенсивное увеличение в размерах. Предпочтительной методикой является лапароскопическая. При решении вопроса о консервативной миомэктомии необходимо принимать во внимание морфотип опухоли. При пролиферирующей миоме можно удалить несколько узлов, но дальнейший рост продолжают множество других зачатков роста. Поэтому рецидивы при консервативной миомэктомии при миоме матки имеют место в 15–37% случаев.
После 40 лет и постменопаузальном возрасте при наличии хирургических показаний необходима операция удаления миоматозной матки, т.к. если миома не регрессировала в первые 2 года постменопаузы, дальнейшее ее существование сопровождается опасностью возникновения онкопатологии (аденокарцинома, саркома). Известный отечественный онколог Я.В. Бохман (1987 г.) считал, что «нерегрессирующая миома матки в постменопаузальном периоде является маркером онкопатологии органов репродуктивной системы».
По нашим данным, факторами риска роста миомы матки являются: наличие кист и кистом яичников, гиперплазия тека–клеток, пролиферативные процессы эндометрия, несвоевременное прекращение гормональной активности яичников (запоздалая менопауза) и чрезмерная ароматизация андростендиона в жировой клетчатке за счет выраженного ожирения, нарушения углеводного обмена или заболевания печени.
Консервативное лечение, проводимое в репродуктивном возрасте, сразу после выявления миоматозных узлов небольших и средних размеров, позволяет в ряде случаев затормозить дальнейший рост опухоли, предупредить операции по удалению матки, сохранить возможность родить ребенка.
Показания к консервативному лечению:
Лечение заключается в нормализации системных нарушений, характерных для больных с миомой матки: хроническая анемия, воспалительные процессы матки и придатков, нарушение кровенаполнения органов малого таза с преобладанием венозного застоя и снижением артериального кровоснабжения, нарушение функционального состояния нервной системы и вегетативного равновесия. К методам коррекции системных нарушений относятся следующие:
Если наступила беременность, даже не запланированная, необходимо ее сохранение, т.к. послеродовая инволюция матки, грудное вскармливание ребенка не менее 4–6 месяцев способствуют изменению гистогенеза миомы, переходу ее из пролиферирующей в простую и в ряде случаев прекращению ее дальнейшего развития.
Для профилактики неизбежного удаления матки при росте опухоли большое значение имеет сохранение и поддержание репродуктивной функции до 40 лет.
Эффективность гормональной терапии весьма различается в зависимости от характера гормональных нарушений, наличия и плотности рецепторов в миоматозных узлах и миометрии. Последние преобладают в недлительно существующих миомах небольших размеров, состоящих преимущественно из гладкомышечного клеточного компонента. В фибромах, где превалирует стромальный компонент, а также в узлах больших размеров гормональные рецепторы, как правило, отсутствуют. Поэтому гормональная терапия у этих пациенток мало эффективна.
Тем не менее она используется при коррекции нарушенного менструального цикла. С этой целью применяют прогестерон и его производные (дидрогестерон, ципротерон ацетат), а также производные андрогенов, 19–норстероиды (левоноргестрел, норэтистерон ацетат). Последние нежелательны в молодом возрасте, при ожирении, сахарном диабете, сердечно–сосудистых заболеваниях.
Наиболее перспективными препаратами в лечении больных с миомой матки являются антигонадотропины (гестринон, даназол), которые обладают антиэстрогенным и антипрогестероновым эффектом, вызывая временную аменорею, а также агонисты гонадотропин–рилизинг гормона (трипторелин, гозерелин, бузерелин), вызывающие состояние обратимого гипогонадизма.
Агонисты гонадотропин–рилизинг гормона
Синтетические аналоги гонадотропин–рилизинг гормона (а–ГнРГ) широко применяются в гинекологической практике, являясь эффективными средствами медикаментозного лечения эндометриоза, миомы матки, меноррагии, гиперандрогении яичникового генеза, бесплодия. В основе их терапевтического действия лежит эффект десенситизации гипофиза с последующей блокадой секреции гонадотропинов и, соответственно, половых стероидов. Эта блокада является обратимой и после отмены а–ГнРГ чувствительность аденогипофиза к гипоталамической стимуляции полностью восстанавливается.
На фоне лечения а–ГнРГ отмечается уменьшение клеточности и гипоплазия клеток миомы, узлы отграничиваются от окружающих тканей, возрастает степень их гиалинизации и коллагенизации, утолщаются стенки сосудов. На ультраструктурном уровне отмечается повреждение клеток с разрывом клеточной мембраны, сморщивание цитоплазмы и интенсивная лимфоцитарная инфильтрация, т.е. некроз клеток в сочетании с повышенным апоптозом, а главное, угнетением пролиферативной активности в миоме.
Снижение циркулирующего в крови эстрадиола способствует повышению сосудистого сопротивления в маточных артериях и в артериях, питающих миоматозный узел, что приводит к редуцированию маточного кровотока и сопровождается уменьшением размеров узла.
Высказано предположение о прямом влиянии а–ГнРГ на опухоль (в ткани миомы выявлены рецепторы ГнРГ). Еще один механизм действия а–ГнРГ может быть связан с их влиянием на факторы локальной регуляции. Доказано, что на фоне их приема достоверно снижается концентрация ЭФР, влиящего на процесс редукции опухоли на уровне миомы или миометрия.
Различные типы а–ГнРГ отличаются друг от друга по биологической активности, времени полураспада, форме выпуска и срокам обратимости эффекта, что не имеет клинического значения.
В России зарегистрированы следующие препараты а–ГнРГ:
1. Депо–гозерелин 3,6 мг п/к; трипторелин 3,75 мг в/м и п/к; лейпрорелин 3,75 мг в/м Препарат представляет собой готовый набор с различными способами введения. Лечение начинают со 2–4 дня менструального цикла: 1 инъекция каждые 28 дней.
2. Эндоназальный спрей – 0,2% раствор бузерелина ацетата 0,9 мг в сутки. Лечение начинают с 1-2 дня менструального цикла: 0,15 мг в каждый нососвой ход 3 раза в день через равные промежуькт времени.
Подготовка к оперативному вмешательству с помощью а–ГнРГ при наличии миомы матки позволяет проводить щадящие органосохраняющие операции с использованием эндоскопической техники. Терапия а–ГнРГ способствует уменьшению размеров миоматозных узлов и связанных с ними симптомов и тем самым позволяет сократить время операции и уменьшить объем кровопотери. После лечения а–ГнРГ возможно наступление беременности.
К настоящему времени описано несколько стратегий длительной терапии а–ГнРГ, позволяющих избежать выраженных побочных явлений при сохранении высокой клинической эффективности:
Вариабельность ответа отдельных миоматозных узлов на лечение связана со степенью гиалинизации и дегенеративных изменений в опухоли, потерей чувствительности к антиэстрогенным воздействиям; первоначальным объемом матки. Вероятный ответ на лечение может быть предсказан в большинстве случаев через 4 недели после первой инъекции.
Препараты хорошо переносятся, не обладают антигенными свойствами, не кумулируют, не влияют на липидный спектр крови. Побочные эффекты: приливы, потливость, сухость во влагалище, головная боль, депрессия, нервозность, изменение либидо, себорея, периферические отеки, ухудшение проспективной памяти, снижение плотности костной ткани.
Прекращение терапии ведет к восстановлению нормального менструального цикла и эстрогенного статуса приблизительно через 59–94 дня после отмены препарата и быстрому повторному росту миомы матки до первоначальных размеров (в течение первых 3–4 менструальных циклов) со всеми клиническими симптомами (хотя некоторые авторы отмечают, что эти симптомы менее выражены).
Даназол назначают по 100–200 мг 1 раз в день (через 30 мин после ужина) в течение 3,5–5 месяцев с использованием методик, позволяющих контролировать их влияние на организм и регрессию миоматозных узлов. Каких–либо побочных эффектов при использовании низкодозированных препаратов мы не наблюдали. У ряда больных не наступает аменорея, а имеет место гипоменструальный синдром. В процессе лечения наблюдается уменьшение размеров матки на 50–60%.
Далее необходимо продолжить общеукрепляющую терапию для нормализации нарушений системы регуляции. На фоне восстановления менструального цикла рекомендуется наступление беременности. Наш опыт свидетельствует о наилучшем эффекте в лечении миомы матки препаратом даназол в низкой дозировке. Морфологическое исследование удаленных после лечения узлов показывает низкую митотическую активность, снижение клеточности и повышение содержания компонентов экстрацеллюлярного матрикса, т.е., по сути, возможность перехода пролиферирующей миомы в простую. Последующая лапароскопическая консервативная миомэктомия дает наименьший процент рецидивов (из 49 наблюдаемых нами пациенток дальнейший рост через 2 года отмечен только у 2 женщин).
Профилактика миомы матки
Возможна ли профилактика миомы матки? По–видимому, возможна. Кроме общих рекомендаций по соблюдению рационального режима жизни, предупреждению распространенных болезней в детском и взрослом возрасте, играют роль исключение абортов, своевременная коррекция гормональных нарушений, адекватное лечение гинекологических заболеваний. Существует и специфическая профилактика. Это своевременная реализация репродуктивной функции. Первые роды рекомендуются в 22 года, вторые в 25 лет, последующие планируемые роды до 35 лет. Поздние первые роды приводят к преждевременному постарению миоцитов, снижению адаптационной способности к растяжению и сокращению. Аборты и воспаления повреждают структуру миометрия. На фоне нарушенного гомеостаза процесс регенерации участков миометрия переходит в пролиферативную опухолевую прогрессию.
Следует принимать во внимание, что самый частый срок обнаружения миомы матки приходится на 30–35 лет, когда суммируются действия повреждающих факторов.
Необходимо сохранять первую беременность, особенно у молодых женщин с так называемой наследственной миомой. Аборт вызывает рост миоматозных узлов и из микроскопических узлов интенсивно формируются растущие миомы. Следует избегать чрезмерного ультрафиолетового облучения, повышенных температурных воздействий, особенно после 30 лет. При наличии наследственного риска (миома матки у матери и близких родственниц) опухоль развивается на 5–10 лет раньше, т.е. в 20–25 лет. Продолжение грудного вскармливания в течение 4–6 месяцев после родов нормализует содержание пролактина, который влияет на изменение гистогенеза миомы.
В заключение необходимо подчеркнуть, что миома матки является результатом соматической мутации клеток миометрия вследствие многочисленных повреждающих факторов. Поэтому в основе профилактики должны превалировать здоровый образ жизни и сохранение репродуктивного здоровья женщин.
Миома матки
Миома матки — заболевание, которым, по данным Минздрава РФ, страдает примерно треть женщин. При этой патологии в стенке органа образуются узлы из гладкомышечной ткани. В миомах нет злокачественных клеток, они не опасны для жизни, но могут вызывать некоторые симптомы, проблемы с беременностью.
«УЗИ показало, что у вас в матке миома», — часто эти слова заставляют женщин сильно переживать. На самом деле всё не так страшно.
Причины возникновения миомы матки
Раньше считалось, что миома матки — доброкачественная опухоль, которая растет из-за дисбаланса между женскими половыми гормонами — эстрогенами и прогестероном. Современной науке известно, что это не так. Ученые и врачи вынуждены признать: на данный момент нельзя назвать точные причины развития миом матки. Существуют две теории:
Эмбриональная теория утверждает, что нарушения возникают еще до того, как девочка появляется на свет. Дело в том, что гладкомышечные клетки в стенке матки плода созревают относительно поздно — к 38 неделе беременности. В кишечнике и мочевом пузыре эти процессы завершаются уже к 16 неделе. Из-за позднего созревания гладкомышечная ткань матки дольше остается в нестабильном состоянии, поэтому в ней выше риск нарушений, приводящих к миоме.
Травматическая теория гласит, что повреждение миометрия происходит уже в течение жизни. К нему могут привести многократные месячные, перенесенные выскабливания и аборты, воспалительные заболевания, неаккуратные действия акушеров во время родов.
Миома матки развивается не из-за гормонов, но они влияют на её рост. Миоматозные узлы практически никогда не возникают у девочек до первых месячных и уменьшаются после менопаузы.
Риск развития миомы матки повышают некоторые факторы:
Миомы чаще возникают у женщин, которые никогда не рожали. Риски снижаются в зависимости от количества беременностей и родов.
Виды миомы матки
Стенка матки похожа на бутерброд, «начинкой» которого как раз и является мышечный слой. Внутри полость органа выстилает слизистая оболочка (эндометрий), снаружи его покрывает серозная оболочка (периметрий). Миоматозные узлы могут расти внутрь или наружу, в зависимости от этого их делят на три вида:
Субсерозные миомы растут на наружной поверхности органа, на широком основании (как холмик) или на ножке (как гриб). Они чаще всего не вызывают симптомов.
Субмукозные миомы выступают в полость органа. Они самые проблемные, так как из-за них чаще всего возникают кровотечения и проблемы с беременностью. Субмукозные миомы делят на три типа:
Интрамуральные миомы расположены внутри мышечного слоя, могут больше расти в сторону полости матки, наружу, или находиться посередине.
Отдельно выделяют миому шейки матки.
Симптомы миомы матки
Большинство женщин не испытывают симптомов и даже не догадываются о том, что у них есть миома матки. Нередко диагноз устанавливают случайно, во время УЗИ по другому поводу. Бывают ситуации, когда у женщины проводят анализ крови, обнаруживают анемию (сниженный уровень гемоглобина), и дальнейшее обследование показывает, что причина — обильные месячные из-за миомы матки.
Чаще всего встречаются три симптома:
Боли в низу живота, в ногах и пояснице, болезненность во время половых актов и другие симптомы встречаются реже и обычно вызваны другими сопутствующими заболеваниями.
Миома матки — НЕ злокачественная опухоль. Но онкологические заболевания могут проявляться схожими симптомами, поэтому нужно посетить гинеколога и пройти обследование.
Чем опасна миома матки?
На этот счет существует немало мифов. В них продолжают верить даже некоторые гинекологи, хотя уже давно проведены серьезные научные исследования, и расставлены все точки над i.
Главное заблуждение — «со временем миома обязательно превратится в рак». И отсюда следует вывод — «страшную опухоль нужно как можно быстрее удалить». На самом деле миома матки не имеет никакого отношения к онкологическим заболеваниям. Злокачественные опухоли миометрия называются лейомиосаркомами. Причины их возникновения неизвестны, и нет никаких доказательств того, что это может произойти из-за миомы матки.
Миоматозные узлы перерождаются в злокачественные опухоли не чаще, чем нормальный миометрий.
Второй распространенный миф гласит, что женщина с миомой матки не сможет забеременеть. На самом деле это далеко не всегда так. И даже если миома становится причиной бесплодия или невынашивания, в большинстве случаев это можно исправить с помощью лечения.
Некоторые гинекологи «старой школы» запугивают женщин, говорят, что им теперь нельзя посещать бани, солярии, отдыхать в теплых странах, заниматься в спортзале, делать массаж и физиопроцедуры, заниматься сексом. Доказано, что это не так. Женщина с миомой матки может вести полноценную, активную жизнь, если нет сильных кровотечений.
Ни один из этих факторов не приведет к тому, что узлы начнут быстро расти. Вообще, рост миом матки — вещь непредсказуемая. В каждом конкретном случае нельзя сказать, как поведет себя заболевание в динамике, какого бы образа жизни ни придерживалась женщина, и какие бы ограничения она ни соблюдала. Поэтому важно регулярно проходить УЗИ и контролировать состояние узлов.
Например, в одном исследовании за женщинами с миомами матки наблюдали в течение года. Результаты оказались очень разными. У одних узлы за это время уменьшились на 25%, у других увеличились на 138%.
Чем же на самом деле опасна миома матки? У некоторых женщин развиваются осложнения:
Чем лечат миому матки современные гинекологи?
В современной гинекологии изменилось не только понимание механизма развития миомы матки, но и подходы к ее лечению. Применяются разные методы, каждый из них имеет свои преимущества и показания. В первую очередь нужно разобраться, нуждается ли женщина в лечении. Если миомы матки небольшие, не растут и не вызывают симптомов, достаточно наблюдения в динамике.
Итак, лечить женщину с миомой матки нужно, если:
Хирургическое лечение
Так как раньше миому матки считали опухолью (пусть и доброкачественной), то и боролись с ней радикально. Зачастую врачи сразу предлагали женщинам удалить матку. «Не планируете больше беременеть? Тогда зачем вам этот мешок с узлами?». Раньше услышать такое от врачей можно было часто. А если так говорит современный гинеколог — от него лучше держаться подальше. Операция хирургического удаления матки (гистерэктомия) — крайняя мера, она допустима, когда по-другому уже совсем нельзя.
Матка нужна не только для вынашивания потомства. Этот орган выполняет в женском организме и другие важные функции. После удаления матки развивается постгистерэктомический синдром, он грозит серьезными осложнениями.
Другой вариант хирургического вмешательства — миомэктомия. Во время операции хирург удаляет только миому, матка остается на месте, и женщина может в будущем забеременеть. Провести хирургическое вмешательство можно разными способами: через разрез, прокол (лапароскопически), с помощью роботизированных установок, без разреза через влагалище.
Последствия удаления миомы матки и беременность
После миомэктомии симптомы миомы матки исчезают, женщина может забеременеть и родить ребенка. Но главный минус хирургического лечения — высокий риск рецидива. Через 4–5 лет примерно у половины прооперированных женщин миомы будут обнаружены снова. Поэтому операция показана в случаях, когда женщина планирует беременность в ближайшее время, а не когда-то потом.
Другие условия, при которых может быть выполнено удаление миомы:
Впрочем, даже один рубец способен создать проблемы во время беременности и стать показанием к кесареву сечению. Другое возможное осложнение — спайки, из-за которых может развиться бесплодие. Не говоря уже о том, что любое хирургическое вмешательство сопряжено с определенными рисками. В последние годы список показаний к миомэктомии сильно сократился, потому что появились новые, малоинвазивные методики.
Современный метод лечения миомы матки — ЭМА
Процедура под названием эмболизация маточных артерий — сокращенно ЭМА — существует уже несколько десятилетий, но широко применять ее для лечения миом матки стали относительно недавно. Из-за этого к ней относятся с недоверием даже некоторые врачи-гинекологи. Но научные исследования убедительно доказали, что это эффективный и безопасный метод, и он подходит для большинства женщин с миомами матки, которым показано лечение.
Суть процедуры в том, что под контролем рентгена в сосуд, питающий миому матки, вводят катетер, а через него — специальный эмболизирующий препарат. Этот препарат состоит из микроскопических частиц, которые закупоривают просвет мелких сосудов. Миоматозный узел перестает получать кислород и питательные вещества, погибает и замещается соединительной тканью. Если миома находится внутри полости органа на ножке, она отделяется и выходит наружу.
Эмболизация маточных артерий имеет некоторые преимущества перед хирургическими методами лечения миомы:
А самое главное — это результат. Исследования показывают, что 98% женщин после ЭМА не нуждаются в каких-либо дополнительных видах лечения. В то же время, после миомэктомии из-за высокой вероятности рецидива миомы женщинам назначают гормональные препараты.
Риск рецидива после ЭМА составляет менее 1%. Если миоматозный узел снова будет обнаружен, процедуру можно провести повторно.
Эмболизация маточных артерий — предпочтительный метод лечения миомы, если женщина планирует беременность в отдаленной перспективе, если в матке обнаружено много узлов.
Почему же гинекологи не всегда рассказывают женщинам об этом виде лечения? Во-первых, некоторые врачи сами плохо осведомлены о процедуре ЭМА при миоме. Они действуют по принципу «а вдруг это еще недостаточно изучено и опасно». Хотя, как мы уже говорили, для таких мыслей нет никаких оснований: эффективность и безопасность ЭМА доказаны в серьезных клинических исследованиях.
Во-вторых, не все врачи владеют техникой ЭМА, и не во всех клиниках есть оборудование для ее проведения. Гинекологи работают по старинке и неохотно направляют «своих» пациентов к другим специалистам.
Что же делать женщине, у которой диагностировали миому матки? Стать хорошо информированной пациенткой. В интернете можно найти массу информации об эмболизации маточных артерий. Если в вашем городе нет специалиста, который практикует этот вид лечения, можно приехать в Европейскую клинику или получить консультацию нашего врача удаленно — для этого отправьте результаты проведенных исследований на нашу электронную почту.
Помогают ли лекарственные препараты?
Медикаментозное лечение миомы матки возможно, но показания к его применению ограничены. Целесообразно применять только один препарат — улипристал ацетат. Он блокирует рецепторы гормона прогестерона и останавливает рост миомы. Узлы уменьшаются в 60% случаев. Рекомендуется проводить два или три цикла лечения с интервалами 2 месяца, при этом регулярно выполнять УЗИ и контролировать рост узлов.
Такая терапия показана только молодым женщинам с миомами матки до 3 см. Ее недостаток в том, что она оказывает только временный эффект. Невозможно предсказать, когда после курса лечения снова начнется рост миом.
Есть ли эффективные меры профилактики миомы матки?
Так как точные причины заболевания неизвестны, то и эффективных методов профилактики не существует.
Риски снижаются у женщин, у которых есть несколько детей. Но, конечно же, защита от миомы матки — далеко не первая в списке причин, по которым женщины планируют беременность, и это не определяющий фактор.
Самая важна мера — это регулярные посещения гинеколога и УЗИ. Они помогают вовремя диагностировать миому матки, оценить ее размеры в динамике и узнать, когда требуется лечение.
В Европейской клинике работает гинеколог Дмитрий Михайлович Лубнин — первый врач в России, защитивший диссертацию, посвященную применению эмболизации маточных артерий для лечения миомы матки. Наш доктор уже много лет практикует ЭМА и хорошо знает все тонкости процедуры, ведения женщин после неё. Запишитесь на консультацию к Дмитрию Михайловичу в Европейской клинике.