Современные препараты инсулина
Поделиться:
Как это работает?
Инсулин — гормон, который вырабатывают бета-клетки поджелудочной железы. Он необходим клеткам организма, чтобы они могли вывести глюкозу из крови и использовать ее для собственных «нужд».
При сахарном диабете 1-го типа поджелудочная железа не может вырабатывать достаточное количество инсулина, и единственная возможность компенсировать опасный дефицит — введение гормона извне в составе инсулинотерапии. При диабете 2-го типа инсулин вырабатывается в достаточном количестве, но клетки организма не реагируют на него нормально — снижается чувствительность тканей к инсулину. Чтобы ее повысить, вводят пероральные гипогликемические препараты, однако в некоторых случаях, например когда невозможно добиться компенсации диабета с помощью одних таблеток, все же назначают инсулин.
Читайте также:
Метформин при диабете
Эндогенный (т. е. поступивший в организм в составе препаратов) инсулин работает так же, как и собственный гормон, увеличивая поглощение глюкозы клетками и уменьшая ее концентрацию в крови. Таким образом препараты инсулина нормализуют углеводный обмен, предотвращают или уменьшают осложнения диабета, такие как поражение сосудов, сердца, глаз, почек и нервов.
Какими бывают препараты инсулина?
Инсулины классифицируются по двум параметрам — способу получения и длительности действия. В соответствии с первой классификацией выделяют инсулины, полученные из поджелудочных желез животных, а также человеческие инсулины, синтезированные способами генной инженерии. Последние считаются препаратами выбора, поскольку лучше переносятся организмом.
Основной критерий, по которому разделяют препараты инсулина, — длительность действия. В зависимости от нее выделяют пять основных групп (см. табл.).
Инсулины
короткого
действия
Инсулины
ультракороткого действия
Инсулин лизпро
Инсулин аспарт
Инсулин глулизин
Инсулины
комбинированного действия
(двухфазные)
Инсулин двухфазный человеческий
полусинтетический
Инсулин двухфазный человеческий
генно-инженерный
Инсулин аспарт двухфазный
Инсулины средней
длительности действия
Инсулин-изофан
Инсулин-цинк суспензия
Инсулины
длительного действия
Инсулин гларгин
Инсулин детемир
Инсулины
пролонгированного
действия
Препараты средней продолжительности действия и длительного действия
За одну единицу действия (или международную единицу) инсулина принимают активность 0,04082 мг кристаллического гормона. Для сравнения — наша поджелудочная железа в норме содержит до 8 мг инсулина, что составляет около 200 ЕД.
Как подбирают инсулин?
Как правило, больному диабетом назначают несколько препаратов инсулина различной длительности действия. Схему лечения подбирают индивидуально, основываясь на состоянии углеводного обмена и ответе конкретного пациента. Чаще всего препараты инсулина применяют в трех разных режимах:
Как вводят инсулин?
Препараты инсулина обычно вводят подкожно, хотя допускается и внутримышечное введение. Инсулины короткого действия в форме растворов (не суспензий!) при диабетической прекоме и коме вводят внутривенно.
Быстрее всего инсулин проникает в кровь при введении в подкожную клетчатку передней брюшной стенки, медленнее из области плеча и передней поверхности бедра. Хуже всего всасывается инсулин, введенный в подлопаточную область или ягодицу.
Современные препараты инсулина выпускаются в форме одноразовых шприц-ручек, позволяющих легко и быстро вводить препарат подкожно. Иногда используются инсулиновые помпы, которые прикрепляются к пациенту и постоянно подают инсулин в кровь через иглу в определенной дозировке, однако такие приспособления для среднестатистического больного пока в диковинку, и самым привычным способом введения остается подкожная инъекция инсулина.
Напоследок отметим, что прогресс не стоит на месте, и сегодня ученые вплотную подобрались к созданию самой удобной формы инсулина — пероральной, в виде таблеток. Но пока работы еще не завершены, и больные диабетом продолжают использовать привычный инсулин в форме инъекционного раствора для подкожного введения.
УЗ «Могилевская городская больница скорой медицинской помощи»
Тема 12. Подбор дозы базального инсулина
Врач может назначить Вам одну или две инъекции продленного инсулина в сутки (утром и вечером).
Сколько инъекций (1 или 2) будет назначено, зависит от времени действия конкретного препарата инсулина (действует он сутки или меньше) и от инсулина, который вводится на еду.
Часто днем фон обеспечивается за счет «хвостов» пищевого инсулина, а длинный инсулин вводится только на ночь.
При схеме, при которой дневной фон поддерживается за счет пищевого инсулина, следует помнить, что если Вы будете пропускать прием пищи и не вводить короткий инсулин, то Вам днем не хватит фонового инсулина.
Потребность в базальном инсулине может меняться в течение суток. Но в целом, правильно подобранная доза базального инсулина в обычном режиме (без острых заболеваний и пр.) меняется редко. Не надо без причины каждый день изменять дозу базального инсулина. Регулировать колебания глюкозы крови в результате приема пищи надо коротким инсулином.
Доза базального инсулина адекватна, если глюкоза крови в пределах целевого уровня утром натощак, ночью и в период пропусков пищи.
Базальный ночной инсулин должен «держать» тот уровень глюкозы, который был перед сном. Т.е. если доза базального инсулина подобрана правильно, то с каким сахаром Вы легли спать, с таким и должны встать.
Какие существуют требования к базальным инсулинам?
Основное требование – отсутствие пика действия. Инсулин должен действовать максимально ровно. Иначе на пике действия возможны гипогликемии. Все генно-инженерные базальные инсулины (протамин, хумулин Н, базал, генсулин Н, протафан и др.) являются пиковыми (имеют пик действия) и это их существенный недостаток. Профиль действия этих инсулинов такой: начало — через 1-2 часа с момента подкожного введения; «пик» — 5-8 часов; общая продолжительность действия — 16-18 часов (изначально была заявлена 24 часа).
Аналоги сверхдлительного действия (лантус, гларгин, левемир, туджео, тресиба) являются беспиковыми инсулинами (инсулины «плоского» действия) и это их огромное преимущество.
Как правильно подобрать фоновый инсулин?
При диабете 2 типа часто инсулинотерапия начинается с инъекции инсулина на ночь («подколка»). При диабете 1 типа базальный инсулин также часто вводится 1 раз вечером.
Оценивать дозу вечернего базального инсулина необходимо по уровню глюкозы крови ночью и утром.
Ночью и утром уровень глюкозы крови находится в пределах целевого уровня, значит, доза инсулина подобрана правильно.
Часто на практике увеличение дозы ночного базального инсулина осуществляется по уровню глюкозы натощак. Если глюкоза крови утром выше целевых значений, просто увеличивается доза ночного инсулина. Это не совсем верный подход. Необходимо сначала разобраться, почему утром высокий уровень глюкозы.
Утренняя гипергликемия – одна из самых сложных проблем в лечении сахарного диабета.
Причиной высокого уровня гликемии утром могут быть:
В этом перечне не перечислены такие технические причины, как неисправность шприц-ручки, загиб канюли, испорченный инсулин, введение в места липодистрофий и др.
Чтобы проверить дозу базального ночного инсулина, надо правильно поужинать. Ужин должен быть не позднее, чем за 4 часа до сна. Также ужин должен быть необильным и «легким». При проверке базы на ужин нельзя есть макароны, гречку, перловку, сложные продукты (пельмени, блины, плов и пр.), творог и продукты из него (сырники, запеканка и др.), жирные продукты. Можно: пшенную кашу, геркулес, отварную картошку, отварные и свежие овощи, отварное мясо, отварная рыба, хлеб. Смысл раннего ужина: если поужинать поздно и соответственно поздно ввести короткий инсулин, то действие короткого инсулина наслоится на действие базального инсулина и нельзя будет правильно оценить дозу базального инсулина. Смысл «легкого» ужина: продукты должны усвоиться организмом до того, как человек ляжет спать, т.е. еда должна быть «быстрой». Если поужинать «медленной» едой, она «вылезет» ночью и всю ночь будет повышать уровень глюкозы крови.
Следующий момент – замеры глюкозы. Если нет мониторинга, замеры надо делать как минимум 5 раз: перед сном; в 00.00; в 03.00; в 06.00 и перед завтраком. Для этого заводится будильник (или спящему пациенту измеряет другой человек). Еще лучше измерять каждые 2 часа. Желательно (многие считают, что обязательно) такую проверку проводить не одну ночь, а три ночи, что исключить случайные колебания. Если четко вырисовывается проблемный участок, на нем надо провести замеры каждый час.
Какие возможны варианты
1) Глюкоза ночью и утром в пределах целевого уровня – оптимальная доза базального инсулина.
На мониторинге мы видим, что глюкоза крови с 01.00 непрерывно растет, значит надо увеличивать дозу базального инсулина. Но, если на ужин ели «тяжелую» пищу (пельмени, макароны, много мяса и др.), то это может «вылезать» еда!
Что можно сделать в таком случае:
а) сместить время инъекции на более позднее время;
б) попробовать увеличить дозу инсулина – если нет тенденции к низкому уровню глюкозы;
в) вводить инсулин в более «медленное» место (ногу);
г) заменить инсулин на аналог.
4) Низкий уровень глюкозы ночью, а утром высокий. Такая ситуация говорит об избытке базального инсулина.
В такой ситуации мы видим, что ночью глюкоза находится в целевом диапазоне, но с 4-5 утра начинается резкий рост. Борьба с «зарей» непроста. Если человек на помпе, на это время выставляется большая доза введения инсулина. Если нет, «зарю» надо «скалывать» коротким инсулином. И часто «скалывать» надо на предупреждение (т.е. путем мониторинга или частых замеров четко определяется, в какое время начинается заря, и короткий инсулин вводится до этого времени, т.к. когда «заря» развернулась, «сколоть» ее непросто).
6) Рост уровня глюкозы после пробуждения («стресс пробуждения», феномен «ноги на пол»).
Ситуация похожа с «утренней зарей», но возникает после того как человек проснулся. Т.е. человек проснулся с нормальным уровнем глюкозы крови, получает базальный инсулин суточного действия, не завтракает и не вводит инсулин короткого действия. Казалось бы, глюкоза крови не должна расти (еды нет, базальный инсулин есть). Однако нередко, чем дольше не ест человек, тем больше растет глюкоза и плохо «скалывается» коротким инсулином. Это печень начинает Вас «кормить», раз не хотите есть сами. В такой ситуации надо ввести привычку завтракать вскоре после пробуждения.
В целом, ситуации с утренней зарей, передозировкой или нехваткой инсулина бывает очень сложно дифференцировать.
Проверка базального инсулина в течение дня осуществляется пропуском пищи. Чтобы оценить базу с утра до обеда, утром не вводится короткий инсулин, до обеда ничего не есть, измерять глюкозу каждый час. Чтобы оценить участок с обеда до ужина, между завтраком и ужином должно пройти не менее 4 часов, в обед не вводится короткий инсулин, пропускается обед, измеряется глюкоза каждый час. Аналогично – участок от ужина до сна. На протяжении всего проверяемого периода не должно быть перекусов, введения дополнительных доз инсулина.
Способ проверки базы пропуском еды не подходит, если дневной фон обеспечивается за счет «хвостов» короткого инсулина (т.е. инсулин длительного действия с продолжительностью действия менее 12 часов вводится 1 раз в сутки на ночь). Проверка базы должна в отсутствие физической активности, острых заболеваний, стрессов. Нельзя проверять базу после перенесенной гипогликемии.
НОЧНАЯ ИНСУЛИНОТЕРАПИЯ И ЕЕ РОЛЬ В ДОСТИЖЕНИИ КОМПЕНСАЦИИ УГЛЕВОДНОГО ОБМЕНА ПРИ ИНСУЛИННЕЗАВИСИМОМ САХАРНОМ ДИАБЕТЕ
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Современные представления о гипергликемии как о важнейшем звене патогенеза инсулиннезависимого сахарного диабета и факторе, препятствующем достижению компенсации заболевания, диктуют необходимость поддержания нормогликемии натощак.
Х роническая гипергликемия натощак является одним из наиболее ранних и постоянных лабораторных признаков инсулиннезависимого сахарного диабета (ИНСД). Доказательство глюкозотоксичности, приводящей с течением времени к нарушению функции в-клеток, заставило изменить взгляд на гипергликемию как только на маркер сахарного диабета. В настоящее время гипергликемию вообще и натощак в частности рассматривают как важнейшее звено патогенеза ИНСД, фактор риска развития атеросклероза и как самостоятельное явление, препятствующее достижению компенсации данного заболевания. Этот факт диктует необходимость достижения и поддержания нормального или близкого к нему состояния углеводного обмена путем максимальной оптимизации терапевтических мероприятий при ИНСД.
Каким образом поддерживается нормогликемия натощак, каковы причины и последствия тощаковой гипергликемии?
Поддержание нормогликемии натощак осуществляет только печень при помощи равновесия между гликогенолизом и глюконеогенезом. Соответственно для гомеостаза глюкозы натощак требуется достаточное содержание гликогена в гепатоцитах и наличие субстратов для глюконеогенеза. Вырабатывающую при этом глюкозу в основном утилизируют инсулиннезависимые ткани (прежде всего мозг и в незначительной степени – инсулинзависимые (мышцы и жировая ткань). Этот процесс регулируют многие нейрогормональные факторы, а при наличии нормального уровня инсулина глюкоза самостоятельно может регулировать процесс освобождения глюкозы печенью за счет короткосрочных (инсулин, глюкагон, катехоламины) и долгосрочных (соматотропный гормон, глюкокортикоиды, тиреодные гормоны) регуляторов.
Печень чрезвычайно чувствительна к изменениям уровня инсулина и глюкагона, так как эти гормоны секретируются непосредственно в печень и прямым образом регулируют данный процесс. Так, снижение уровня инсулина тут же приводит к медленному повышению продукции глюкозы печенью и длительной гипергликемии. Снижение уровня глюкагона уменьшает продукцию глюкозы печенью и соответственно приводит к восстановлению уровня гликемии. При наличии периферической инсулинорезистентности (ИР), как при ИНСД или висцеральном ожирении, происходят значительные изменения в колебаниях подъемов уровня глюкозы в крови натощак. Островки Лангерганса очень чувствительны к этим изменениям и в норме немедленно отвечают на них повышением продукции инсулина и снижением выработки глюкагона. Это, в свою очередь, должно повышать периферическую утилизацию глюкозы и снижать продукцию глюкозы печенью. Таким образом, при имеющейся ИР гликемия какое-то время остается нормальной, а инсулинорезистентность компенсируется ответной гиперинсулинемией. Однако это не может продолжаться бесконечно, и как только компенсаторная гиперинсулинемия оказывается недостаточной для преодоления имеющейся ИР, гликемия в состоянии натощак резко повышается. Результаты исследования базальной и стимулированной секреции инсулина у больных ИНСД явно указывают на наличие признаков относительного дефицита гормона. Так, в частности, доказан факт недостаточной базальной секреции инсулина, несмотря на наличие гиперинсулинемии по крайней мере в течение первых лет заболевания. Кроме того, тест с острой стимуляцией секреции инсулина указывает на выпадение первой быстрой фазы секреции этого гормона. При этом глубина инсулинсекреторного дефекта прямо коррелирует со степенью гипергликемии натощак. Так, при уровне утренней гликемии ниже порогового базальная инсулинемия и инсулиносекреторный ответ на различные стимулы практически не отличаются от нормы. Однако при наличии гипергликемии натощак стимуляция b- клеток глюкозой в большей и аргинином в меньшей степени тут же выявляет значительные нарушения инсулинового ответа. С клинической точки зрения данное явление означает, что при наличии гипергликемии натощак инсулиносекреторный ответ в-клеток на стимуляцию производными сульфонилмочевины (ПСМ) в течение последующего отрезка времени как минимум окажется недостаточным, а достижение компенсации заболевания будет практически невозможным.
Относительный дефицит инсулина у больных ИНСД, несмотря на ГИ, связывают с нарушением функции b- клеток, обусловленным глюкозотоксичностью. Последняя проявляется в виде снижения способности глюкозы потенцировать инсулиносекреторный ответ b- клеток на нейрогуморальные и прочие (не связанные с глюкозой) стимулы, которые чрезвычайно важны в поддержании базального и постпрандиального уровня инсулинемии.
Не последнюю роль в поддержании гипергликемии натощак при ИНСД играет нарушение секреции глюкагона. Учитывая тот факт, что a- клетки, как и b- клетки, являются глюкозочувствительными, первые с течением времени также теряют нормальную способность отвечать на повышение гликемии снижением продукции глюкагона даже при очень выраженной гипергликемии. Не исключено, что первичный дефект описанного нарушения секреторной способности a- клеток связан с патологическими процессами, происходящими в b- клетках. Кровоток в островках Лангерганса осуществляется от b- клеток к a- клеткам, и вполне возможно, что процессы, приводящие сначала к нарушению секреции инсулина, являются и причиной неспособности а-клеток подавлять секрецию глюкагона.
Независимо от уровня дефекта, приводящего к гипергликемии натощак, можно утверждать, что при ИНСД в любом случае имеется недостаточная секреция инсулина даже при наличии относительной гиперинсулинемии. С течением времени гипергликемия per se, как уже было показано ранее, в силу глюкозотоксичности нарушает секрецию инсулина и, возможно, искажает секрецию глюкагона.
Следующую важную роль относительный дефицит инсулина играет в метаболизме СЖК. Так, адекватное количество инсулина подавляет липолиз и гиперпродукцию СЖК. В исследованиях было четко показано, что в случаях, наибольшей утренней гипергликемии, а следовательно, наименьшей инсулинемии, в крови больных ИНСД выявляется максимальная концентрация СЖК. Введение таким больным высоких доз инсулина приводило к поддержанию нормогликемии и снижению СЖК. Характерно, что уровень СЖК нормализовался на фоне максимальных доз инсулина.
СЖК играют важнейшую роль в развитии инсулинорезистентности и поддержании гипергликемии у больных ИНСД.
Более 20 лет назад Рэндл доказал, что повышение окисления СЖК в мышцах препятствует утилизации и окислению в них глюкозы вследствие воздействия СЖК на различные ферменты гликолиза. В настоящее время доказано, что повышенное окисление СЖК оказывает влияние на все основные внутриклеточные процессы, приводящие к инсулинорезистентности, а именно: снижает транспорт глюкозы внутрь клеток, а также – активность гликогенсинтетазы и пируватдегидрогеназы. Кроме того, избыточное окисление СЖК в печени стимулирует повышенную продукцию глюкозы в ней. Последнее явление было доказано даже у абсолютно здоровых лиц. Так, искусственно созданный избыточный приток СЖК в печень резко стимулировал глюконеогенез (ГНГ). Скорее всего, это связано со способностью Ацетила-СоА, образующегося в процессе окисления СЖК, стимулировать активность аллостерической пируваткарбоксилазы, ключевого фермента ГНГ. Кроме того, Ацетил-СоА снижает активность пируватдегидрогеназы. Результатом последнего действия будет ускорение окисления СЖК в печени и мышцах, и, как следствие, повышенное образование лактата из глюкозы, одного из главных субстратов для ГНГ.
Кроме изложенных эффектов СЖК, следует отметить, что последние оказывают прямое подавляющее действие на связывание и интернализацию инсулина гепатоцитами. Это в свою очередь приводит к снижению синтеза гликогена в печени, усиливает периферическую ГИ и также активизирует ГНГ.
При ИНСД, особенно сопровождающимся висцеральным ожирением, наблюдают повышенный липолиз. Это также связано с избыточным содержанием СЖК, ускорящим процессы их утилизации клетками и окисления липидов, что подавляет естественную способность инсулина ингибировать липолиз. Таким образом, повышенное образование СЖК, обусловленное относительным дефицитом инсулина, препятствует утилизации глюкозы в мышцах и стимулирует ГНК в печени. Совместно эти механизмы ведут к гипергликемии и ИР.
Таким образом, изложенные данные четко демонстрируют важную роль обеспечения нормогликемии в ночные и утренние часы для достижения компенсации углеводного обмена в течение всех суток.
Учитывая значимость нормализации гликемии натощак, нами была поставлена цель разработать оптимальные терапевтические подходы, обеспечивающие удовлетворительный уровень сахара в крови в течение ночи и утром.
Под нашим наблюдением находилось 204 пациента в возрасте от 38 до 72 лет, у которых в соответствии с критериями компенсации, предложенными European NIDDM Policy Group (1993), имела место суб- или декомпенсация сахарного диабета. Так, у всех больных уровень гемоглобина A1c превышал 7,5% (8,6±0,9), а гликемия натощак – 7,8 ммоль/л (9,1±1,1).
Подавляющее большинство больных получали различные ПСМ (92,6%), комбинацию ПСМ и глюкобая (3%) и 4,4% – метформин.
Прежде всего, больные все без исключения были обучены принципам расчета диеты и самоконтроля. Ежедневно вместе с больным производили анализ и коррекцию полученных при самоконтроле данных, которые тщательно сопоставляли с количеством принятой пищи. Проведенные мероприятия позволили достичь у 20,6% больных компенсации сахарного диабета, не меняя лечения вообще. Всем остальным пациентам терапия была изменена следующим образом.
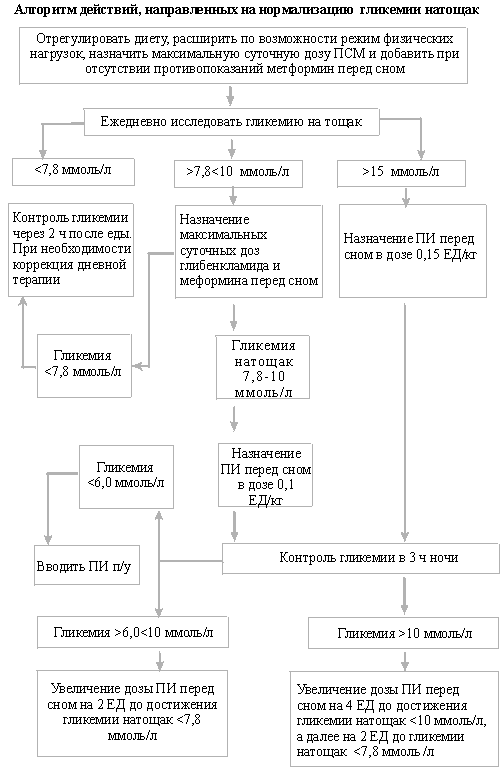
112 (54,9%) пациентов с гликемией натощак, превышающей 10,0 ммоль/л, перед сном в 22 ч был назначен пролонгированный инсулин протафан, монотард, инсуман “Базаль” или хумулин “N” в начальной дозе 0,15 ЕД/кг фактической массы тела. Дозу ПСМ увеличивали до максимальной суточной, или чаще назначали глибенкламид в дозе 15 мг/сут (10 мг + 5 мг). Если у больных лабораторные признаки декомпенсации сахарного диабета сочетались со значительной потерей массы тела, перед основными приемами пищи временно добавляли инсулин короткого действия.
Для исключения ночной гипогликемии, а также для решения вопроса о скорости увеличения дозы пролонгированного инсулина перед сном контролировали гликемию в 3 ч ночи. В том случае, если гликемия оказывалась выше 10 ммоль/л, дозу инсулина перед сном сразу же увеличивали на 4 ЕД, в пределах
6 – 10 ммоль/л — на 2 ЕД. Осуществляли ежедневный контроль гликемии натощак и каждые 2 – 3 дня – в 3 ч ночи. У пациентов, длительно пребывавших в состоянии декомпенсации сахарного диабета, во избежание гипогликемии лавировать дозами инсулина при снижении гликемии натощак ниже 10 ммоль/л следует с осторожностью. У данной категории больных трудно прогнозировать полноценный ответ печени с точки зрения своевременной и адекватной продукции глюкозы в случае недостаточного употребления с пищей углеводов или незначительной физической нагрузки. В том случае, если гликемия в 3 ч ночи оказывалась ниже 6,0 ммоль/л, мы рассматривали вопрос о необходимости перемещения пролонгированного инсулина с 22 ч на более раннее время, например, перед ужином.
Описанные мероприятия в виде постепенного увеличения дозы пролонгированного инсулина перед сном производили до того момента, пока гликемия натощак не оказывалась ниже 7,8 ммоль/л.
Другой группе, состоящей из 50 (24,5%) больных, у которых исходно гликемия натощак находилась в пределах 7,8 – 10 ммоль/л, для подавления ночного ГНГ перед сном добавляли сиофор (метформин) в дозе 500 – 850 мг. Противопоказаниями для назначения сиофора являлись клиренс креатинина менее 50 мл/мин, нарушение функции печени (гепатит, повышение печеночных ферментов), гипоксические состояния любой этиологии, злоупотребление алкоголем, беременность и лактация. 12 (5,9%), пациентов мероприятия оказались недостаточными, а у 8 (3,9%) имелись противопоказания для применения сиофора. Этим больным также, как и пациентам предыдущей группы, перед сном был назначен пролонгированный инсулин в дозе 0,1 ЕД/кг фактической массы тела. Дальнейший контроль гликемии и постепенное изменение дозы инсулина соответствовали описанным ранее.
Такую последовательную тактику увеличения дозы инсулина проводили до того момента, когда гликемия натощак стабильно устанавливалась на уровне ниже 7,8 ммоль/л. Этот уровень гликемии натощак, исключающий декомпенсацию заболевания, мы расценивали как первый важный этап достижения компенсации сахарного диабета. Было доказано, что с одной стороны указанная гликемия уже снижает проявление глюкозотоксичности и способствует нормализации секреции инсулина. С другой стороны, при таком уровне гликемии натощак и в 3 ч ночи практически полностью исключается риск развития гипогликемических эпизодов, особенно в самое опасное ночное время.
Следующим важным этапом лечения было решение вопроса об индивидуальных критериях компенсации заболевания у каждого пациента.
Известно, что одним из критериев компенсации ИНСД является гликемия натощак ниже 6,1 ммоль/л. В то же время широко распространено мнение, что у лиц пожилого возраста критерии компенсации могут быть менее жесткими, учитывая опасность возникновения плохо распознаваемых ими гипогликемий. Однако не вызывает сомнения тот факт, что декомпенсация сахарного диабета у лиц старческого возраста активизирует катаболические процессы, предрасполагает к развитию острых и ускоряет прогрессирование поздних осложнений сахарного диабета. Десятилетнее наблюдение за пожилыми больными, страдающими ИНСД, показало, что при декомпенсации заболевания частота инсультов и сердечно-сосудистых заболеваний резко возрастает независимо от длительности заболевания (М. Uusitupa и соавт., 1993). При этом смертность от описанных причин прогрессивно увеличивается при возрастании уровня гемоглобина A1c c 8,7% до 9,1% (J. Kuusisto;
L. Mykkanen; K. Pyorala и соавт., 1994).
Анализ литературных данных и собственный опыт в достижении компенсации заболевания у больных ИНСД позволяют нам утверждать, что независимо от возраста больного приоритетными позициями при выборе критериев компенсации в каждом конкретном случае являются следующие: сохранный интеллект пациента; наличие у него личных средств самоконтроля; ежедневный контроль гликемии и высокий уровень знаний, позволяющий больному принимать правильное решение на основании полученных им при самоконтроле данных. Если больной прежде всего соответствовал перечисленным критериям, а также у него в анамнезе отсутствовали данные о перенесенном ОНМК и нестабильной стенокардии, мы постепенно переходили к следующей цели терапии — установлению уровня гликемии натощак ниже 6,1 ммоль/л. Пути ее достижения полностью соответствуют выше описанным.
Наблюдение за больными показало, что даже при довольно быстром снижении гликемии с явно высоких цифр до значений ниже 10 ммоль/л, пациенты сразу же отмечали положительную динамику в самочувствии. Интересно, что улучшение самочувствия замечали даже те лица, которые исходно не предъявляли явных жалоб, типичных для декомпенсации сахарного диабета, в связи с неспособностью их распознать или правильно охарактеризовать.
После достижения желаемой гликемии натощак приступали к постоянному контролю и коррекции уровня сахара в крови после еды. Такую последовательную тактику подбора адекватной сахароснижающей терапии мы считали абсолютно безопасной и обоснованной. По мере нормализации тощаковой гликемии на фоне обеспечения необходимой инсулинизации организма, снижения ГНГ и липолиза в ночное время постепенно ликвидировалась глюкозотоксичность и уменьшалась ИР. Это, в свою очередь, способствовало улучшению гликемии в течение всего дня и значительно облегчало достижение компенсации в дальнейшем. Попытки одновременно корригировать все сахароснижающие средства, получаемые больным в течение суток, мы считали необоснованными. С одной стороны, абсолютно очевидна необходимость начального достижения близких к норме цифр гликемии натощак. С другой стороны, стремление контролировать сразу все или несколько гликемических “точек” требует частого и систематического контроля уровня сахара, что отрицательно сказывалось на отношении больного к самому процессу самоконтроля и препятствовало концентрации внимания на достижении хотя бы одной поставленной цели терапии.
Результаты работы позволили создать алгоритм лечебных мероприятий по нормализации гликемии в ночные часы.
 Читайте также:
Читайте также: