Ремоделирование левого желудочка после острого инфаркта миокарда и прогностическая роль биомаркеров
Несколько классических биомаркеров используются для диагностики ИМ или острого коронарного синдрома. В последнее время были выявлены новые маркеры для предоставления диагностической и прогностической информации, а также исхода инфаркта миокарда или острого коронарного синдрома, которые показали значительную связь с ремоделированием левого желудочка и плохим прогнозом после инфаркта миокарда.
Ремоделирование ЛЖ после ИМ было разделено на две фазы: ранняя фаза (через 72 часа) и поздняя фаза (после 72 часов). В ранней фазе ремоделирования расширение инфаркта происходит в результате деградации коллагеновых структур межмиоцитов сериновыми протеазами и активации матричных металлопротеиназ (ММР), высвобождаемых из нейтрофилов. Напряжение стенки ЛЖ стимулирует механорецепторы и передает внутриклеточные сигналы посредством высвобождения ангиотензина II (Ang II), что представляет собой усиленный синтез миофибрилл. Нарушение гемодинамики кровообращения запускает симпатическую адренергическую систему, которая стимулирует катехоламины, активирует систему ренин-ангиотензин-альдостерон и индуцирует выработку предсердных и мозговых натрийуретических пептидов (ANP, BNP). Поздняя фаза ремоделирования включает гипертрофию миоцитов и изменения в структуре желудочка, чтобы распределить увеличенное напряжения на стенке ЛЖ. На этом этапе гипертрофия миоцитов инициируется активацией нейрогормональной и ренин-ангиотензиновой систем, расширением миокарда и паракринно-аутокринными факторами.
Ремоделирование ЛЖ развивается через нескольких различных механизмах
1. Воспаление (С-реактивный белок, TNF-α, растворимые рецепторы TNF, Fas, интерлейкины (I, 6 и 18), остеопротегерин, адипонектин)
2. Гипертрофия / фиброз (матричные металлопротеиназы, коллагеновые пропептиды, галектин-3, растворимый ST2).
4. Разное (микроРНК, кивезин Q6, VEGFR-1)
Учитывая патогенетические механизмы ИМ, несколько классических биомаркеров были использованы для диагностики ИМ или острого коронарного синдрома. В последнее время были выявлены новые маркеры для предоставления диагностической и прогностической информации и исхода инфаркта миокарда или острого коронарного синдрома.
Три биомаркера оценивают различные пути, вовлеченные в патогенез ремоделирования ЛЖ:
1. Увеличение тропонина I (TnI) указывает на повреждение миоцитов
2. Мозговой (B-тип) натрийуретический пептид (BNP) увеличивается в ответ на перегрузку LV
3. С-реактивный белок (СРБ) является маркером воспаления
Тропонин I входит в состав тропонинового комплекса. Тропониновый комплекс состоит из трех субъединиц, которые регулируют кальций-опосредованный сократительный процесс поперечно-полосатой мышцы. К ним относятся тропонин C, который связывает Ca2 +, тропонин I (TnI), который связывается с актином и ингибирует взаимодействия актин-миозин, и тропонин T (TnT), который связывается с тропомиозином, тем самым фиксируя комплекс тропонина. После повреждения миоцитов начальное высвобождение cTnT и cTnI происходит из цитозольного пула с последующим высвобождением из структурного (связанного с миофиламентом) пула. Для ИМ сердечный тропонин T (cTnT) и сердечный тропонин I (cTnI) считаются более чувствительными и специфичными, чем другие биомаркеры сердца. cTnT и cTnI остаются в кровотоке приблизительно более 10 дней, достигают пика приблизительно через 1-2 дня после повреждения миокарда, как это было предложено Thygesen и Alpert в 2000 г. Из-за длительного высвобождения в крови эти биомаркеры являются основными диагностическими критериями острого повреждения миокарда. Исследования показали, что у пациентов с повышенным уровнем cTnI частота сердечной смертности и сердечных осложнений была значительно выше, так чаще развивался летальный исход, нефатальный инфаркт миокарда, требовалась реваскуляризация сосуда-мишени.
Натрийуретические пептиды (bnp и nt-probnp)
В исследовании DETECT было показано, что повышенные уровни NT-pro-BNP в плазме крови на исходном уровне были связаны с повышенным 5-летним коэффициентом риска для смертности от всех причин (HR 5,02; CI 3,26-7,72; p
Сердечная недостаточность
Сердечный цикл
Сердечный цикл состоит из очень тонко и точно синхронизированных электрических и механических процессов, которые приводят к ритмичному сокращению предсердий и желудочков, благодаря чему кровь поступает в малый и большой круг кровообращения. Механическая систола отражает сокращение желудочков, а диастола — их расслабление и наполнение кровью. Во время сердечного цикла кровь из системных и легочных вен непрерывно поступает в сердце через правое и левое предсердия, соответственно. Во время диастолы кровь поступает из предсердий в желудочки через открытые трехстворчатый и митральный клапаны. Сокращение желудочков означает начало механической систолы, в результате которой кровь выбрасывается в сосуды малого и большого круга кровообращения.
Понятие сердечная недостаточность
В норме сердце при относительно низком давлении во время диастолы принимает в себя кровь и при более высоком давлении в систолу проталкивает кровь вперед. Сердечная недостаточность определяется как неспособность сердца перекачивать объем крови, необходимый для обеспечения метаболических потребностей организма («систолическая дисфункция») или возможность обеспечивать эти потребности только благодаря ненормально высокому давлению заполнения полостей сердца («диастолическая дисфункция»), или за счет обоих этих механизмов.
Причины сердечной недостаточности
Сердечная недостаточность может быть основным проявлением практически всех болезней сердца, включая атеросклероз коронарных сосудов, инфаркт миокарда, приобретенные пороки клапанов сердца, врожденные пороки сердца, аритмии и кардиомиопатии.
В зависимости от снижения функциональной способности того или иного желудочка сердца, различают:
Все возможные этиологические факторы по механизму развития левожелудочковой сердечной недостаточности можно разделить на:
В свою очередь, левожелудочковая сердечная недостаточность — наиболее частая причина развития правожелудочковой недостаточности, которая в данном случае обусловлена увеличением постнагрузки из-за дисфункции левого желудочка и повышения сопротивления легочных сосудов.
Причинами развития правожелудочковой недостаточности наиболее часто являются
Как и в случае с левожелудочковой недостаточностью, изолированная правожелудочковая недостаточность негативно влияет на функциональную способность левого желудочка, так как уменьшение выброса крови правым желудочком приводит к снижению наполнения левого желудочка и, как следствие, к уменьшению ударного объема и сердечного выброса.
К факторам, провоцирующим возникновение симптомов застоя у больных с компенсированной сердечной недостаточностью, относятся
Состояния, сопровождающиеся активацией метаболических процессов
Увеличение объема циркулирующей крови
Состояния, сопровождающиеся повышением постнагрузки
Признаки сердечной недостаточности
✔ Наиболее выраженным симптомом хронической левожелудочковой недостаточности является одышка при нагрузке, что связано с венозным застоем в легких или низким сердечным выбросом. По мере прогрессирования заболевания одышка может наблюдаться и в состоянии покоя.
✔ Часто сердечная недостаточность сопровождается ортопноэ, ночными приступами сердечной астмы и ночным кашлем. Ортопноэ — это затруднение дыхания в положении лежа и уменьшающееся в сидячем положении. Причиной данного симптома служит перераспределение крови из органов брюшной полости и нижних конечностей в легкие в положении лежа. В некоторых случаях, ортопноэ бывает настолько выражено, что больной вынужден спать в положении сидя.
✔ Ночные приступы сердечной астмы — это тяжелые приступы одышки во время ночного сна. Данный симптом наблюдается в положении лежа при проникновении в кровь жидкости из отеков нижних конечностей, что приводит к увеличению объема циркулирующей крови и венозного возврата в сердце и легкие.
✔ Ночной кашель — также является симптомом застоя крови в легких, его механизм развития идентичен механизму развития ортопноэ. В некоторых случаях может наблюдаться кровохаркание, что обусловлено разрывом вен бронхов из-за их полнокровия.
✔ К типичным проявлениям сердечной недостаточности относятся спутанность сознания и уменьшение дневного диуреза, вследствие уменьшения кровоснабжения головного мозга и почек, соответственно. Иногда может быть усилен ночной диурез, так как в положении лежа кровоснабжение почек улучшается. Также характерна общая слабость и быстрая утомляемость, ввиду недостаточного кровоснабжения скелетной мускулатуры.
✔ Больные с изолированной правожелудочковой недостаточностью, нередко испытывают чувство дискомфорта в правом подреберье, что обусловлено избыточным кровенаполнением печени и растяжением ее капсулы. В тяжелых случаях, возможно скопление жидкости в брюшной полости (асцит). Также характерным признаком является развитие периферических отеков, особенно на лодыжках. Если больной длительное время находился в вертикальном положении, то такие отеки усиливаются к концу дня, исчезая при этом утром.
На практике для оценки тяжести сердечной недостаточности часто используют классификацию Нью-Йоркской Ассоциации кардиологов (NYHA):
I класс — Физическая активность не ограничена
II класс — Легкое ограничение активности. Появление одышки и слабости после умеренной физической нагрузки
III класс — Выраженное ограничение активности. Одышка после минимальной физической нагрузки
IV класс — Тяжелое ограничение активности. Симптомы сердечной недостаточности в покое
Принципы медикаментозного лечения сердечной недостаточности
Лечение сердечной недостаточности должно быть направлено на достижение следующих целей:
Хирургическое лечение сердечной недостаточности
Сердечная недостаточность у больных кардиохирургического профиля встречается в самых различных возрастных группах и при самых разнообразных заболеваниях сердца. Интенсивному лечению, в том числе и хирургическому, подлежат пациенты с высокой угрозой для жизни и резистентные к медикаментозной терапии. К этой категории относятся больные с дилатационной кардиомиопатией, ишемической кардиомиопатией, гипертрофической обструктивной кардиомиопатией (ГОКМП) и посткардиотомной (послеоперационной) сердечной недостаточностью.
Фармакологические методы лечения сердечной недостаточности, бесспорно, играют важнейшую роль, однако имеющиеся в настоящее время препараты оказывают весьма опосредованный и нестойкий эффект у пациентов в терминальной стадии заболевания. Однолетняя выживаемость таких больных составляет не более 50%. И это притом, что ежегодно синтезируется более 30 новых препаратов, направленных на лечение сердечной недостаточности. Единственным признанным эффективным вариантом лечения критической сердечной недостаточности остается трансплантация сердца. На сегодняшний день в мире выполнено более 70 000 операций по трансплантации сердца. При этом ежегодно выполняется более 3 000 операций, из них около 2 000 в США. Однако количество больных, нуждающихся в пересадке сердца, значительно превышает количество доноров. Как результат этого – высокая, увеличивающаяся с каждым годом смертность пациентов, находящихся в «листе ожидания». Такая неутешительная динамика требует развития новых способов лечения критической сердечной недостаточности, и интерес к данной проблеме за последнее время значительно возрос среди ученых всего мира. Подтверждением этому является успешная разработка систем вспомогательного кровообращения, полностью или частично облегчающих работу патологически измененного сердца.
Под понятием «система вспомогательного кровообращения» следует понимать механические системы, производящие перемещение крови с целью снижения работы миокарда и/или увеличения его энергоснабжения.
Морфология миокарда левого желудочка с различным характером кинеза его стенок у больных ишемической кардиомиопатией
1 ФГБУ НИИ кардиологии СО РАМН; 2 ГБОУ ВПО СибГМУ Минздрава России (Томск, Россия);
В прогнозе исходов ишемической кардиомиопатии (ИКМП) ключевая роль отводится морфофункциональному состоянию миокарда и его морфометрической оценке (J. Hare et al, 1992; С.Л. Дземешкевич, Л.У. Стивенсон, 2009). К сожалению, при описании морфологической картины миокарда больных ИКМП не характеризуется место взятия биопсии для исследования, а диффузный характер изменений принимается аксиоматически по аналогии с другими видами кардиомиопатий.
Цель исследования:
оценить морфологию миокарда стенок левого желудочка (ЛЖ) с различным характером кинеза по данным ЭхоКГ у больных ИКМП с передневерхушечной аневризмой.
Объектом исследования стал миокард 36 больных ИКМП обоего пола с инфарктами миокарда в анамнезе, подвергнутые реконструкции ЛЖ в отделении сердечно-сосудистой хирургии ФГБУ «НИИ кардиологии» СО РАМН с 2011 по 2012 года. У пациентов брали биопсии миокарда передней, задней, боковой стенки ЛЖ и МЖП со стороны ЛЖ с сопоставлением локализации взятия материала с её сократимостью (а-, гипо-, дис- и нормокинез). Из биоптатов готовили гистологические препараты по стандартной методике. Для количественной характеристики изменений применяли измерение удельного объема отека, сосудов, паренхимы и стромы миокарда методом точечного счета в 5–7 случайных полях зрения каждого среза с помощью программ обработки графических изображений (AxioVision, CarlZeiss; ImageJ, NIH USA). Соотношения локализации биопсии и сократительной способности миокарда в этом сегменте по данным ЭхоКГ находились в статистической зависимости, выявленной с помощью критерия Хи-квадрат Пирсона (X = 113,949, p
Аневризма левого желудочка сердца
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
В результате ткань истончается и растягивается, образуя выпячивание- аневризму. Чаще всего поражается левый желудочек в передней верхней части.
Аневризма левого желудочка сердца классифицируется по нескольким признакам:
1. По времени появления:
2. По форме проявления:
В практике более часто встречаются диффузные формы, реже диагностируют расслаивающуюся и грибовидную аневризмы.
Симптомы и причины появления
Основная причина появления аневризма — инфаркт миокарда. Так же появление истонченных, выпирающих участков ткани на сердце может быть спровоцировано такими причинами, как:
Симптоматически наличие аневризмы левого желудочка сердца определить невозможно, но поскольку она вызывает нарушения работы сердца то и, соответственно, вызывает общие признаки расстройства сердечной деятельности. Среди них:
Диагностировать аневризму желудочка сердца может врач-кардиолог. После осмотра пациента и получения результатов всех необходимых исследований, в том числе ЭКГ, УЗИ и МРТ. Своевременная диагностика поможет избежать тяжелейших осложнений, часто смертельных. Для определения плана лечения необходимо точно знать локализацию, структуру и размеры аневризмы.
Методы диагностики

Главные способы диагностирования аневризмы основаны на последовательном выявлении клинических и инструментальных признаков. Начинается обследование с опроса больного, сбора анамнеза, некоторых лабораторных исследований крови и мочи — эти данные позволяют обнаружить сопутствующие заболевания, наличие которые может повлиять на развитие аневризмы. Пациент также получает направление на ЭКГ, МРТ или УЗИ и другие исследования.
Традиционные методы диагностики и информация, которую они предоставляют:
Комплексное всестороннее обследование пациента позволяет получить полную картину деформации тканей желудочка, а значит, назначить точное и наиболее эффективное лечение. Помимо медикаментозной терапии, больным с выявленной аневризмой левого желудочка сердца может быть назначено хирургическое вмешательство. Обычно такое решение принимается лечащим врачом в случае, если размеры поврежденной ткани превышают 20% площади стенки.
Методы лечения
В связи с относительно благоприятным прогнозом при бессимптомных аневризмах левого желудочка (ЛЖ), показания к хирургическому лечению у таких пациентов относительны. Тем не менее, у пациентов, которым показана хирургическая реваскуляризация миокарда (АКШ), в некоторых случаях необходимо выполнять хирургическое восстановление правильной формы левого желудочка.
Хирургическое лечение абсолютно показано пациентам, у которых в результате инфаркта миокарда появилась дисфункция ЛЖ с участками акинезии и дискинезии его стенок и закономерным увеличением объема ЛЖ: > 80 мл / м 2 при сокращении и > 120 мл / м 2 в момент расслабления, а также при угрозе разрыва аневризмы и в случае тромбоэмболического синдрома при тромбированных аневризмах.
При правильном профессиональном подходе, внимательном изучении функции ЛЖ по данным ЭхоКГ, оценке формы и локализации аневризмы, фракции выброса сокращающейся (уцелевшей) части ЛЖ – операция по устранению левожелудочковой аневризмы является вполне оправданной, так как впоследствии снижается напряжение в стенке ЛЖ, мышечные волокна вновь направляются в правильную сторону, возрастает систолическая и улучшается диастолическая функция ЛЖ.
Относительные противопоказания: крайне высокий риск анестезии, отсутствие «живого» миокарда за пределами аневризмы, низкий сердечный индекс.
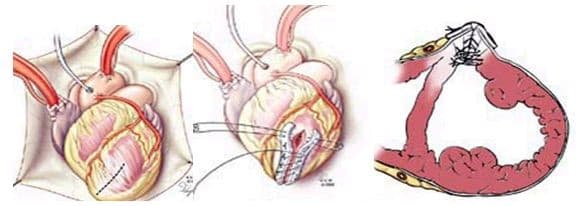
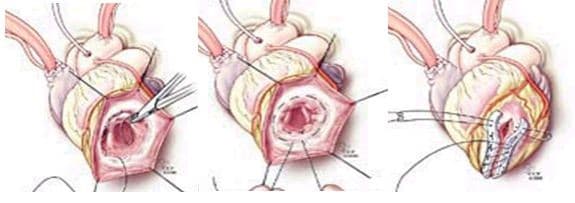
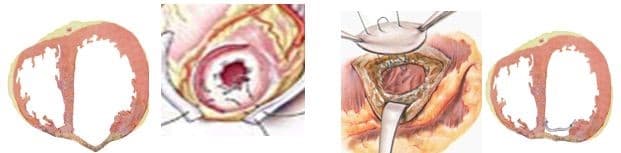
При хирургическом лечении аневризмы ЛЖ выполняется стандартный доступ путем срединной стернотомии. Аппарат искусственного кровообращения подключается как для АКШ, для удобства устанавливается дренаж ЛЖ через правые легочные вены. После кардиоплегии участок аневризмы выглядит как белесая, фиброзная площадка, впалая в полость левого желудочка. Выполняется разрез аневризмы вдоль передней нисходящей артерии, отступая от нее не менее 1,5 см. Имеющийся в полости тромб удаляется, исключая оставление даже очень мелких фрагментов. Часто такие операции сопровождаются вмешательством на митральном клапане, а также шунтированием передней нисходящей артерии и других артерий при наличии показаний. Оценив объем резецированного участка приступают к ремоделированию и восстановлению геометрии ЛЖ. Методик для этого предложено много, ниже мы приведем основные из них. После завершения хирургических манипуляций на сердце, выполняется важный процесс изгнания воздуха из полостей сердца, следом к сердцу пускают кровоток, снимая зажим с аорты, и через пару минут происходит восстановление сердечной деятельности. Окончание сеанса искусственного кровообращения для оперированного ЛЖ может стать настоящим испытанием и потребовать применение до трех инотропных и вазопрессорных препаратов, а также внутриаортальной баллонной контрапульсации.
Техники ремоделирования ЛЖ
Прогресс не стоит на месте, и методики постоянно совершенствуются, но основные хирургические принципы для лечения данной патологии представлены вашему вниманию и заключаются в стремлении к уменьшению полости ЛЖ за счет резекции нефункционального аневризматического мешка и восстановлению близкой к нормальной геометрической формы ЛЖ применяя разной формы заплаты и кисетные пластики.
Результаты хирургического лечения аневризмы левого желудочка сердца
Частым осложнением после операции по поводу аневризмы ЛЖ является синдром малого выброса, который развивается вследствие чрезмерного уменьшения размеров полости ЛЖ, а так же желудочковые нарушения ритма и легочная недостаточность.
30-ти дневная летальность в последние годы снизилась и составляет 3-7%. Факторы повышенного риска операции это: пожилой возраст, женский пол, операция в экстренном порядке, а так же операция дополненная протезированием митрального клапана, исходно низкая сократительная способность миокарда (ФВ менее 30%), умеренная и высокая легочная гипертензия, почечная недостаточность.
В нашей клинике успешно выполняются все виды операций на сердце включая хирургическое ремоделирование и пластику при аневризмах ЛЖ.
Дисфункция левого желудочка у больных ИБС: современные методы диагностики, медикаментозной и немедикаментозной коррекции
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Российский кардиологический научно-производственный комплекс МЗ РФ, Москва
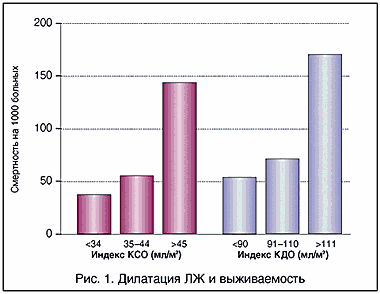
Рис. 1. Дилатация ЛЖ и выживаемость
Рис. 2. Выживаемость больных ХСН в подгруппах с КДР ЛЖ 5,5 см
Таким образом, формирование зоны асинергии миокарда и ее протяженность существенно влияют на течение заболевания и судьбу больного. Как показало исследование Hammermeister K.E. et al.,1979, смертность больных, перенесших инфаркт миокарда с развитием сердечной недостаточности, находится в тесной корреляции с индексом конечного систолического и конечного диастолического объемов левого желудочка (рис. 1). В отделе сердечной недостаточности института кардиологии имени А.Л. Мясникова на основании длительного (до двадцати лет) наблюдения показано, что шестилетняя выживаемость пациентов с диастолическим размером левого желудочка менее 5,5 см на 100% выше, чем у больных с дилатацией левого желудочка более 5,5 см (рис. 2). То же самое относится и к насосной функции левого желудочка. У пациентов с фракцией выброса левого желудочка более 50% риск смерти ниже на 28% по сравнению с больными, имеющими сниженную функцию желудочка (рис. 3).
Рис. 3. Выживаемость больных ХСН в подгруппах с сохраненной и со сниженной сократимостью ЛЖ
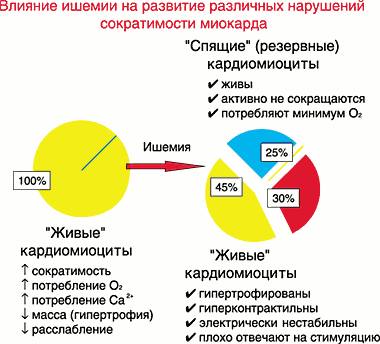
Что же происходит с миокардом при его ишемии? Достаточно упрощенно это представлено на рис. 4. Как видно, нарушение баланса между поступлением кислорода и потребности в нем миокарда приводит к некрозу примерно трети объема кардиомиоцитов. Примерно 45% кардиомиоцитов сохраняют свою жизнеспособность, однако находятся в состоянии компенсаторного гиперкинеза и гипертрофии. Кроме того, они электрически нестабильны. Наибольший интерес представляют 25% кардиомиоцитов, которые активно не сокращаются, но сохраняют минимальное потребление кислорода и основные компоненты клеточного метаболизма, то есть они «живы», но находятся как бы в резерве.
Для обозначения подобных участков миокарда были предложены различные термины, в зависимости от степени и длительности ишемии и выраженности структурно-метаболических изменений. Наиболее распространенными являются:
Оглушенный (Stunned) миокард (Braunvald Е. 1982). Браунвальд определил его, как запаздывание восстановления региональной дисфункции миокарда после острого периода ишемии, сопровождающегося последующей реперфузией. При этом повреждение миокарда зависит как от самого эпизода ишемии, так и от постишемической реперфузии. Длительная ишемия, по мнению Rahimtoola S.H.et al. 1985, приводит к появлению Спящего (Hibernating) миокарда – явления, скорее, компенсаторно-приспособительного к хронической нехватке кислорода даже в состоянии покоя. Но что наиболее важно, эти виды диссинергии миокарда, по данным Rozanski A.et al. 1981, носят обратимый характер как при восстановлении кровотока, так и при нормализации баланса поступление/потребление миокардом кислорода. Дальнейшие исследования позволили объединить оба эти состояния термином Жизнеспособный (Viable) миокард. При этом данные участки миокарда являются гипо- или акинетичными, но сохраняют определенный уровень метаболизма и резерв сократимости. Кроме того, как было сказано выше, их функция может быть восстановлена инструментально или медикаментозно.
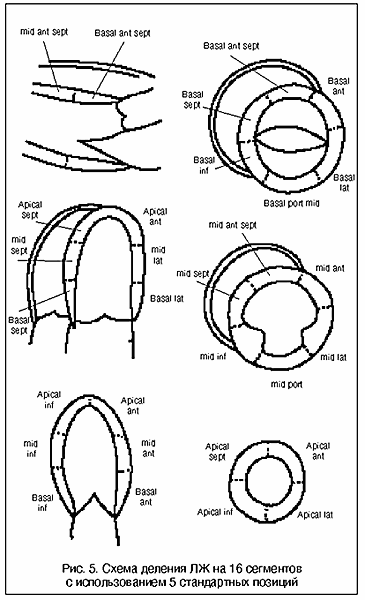
Рис. 5. Схема деления ЛЖ на 16 сегментов с использованием 5 стандартных позиций
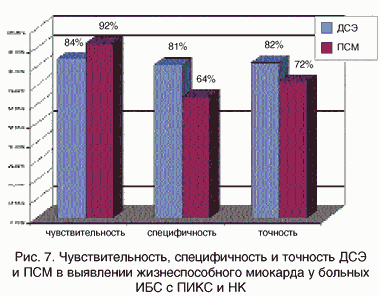
Рис. 7. Чувствительность, специфичность и точность ДСЭ и ПСМ в выявлении жизнеспособного миокарда у больных ИБС с ПИКС и НК
Рис. 8. Чувствительность, специфичность и точность комбинации ДСЭ и ПСМ в выявлении жизнеспособного миокарда у больных ИБС с ПИКС и НК
В качестве методов контроля при добутаминовой пробе могут быть использованы и другие методы (МР-томография, электронно-лучевая томография). Но они либо очень дороги, а потому малодоступны, либо инвазивны, как, например, рентгеноконтрастная вентрикулография. Несомненные преимущества, с точки зрения диагностики, имеет позитронно-эмиссионная томография, которая позволяет непосредственно оценить потребление кислорода и метаболизм гипокинетичных кардиомиоцитов.Однако этот метод чрезвычайно дорогостоящий и требует наличия короткоживущих изотопов.
Рис. 10. Изменение показателей внутрисердечной гемодинамики, ФК НК, ИА и ИНПМ у больных ИБС на фоне хирургической реваскуляризации и медикаментозной терапии
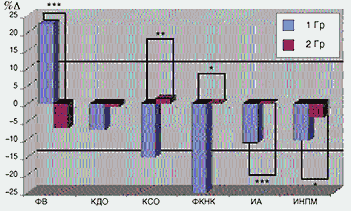
Рис. 12. Изменение показателей центральной гемодинамики, ФКНК, региональной сократимости и перфузии миокарда у больных ИБС с наличием (1 гр.) и отсутствием (2 гр.) жизнеспособного миокарда на фоне терапии карведилолом
Рис. 13. Изменение показателей центральной гемодинамики, ФКНК, региональной сократимости и перфузии миокарда у больных ИБС с наличием (1 гр.) и отсутствием (2 гр.) жизнеспособного миокарда на фоне терапии эналаприлом
Рис. 14. Изменение показателей центральной гемодинамики, ФКНК, региональной сократимости и перфузии миокарда у больных ИБС с наличием (1 гр.) и отсутствием (2 гр.) жизнеспособного миокарда на фоне терапии комбинацией эналаприла с бисопрололом
Обратимся к другим классам препаратов. Как показали иследования, выполненные в нашем институте (М.А. Саидова, 1999), если разделить пациентов, получающих медикаментозное лечение, на группы с наличием и отсутствием жизнеспособного миокарда, использование препарата карведилол, обладающего b-блокирующими, в меньшей степени a-блокирующими свойствами, а также некоторой антиоксидантной активностью, позволяет существенно улучшить показатели функции левого желудочка и клиническое состояние больных, имеющих жизнеспособный миокард (рис. 12). Использование ингибиторов АПФ, в частности, эналаприла (рис. 13), также позволяет улучшить состояние больных, имеющих жизнеспособный миокард, однако в несколько меньшей степени, чем при использовании бета-блокаторов. Наиболее целесообразно использование комбинации ингибитор АПФ и b-блокатор (рис. 14). Как видно, прием эналаприла и бисопролола в наибольшей степени увеличивает фракцию выброса левого желудочка и улучшает функциональный класс недостаточности кровообращения. Это вполне объяснимо, так как суммируются положительные эффекты b-блокаторов (нормализация потребления миокардом кислорода за счет более экономной работы сердца, нейромодулирующее действие на САС) и ингибиторов АПФ (периферическое разгрузочное действие, нейромодулирующее действие на РААС).
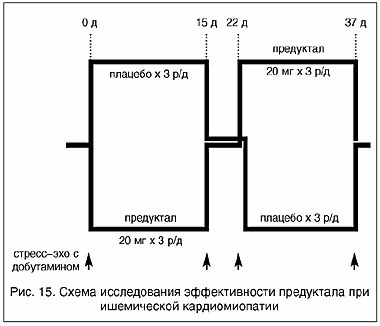
Рис. 15. Схема исследования эффективности предуктала при ишемической кардиомиопатии
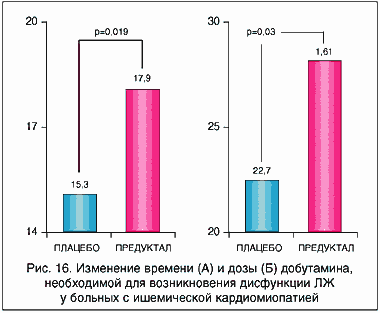
Рис. 16. Изменение времени (А) и дозы (Б) добутамина, необходимой для возникновения дисфункции ЛЖ у больных с ишемической кардиомиопатией
Рис. 17. Снижение индекса асинхронии сокращений ЛЖ у больных с ишемической кардиомиопатией
Рис. 18. Оптимальная тактика ведения больных с ИБС
Резюмируя вышесказанное, можно предложить следующий алгоритм обследования и ведения пациентов с ИБС, имеющих локальные нарушения сократимости миокарда, снижение фракции выброса левого желудочка, в том числе и с клиническими проявлениями ранних стадий сердечной недостаточности (рис. 18). Все они должны пройти процедуру диагностики наличия жизнеспособного миокарда с использованием методик, применяющихся в данном специализированном стационаре. В случае выявления жизнеспособного миокарда они должны пройти ту или иную процедуру реваскуляризации (АКШ, ангиопластика), либо, при невозможности радикального вмешательства, медикаментозное лечение (ингибиторами АПФ, бета-блокаторами, триметазидином). И в том и в другом случае могут быть обеспечены хороший клинический эффект и благоприятный прогноз на выживание. При этом положительное воздействие реваскуляризации или медикаментозного лечения может быть значительно шире, нежели просто усиление сократимости акинетичных ранее сегментов. Например, усиление кровотока в эпикардиальных слоях жизнеспособного миокарда при мелкоочаговом инфаркте миокарда не изменит и так сохранившуюся сократительную способность, но будет предотвращено возможное ремоделирование левого желудочка, обеспечена большая электрическая стабильность миокарда, то есть будут предотвращены жизненно опасные аритмии. Если у пациента не выявлено жизнеспособного миокарда, то проведение АКШ или ангиопластики тоже возможно – для уменьшения клинических проявлений заболевания, в частности, стенокардии напряжения, – это позволит даже несколько улучшить качество жизни больного, при этом врач должен четко представлять, что даже удачно проведенная операция не изменит неблагоприятного прогноза пациента. Это же касается и симптоматиче ского медикаментозного лечения, способного дать лишь кратковременное клиническое улучшение. Как помочь этой самой тяжелой категории больных? В настоящее время единственной реальной альтернативой пессимистическому прогнозу является трансплантация сердца. Промежуточным и, как показывают клинические наблюдения последних лет, достаточно длительным этапом может стать имплантация искусственного левого желудочка в обход имеющегося. В перспективе, и может быть, не столь отдаленной, это будет подсадка в сердце генетически измененных собственных стволовых клеток для обеспечения роста новых кардиомиоцитов, а также стимуляция неоангиогенеза как с использованием медикаментозных средств или нейрогуморальных медиаторов, так и физических воздействий, например, прерывистой ишемии (прекондиционирования).
Список литературы Вы можете найти на сайте http://www.rmj.ru
Предуктал (торговое название)
1. Саидова М.А., Беленков Ю.Н., Атьков О.Ю., и др. Исследование жизнеспособности миокарда у больных ишемической болезнью сердца с выраженной дисфункцией левого желудочка и хронической недостаточностью кровообращения. Кардиология № 6: 20–4, 1998.
2. Саидова М.А. Возможности медикаментозного и хирургического восстановления сократимости жизнеспособного миокарда у больных ИБС и ДКМП с хронической недостаточностью кровообращения.
Автореферат докторской диссертации, М., 1999.
3. Braunvald E., Kloner RA., The stunned myokardium: Prolonged, postishemic ventricular disfunction. Circulation. 1982; 66: 1146–9.
4. Rahimtoola SH. A perspective on the three large multicenter randomized clinical trials of coronary bypass surgery for chronic stable angina. Circulation. 1985; 72 (V): 123–35.