Чудо-таблетку от коронавируса паксловид оценил российский иммунолог
Каков принцип действия новых средств от COVID-19
Несмотря на то, что таблетки еще не получили «добро» от FDA, об их поставках для своих граждан уже договорились Великобритания и Австралия. А подтолкнули их к этому публикации о предварительных результатах исследования. В эксперименте участвовали 775 взрослых пациентов, которые принимали по две таблетки паксловида два раза в день в течение пяти дней. В итоге число госпитализированных и умерших снизилась в этой группе по сравнению с контрольной, где принимали плацебо, на 88 процентов. Из тех, кто принимал препарат, нуждался в госпитализиции менее 1 процента пациентов при нулевом количестве умерших. Для сравнения, в контрольной группе было госпитализировано 7 процентов пациентов и семеро человек скончались.
— Паксловид — это оригинальный препарат, который действительно показывает сейчас в клинических исследованиях большую эффективность, – говорит Николай Крючков. – Однако предварил его появление, можно сказать, поднял информационную волну, другой препарат, о котором на несколько дней раньше заявили другие фармацевты. Это тоже эффективный противовирусный препарат молнупиравир, на который британский регулятор дал разрешение раньше, чем FDA. Правда, в отличие от паксловида он менее эффективен, снижает уровень госпитализаций и смертей только на 50 процентов.
Оба эти препарата на самом деле не отличаются особой новизной. Они создавались больше десяти лет назад как противогриппозные средства.
– В чем заключается их принцип действия?
Поскольку протеаза есть у гриппа и у многих других вирусов, паксловид изначально разрабатывали как универсальное средство.
– Почему именно на паскловид сделали сейчас ставку ученые? Ведь существует множество других универсальных противовирусных средств.
– Сходное с ним вещество несколько лет назад показало эффективность при инфекционном перитоните у кошек. Эту болезнь тоже вызывает коронавирусная инфекция. Поэтому разработчики и решили, что на других коронавирусах он тоже может сработать. Готовили его сначала для MERS, который не получил широкого распространения. Теперь, когда наступила пандемия SARS-CoV-2, он оказался самым эффективным. Но я думаю, что по окончании всех необходимых клинических испытаний, разрыв между двумя противоковидными лидерами будет меньше, к примеру, 50 и 70 процентов эффективности.
— На какие действующие препараты они похожи по эффективности?
— Таких нет. Даже несмотря на то, что применяемый сегодня в клиниках фавипиравир близок по принципу действия к молнупиравиру (также нарушает геном вируса), рядом его не поставишь. Как и другое средство – ремдесивир.
— У сильных препаратов могут быть ощутимые побочные эффекты. Какими отличаются паксловид и молнупиравир?
— Побочные эффекты, конечно, есть, я сейчас не могу их назвать. Но частота их появления – не больше 3-4 процентов случаев.
— Российские наработки для подобного рода сильных противовирусных средств есть?
— Нет. Хорошо, что хотя бы вакцины мы создать успели. Надо понимать, что препараты такого уровня создаются не на пустом месте. У американцев давно уже были патенты на похожие соединения.
Новости что за лекарство
Капсулы твердые желатиновые, №0, корпус и крышечка темно-коричневого цвета, непрозрачные.
| 1 таб. | |
| аторвастатина кальция тригидрат | 86.74 мг, |
| что соответствует содержанию аторвастатина | 80 мг |
Фармакологическое действие
Гиполипидемическое средство из группы статинов. По принципу конкурентного антагонизма молекула статина связывается с той частью рецептора коэнзима А, где прикрепляется ГМГ-КоА-редуктаза. Другая часть молекулы статина ингибирует процесс превращения гидроксиметилглутарата в мевалонат, промежуточный продукт в синтезе молекулы холестерина. Ингибирование активности ГМГ-КоА-редуктазы приводит к серии последовательных реакций, в результате которых снижается внутриклеточное содержание холестерина и происходит компенсаторное повышение активности ЛПНП-рецепторов и соответственно ускорение катаболизма холестерина (Xc) ЛПНП.
Гиполипидемический эффект статинов связан со снижением уровня общего Хс за счет Хс-ЛПНП. Снижение уровня ЛПНП является дозозависимым и имеет не линейный, а экспоненциальный характер. Ингибирующий эффект аторвастатина в отношении ГМГ-КоА-редуктазы примерно на 70% определяется активностью его циркулирующих метаболитов.
Статины не влияют на активность липопротеиновой и гепатической липаз, не оказывают существенного влияния на синтез и катаболизм свободных жирных кислот, поэтому их влияние на уровень ТГ вторично и опосредовано через их основные эффекты по снижению уровня Хс-ЛПНП. Умеренное снижение уровня ТГ при лечении статинами, по-видимому, связано с экспрессией ремнантных (апо Е) рецепторов на поверхности гепатоцитов, участвующих в катаболизме ЛППП, в составе которых примерно 30% ТГ. По сравнению с другими статинами (за исключением розувастатина) аторвастатин вызывает более выраженное снижение уровня ТГ.
Помимо гиполипидемического действия, статины оказывают положительное влияние при дисфункции эндотелия (доклинический признак раннего атеросклероза), на сосудистую стенку, состояние атеромы, улучшают реологические свойства крови, обладают антиоксидантными, антипролиферативными свойствами.
Аторвастатин снижает уровень холестерина у больных с гомозиготной семейной гиперхолестеринемией, которая обычно не поддается терапии гиполипидемическими средствами.
«Хороший новогодний подарок нам всем»: в России зарегистрировано самое дорогое лекарство в мире «Золгенсма»
«Глобальная новость»
Министерство здравоохранения РФ 9 декабря одобрило препарат онасемноген абепарвовек («Золгенсма») для лечения спинальной мышечной атрофии (СМА). Соответствующая информация опубликована на портале Государственного реестра лекарственных средств. Дата окончания регистрационного удостоверения — 9 декабря 2026 года.
Спинальная мышечная атрофия — тяжёлое генетическое заболевание, которое проявляется в постепенном отмирании отвечающих за движение мышц нейронов. Пациент (а чаще всего и в самых тяжёлых формах СМА проявляется у маленьких детей) сначала перестаёт ходить, потом сидеть, глотать и в итоге — дышать.
В мире зарегистрировано три лекарства, которые помогают остановить развитие заболевания: «Спинразу» (нусинерсен) и «Эврисди» (рисдиплам) необходимо принимать пожизненно, тогда как «Золгенсма» применяется однократно. Но именно этот препарат производства швейцарской компании Novartis считается самым дорогим в мире — стоимость единственного необходимого пациенту укола составляет порядка 160 млн рублей.
Как отмечает глава фонда «Семьи СМА» Ольга Германенко, «Спинраза» и «Эврисди» были зарегистрированы в России за девять и восемь месяцев соответственно. Процесс регистрации «Золгенсмы» продлился почти полтора года. Германенко полагает, что причина могла заключаться в том, что это первый таргетный препарат генной терапии в стране.
«Не сомневаюсь, что регуляторные органы и компания-производитель приложили все усилия, чтобы ускорить процесс, но новые технологии, новые нюансы, ранее не учтённые законодательством, требуют дополнительного времени на проработку, — пояснила она RT. — То, что регистрация такого лекарства всё-таки произошла, — это, мне кажется, глобальная новость и для пациентского сообщества, и для медиков, и для фармацевтической промышленности, поскольку открывает дверь для других таргетных генотерапевтических препаратов, в том числе и от других заболеваний».
Регистрация «Золгенсмы» в России, по мнению Ольги Германенко, повысит доступность препарата. Во-первых, упрощается и ускоряется сама процедура ввоза лекарства. Во-вторых, зарегистрированное лекарственное средство не требует проведения федерального консилиума, то есть может назначаться врачебной комиссией на местах, отмечает эксперт. А это значит, что не надо ждать своей очереди на госпитализацию в федеральный центр и ехать туда с другого конца страны, что жизненно важно для новых пациентов, у которых только выявили СМА.
«Конечно, в отдельных случаях, где возникают какие-то сомнения, лучше заручиться поддержкой федерального центра, но, по крайней мере, это уже не обязательно, — добавляет глава фонда «Семьи СМА». — Например, заключение федеральных специалистов может понадобиться, если пациенты уже лечатся и хотят сменить терапию».
Зарегистрированную «Золгенсму» теперь можно внести в клинические рекомендации и протоколы лечения пациентов, как до этого — «Спинразу» и «Эврисди», продолжает Ольга Германенко. До сих пор некоторые врачи ссылались на отсутствие препарата в этих документах (а незарегистрированное лекарство и не могло там появиться) и отказывались назначать его детям.
«Расширение рамок»
Также 9 декабря экспертный совет фонда «Круг добра» расширил возрастные рамки применения «Золгенсмы». С соответствующим предложением в сентябре 2021 года выступил председатель правления фонда Александр Ткаченко.
Ранее врачи ориентировались на инструкцию к препарату, согласно которой его можно вводить до достижения ребёнком двух лет. Летом 2020 года специалисты в ЕС, а затем и американские медики пришли к консенсусу, что критерий веса более важен, чем возраст, и стали ориентироваться на этот показатель, добавляет Германенко. Расширение возрастных рамок убирает противоречие между формальной трактовкой инструкции и реальной возможностью применения препарата.
«Решение открывает возможность для фонда обеспечивать лекарственным препаратом «Золгенсма» вновь выявленных детей со СМА, не получавших какой-либо патогенетической терапии, и детей со СМА, которые получали другое лечение и которым терапия препаратом «Золгенсма» будет назначена или рекомендована врачебной комиссией и подтверждена федеральным консилиумом», — уточнили в пресс-службе «Круга добра».
При этом участники заседания экспертного совета особо подчеркнули, что лечение «Золгенсмой» нельзя сочетать с другими видами патогенетической терапии, пока не будет доказано, что комбинировать или использовать одно лекарство от СМА после другого безопасно и эффективно.
«Круг добра», фонд поддержки детей с тяжёлыми, жизнеугрожающими и хроническими заболеваниями, включая редкие (орфанные), был создан в январе 2021 года указом президента России.
Помощь пациентам, в том числе закупка дорогостоящих лекарств, среди которых «Золгенсма», осуществляется за счёт повышенной ставки НДФЛ для доходов свыше 5 млн рублей в год. В августе 2021 года фонд и компания Novartis подписали договор о поставке «Золгенсмы». При этом, как сообщал Александр Ткаченко, в ходе переговоров удалось добиться «существенного, небывалого снижения цены».
Сейчас лекарства за счёт фонда получают 1076 детей со СМА, в том числе 21 ребёнок — «Золгенсму». Ольга Германенко надеется, что регистрация препарата даст возможности для переговоров с производителем о дополнительном снижении цены: «Препарат дорогой, и мы понимаем, что чем ниже будет цена, тем больше пациентов смогут получить необходимое лечение».
Подводный камень
«Сразу две хорошие новости практически одновременно. Мне кажется, это очень хороший новогодний подарок нам всем», — говорит глава фонда «Семьи СМА». Однако, по словам Ольги Германенко, в регистрации «Золгенсмы» есть один, но существенный подводный камень.
«После регистрации и до момента ввода препарата в гражданский оборот проходит от двух до шести месяцев, в течение которых компания-производитель должна выпустить российскую упаковку, положить в коробочки российскую инструкцию, включить лекарство в систему маркировки — в общем, ещё целый перечень задач, которые компания должна успеть выполнить как можно быстрее. Из-за всего этого препарат становится вообще недоступен к ввозу до завершения всех процедур. По нашему опыту, в среднем этот срок составляет четыре месяца», — говорит она.
Такая ситуация наиболее опасна для новых пациентов, у которых СМА только что выявили, или для тех, кто переходит на «Золгенсму» с другого вида терапии, в частности с лечения препаратом бранаплам, от исследований которого производитель отказался минувшим летом. «Очень страшно за них. Если препарат не сможет быть ввезён, то пациенты не смогут ждать несколько месяцев — и тогда нам нужно будет срочно начинать лечить их другими препаратами. В этой ситуации, конечно, хотелось бы поскорее найти решение», — отмечает Ольга Германенко.
Впрочем, по словам эксперта, решение этой проблемы начали искать заблаговременно. 7 декабря на заседании коллегии по вопросам обеспечения лекарственными препаратами, которое провёл министр здравоохранения России Михаил Мурашко, было предложено облегчить условия доступа к таким лекарствам, как «Золгенсма». В частности, предполагается проработать возможность обращения недавно зарегистрированных в РФ препаратов, которые ранее уже закупались «Кругом добра», в течение полугода после регистрации в зарубежной лекарственной упаковке.
Вирус жадности. «Главное российское лекарство» от COVID-19 оказалось пустышкой, закупленной в Китае и крайне токсичной
The Insider
Российские препараты от коронавируса «Авифавир» и «Коронавир» считаются отечественной разработкой, пропагандисты называли их революцией в медицине, сравнимой по масштабам с изобретением пенициллина. Госконтракты на их поставки уже превысили 10 млрд рублей. Но, как выяснил The Insider, российские фармкомпании на самом деле за ничтожные суммы закупили действующие вещества у китайских фирм, представленных на маркетплейсе Alibaba, причем никаких доказательств эффективности этих препаратов до сих пор нет. Более того, лекарство крайне токсично и опасно, но широко применяется без оглядки на серьезные побочные эффекты, среди которых проблемы развития плода и моторные нарушения. Торговля опасной пустышкой уже принесла фармкомпаниям миллиардные прибыли.
«Россия первой в мире зарегистрировала на сегодняшний день уже два препарата прямого противовирусного действия с доказанной эффективностью», — восторгался пропагандист Дмитрий Киселев в эфире «Вестей» в июле 2020 года. — И именно против COVID-19 это самые сильные на сегодняшний день „Авифавир” от компании „ХимРар” и „Арепливир” от „Промомеда”. Они предотвращают размножение вируса в организме, а эффективность этих таблеток по результатам клинических исследований — 90%. Лучших результатов против COVID-19 пока нет ни у одного другого лекарственного средства в мире».
Правда в словах пропагандиста была только в одном: весной 2020 года Минздрав действительно одобрил «Авифавир», «Арепливир» и «Коронавир» для лечения коронавирусом, и действительно нигде в мире «противовирусные» средства против коронавируса не использовались. В основе этих препаратов на самом деле лежит действующее вещество фавипиравир, которое было изобретено и запатентовано в Японии в начале 2000-х как средство от тяжелого течения гриппа, а также испытывалось на пациентах с вирусом Эболы, но в массовом производстве фавипиравир в итоге никогда не был и в самой Японии не применялся, так как его эффективность доказать не удалось.
Однако в середине марта 2020 года официальные лица Китая внезапно заявили о высокой эффективности фавипиравира против коронавируса. Именно тогда целый ряд крупных российских компаний — «Р-Фарм», «Промомед», а также фирма «ХимРар» при поддержке Российского фонда прямых инвестиций (РФПИ) приняли решение наладить производство российского аналога. «В марте мы услышали новость, что среди сотен препаратов, испытываемых в КНР, один показал прорывные результаты, в два раза улучшив результаты лечения», — так описывал начало работ над препаратом председатель совета директоров «ХимРара» Андрей Иващенко на одной из пресс-конференций.
Буквально за месяц при поддержке РФПИ дочерняя компания «ХимРар» — фирма «Кромис» — не просто воссоздала препарат, но 23 апреля зарегистрировала в Минздраве начало клинического исследования «Авифавира» с 60 добровольцами. Официально оно продолжалось до 31 декабря 2020 года, а число участников расширили до 300 человек. Но на самом деле итогов исследования никто не ждал: уже в конце мая 2020 года препарат начали применять для лечения пациентов.
Такой успех производители в «ХимРар» объясняли тем, что пять лет назад компания уже работала над похожим препаратом и синтезировала химию фавипиравира. РФПИ и «ХимРар» настаивали, что им удалось самостоятельно синтезировать действующее вещество и проверить его на эффективность в кратчайшие сроки. В мае телеканал «Россия-1» показал сюжет, где говорилось, что на синтез лекарства у «ХимРара» ушло две недели, а купить ни сам препарат, ни сырье для него «не удалось ни одной стране мира»
Тонны веществ из Китая
Как удалось выяснить The Insider, в действительности у препарата «Авифавир» было китайское происхождение — российские фармкомпании просто по дешевке закупили «ингредиенты» на китайском рынке.
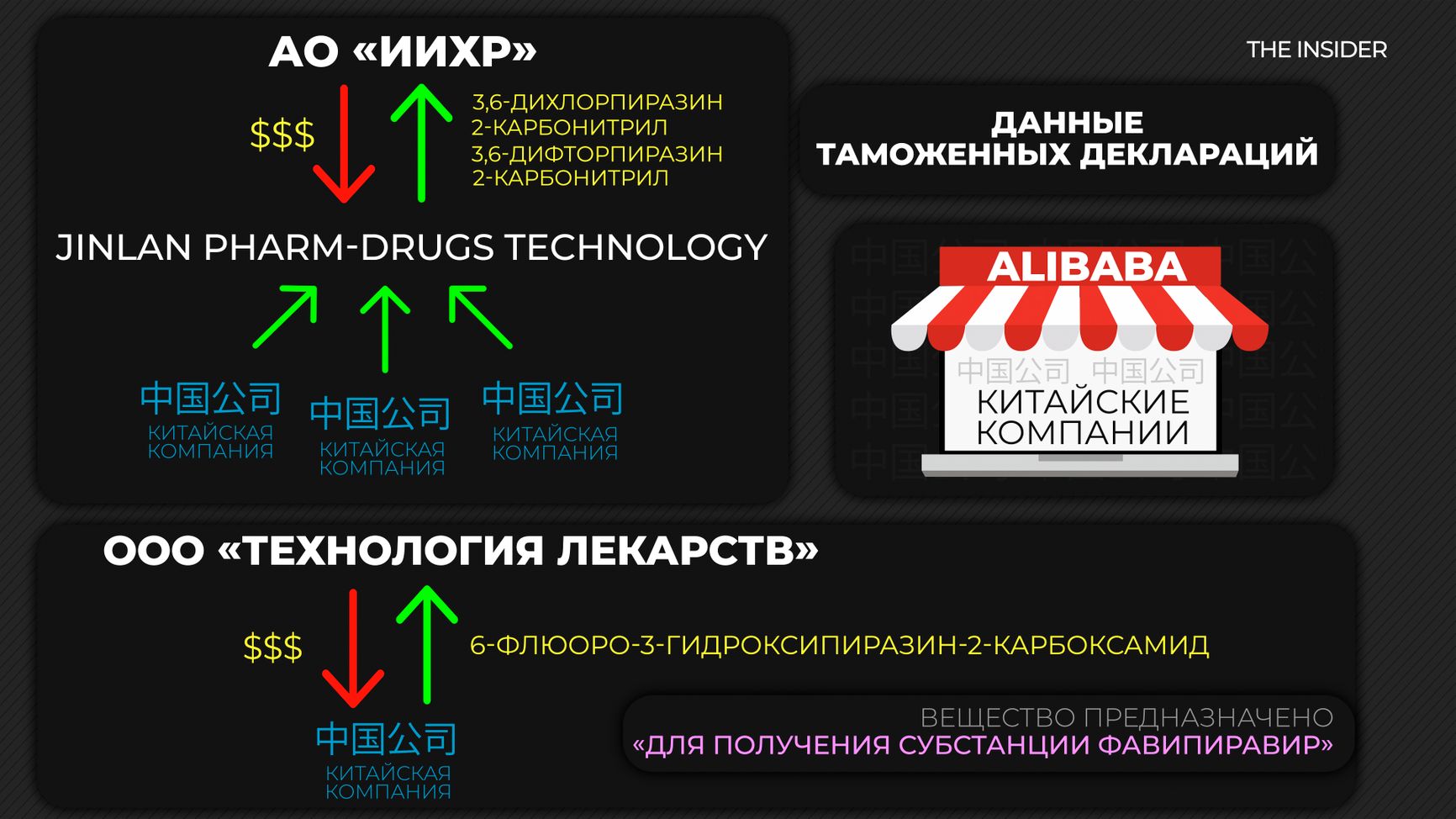
В распоряжении редакции имеются номера деклараций на ввоз вещества. Так, 2 и 6 апреля, а затем 11 мая и 18 июня на производство компании «ХимРар» в Химках от китайского поставщика приехали почти 90 кг веществ, из которых за несколько операций можно получить фавипиравир. Задекларированная стоимость интермедиатов — всего 23 млн рублей, ничтожная сумма по сравнению с миллиардными бюджетами госзакупок. По оценке китайского продавца, компании Jinlan Pharm-Drugs Technology Co., из такого количества можно изготовить десятки тысяч таблеток — с ним корреспондент The Insider общался на маркетплейсе Alibaba, где в 2020 году был представлен магазин компании, и в нем можно было купить субстанцию фавипиравира. В 2021 году купить эту субстанцию на Alibaba уже невозможно — по требованию лицензиата такие товары были заблокированы. Однако на сайте поставщика ссылка на товар все еще имеется.
Аналогично «ХимРару» действовали и остальные российские компании. Судя по данным таможни, 30 мая 2020 года дочерняя компания «Р-Фарм» — «Технология лекарств» — получила 5 бочек с 50 кг уже готового фавипиравира. Вещество обошлось фирме в 48 млн рублей. В общей сложности, как оказалось, с начала 2020 года компания «Р-Фарм» ввезла в Россию почти 4 тонны субстанции для приготовления таблеток фавипиравира. Об этом свидетельствуют данные базы таможенных деклараций Import Genius.
Тот факт, что дочерние компании «ХимРара» и «Р-Фарм» на самом деле импортировали субстанцию для производства лекарств, The Insider подтвердили два независимых источника в фармацевтической отрасли.
Закупленное российскими компаниями вещество — это промежуточный продукт, получающийся ближе к концу синтеза финального вещества. К такому выводу пришли пожелавшие сохранить анонимность специалист по разработке лекарств и химик-синтетик одного из российских фармпроизводителей, изучившие по просьбе The Insider декларации «Р-Фарм» и «ИИХР».
«Обычно синтез начинается с более простых молекул, которые не имеют такой относительно сложно-разветвленной структуры», — поясняет специалист по разработке лекарств. Из веществ, закупленных «ИИХР», в три стадии получается фавипиравир, говорит химик-синтетик, по его подсчетам, этого объема должно хватить на 460 курсов или 33 тысячи таблеток. «Но у таких покупок есть риски. В начале синтеза промежуточного вещества могли не соблюдаться какие-то условия и реакции шли не в идеальных условиях, а значит, продукт может содержать примеси», — говорит фармаколог.
Между тем продавцы вещества, которые поставляли вещество из Китая российским фармкомпаниям, не смогли подтвердить корреспонденту The Insider, что они сами производят этот препарат, а не закупают его где-то еще. Зато они утверждают, что вещества пользуются большим спросом у покупателей из России, и из Китая их поставляют «тоннами».
Туманный патент и опасные модификации
Но могли ли российские компании все-таки действительно синтезировать вещество самостоятельно?
Теоретически в сжатые сроки воспроизвести молекулу активного вещества возможно. В таких случаях используется патент оригинального производителя, но само описание синтеза в нем, как правило, «туманно», рассказывает The Insider научный сотрудник одного из российских фармпроизводителей (химик-синтетик). Компании специально так составляют патенты, чтобы защитить свою интеллектуальную собственность.
Профессор НИУ-ВШЭ, президент Общества специалистов доказательной медицины Василий Власов считает, что за месяц можно синтезировать субстанцию, но наладка индустриального синтеза может занимать месяцы. Такого же мнения придерживается и специалист по разработке и регулированию лекарств. «Быстро разработать технологию промышленного производства невозможно. При ее создании проводятся пуско-наладочные испытания, не одна и не две опытные серии, никто не обкатанную технологию, которая существует только на бумаге, не начнет использовать для получения препарата», — говорит он.
Отдельные вопросы у профессионального сообщества вызывают сообщения гендиректора «ХимРара» Иващенко о том, что компании удалось модифицировать препарат. «В отношении лекарств никакие скрытые модификации недопустимы. Если они модифицировали что-то, то какой противовирусной активностью этот препарат обладает?» — говорит специалист-фармаколог. С ним согласен и Власов: «Если препарат изменен и воспроизведен не фавипиравир, то это лекарство должно проходить полный цикл клинических исследований».
Исследования на добровольцах
Первое исследование фавипиравира на эффективность против COVID-19 было зарегистрировано в Китае в середине февраля 2020 года. Первые результаты казались вполне обнадеживающими: госпитализированные пациенты быстрее избавлялись от вируса, а снимки грудной клетки показывали положительную динамику. Исследование с самой большой выборкой пациентов прошло также в Китае в конце февраля. В нем фавипиравир сравнивали с арбидолом (как с плацебо), и лекарство не показало эффективности. В исследовании участвовали 240 человек.
Параллельно началось сравнение эффективности фавипиравира с калетрой — лекарством от ВИЧ, которое во всем мире пробовали применять также от нового коронавируса. Для исследования отобрали 80 человек. Результаты фавипиравира оказались немного лучше калетры, однако в опубликованной в итоге статье говорится, что, так как выборка пациентов была маленькой, а дизайн исследования не совсем корректный, его нельзя считать доказательством эффективности фавипиравира, и требуются дополнительные исследования. Однако именно на эту статью ссылается Минздрав России, поясняя, почему выбрал фавипиравир как рекомендованное лекарство. Статья с результатами исследования была опубликована 18 марта, и ровно в этот же день китайский регулятор поспешил заявить об эффективности китайского лекарства от нового вируса.
В Великобритании, Франции, США, на Ближнем Востоке и в Южной Азии проводили свои исследования эффективности фавипиравира. Однако, во-первых, они исследовали оригинальный японский препарат, который производится под маркой «Авиган» или индийские лицензионные дженерики. Во-вторых, хотя некоторые из таких исследований показали эффективность препарата по сравнению с другими антивирусными лекарствами (например, ремдесивиром), речь шла о легкой и среднетяжелой форме коронавируса, так что даже если бы этим результатам можно было доверять, они все равно нерелевантны — препарат очень токсичен, и потому для лечения легких форм коронавируса применяться все равно не может.
В крупнейшей мировой базе данных о клинических исследования препаратов ClinicalTrials есть информация о том, что исследование «Авифавира» в июне 2020 года одновременно в 22 больницах проводила профессор МГУ Елена Павликова и доктор медицинских наук Никита Ломакин из ЦКБ. В августе 2020 года они опубликовали результаты исследования в журнале Clinical Infectious Diseases. Однако оказалось, что исследование спонсировали РФПИ и инновационный центр «Сколково», резидентом которого является производитель лекарства — «Химрар». Всего в исследовании участвовали 60 человек, 40 из которых получали авифавир и другие лекарства (какие — не указано), а 20 — разные антивирусные препараты, в основном гидроксихлорохин, наравне с антибиотиками и жаропонижающими. Два человека с более тяжелым течением болезни скончались за время исследования. Авторы приходят к выводу о том, что «Авифавир» работает лучше «стандартной терапии», хотя по истечении 10 дней лечения p-критерий (уровень значимости полученных результатов, определяющий, насколько статистически значим исход эксперимента) составлял 0,155. Чем больше этот показатель, тем больше вероятность того, что полученный результат скорее случаен, чем является следствием проведенных манипуляций. В медицине обычно используется в качестве порогового показатель p-критерия не больше 0,05, иногда 0,01, то есть российские исследователи на порядок отклонились от стандартных требований. Авторы исследования подчеркивают, что именно эти клинические испытания на 60 добровольцах стали причиной того, что препарат был включен в рекомендации Минздрава.
«Этот препарат изначально исследовали против обычного гриппа, и он показал очень маленькую эффективность. Поэтому в виду его токсичности его нигде не разрешили. Разрешили только в Японии и то, как запасной вариант. В Японии также проводилось исследование его эффективности против коронавируса. И это исследование также не показало большой эффективности. В России были исследования фавипиравира, но все они очень низкого качества. Ими руководил уролог Дмитрий Пушкарь, почему это доверили урологу?», — поражается эпидемиолог Василий Власов. В мае 2020 года главный уролог Минздрава России Дмитрий Пушкарь рассказывал «Российской газете», что в Японии препарат «пришелся очень ко двору при лечении различных вирусных инфекций, включая самые сложные», хотя в действительности он никогда не применялся против болезней, а только исследовался для лечения гриппа и вируса Эбола.
Японская компания разработчик Fujifilm Toyama Chemical еще в сентябре 2020 году сообщила о низких показателях эффективности вещества фавипиравир — по данным их исследования, те, что принимали препарат, выписались из больницы через 12 дней, те, кому давали плацебо, — через 15. «Продолжительность заболевания что двенадцать, что четырнадцать дней — для меня одно и то же. Получается, что сумму в 20–25 тысяч рублей вы платите за сокращение лечения на два дня. И при этом нет данных о снижении смертности: уменьшает этот препарат ее или нет», — говорил в интервью «Известиям» доктор биологических наук, профессор, член-корреспондент РАН, заведующий лабораторией биотехнологии и вирусологии факультета естественных наук НГУ Сергей Нетесов.
Результаты клинического исследования одной из крупнейших фармкомпаний России АО «Р-Фарм» были опубликованы в сентябре 2020 года в российском журнале «Медицинский оппонент». В исследовании участвовала медицинский директор ООО «Технология лекарств» Ольга Филон, финансировалось исследование компанией «Р-Фарм». В испытаниях также участвовали 60 человек, 40 из которых получали фавипиравир, а еще 20 — другие препараты, которые авторы не раскрывают. Кроме того, почти все пациенты получали антибиотики, антикоагулянты и жаропонижающие, то есть стандартную одобренную Минздравом терапию. В отличие от исследования «Химрара», специалисты не привлекли к испытаниям тяжело больных пациентов, и ни один пациент не скончался. Время уничтожения вируса в организме пациентов, получавших фавипиравир, практически не отличалось от остальных пациентов, улучшение состояния пациентов наступало на 3,5 дня раньше.
Практика, при которой фармкомпании финансируют клинические испытания собственных препаратов, считается сомнительной в научном сообществе. К примеру, британский автор Бен Голдакр в своей книге «Вся правда о лекарствах: мировой заговор фармкомпаний» (Bad Pharma: How Drug Companies Mislead Doctors and Harm Patients) приводит статистику того, что чаще всего такие исследования комплиментарны, а исследования, в которых эффективность препарата не была доказана, просто не публикуются. Кроме того, исследования часто имеют плохой дизайн, проводятся на небольшом количестве испытуемых (как произошло, к примеру, в случае с российскими дженериками фавипиравира), а результаты могут быть искажены в пользу определенного препарата.
В то время как эффективность фавипиравира крайне сомнительна, его опасные побочные эффекты, напротив, хорошо доказаны. Из-за своей токсичности препарат запрещен детям, беременным, кормящим женщинам, а также людям с тяжелой печеночной или почечной недостаточностью. Из-за высокой вероятности негативного влияния на плод людям, принимавшим препарат, рекомендовано в течение нескольких месяцев уделять особенное внимание контрацепции. Также, при исследовании в Японии было выявлено, что применение препарата может приводить к моторным нарушениям у пациентов: синдрому беспокойных ног, а также повышенному риску падений. Эксперты считают, что это может быть связано с воздействием лекарства на центральную нервную систему.
Препараты с такой высокой токсичностью обычно применяются только в случаях, когда их эффективность высока и пациент находится в тяжелом состоянии, то есть риски от болезни перевешивают риски от применения препарата. Кроме того, токсичные препараты применяются только в больницах под строжайшим контролем врачей. В случае с российскими дженериками фавипиравира все эти требования были нарушены.
Несколько сотрудников московских госпиталей, специализирующихся на лечении коронавируса, подтвердили The Insider, что лекарства на основе фавипиравира («Коронавир» и «Авифавир») регулярно выдаются пациентам и стоят в планах лечения тяжело больных. «Изначально фармкомпании зарегистрировали российские аналоги как лекарство против тяжелых случаев болезни, которое, в силу его токсичности, должно применяться в больницах. Но на практике его выдают и при легкой форме [во время лечения на дому]», — отмечает Власов.
Врач-терапевт одной из московских поликлиник также подтвердил The Insider, что все подтвержденные случаи Covid-19 сейчас даже при домашнем режиме в Москве лечатся российскими дженериками фавипиравира.
Деньги не заразны
Массовые поставки «Авифавира» в регионы страны начались еще в июне 2020 года и с тех пор наращиваются. По расчетам The Insider на основании данных портала госзакупок, к 1 августа 2021 года власти закупили российского дженерика не менее чем на 10 млрд рублей. Только компания «Р-Фарм» напрямую поставила в больницы препарат на сумму около 5 млрд рублей. Большая часть торгов была оформлена как закупка у единственного поставщика.
Первые упаковки «Авифавира», вышедшие на рынок, продавались больницам по цене в 22 тысячи рублей за 40 таблеток — фантастически высокая цена, учитывая закупочную стоимость фавипиравира в Китае (не говоря уже о том, что любая цена за неэффективное лекарство слишком высокая). Когда на рынок вышел «Коронавир», его цена для разных больниц колебалась от 3 до 5 тысяч рублей за пачку из 50 таблеток. Осенью 2020 года препарат вышел и в розничную продажу, в аптеках он стоит в районе 5 тысяч рублей за пачку. При этом на родине препарата в Японии его продажа в рознице строго запрещена и разрешено только применение в стационаре.