Нуклеиновый обмен что это
О значении нуклеопротеидов и нуклеиновых кислот было указано выше (см. Химия нуклеопротеидов) Помимо их главной роли в хранении и реализации наследственной информации, следует указать на важную регуляторную функцию адениловой системы и свободных нуклеотидов, контролирующих в качестве коферментов скорость метаболических процессов. С другой стороны, нет никаких экспериментальных доказательств, что нуклеиновые кислоты являются незаменимыми пищевыми факторами и вряд ли играют существенную роль в качестве энергетического материала. Поскольку структурными мономерными компонентами нуклеиновых кислот являются мононуклеотиды, состоящие в свою очередь из азотистых оснований, пентоз и фосфорной кислоты, естественно, будут рассмотрены (помимо краткого изложения вопросов переваривания и всасывания нуклеиновых кислот) проблемы метаболизма этих индивидуальных блоков нуклеиновых кислот, как и самих макромолекул. В частности, будут детально изложены пути биосинтеза и распада пуриновых и пиримидиновых нуклеотидов, современные представления о механизмах синтеза и деградации ДНК и РНК в живых организмах, а также участие нуклеиновых кислот в биосинтезе белка.
В первом приближении обмен нуклеиновых кислот можно представить в следующем общем виде (по Кантарову и Шепартцу):
Всасываются преимущественно нуклеозиды, и в таком виде часть азотистых оснований может быть использована для синтеза нуклеиновых кислот организма. Если же происходит дальнейший распад нуклеозидов до свободных пуриновых и пиримидиновых оснований, то гуанин не используется для синтетических целей. Что касается других оснований, то, как показывают опыты с меченным по азоту аденином и урацилом, в тканях они могут включаться в состав нуклеиновых кислот. Однако экспериментальные данные свидетельствуют о том, что биосинтез азотистых оснований, входящих в состав нуклеиновых кислот органов и тканей, протекает преимущественно, если не целиком, de novo из низкомолекулярных азотистых и безазотистых предшественников.
Обмен нуклеотидов
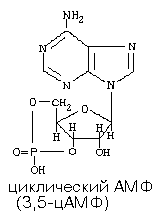
Нуклеотиды являются вездесущими компонентами жизни, участвуя в большинстве биохимических реакций. АТФ является энергетической валютой клетки, производные аденина служат коферментами, циклические нуклеотиды цAMФ и цГМФ играют роль вторичных мессенджеров. Наконец, нуклеотиды — это мономерные звенья РНК и ДНК.
Пути биосинтеза нуклеотидов служат мишенью для противоопухолевых и некоторых антибактериальных препаратов, а нарушения в путях их катаболизма ловят ступни в капкан.
Строение нуклеотидов
Нуклеотиды состоят из трех компонентов: азотистого основания, пентозы и фосфата. Нуклеотид без фосфата называется нуклеозидом. Азотистые основания — это производные пурина и пиримидина (рис. 1).
Рисунок 1. | Главные азотистые основания. Некоторые названия отражают историю открытия этих соединений. Гуанин был выделен из перуанского гуано (птичьего помета), тимин — из тимуса быка, аденин — из поджелудочной железы. Урацил получил свое название от мочевой кислоты, из которой его пытались синтезировать. Б. Структурная формула нуклеотидов. В дезоксирибонуклеотидах OH-группа при 2’-углероде замещена на H.
В ДНК и РНК пуриновые основания одинаковые — аденин и гуанин, а пиримидиновые разные: в ДНК тимин, в РНК урацил и в обеих цитозин. Дезоксирибонуклеотиды, образующие ДНК, содержат 2’-дезокси-D-рибозу, а рибонуклеотиды РНК — D-рибозу. Термин «нуклеотид» может обозначать как рибо-, так и дезоксирибоформы.
Биосинтез пуринов
Синтез пуринов de novo сложен и энергозатратен, поэтому в физиологических условиях пул пуринов поддерживается в основном за счет путей их реутилизации (исключение составляют быстроделящиеся клетки). Всасывание нуклеотидов из пищи мало, так как почти все остатки нуклеиновых кислот катаболизируются эпителием тонкой кишки.
Аденин и гуанин образуются из общего предшественника — инозината (IMP). Пуриновое ядро постепенно собирается на остатке 5-Фосфорибозил-1-пирофосфата (PRPP). Все четыре атома азота происходят из аминокислот: два из глутамина, один из аспартата и один из глицина (рис. 2–4).
Рисунок 2. | Синтез пуриновых нуклеотидов de novo: часть 1, образование пуринового кольца инозината. После стадии ③ R обозначает 5-фосфо-D-рибозильную группу. Снизу изображено происхождение атомов пуринового кольца.
Зависимость синтеза пуринов от фолатов на стадиях 3 и 9 означает, что ингибиторы метаболизма фолиевой кислоты являются непрямыми ингибиторами синтеза пуринов, а значит, и ингибиторами деления клетки.
Рисунок 3. | Биосинтез AMP и GMP из IMP.
Регуляция этого пути сложна и мало изучена. Известно, что AMP, GMP и IMP ингибируют его по механизму отрицательной обратной связи. В недавних исследованиях [1] было показано, что шесть ферментов биосинтеза пуринов собираются в пуриносому, являющую собой новый уровень организации ферментов.
Рисунок 4. | Обзорная схема синтеза пуриновых нуклеотидов.
Реутилизация пуринов
Свободные пуриновые основания постоянно высвобождаются в клетке в процессе катаболизма нуклеотидов, и их большая часть повторно используется для синтеза нуклеотидов в более простом пути, нежели синтез de novo.
Один из таких путей настолько прост, что состоит из одной реакции, катализируемой аденозинфосфорибозилтрансферазой: Аденин + PRPP → AMP + PPi
Свободный гуанин и гипоксантин реутилизируются в похожем пути под действием гипоксантин-гуанин-фосфорибозилтрансферазы. Мутация гена вышеназванного фермента вызывает синдром Лёша — Нихена. Это сцепленное с мужским полом заболевание, манифестирующее в раннем возрасте и характеризующееся деформирующим артритом и неврологическими нарушениями. Мальчики с синдромом Лёша — Нихена плохо ориентируются в пространстве, очень враждебны и склонны к саморазрушению вплоть до откусывания себе пальцев.
Биосинтез пиримидинов
Если при синтезе пуриновых нуклеотидов азотистое основание кусочек за кусочком собирается на остатке рибозилфосфата, то при синтезе пиримидинов к рибозе оно присоединяется уже в готовом виде (рис. 5).
Рисунок 5. | Синтез пиримидиновых нуклеотидов. Стадия 1: Синтез карбамоилфосфата. 2: Конденсация аспартата и карбамоилфосфата с образованием N-карбамоиласпартата. 3: Внутримолекулярная конденсация, катализируемая дигидрооротазой с образованием шестичленного гетероцикла (дигидрооротата). 4: Окисление дигидрооротата до оротата. 5: присоединение к оротату рибозо-5-фосфата (PRPP). 6: Декарбоксилирование оротодилата до уридилата. Ферменты 5 и 6 стадий образуют комплекс и называются УМФ-синтазой.
Источник: Campbell M. K., Farell S. O. Biochemistry
Мутации гена UMPS, кодирующего УМФ-синтазу вызывают оротацидурию — редкое (описано лишь 20 случаев) аутосомно-рецессивное заболевание, проявляющееся тяжелой мегалобластной анемией, задержкой развития вследствие дефицита пиримидиновых нуклеотидов и повышенным содержанием оротовой кислоты в моче.
Нуклеозидмонофосфаты превращаются в нуклеозидтрифосфаты под действием нуклеозидмонофосфаткиназ и нуклеозиддифосфаткиназ. Последние необычны тем, что являются неспецифичными ни по основанию, ни по пентозе.
Цитидилатсинтетаза образует цитидилат из UTP.
Прежде чем описать синтез тимидилата, необходимо упомянуть об образовании дезоксирибонуклеотидов, так как его синтез de novo возможен только из дезоксирибонуклеотидного предшественника.
Образование дезоксирибонуклеотидов
Строительные блоки ДНК образуются из соответствующих рибонуклеотидов непосредственным восстановлением 2’-углеродного атома рибозы с образованием 2’-дезоксипроизводного. Реакция катализируется рибонуклеотидредуктазой, ее субстраты — нуклеозиддифосфаты, в ней также участвуют тиоредоксин и тиоредоксинредуктаза.
Рисунок 6. | Восстановление рибонуклеотидов до дезоксирибунклеотидов.
Регуляция рибонуклеотидредуктазы весьма необычна и служит для поддержания баланса четырех нуклеотидов, необходимых для синтеза ДНК. Каждая субъединица имеет 2 типа регуляторных центров: один центр регулирует активность (ATP +, dATP-), второй влияет на субстратную специфичность. Например, если со вторым центром связывается ATP или dATP, фермент начинает отдавать предпочтение восстановлению UDP или CDP, а когда UTP и СTP становится слишком много, возвращается к ADP. ATP выступает главным стимулятором восстановления всех рибонуклеотидов, а dATP в больших концентрациях выключает фермент.
Биосинтез тимидилата
Непосредственный предшественник тимидилата — dUMP. Превращение катализируется тимидилатсинтазой и сопряжено с окислением метилентетрагидрофолата до дигидрофолата (рис. 7).
Рисунок 7. | Синтез тимидилата.
Источник: Campbell M. K., Farell S. O. Biochemistry
Синтез тимидилата является мишенью некоторых противоопухолевых препаратов. Так, в химиотерапии используется ингибитор тимидилатсинтазы — фторурацил (вернее, его метаболит FdUMP), ингибитор дигидрофолатредуктазы — аминоптерин и структурный аналог фолата — метотрексат. Потребность раковых клеток в нуклеотидах гораздо выше, чем у нормальных клеток, поэтому они более чувствительны к ингибиторам биосинтеза тимидилата.
Катаболизм нуклеотидов
Катаболизм пиримидинов
С помощью нуклеотидазы и фосфорилазы от пиримидиновых нуклеотидов отщепляются фосфаты и рибоза, а оставшиеся свободные азотистые основания подвергаются дезаминированию и гидрированию (рис. 8).
Рисунок 8. | Катаболизм пиримидинов. Источник: Campbell M. K., Farell S. O. Biochemistry
Пути распада пиримидинов ведут главным образом к NH4+ и далее к мочевине.
Катаболизм пуринов
Пуриновые нуклеотиды теряют свои фосфаты под действием 5’-нуклеотидазы.
Аденилат превращается в аденозин, который дезаминируется аденозиндезаминазой (ADA) с образованием инозина, который гидролизуется нуклеозидазой до гипоксантина и рибозы. Ксантиноксидаза окисляет гипоксантин до ксантина и затем до мочевой кислоты. (рис. 9)
Рисунок 9. | Катаболизм пуриновых нуклеотидов. Общий метаболит катаболизма пуринов — ксантин. Превращение ксантина в мочевую кислоту катализирует ксантиноксидаза. В правом верхнем углу изображена аденозиндезаминаза (ADA)
У большинства млекопитающих мочевая кислота окисляется до более растворимого соединения — аллантоина, однако у человека, далматинов, приматов и птиц она является конечным экскретируемым продуктом катаболизма пуринов, и здесь время поговорить о подагре.
Заболевания, связанные с катаболизмом пуринов
1. Гиперурикемия и подагра.
Повышенное содержание мочевой кислоты в крови называется гиперурикемией (> 360 мкмоль/л для женщин и > 400 мкмоль/л для мужчин). У этого состояния может быть множество причин: дефект генов, отвечающих за экскрецию уратов почками и кишечником, богатая пуринами и/или фруктозой диета, низкоуглеводная диета, голодание, синдром лизиса опухоли, прием препаратов (диуретиков, аспирина, никотиновой кислоты и др.), синдром Лёша-Нихена, большие дозы алкоголя и другие, но всех их можно поделить на два типа: гиперпродукция уратов и снижение их экскреции. Гиперурикемия далеко не всегда сопровождается подагрой, но подагра гиперурикемией — всегда. Подагра — это метаболическое заболевание, характеризующееся отложением кристаллов уратов натрия преимущественно в плюснефаланговых суставах, поражением почек и приступами острого подагрического артрита.
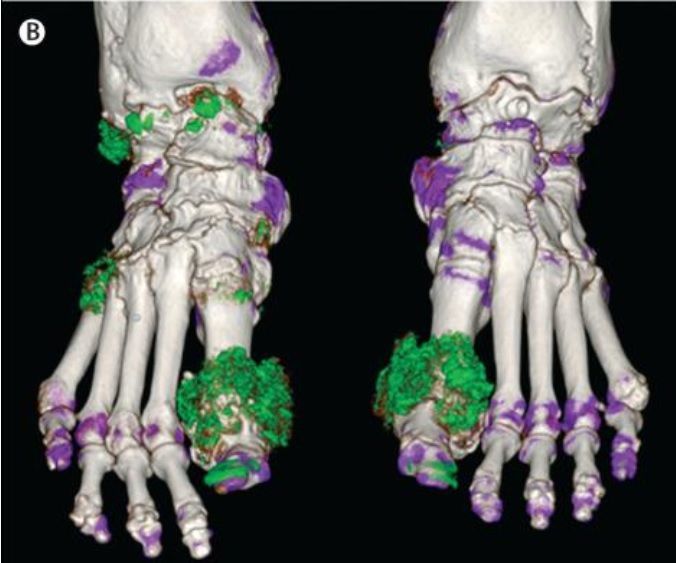
Рисунок 10. | Двухэнергетическая КТ стоп пациента с тофусной подагрой. Депозиты урата показаны зеленым цветом ( на ногтях – артефакт)
Этиология, патогенез и терапия подагры заслуживают отдельной статьи. Здесь я упомяну только о препаратах, влияющих на катаболизм пуриновых нуклеотидов, — ингибиторах ксантиноксидазы (фермента, превращающего ксантин в мочевую кислоту, см. рис. 9). Один из них — аллопуринол, структурный аналог гипоксантина, конкурентный ингибитор ксантиноксидазы. К неконкурентным ингибиторам относится фебуксостат. Оба препарата снижают уровень мочевой кислоты в крови и используются для предотвращения приступов подагры.
2. Дефицит аденозиндезаминазы ведет к одному из типов тяжёлого комбинированного иммунодефицита (SCID, синдром Глянцмана — Риникера, в 30 % случаев вызывается дефицитом ADA), характеризующемуся неспособностью T- и B- лимфоцитов к пролиферации и продукции антител.
Отсутствие аденозиндезаминазы ведет к значительному накоплению dATP, который ингибирует нуклеотидредуктазу, в результате чего возникает дефицит всех дезоксирибонуклеотидов (рис. 11). ADA является Zn-зависимым ферментом, поэтому нарушения в делении лимфоцитов возможны и при дефиците в организме цинка.
Рисунок 11. | Недостаточность аденозиндезаминазы приводит к нарушениям репликации ДНК
Глава 13. ОБМЕН СЛОЖНЫХ БЕЛКОВ
ОБМЕН НУКЛЕИНОВЫХ КИСЛОТ
Нуклеиновые кислоты составляют существенную небелковую часть сложного класса органических веществ, получивших название нуклеопротеинов (см. главу 2); последние являются основой наследственного аппарата клетки хромосом. Белковые компоненты нуклеопротеинов подвергаются многообразным превращениям, аналогичным метаболизму белков и продуктов их распада – аминокислот, подробно рассмотренному в главе 12. О нуклеиновых кислотах, их структуре и функциях в живых организмах в последнее время накоплен огромный фактический материал, подробно рассмотренный в ряде специальных руководств и монографий. Помимо уникальной роли нуклеиновых кислот в хранении и реализации наследственной информации, промежуточные продукты их обмена, в частности моно-, ди- и трифосфатнуклеозиды, выполняют важные регуляторные функции, контролируя биоэнергетику клетки и скорость метаболических процессов. В то же время нуклеиновые кислоты не являются незаменимыми пищевыми факторами и не играют существенной роли в качестве энергетического материала. Далее детально рассматриваются (помимо краткого изложения вопросов переваривания) проблемы метаболизма нуклеиновых кислот и их производных, в частности пути биосинтеза и распада пуриновых и пиримидиновых нуклеотидов, современные представления о биогенезе ДНК и РНК и их роли в синтезе белка.
Переваривание нуклеопротеинов и всасывание продуктов их распада осуществляются в пищеварительном тракте. Под влиянием ферментов желудка, частично соляной кислоты, нуклеопротеины пищи распадаются на полипептиды и нуклеиновые кислоты; первые в кишечнике подвергаются гидролитическому расщеплению до свободных аминокислот. Распад нуклеиновых кислот происходит в тонкой кишке в основном гидролитическим путем под действием ДНК- и РНКазы панкреатического сока. Продуктами реакции при действии РНКазы являются пуриновые и пи-римидиновые мононуклеотиды, смесь ди- и тринуклеотидов и резистентные к действию РНКазы олигонуклеотиды. В результате действия ДНКазы образуются в основном динуклеотиды, олигонуклеотиды и небольшое количество мононуклеотидов. Полный гидролиз нуклеиновых кислот до стадии мононуклеотидов осуществляется, очевидно, другими, менее изученными ферментами (фосфодиэстеразами) слизистой оболочки кишечника.
В отношении дальнейшей судьбы мононуклеотидов существует два предположения. Считают, что мононуклеотиды в кишечнике под действием неспецифических фосфатаз (кислой и щелочной), которые гидролизируют фосфоэфирную связь мононуклеотида («нуклеотидазное» действие), расщепляются с образованием нуклеозидов и фосфорной кислоты и в таком виде всасываются. Согласно второму предположению, мононуклеотиды всасываются, а распад их происходит в клетках слизистой оболочки кишечника. Имеются также доказательства существования в стенке кишечника нуклеотидаз, катализирующих гидролитический распад моно-нуклеотидов. Дальнейший распад образовавшихся нуклеозидов осуществляется внутри клеток слизистой оболочки преимущественно фосфороли-тическим, а не гидролитическим путем.
Всасываются преимущественно нуклеозиды, и в таком виде часть азотистых оснований может быть использована для синтеза нуклеиновых кислот организма. Если происходит дальнейший распад нуклеозидов до свободных пуриновых и пиримидиновых оснований, то гуанин не используется для синтетических целей. Другие основания, как показывают опыты с меченными по азоту аденином и урацилом, в тканях могут включаться в состав нуклеиновых кислот. Однако экспериментальные данные свидетельствуют, что биосинтез азотистых оснований, входящих в состав нуклеиновых кислот органов и тканей, протекает преимущественно, если не целиком, de novo из низкомолекулярных азотистых и безазотистых предшественников.
Таким образом, синтез нуклеиновых кислот, мономерными единицами которых являются мононуклеотиды, будет определяться скоростью синтеза пуриновых и пиримидиновых нуклеотидов; синтез последних в свою очередь зависит от наличия всех составляющих из трех компонентов. Источником рибозы и дезоксирибозы служат продукты превращения глюкозы в пентозофосфатном цикле. Пока не получены доказательства существенной роли пищевых пентоз в синтезе нуклеиновых кислот. Фосфорная кислота также не является лимитирующим фактором, поскольку она поступает в достаточном количестве с пищей. Следовательно, биосинтез нуклеиновых кислот начинается с синтеза азотистых оснований (точнее, мономерных молекул – мононуклеотидов).
ОБМЕН НУКЛЕИНОВЫХ КИСЛОТ
Молекулы нуклеиновых кислот заряжены отрицательно, поэтому они образуют с положительно заряженными белковыми компонентами ионные связи.
| Азотистое основание | Нуклеозид | Нуклеотид |
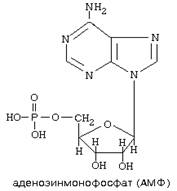
| Аденин | Аденозин | аденозинмонофосфат(АМФ) |
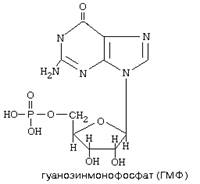
| Гуанин | Гуанозин | гуанозинмонофосфат(ГМФ) |
| Урацил | Уридин | уридинмонофосфат (УМФ) |
| Тимин | Тимидин | тимидинмонофосфат (ТМФ) |
| Цитозин | Цитидин | цитидинмонофосфат (ЦМФ) |
 |
 |
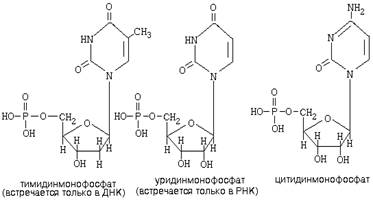
Один из них обозначается как 3′-конец, а другой – 5′-конец. Начальным считается 5’-конец.
Молекулярная масса нуклеиновых кислот сильно варьирует, но в целом очень большая, особенно у ДНК. В ядре клетки человеческого организма содержится 46 молекул ДНК, в составе каждой из них – 3,5 миллиарда пар мононуклеотидов. В митохондриях есть циклическая ДНК, ее молекула содержит 16 тысяч пар мононуклеотидов. Сначала была расшифрована структура митохондриальной ДНК. В ней закодирована информация о строении 13-ти полипептидных цепей, 2-х рибосомальных РНК и 22-х транспортных РНК. Поскольку митохондриальная ДНК не связана с белковыми компонентами, она сильнее подвержена мутациям, по сравнению с ядерной. Известно много митохондриальных генетических заболеваний, связанных с ее мутациями, проявляющихся нарушениями тканевого дыхания и окислительного фосфорилирования. В отличие от ядерной РНК, наследование таких нарушений идет только по материнской линии.
Общее количество белков, закодированных в человеческой ДНК, не превышает 100 тысяч. В настоящее время геном человека полностью расшифрован.
БИОЛОГИЧЕСКАЯ РОЛЬ НУКЛЕИНОВЫХ КИСЛОТ.
1. ДНК: хранение генетической информации.
2. У РНК функции более многообразны:
а) хранение генетической информации (информосомы, некоторые РНК-вирусы;
в) каталитическая функция: некоторые молекулы РНК способны катализировать реакции гидролиза 3’,5’-фосфодиэфирной связи в самой молекуле РНК. Показано, что некоторые молекулы РНК способны одним своим участком катализировать гидролиз фосфодиэфирных связей другого участка своей молекулы. Такое явление обозначается термином «самосплайсинг». Каталитические РНК называют рибозимами.
1. Структурная.
Из мононуклеотидов построены нуклеиновые кислоты, некоторые коферменты и простетические группы ферментов.
2. Энергетическая.
НМФ + АТФ Û НДФ + АДФ
 |
НДФ + АТФ Û НТФ + АДФ
Эти переходы протекают очень легко.
3. Регуляторная.
Азотистое основание аденин является более универсальным, чем остальные: у него такое взаимное расположение аминогруппы с фосфатом, что возможен синтез АТФ из АДФ и неферментативным путем.
ОБМЕН НУКЛЕИНОВЫХ КИСЛОТ
Нуклеиновые кислоты в организме постоянно обновляются. В норме синтез и распад находятся в состоянии динамического равновесия.
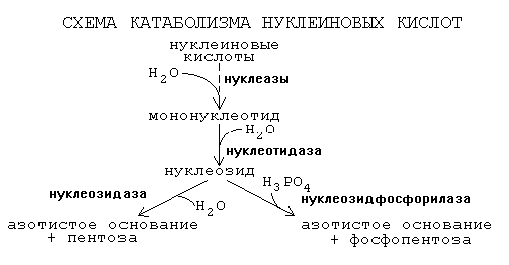
КАТАБОЛИЗМ НУКЛЕИНОВЫХ КИСЛОТ
Начинается с гидролиза 3′,5′-фосфодиэфирной связи под действием ферментов нуклеаз:
Среди ДНКаз и РНКаз различают:
— экзонуклеазы (5′ и 3′);
Далее происходит отщепление фосфата от мононуклеотида с участием ферментов нуклеотидаз с образованием нуклеозидов.
Нуклеазы очень многообразны. Различают ДНКазы и РНКазы. Отличаются друг от друга по месту действия. Бывают эндонуклеазы (расщепляют внутренние 3’5′-фосфодиэфирные связи) и экзонуклеазы (отщепляют концевые мононуклеотиды). Встречается 2 типа экзонуклеаз: 3′-экзонуклеазы – отщепляют мононуклеотид с 3′-конца молекулы, и 5′-экзонуклеазы – отщепляют 5′-концевой мононуклеотид.
Нуклеазы могут отличаться друг от друга и по специфичности. Пищеварительные нуклеазы и нуклеазы лизосомальные отличаются низкой специфичностью, у них упрощенное строение активного центра. У высокоспецифичных нуклеаз очень сложное строение активного центра. Они способны «узнавать» целую последовательность нуклеотидов из 4-10 пар и расщеплять одну-единственную связь в строго определенном месте (если «узнаваемый» участок содержит содержит 4 нуклеотидные пары, то расщепляется, в среднем, одна связь из 250 возможных). Такие высокоспецифичные ДНКазы называются рестриктазами.Участки ДНК, «узнаваемые» рестриктазами, называются полиндромными последовательностями. Рестриктазы широко применяются в генной инженерии.
Пентозы, образующиеся в ходе катаболизма нуклеиновых кислот, могут быть утилизированы во II-м этапе ГМФ-пути.
КАТАБОЛИЗМ ПИРИМИДИНОВЫХ АЗОТИСТЫХ ОСНОВАНИЙ
Обмен нуклеиновых кислот



Нуклеиновые кислоты играют очень важную роль в жизнедеятельности организмов и наряду с белками определяют главнейшие звенья обмена веществ, явления роста и размножения организмов, а также передачу наследственной информации. Содержание ДНК на одну клетку довольно постоянно. В органах и тканях, характеризующихся быстрым ростом, интенсивно идет клеточное деление, значит, с такой же интенсивностью идет новообразование, синтез новых молекул ДНК. С другой стороны, в старых органах и тканях, характеризующихся интенсивным отмиранием клеток, преобладает распад молекул дезоксирибонуклеиновой кислоты. Содержание РНК в среднем на 1 клетку не остается постоянным в течение всего жизненного цикла клетки. Сразу после клеточного деления оно невысоко, но быстро увеличивается и достигает максимума в период наиболее интенсивного роста клетки, когда напряженность обмена веществ, и прежде всего интенсивность синтеза белков, в клетке бывает самой высокой. В дальнейшем содержание РНК в клетке снижается, происходит ее распад. Таким образом, простые определения содержания ДНК и РНК в клетках и тканях показывают, что в организмах постоянно идут процессы синтеза и распада нуклеиновых кислот.
Биосинтез нуклеиновых кислот. Основными структурными элементами, из которых построены молекулы ДНК и РНК, являются нуклеотиды – соединения, состоящие из рибозы и дезоксирибозы, азотистого основания и фосфорной кислоты. Поэтому образованию нуклеиновых кислот в клетках должен, очевидно, предшествовать синтез нуклеотидов. На второй стадии биосинтеза происходит фосфорилирование нуклеотидов с образованием соответствующих ди- и трифосфатов, имеющих макроэргические фосфатные связи. На третьей, последней стадии синтеза нуклеиновых кислот соответствующие фосфорилированные нуклеотиды полимеризуются, и возникают молекулы ДНК и РНК. Все животные организмы способны синтезировать нуклеиновые кислоты из простых соединений и не нуждаются в доставке их с пищей. Хорошим примером этому служит рост молодых животных, которые питаются только молоком.
Биосинтез пуриновых нуклеотидов. В отличие от многих других синтетических процессов, биосинтез пуриновых нуклеотидов происходит чаще всего не при взаимодействии соответствующих веществ, входящих в состав этих нуклеотидов (пуриновых оснований, рибозы, дезоксирибозы и фосфорной кислоты), а в результате более сложных реакций. Оказалось, что исходным соединением при биосинтезе нуклеотидов является рибоза, или рибозо-5-фосфат. К рибозо-5-фосфату затем последовательно присоединяются отдельные атомы или группы атомов, из которых постепенно строится гетероциклический скелет пуринового основания. В образовании этого скелета принимают участие атомы азота и углерода ряда аминокислот, муравьиной кислоты и угольной кислоты. Процесс требует значительной затраты энергии. Донором формильных остатков (остатков муравьиного альдегида) является производное фолиевой кислоты – ангидроформилтетрагидрофолиевая кислота (АФТГФК). Синтез АФТГФК происходит из тетрагидрофолиевой кислоты (ТГФК) с участием АТФ по схеме:
Промежуточным продуктом в синтезе пуриновых нуклеотидов является инозиновая кислота. Она состоит из пуринового основания – гипоксантина, рибозы и фосфорной кислоты. Пуриновые нуклеотиды – адениловая, дезоксиадениловая, гуаниловая и дезоксигуаниловая кислоты – образуются из инозиновой кислоты в результате довольно простых превращений. Рибозо-5-фосфат, необходимый для синтеза нуклеотидов, образуется в растениях в процессе фотосинтеза или при окислении углеводов через пентозофосфатный цикл. Процесс биосинтеза инозиновой кислоты довольно сложен и идет через несколько стадий.
Суммарное уравнение биосинтеза инозиновой кислоты из простейших предшественников можно схематически представить следующим образом:

При этом две молекулы аммиака отщепляются от глютамина и одна – от аспарагиновой кислоты, а остатки муравьиной кислоты переносятся от 2 молекул ангидроформилтетрагидрофолиевой кислоты. Всего для синтеза 1 молекулы инозиновой кислоты из рибозо-5-фосфата необходимо 5 молекул АТФ. Но при расчете общего количества энергии следует учитывать, что при образовании каждой молекулы инозиновой кислоты необходимо девять молекул АТФ. Синтез адениловой кислоты из инозиновой кислоты идет в две стадии через аденил-янтарную кислоту. Донором атома азота является аспарагиновая кислота. Эта реакция во многом напоминает реакцию синтеза инозиновой кислоты. Основное различие состоит в используемых макроэргических соединениях, которые дают энергию для синтеза С-N-связи. В реакции участвует АТФ, а в реакции синтеза адениловой кислоты – гуанозинтрифосфат (ГТФ). На 2-й стадии от аденилянтарной кислоты отщепляется фумаровая кислота, и образуется адениловая кислота. Обе реакции синтеза адениловой кислоты катализируются ферментом аденилосукцинатлиазой. Биосинтез гуаниловой кислоты из инозиновой кислоты также идет в две стадии и требует затрат энергии. На 1-й стадии инозиновая кислота окисляется до ксантиловой кислоты при помощи восстановленного никотинамидадениндинуклеотида. Эта реакция катализируется ферментом инозин-5-фосфатдегидрогеназой. На 2-й стадии происходит аминирование ксантиловой кислоты, которое требует затрат энергии. Донором атома азота здесь является глутамин. В результате реакции образуется гуаниловая кислота, аденозинмонофосфат и пирофосфорная кислота. Пуриновые дезоксирибонуклеотиды – дезоксиадениловая и дезоксигуаниловая кислоты, которые необходимы для биосинтеза ДНК, – образуются аналогично. Исходным продуктом для их синтеза также является рибоза, а превращение производных рибозы в производные дезоксирибозы осуществляется в результате их восстановления на уровне нуклеотидов при сохранении гликозидной связи между пентозой и основанием. Для восстановления необходим НАДФ*Н2.

Биосинтез пиримидиновых нуклеотидов. Механизм биосинтеза пиримидиновых нуклеотидов, так же как и пуриновых нуклеотидов, был выяснен в основном лишь в последние годы. Хотя по своей структуре пуриновые и пиримидиновые нуклеотиды довольно близки между собой, тем не менее пути их биосинтеза резко различны. Если при биосинтезе пуриновых нуклеотидов исходным соединением является рибозо-5-фосфат, к которому постепенно присоединяются отдельные атомные группировки, то биосинтез пиримидиновых нуклеотидов начинается с самых простых соединений (аммиака и углекислоты), а рибофосфат присоединяется лишь на заключительных стадиях синтеза. Промежуточным продуктом в синтезе производных пиримидина является оротовая кислота.
Но в результате этих реакций синтез нуклеотидов происходит не всегда. В тех случаях, когда в тканях и клетках растений имеются свободные пуриновые и пиримидиновые основания (которые возникают в результате распада нуклеиновых кислот), они могут непосредственно использоваться для синтеза нуклеотидов. При синтезе из свободных оснований вначале образуются нуклеозиды, которые затем фосфорилируются и превращаются в нуклеотиды.
На первом этапе под действием фосфотрансфераз фосфатный остаток переносится от АТФ на рибозу или дезоксирибозу с образованием пентозофосфатов. Затем пентозофосфат, соединяясь с основанием, превращается в нуклеотид и свободную фосфорную кислоту. На последнем этапе нуклеотид фосфорилируется с участием АТФ и превращается в нуклеотид. Схематически процесс биосинтеза нуклеотида из свободного основания можно представить следующим образом (на примере синтеза адениловой кислоты):

Синтез ДНК. Химические анализы показывают, что количество ДНК в течение жизненного цикла клетки постоянно. Но в период клеточного деления количество ДНК резко возрастает, и ее концентрация увеличивается ровно в два раза. Таким образом, после деления клетки содержание ДНК в дочерних клетках остается таким же, каким оно было в материнской клетке.
Молекула ДНК представляет собой две комплементарные полинуклеотидные цепи, скрученные вокруг общей оси, причем в цепях аденин соответствует тимину, а гуанин – цитозину, соединенным водородными связями. Таким образом, каждая цепь ДНК служит специфической структурой, которая может соединяться только с комплементарной структурной цепью и точно определять структуру вновь создаваемой цепи. В процессе удвоения молекул ДНК в период клеточного деления прежде всего разрываются водородные связи между цепями, цепи раскручиваются и расходятся. После этого под действием соответствующих ферментов к каждой из одиночных цепей присоединяются новые нуклеотиды. Но так как сочетание должно быть строго определенным, то на каждой образовавшейся цепи строится вторая комплементарная цепь прежнего состава.
Этот процесс удвоения ДНК представлен на схеме:







Таким образом, благодаря принципу комплементарности в строении молекулы из одной молекулы ДНК образуются две совершенно одинаковые молекулы. Способность ДНК давать строго определенные, подобные себе новые молекулы играет определяющую роль в явлениях наследственности и в передаче генетической информации. ДНК определяет синтез специфических белков в клетке, и изменения в ее структуре будут вести к синтезу неспецифических для данной клетки и организма белков, что в конечном итоге вызывает изменения в обмене веществ и свойствах организма. Поэтому сама ДНК должна сохранять постоянство строения, не изменять его даже при делении клеток, что и достигается в результате специфического механизма самоудвоения ее молекулы. В периоды между делениями клеток молекула ДНК остается очень инертной, стабильной, что резко отличает ее от всех других веществ – белков, углеводов, липидов, которые подвергаются непрерывному обмену и обновлению. Одним из наиболее крупных достижений биохимии явилось выделение и очистка ферментов, катализирующих синтез нуклеиновых кислот. Эти работы позволили воспроизвести синтез ДНК и РНК вне живой клетки. В 1956 году А. Корнберг выделил и очистил из экстрактов кишечной палочки фермент, катализирующий синтез ДНК из ее простых предшественников. Фермент был назван ДНК-полимеразой, а впоследствии получил название – ДНК-нуклеотидилтрансфераза. Позднее этот фермент был выделен из других объектов. Он катализирует синтез ДНК только из соответствующих трифосфатов, при замене трифосфатов на дифосфаты или монофосфаты синтеза ДНК не было. Необходимым условием для выявления максимальной активности ДНК-нуклеотидилтрансферазы является одновременное присутствие в среде трифосфатов всех четырех дезоксирибонуклеозидов (дезокситимидина, дезоксицитидина, дезоксигуанозина, дезоксиаденозина), а также ионов магния и небольшого количества ДНК (так называемой затравки). Суммарную реакцию синтеза ДНК можно представить следующим образом:




где g АТФ, g ЦТФ, g ГТФ, g ТТФ – соответственно дезоксиаденозинтрифосфат, дезоксицитидинтрифосфат, дезоксигуанозинтрифосфат и дезокситимидинтрифосфат, g АФ, g ЦФ, g ГФ, g ТФ – соответствующие нуклеотиды, соединенные в цепь, ФФ – неорганический пирофосфат. Эта реакция обратима, и процесс идет в сторону синтеза при условии выделения из среды неорганического пирофосфата. Состав ДНК в процессе ее биосинтеза обычно не меняется, однако в некоторых случаях изменения все же происходят. Например, в силу каких-то причин имеющиеся основания могут быть заменены их аналогами или вовсе выпасть из молекулы. Такие изменения состава ДНК носят название «случайных ошибок» биосинтеза ДНК. Совершенно очевидно, что если в результате «случайных ошибок» образуется ДНК не характерная для данного вида, то она после самоудвоения дает начало таким же не характерным молекулам, что приводит к спонтанным мутациям организма. Но такие «случайные ошибки» встречаются исключительно редко. Однако часто мутации можно увеличить искусственно, если подвергнуть организм действию ионизирующей радиации, ультрафиолетовых лучей или химических веществ под названием мутагены. К мутагенам относят некоторые аналоги пуриновых и пиримидиновых оснований, алкирующие агенты – иприт, некоторые антибиотики, алкалоиды, азотистую кислоту.
Синтез РНК. Содержание РНК во всех клетках не постоянно, а может резко изменяться в зависимости от вида, возраста и физиологического состояния организма или ткани. Обычно количество РНК больше в молодых клетках, через в старых. Кроме того, в клетках содержатся различные по свойствам и молекулярному весу виды РНК: рибосомная, транспортная и информационная. Все это создает значительные трудности при изучении проблемы биосинтеза рибонуклеиновых кислот. В настоящее время считают, что биосинтез рибонуклеиновых кислот может происходить в результате одного из следующих типов реакций:
· наращивания имеющихся полинуклеотидных цепей;
· ДНК–зависимого синтеза РНК;
· РНК–зависимого синтеза РНК.
1.Синтез РНК из рибонуклеозиддифосфатов катализирует фермент полинуклеотидфосфорилаза. Для действия фермента необходимо наличие в реакционной среде ионов магния, при синтезе РНК освобождается неорганический фосфат. Реакция синтеза РНК идет по схеме:


В качестве источников дифосфатов могут служить АДФ, УДФ, ГДФ и ЦДФ. Для синтеза высокомолекулярных полимеров в реакционную смесь необходимо добавлять некоторое количество «затравки». Состав «затравки» не оказывает влияния на состав синтезируемого продукта. В качестве «затравки» можно взять любую РНК или любой полинуклеотид. Состав синтезирующейся РНК зависит только от количества и соотношения нуклеозиддифосфатов в реакционной среде. Если в среде будет преобладать какой-нибудь нуклеозиддифосфат, то он же преобладает в составе РНК.