Оценка нутритивного статуса пациента
Для оценки нутритивного статуса пациента в повседневной клинической практике принято использование целого комплекса соматометрических и клинико-лабораторных параметров. Эти параметры условно подразделяются на обязательные (первого уровня) и дополнительные (второго уровня). Обязательные параметры включают в себя данные антропометрических, клинических и лабораторных исследований. Данные параметры могут и должны быть использованы врачом любой специальности для определения текущего нутритивного статуса. Дополнительные параметры необходимы для более детального анализа трофологического состояния пациента и обычно используются специалистами по искусственному питанию. Данные параметры позволяют определить отдельные конституциональные показатели, такие как, например, жировая масса тела, мышечная масса тела и их соотношение.
К антропометрическим (соматометрическим) параметрам, чье измерение формально является обязательным при физикальном обследовании больного, относятся: росто-весовые показатели и их производные (масса тела, рост, идеальная масса тела и величина ее отклонения, индекс массы тела), окружность плеча и толщина кожно-жировой складки.
Идеальная масса тела рассчитывается по следующим формулам:
ИдМТ для мужчин = Рост – 100 – (Рост – 152) х 0, 2.
ИдМТ для женщин = Рост – 100 – (Рост – 152) х 0, 4.
ИдМТ измеряется в килограммах, рост — в сантиметрах.
Отклонение фактической массы тела (ФМТ) от идеальной массы рассчитывают по формуле:
Снижение массы от идеальной (%) = 100 х (1 – ФМТ/ИдМТ).
Кроме того, для определения нормальной массы тела теоретически может быть применён целый ряд индексов: индекс Брока, индекс Брейтмана, индекс Бернгарда, индекс Давенпорта, индекс Одера, индекс Ноордена, индекс Татоня. Однако наиболее часто в клинической практике для ориентировочной оценки нутритивного статуса используется индекс массы тела. Данный показатель был разработан Adolphe Quetelet в 1869 г. и рассчитывается по формуле:
ИМТ = m/h2, где m – вес в кг, h – рост в метрах
В соответствии с рекомендациями ВОЗ показатели Индекса Массы Тела (ИМТ, индекс Кетле) с учетом возраста интерпретируются следующим образом:
Состояние нутритивного статуса современных детей, возможность его коррекции. Часть 1
Изучение состояния трофологического статуса дошкольников с различными отклонениями в состоянии здоровья и частыми респираторными заболеваниями и эффективность метода энтеральной (пероральной) нутритивной поддержки в комплексе реабилитационных мероприятий
Пусть пища будет для них лекарством, а не лекарство пищей!
Гиппократ
Как известно, детский организм формируется под сочетанным влиянием генетически детерминированной программы развития и факторов внешней среды. Последние не только влияют на степень реализации генетической программы, но в раннем возрасте нередко могут существенно модифицировать эту программу. Среди этих факторов наиважнейшим является характер питания ребенка. Через питание могут осуществляться любые управляющие воздействия, как негативные, так и позитивные.
Гиподинамия, характерная для большинства современных людей, в том числе и детей, привела к существенному уменьшению объема рациона, а следовательно, к уменьшению количества поступающих в организм пищевых ингредиентов. Кроме того, в процессе своего же эволюционного развития организм утерял «ключи» синтеза ряда жизненно важных компонентов пищи.
Несбалансированное питание в детском возрасте не обеспечивает растущий организм ребенка необходимыми для его нормального физического, психического и интеллектуального развития энергией и пищевыми веществами. Неполноценность рациона приводит к снижению антиоксидантной защиты организма, одного из основных факторов стрессоустойчивости и неспецифической профилактики хронических заболеваний у детей. Недостаточное снабжение организма витаминами, микроэлементами сопровождается нарушением формирования, а затем и функционирования иммунной системы, что проявляется несостоятельностью защитно-адаптационных механизмов, снижением устойчивости организма ребенка к действию различных неблагоприятных факторов окружающей среды, в том числе экологических [2].
Обеспеченность детей такими микронутриентами, как витамины С, В, фолиевая кислота, каротин; минеральные вещества, такие как кальций, железо, йод, фтор, селен, цинк, в настоящее время оценивается специалистами как кризисная [11].
Установлено, что дети раннего возраста с легкой и умеренной степенью недостаточности питания подвергаются риску умереть в 2 раза, а при тяжелой в 7 раз чаще, чем более упитанные дети [6].
Однако даже при идеальном аппетите и пищевом поведении ребенка достичь сегодня оптимального питания, особенно в плане обеспеченности микронутриентами, очень сложно, поэтому очевидна необходимость организации адекватной нутритивной поддержки детей. В индивидуальной нутритивной поддержке особенно нуждаются часто болеющие дети, дети с дефицитом или избытком массы тела, хроническими заболеваниями для профилактики развития или коррекции полигиповитаминоза.
Целью нашего исследования было изучение состояния трофологического статуса дошкольников с различными отклонениями в состоянии здоровья и частыми респираторными заболеваниями и эффективность метода энтеральной (пероральной) нутритивной поддержки в комплексе реабилитационных мероприятий.
Материалы и методы
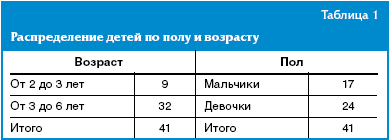
В исследование был включен 41 ребенок в возрасте от 2 до 6 лет, посещающий специализированные детские образовательные учреждения (ДОУ) для детей с аллергическими заболеваниями. Распределение детей по полу и возрасту представлено в табл. 1.
У всех детей наряду с клинической оценкой состояния питания проводилось взвешивание на цифровых напольных весах Body Fat Analyser BF662 (Tanita Corporation, Tokyo, Japan), позволяющее определить как общую массу тела, так и процентное содержание жира в организме. Процедура взвешивания выполнялась в соответствии с требованиями Tanita Corporation, оценка результатов — по унифицированным центильным шкалам Tanita Corporation для детей соответствующего возраста [13]. Выраженность подкожного жирового слоя оценивалась по результатам измерения толщины 4 кожных складок (над бицепсом и трицепсом плеча, в подлопаточной области и над гребнем подвздошной кости). Измерения проводились в соответствии с общепринятыми требованиями, с помощью электронного пружинного калипера FatTrackII (точность 1 мм). Результаты калиперометрии оценивались в соответствии с центильными шкалами для детей [3].
Наряду с оценкой трофологического статуса оценивалось качество жизни по методологии оценки состояния здоровья детей различных возрастных периодов по критериям качества их жизни [6]. Выделялись и оценивались блоки физического функционирования (двигательная активность, способность к координации и др.), психоэмоционального функционирования (возбудимость, тревожность, сон, поведение), социального (контакты с другими детьми, поведение и др.) и умственного развития с оценкой способности к обучаемости (внимание, память, речь). Каждый блок содержит по пять признаков, характеризующих соответствующие проблемы и пять вариаций оценки каждого признака в баллах: никогда не встречается — 0 баллов; почти никогда не наблюдается — 1 балл, иногда — 2 балла, часто — 3 балла, почти всегда — 4 балла.
Результаты и их обсуждение
Наиболее распространенными заболеваниями у обследованных дошкольников были остаточные явления рахита и нарушения осанки, атопический дерматит в стадии ремиссии, диагносцированные у 49% детей. 46% дошкольников имели патологию носоглотки (гиперплазию миндалин II–III степени, хронический аденоидит). 27% детей часто (5–6 и более раз в год) болели острыми инфекционными заболеваниями.
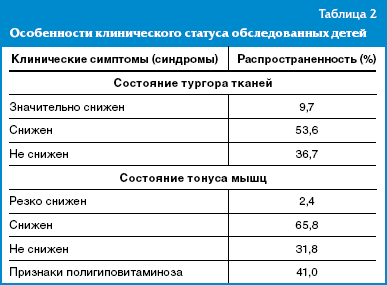
Результаты оценки исходного нутритивного статуса детей (табл. 2) свидетельствовали о наличии различных проявлений трофологических расстройств у абсолютного большинства детей (снижение тургора тканей, тонуса мышц).
Почти у половины наблюдаемых детей (41%) наблюдались те или иные признаки полигиповитаминоза (отечность межзубных сосочков, красная кайма у шейки зубов, разрыхленность и покраснение или синюшность десен, гипертрофический глоссит, «географический» язык, атрофия сосочков языка, сухость кожи и др.).
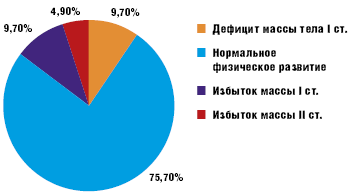
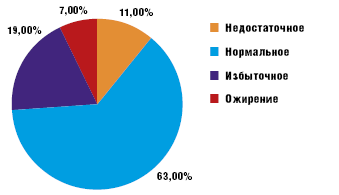
Оценка физического развития по данным антропометрии (соответствие массы длине тела) согласно региональным стандартам свидетельствовала об отсутствии существенных отклонений в физическом развитии большинства детей (рис. 1).
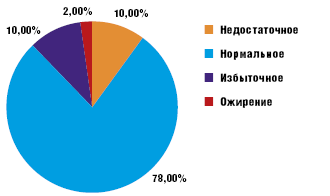
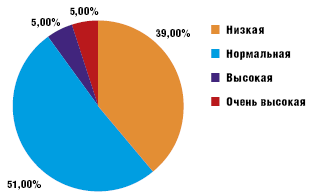
Аналогичные данные были получены при расчете индекса массы тела — индекса Кетле (рис. 2).
Как известно, антропометрические данные не отражают качественного состава тела человека и не могут служить единственным критерием оценки нутритивного статуса [8, 12].
Подтверждением этого утверждения являются результаты выполненного нами исследования состояния питания ребенка с помощью определения массовой доли жира биоимпедансным методом (рис. 3) и толщины подкожно-жирового слоя (рис. 4).
Полученные данные свидетельствовали, что у 26% детей имела место избыточная доля жировой ткани в организме, и в то же время только у 10% детей мы обнаружили увеличение подкожно-жирового слоя по данным калиперометрии. Уменьшение толщины подкожно-жировых складок выявлено у 39% детей и всего лишь у 11% — недостаток доли жира.
Таким образом, полученные результаты свидетельствуют о нарушении трофологического статуса у значительно большего количества обследованных дошкольников, чем по данным антропометрии. Не вполне сопоставимые результаты, полученные по методикам исследования процентного содержания жира в организме и калиперометрии, связаны с тем, что последние характеризуют качественное состояние различных компартментов организма человека. В частности, увеличение доли жировой ткани в организме ребенка естественно сопровождается уменьшением доли безжировой, так называемой «тощей», массы. Тощая (обезжиренная) масса тела состоит из скелетной и гладкой мускулатуры, массы висцеральных органов, клеток опорно-двигательного аппарата. В то же время тощая масса тела подразделяется на внеклеточную массу и клеточную массу. При недостаточном питании на начальном этапе, прежде всего, расходуется клеточная масса, причем в 80% — за счет мышц [5]. Снижение тонуса мышц, выявленное нами почти у 70% детей, является косвенным подтверждением страдания клеточного компартмента организма.
Известно, что снижение клеточной массы тела часто сопровождается увеличением внеклеточной, как правило интерстициальной, жидкости [5]. Выявленное в нашем исследовании снижение тургора тканей более чем у 60% детей и уменьшение толщины подкожно-жировых складок является свидетельством повышенной гидрофильности тканей организма современного ребенка (состояние паратрофии).
Н. Л. Черная *, доктор медицинских наук, профессор
Г. В. Мелехова *
Л. Н. Старунова *
И. В. Иванова *, кандидат биологических наук
Н. И. Рыжова **
* Ярославская государственная медицинская академия,
** МДОУ Детский сад комбинированного вида № 215, Ярославль
Нутритивный статус что это такое
Резюме. В статье представлен обзор литературы по проблеме диагностики и коррекции нутритивной недостаточности у больных раком желудка. Недостаточность питания у больных раком желудка приводит к ухудшению качества жизни пациентов, увеличению числа послеоперационных осложнений, увеличению послеоперационной летальности. Проанализирована безопасность и эффективность влияния энтеральной нутритивной поддержки на течение послеоперационного периода у больных раком желудка. Оценка нутритивного статуса больных раком желудка на всех этапах лечения пациента и своевременная коррекция риска развития недостаточности питания, активная персонализированная нутритивная поддержка пациентов с диагностированной нутритивной недостаточностью – обязательный элемент современного лечения рака желудка.
Ключевые слова: рак желудка, нутритивный статус, нутритивная недостаточность, нутритивная поддержка, индекс массы тела (ИМТ), послеоперационные осложнения.
Рак желудка (РЖ) является актуальной проблемой онкологии. На сегодняшний день в мире регистрируются высокие показатели заболеваемости и смертности от данного заболевания [1]. Количество впервые выявленных случаев РЖ в 2018 году по данным ВОЗ составило более 1 миллиона, без существенной динамики по сравнению с данными 2012 года. В структуре общей онкологической заболеваемости занимает устойчивое 5 место. Более половины впервые диагностированных случаев заболевания зарегистрировано в странах Азии (75,4%). В структуре смертности от онкологических заболеваний РЖ занимает 3 место. Несмотря на успехи современной медицины, внедрение высокоинформативных методов диагностики, таргетной терапии, ежегодно в мире от данной опухоли продолжают погибать около 800000 человек. Стандартизированные по возрасту показатели заболеваемости у мужчин в 2 раза выше, чем у женщин [1]. В России в 2017 году выявлено около 35000 новых случаев заболеваемости РЖ, при этом у большинства пациентов заболевание было диагностировано в стадии местного и отдаленного распространения (III стадия – 23,8%, IV стадия – 39,9%) [2]. В Красноярском крае в 2017 году диагноз РЖ был впервые установлен 725 пациентам. Летальность на первом году заболевания с момента установления диагноза составила 44,2% [2].
Согласно практическим рекомендациям RUSSCO по лекарственному лечению РЖ, выбор тактики лечения определяется степенью распространенности опухолевого процесса и функциональным состоянием пациента. Основным методом радикального лечения РЖ является хирургическое вмешательство, дополняемое в большинстве случаев системной противоопухолевой терапией [3, 4].
Нутритивная недостаточность у больных раком желудка не всегда позволяет провести лечение в полном объеме [5, 6].
Европейским обществом по клиническому питанию (European Society for Clinical Nutrition and Metabolism, ESPEN, 2015) нутритивной недостаточностью называется состояние, при котором в результате недостаточного поступления в организм или усвоения в нем питательных веществ отмечаются изменения в компонентном составе организма, в частности, снижение тощей массы тела, приводящие к нарушению физических и психических функций организма, ухудшающие клинический исход заболевания. По результатам исследования ECOG в 2003 г., включавшего 3047 онкологических больных, выявлено, что частота нутритивной недостаточности при опухолевом поражении органов желудочно-кишечного тракта (ЖКТ) колеблется от 70 до 83%. Наиболее часто нутритивная недостаточность встречается при раке желудка и пищевода (75-80%) [5].
Для улучшения результатов лечения рака желудка, снижения частоты развития послеоперационных осложнений, профилактики рецидивов заболевания, повышения качества жизни пациентов важную роль играет поддерживающая терапия, в частности, снижение риска развития недостаточности питания, адекватная и своевременная нутритивная поддержка 7.
Отсутствие персонифицированного подхода к коррекции нутритивного статуса у больных раком желудка остается одной из важных нерешенных проблем мирового сообщества на сегодняшний день [9, 11].
Оценка нутритивного статуса
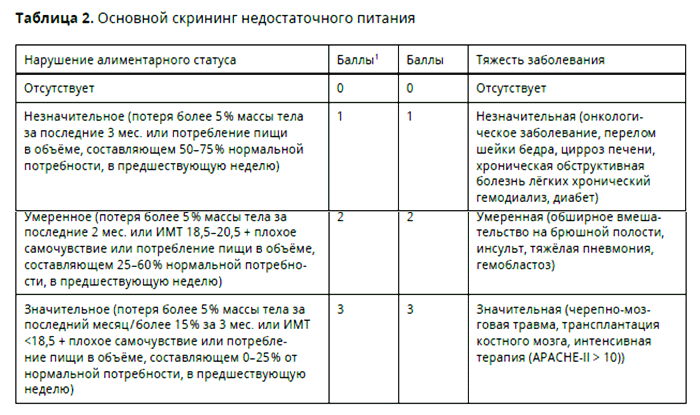
Для определения недостаточности питания необходимо оценивать нутритивный статус пациента [9, 12-14]. Оценка нутритивного статуса базируется на определении антропометрических, лабораторных и морфофункциональных критериев [15]. Для определения риска развития нутритивной недостаточности используются различные скрининговые шкалы [16]. Для больных раком желудка, которым планируется оперативное лечение, Европейским обществом клинического питания и метаболизма (ESPEN) рекомендован скрининг нутритивного статуса по шкале «Оценка нутритивного риска» (Nutritional Risk Screening) NRS 2002. Данная шкала состоит из двух блоков – предварительного скрининга и финальной оценки недостаточности питания 17.
Баллы из левой и правой колонок суммируются. У пациентов в возрасте ≥70 лет к полученной сумме прибавляется 1 балл. При итоговом количестве баллов ≥3 имеется риск недостаточности питания, необходимо проведение нутритивной поддержки. Если количество баллов 5% массы тела за последние 2 мес. или ИМТ 18,5-20,5 в сочетании с плохим самочувствием или потребление пищи в объеме 25-60% от нормальной потребности за последние 7 дней).
В 2018 г. ESPEN и ASPEN (Американской ассоциацией парентерального и энтерального питания) также были предложены критерии оценки недостаточности питания GLIM (Global Leadership Initiative on Malnutrition).
Лабораторные методы оценки нутритивного статуса позволяют определить степень нутритивной недостаточности: легкую, среднюю, тяжелую.
Таблица 3. Оценка степени нутритивной недостаточности [20].
Трофологический статус и панкреатические ферменты
Описаны методы оценки трофологического (нутритивного) статуса пациента, роль протеолитических ферментов поджелудочной железы для коррекции нутритивного статуса, показано, что препараты панкреатических ферменты должны использоваться в комплексных схемах те
Methods of evaluation of trophologic (alimentary) status of patient, the role of proteolytic enzymes of pancreas for correction of nutritive status are described. As it is shown pancreas enzymes preparations should be applied in complex therapy schemata for different pathologies.
Анализ трофологического (нутритивного) статуса пациента, являющийся необходимым компонентом оценки как здоровья, так и тяжести болезни, складывается из анализа широкого спектра данных, включая клинические и соматометрические. К первым относятся психомоторное развитие, психоэмоциональный статус (настроение), аппетит, состояние кожных покровов и подкожного жирового слоя, слизистых оболочек, мышечного тонуса и мн. др., включая особенности полового развития.
Соматометрические показатели включают массу тела, рост, окружность головы и плеча, толщину кожно-жировой складки над трицепсом, величину окружности мышц плеча и некоторые другие. Их нормальные значения лежат в пределах среднего квадратичного отклонения (M ± 1σ) или 25–75 перцентилей при использовании центильных таблиц.
Расчетные соматометрические индексы также широко используются в клинической практике. Наиболее известным из них является показатель отклонения массы тела (ПОМТ), выраженный в % и равный
ПОМТ = ФМТ (кг)/РМТ (кг) × 100%,
где ФМТ — фактическая масса тела, а РМТ — расчетная масса тела. Нормальными значениями ПОМТ принимаются 90–110%.
Индекс массы тела (ИМТ) (индекс Quetelet) рассчитывается как отношение ФМТ в кг к значению роста (в метрах), взятом в квадрате. Нормальные значения ИМТ представлены ниже:
Для оценки трофологического статуса используются также и специальные методы исследования, которые подразделяются на статические показатели и функциональные тесты. К последним относятся, в частности, определение аномальных метаболитов, активности ферментов, in vitro тесты, провокационные патофизиологические реакции.
Для оценки текущего питания могут быть использованы исследования кала (определение содержания минеральных веществ, липидов), мочи (витамины группы В, кроме В12 и фолацина, витамин С, макро- и микроэлементы, включая Na, K, Ca, Mg, Se, аминокислоты и мн. др.), желчи (холестерин), крови (липиды, витамины, макро- и микроэлементы).
Оценка среднесрочного и долгосрочного питания может быть проведена при исследовании эритроцитов (витамины В1, В2, В6, ниацин, фолацин, Se, Cu), лейкоцитов (витамин С, Zn), волос и ногтей (микроэлементы Zn, Cu и др.), жировой ткани (жирные кислоты) [1].
Маркерами белковой недостаточности являются показатели биохимического исследования крови. Определение уровня общего белка в крови и альбумина являются наиболее доступными из них, однако не самыми точными, что связано с относительно длительным периодом полураспада (в пределах 15–20 дней). Более точным является определение трансферрина (в норме: 2–4 г/л, Т1/2–8 дней) и транстиретина (в норме: 170–350 мг/л, Т1/2–2–3 дня).
По снижению белковых маркеров выделяют три степени белковой недостаточности: легкая — снижение показателей в пределах от 10% до 20%, средняя более 20% до 30%, тяжелая — более 30%.
Другими маркерами белковой недостаточности являются альфа1?кислый гликопротеин (орозомукоид), альфа1?
антитрипсин, С-реактивный белок (СРБ). При этом признаками белковой недостаточности считается повышение указанных показателей на 5% и выше.
Также может рассчитываться прогностический индекс воспаления и состояния питания (ПИВСП), предложенный Carpeintier и Ingenbleek, который опирается на концентрацию сывороточного альбумина и транстиретина, а также на активность воспалительного процесса [2, 3]:
ПИВСП = альфа-1 КГП × СРБ × Альб × ТТР,
где альфа-1 КГП — концентрация альфа-1 кислого гликопротеина (мг/л), СРБ — С-реактивный белок (мг/л), Альб — уровень альбумина (г/л), ТТР — уровень транстиретина (мг/л) [4].
Показателями трофологического статуса также являются абсолютное число лимфоцитов, фактический расход энергии и многие другие.
Коррекция нутритивного статуса представляет собой многоплановый процесс, включающий, помимо устранения основного патологического процесса, также коррекцию питания, процессов переваривания и всасывания и метаболических процессов.
Адекватная функция пищеварительных желез, очевидно, необходима для нормального течения метаболических процессов в организме, включая рост и развитие. Секреция панкреатических ферментов, обеспечивающих основные процессы переваривания белков, жиров и углеводов, приведена в табл. 1.
К протеолитическим ферментам поджелудочной железы относятся трипсин, химотрипсин, эластаза и многие другие. Все протеолитические ферменты поджелудочной железы продуцируются в неактивном виде, и в дальнейшем происходит их активация трипсином. Сам трипсин также секретируется в виде неактивного трипсиногена, и его активация происходит в двенадцатиперстной кишке кишечной энтерокиназой. В свою очередь неактивная энтерокиназа активируется дуоденазой, также продуцируемой клетками двенадцатиперстной кишки.
Протеолитическое действие панкреатического секрета обуславливается тремя эндопептидазами — трипсином, химотрипсином и эластазой, которые расщепляют белки и полипептиды, поступающие из желудка. Трипсин специфически действует на пептидные связи, образуемые основными аминокислотами, химотрипсин — на связи между остатками незаряженных аминокислот, в то время как эластаза расщепляет связи, примыкающие к остаткам малых аминокислот, таких как глицин, аланин и серин. Активация трипсиногена осуществляется энтерокиназой, которая гидролизует его лизиновую пептидную связь. Образовавшийся трипсин действует как на новые молекулы трипсиногена, так и на химотрипсиноген, проэластазу и прокарбоксипептидазу — с высвобождением соответственно химотрипсина, эластазы и карбоксипептидазы.
К липолитическим ферментам относятся триацилглицероллипаза (панкреатическая липаза, расщепляющая триглицериды), фосфолипазы и некоторые другие. Кроме того, желчные кислоты активируют липазы, а также предварительно эмульгируют жиры, облегчая воздействие на них ферментов. Амилолитическая активность (расщепление крахмала) панкреатического секрета определяется амилазой, единственным панкреатическим ферментом, который секретируется сразу в активной форме.
Таким образом, экзокринная панкреатическая секреция обеспечивает основные процессы переваривания нутриентов, в связи с чем функциональное состояние поджелудочной железы в значительной степени определяет характер трофологического статуса больного. Так, в экспериментальных исследованиях было показано, что прибавка массы молодых животных достоверно коррелирует с экзокринной функцией поджелудочной железы [5, 6]. Аналогичные закономерности выявлены и в клинической практике, в связи с чем важной составляющей процесса коррекции нутритивного статуса является терапия препаратами панкреатических ферментов.
Высокоактивные препараты панкреатических ферментов (такие как Креон ® ), характеризуются высоким качеством субстрата, защитой от преждевременной активации в полости рта и пищеводе (капсула), определенным размером минимикросфер (1,0–1,2 мм), обеспечивающим равномерное перемешивание с желудочным и кишечным содержимым, а также защитой от инактивации в желудке (рН-чувствительная оболочка минимикросфер).
Высокоактивные препараты пищеварительных ферментов широко используются для лечения заболеваний, сопровождающихся экзокринной панкреатической недостаточностью, как абсолютной, так и относительной. Высокая эффективность их как трофологического фактора была показана впервые при лечении больных с муковисцидозом. Применение этих препаратов не только эффективно корригировало тяжелую панкреатическую недостаточность, характерную для данного заболевания, но и позволило изменить характер питания, повысить усвоение всех нутриентов, существенно улучшить нутритивный статус и, в итоге, не только увеличить продолжительность жизни больных, но и повысить ее качество.
Панкреатическая недостаточность по данным Научно-клинического отдела муковисцидоза ГУ МГНЦ РАМН (Москва) наблюдается у 95,3% пациентов с манифестацией в первые дни жизни. Следствием ее является нарушение всасывания жиров и белков. При этом до 50% поступившего белка может быть потеряно со стулом. У больных муковисцидозом обычно отмечается хорошее всасывание углеводов, однако метаболизм их может быть нарушен, вплоть до развития в старшем возрасте сахарного диабета [7].
Так, по данным Н. И. Капранова и соавт. после введения в терапию детей с муковисцидозом препарата Креон ® число госпитализаций уменьшилось примерно на 30%, также как и число курсов антибактериальной терапии, а качество и продолжительность жизни существенно повысились. Более того, в среднем суммарная стоимость лечения высокоактивными препаратами оказалась примерно в 2–3 раза ниже, по сравнению с применением препаратов средней степени активности, не говоря уже о более высокой фармакологической эффективности [8].
В работах Н. Ю. Каширской и соавт. было показано, что переход на диету без ограничения жиров у больных муковисцидозом возможен при условии адекватной заместительной терапии [7]. При этом достоверно меняется липидный спектр сыворотки крови. Высокожировая, высококалорийная диета в сочетании с приемом микросферических ферментов с рН-чувствительной оболочкой в состоянии поддерживать нормальный нутритивный статус и липидный состав плазмы крови больного муковисцидозом на нормальном уровне, что согласуется с данными зарубежных исследователей [9]. Кроме того, увеличение жирового состава пищи и применение новых форм панкреатических ферментов ведет к увеличению полиненасыщенных жирных кислот в составе фосфолипидов и их метаболитов. Последние работы в области повышения эффективности лечения больных муковисцидозом подтверждают и развивают эту концепцию [10].
Целиакия, наследственное заболевание, связанное с непереносимостью глютена, белка некоторых злаков, характеризуется синдромом мальабсорбции, при котором нарушеается кишечное всасывание практически всех нутриентов. Основой лечения целиакии является безглютеновая диета, которая дополняется посиндромной терапией, в т. ч. направленной на улучшение пищеварительных процессов в кишечнике. Практически обязательным компонентом этой терапии в последние годы стало применение высокоактивных препаратов панкреатических ферментов (Креон ® 10 000 или Креон ® 25 000).
По нашим данным, повышение экскреции триглицеридов с калом, указывающее на экзокринную недостаточность поджелудочной железы, наблюдается у 18% больных в активную стадию целиакии и у 52% — в стадию ремиссии. Механизм вовлечения поджелудочной железы в патологический процесс при целиакии, в первую очередь, связан с нарушением ее гуморальной регуляции со стороны кишечника на фоне атрофических изменений в слизистой оболочке, а также с неспецифическими метаболическими нарушениями у ребенка с тяжелой мальабсорбцией [11].
Исходя из этого, в план обследования больного целиакией должны входить ультразвуковое исследование поджелудочной железы, оценка ее экзокринной функции (оптимальным методом является определение эластазы-1 в кале, но могут быть использованы такие косвенные методы, как липидограмма кала), а также определение активности панкреатических ферментов в крови (трипсина, липазы или эластазы-1 в крови). В состав комплексной терапии целиакии должны входить препараты панкреатических ферментов (например, Креон ® ), назначение которых имеет патогенетическое значение. В большинстве случаев целесообразно использование препарата Креон ® 10000.
По данным ретроспективного анализа детей с целиакией в возрасте от 11 месяцев до 6 лет введение этих препаратов в состав терапии сокращает сроки купирования диарейного синдрома, а также интенсифицирует восстановление нутритивного статуса больных. Данные, касающиеся соматометрических показателей, а также динамики показателей белкового обмена, представлены в табл. 2 и 3).
Обращают внимание различия в итоговом значении ПОМТ через 2 месяца. В дальнейшем этот показатель, также как и другие, практически выравнивается. Эти изменения происходят на фоне нормализации стула — как его частоты, так и консистенции. Корреляция между частотой стула и ПОМТ — отрицательная сильная достоверная (r = 0,72; p ® 10 000)
Полученные данные указывают на большое значение состояния экзокринной секреции поджелудочной железы для восстановления трофологического статуса при целиакии, а также на необходимость назначения высокоактивных препаратов панкреатических ферментов с целью сокращения сроков восстановительного процесса.
Таким образом, панкреатические ферменты — важные трофологические факторы, которые обеспечивают восстановление трофологического статуса пациента при самой разнообразной патологии, а препараты панкреатических ферментов должны использоваться в комплексных схемах их коррекции.
Литература
С. В. Бельмер*, доктор медицинских наук, профессор
Е. В. Митина*
Н. А. Анастасевич*
Л. М. Карпина**
Н. С. Сметанина**, доктор медицинских наук, профессор
*ГБОУ ВПО РНИМУ им. Н. И. Пирогова Минздравсоцразвития, **РДКБ, Москва





_550.gif)



