Патология системы гемостаза и ее влияние на репродуктивную функцию
Многие исследования и открытия в области гемостазиологии помогли пересмотреть причины, патогенез, концепцию лечения и профилактики важнейших осложнений беременности (синдром привычной потери плода, преждевременная отслойка нормально расположенной плаценты, гестозы, антенатальная гибель плода, тромботические осложнения у беременных и в послеродовом периоде) [5].
Физиологические и патологические изменения в системе свертывания
Беременность – особенное состояние организма, при котором происходят существенные изменения гемостаза: на фоне гормональных перестроек меняется тонус сосудистых стенок, растет потенциал свертывающей системы крови, увеличивается объем циркулирующей крови. Нарушение этого хрупкого равновесия в системе гемостаза на фоне беременности может привести к высокому риску развития тромботических осложнений, кровотечений и акушерских потерь [4].
Частота этих осложнений существенно возрастает при носительстве генетических дефектов системы гемостаза, объединенных термином «наследственная тромбофилия» (мутация в гене протромбина, Лейденовская мутация, дефицит АТ III, дефицит протеина С и S, дезагрегационная тромбоцитопатия и т. д.), и при приобретенных формах нарушениях гемостаза (гипергомоцистеинемия, АФС, СКВ, метабо- лический синдром, варикозная болезнь вен и т. д.) [4]. Сравнительно недавно стала изучаться роль тромбофилии и в патогенезе развития нарушений имплантации плодного яйца, нарушений формирования маточно-плацентарного кровотока и, соответственно, в формировании гестозов («токсикозов») у беременных. Таким образом, наличие тромбофилии представляет серьезный риск не только для исхода беременности, но и является угрозой жизни и здоровью беременной женщины и плоду [2].
Клинические проявления тромбофилий во время беременности очень многообразны. Но своевременное выявление, диагностика (комплекс включает в себя такие исследования, как генетический анализ, гомоцистеин, антифосфолипидные антитела, оценка функционального состояния тромбоцитов, коагулограмма) и правильная трактовка анамнеза и показателей позволяют диагностировать наличие тромбофилии и, соответственно, вовремя начать лечение для предотвращения осложнений (как акушерских, так и тромботических) [2].
Клинический пример 1:
«Пациентка А. 28 лет. Диагноз: наследственная предрасположенность к тромбофилии (гете- розиготы F2, F13, ITGB3, FGB), состоявшийся тромбоз в анамнезе (ТЭЛА после кесарева сечения (КС) 2012 г.). Обратилась на малом сроке беременности. Ведение беременности на низкомолекулярных гепаринах (НМГ), антиагрегантах, симптоматической терапии. Мониторинг показателей гемостаза, допплера. Коррекция терапии по показателям. Плановое КС. Профилактика тромботических осложнений в послеродовом периоде (НМГ в течение 6 нед.).»
Классификации тромбофилий
Методы диагностики тромбофилии
«Пациентка Д. 42 года. Д-з: наследственная предрасположенность к тромбофилии (гетерозиготы F5, PAI-1, ITGA2, MTHFR677), СППП, возрастной фактор, латентный железодефицит. В анамнезе: роды – 2, замершие беременности на раннем сроке – 3. Обрати- лась после ЗБ. Проведены восстановительная терапия и дообследование, прегравидарная подготовка. При наступлении беременности продолжена терапия: НМГ, фолиевая кислота, антиоксиданты, препараты железа. Срочные роды. Профилактика тромботических осложнений в послеродовом периоде (НМГ в течение 6 нед.).»
Своевременное выявление рисков тромботических осложнений, рисков патологии и угрозы вынашивания беременности позволяет правильно сформировать эффективные методы профилактики и лечения. При таком подходе терапия действует на основную причину заболевания, а не только купирует симптоматику [1].
Основные принципы терапии
Клинический пример 3:
«Пациентка В. 33 г. Д-з: наследственная предрас-положенность к тромбофилии (патологиче-ская гомозигота PAI-1, гетерозиготы интегрин а2, в3, FGB), первичное бесплодие, сочетанный фактор (ЭКО – 1 отрицательный результат, два криопереноса – отрицательный результат). УЗИ с цветовым допплеровским картированием (ЦДК): гипоплазия эндометрия, нарушение показателей гемодинамики маточного кровотока. Обратилась для планирования криопереноса. Подготовка к криопереносу (НМГ, антиагреганты, антиоксиданты). Показатели на фоне лечения с положительной динамикой. Произведен криоперенос. Получена беременность (бихориальная, биамниотическая двойня). Ведение беременности на НМГ, контроль показателей гемостаза. Коррекция назначений по показателям (На 5–6 нед. – ретрохориальная гематома (РХГ), на 20–21 нед. – нарушение гемодинамики маточно-плацентарного кровотока 1А степени). Плановое КС 35–36 нед. Профилактика тромботических осложнений в послеродовом периоде (НМГ).»
Базовыми препаратами в процессе подготовки, ведения беременности и послеродового периода, конечно, являются противотромботические препараты – низкомолекулярные гепарины, антиагреганты, а также фолиевая кислота в индивидуально подобранной дозировке и, по показаниям, вспомогательная терапия (препараты железа, антиоксиданты, препараты прогестерона, глюкокортикоиды) [3].
1. Доброхотова Ю. Э., Щеголев А. А., Комраков В. Е. и др.; Под ред. Ю. Э. Доброхотовой, А. А. Щеголева. Тромботические состояния в акушерской практике. – М.: ГЭОТАР-Медиа, 2010.
2. Макацария А. Д., Бицадзе В. О. Тромбофилические состояния в акушерской практике. – М.: РУССО, 2001. – 704 с.
3. Мхеидзе Н. Э. Клиническое значение выявления генетической и приоб- ретенной тромбофилии у беременных с преждевременной отслойкой нормально расположенной плаценты в анамнезе. – М., 2006.
4. Репина М. А., Сумская Г. Ф., Лапина Е. Н. Наследственные нарушения системы гемостаза и беременность. – СПб, 2008.
5. Физиология и патология гемостаза. Под ред. д. м. н. проф. Н. И. Стуклова. – М.: ГЭОТАР-Медиа, 2016.
Пренатальная (дородовая) диагностика врожденной патологии плода
Рождение здорового ребенка – естественное желание каждой беременной женщины. Но, к сожалению, надежды на счастливое материнство не всегда оправдываются. Около 5% новорожденных имеют различные врожденные заболевания. Скрининг в 1 и во 2 триместрах беременности позволяет определить, насколько велик риск врожденной патологии у будущего ребенка.
В настоящее время существуют достаточно эффективные методы пренатальной (дородовой) диагностики многих заболеваний плода, которые можно выявить с 11 недели беременности. Своевременное проведение скрининговых обследований дает возможность определить большой спектр патологии плода и увидеть ультразвуковые признаки хромосомных аномалий.
Что такое ранний пренатальный скрининг и когда он проводится
Скрининг (от англ. «просеивание») – это совокупность исследований, позволяющих определить группы беременных, у которых существует риск рождения ребенка с хромосомными аномалиями и врожденными пороками. Но ранний скрининг – это только начальный, предварительный этап обследования, после которого женщинам, с выявленным риском врожденных аномалий, рекомендуется более детальное диагностическое обследование, которое точно подтвердит или исключит наличие патологии.
Что включает в себя ранний пренатальный скрининг
В комплексное обследование входят:
Полученные данные: анамнез, УЗИ и биохимические маркеры помещают в специально разработанную программу Astraia, которая рассчитывает риск рождения ребенка с врожденными аномалиями. Комбинация данных исследований увеличивает эффективность выявления плодов с синдромом Дауна и другими хромосомными заболеваниями.
Что такое программа Astraia
Astraia – это профессиональная программа, вычисляющая вероятность хромосомных аномалий у плода. Программа была разработана Фондом Медицины Плода (Fetal Medicine Foundation – FMF) в Лондоне и успешно апробирована на огромном клиническом материале во многих странах мира. Она постоянно совершенствуется под руководством ведущего специалиста в области пренатальной диагностики профессора Кипроса Николаидеса, в соответствии с последними мировыми достижениями в области медицины плода.
Специалист, проводящий ранний пренатальный скрининг, должен иметь международный сертификат FMF, дающий право на выполнение данной диагностики и работу с программой Astraia. Сертификат подтверждается ежегодно после статистического аудита проделанной за год работы и сдачи сертификационного экзамена. Таким образом обеспечивается высокая диагностическая точность полученных рисков.
Проведение раннего пренатального скрининга с помощью данной программы регламентировано приказом Министерства Здравоохранения РФ от 1 ноября 2012 г. № 572н «Об утверждении порядка оказания медицинской помощи по профилю «акушерство-гинекология» (за исключением использования вспомогательных репродуктивных технологий)».
Ранний пренатальный скрининг позволяет вычислить следующие риски:
Что оценивается при УЗИ в 1 триместре
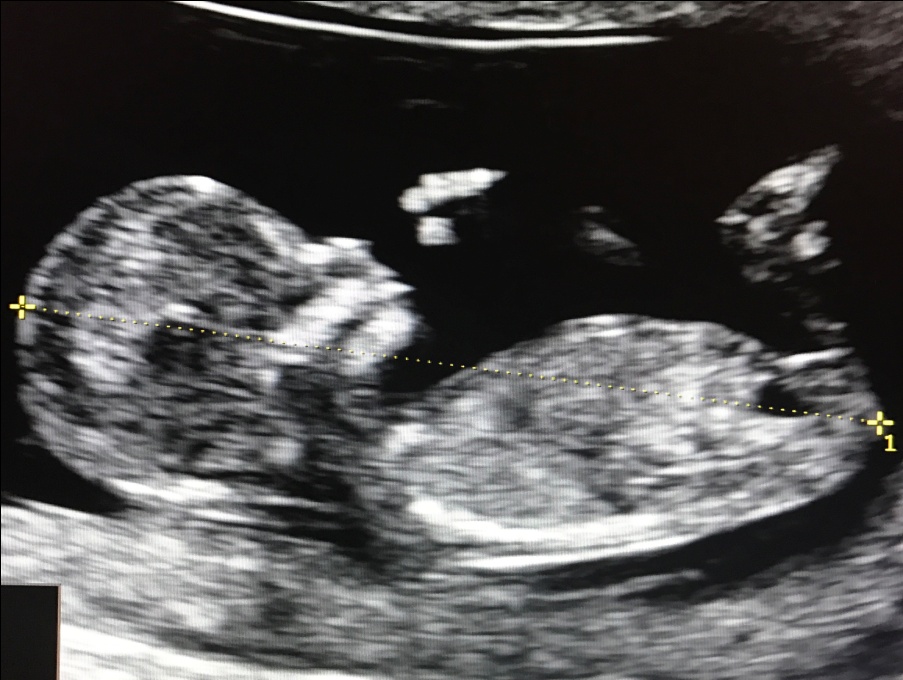
1. Копчико-теменной размер (КТР) плода
Правильное измерение КТР плода
2. Маркеры хромосомной патологии:
— толщина воротникового пространства (ТВП) – является основным признаком хромосомной патологии у плода. Патологической величиной считается увеличение ТВП больше 95-й процентили для каждого срока гестации. Каждое увеличение ТВП повышает риск существования хромосомной аномалии у плода.
ТВП в норме ТВР при патологии
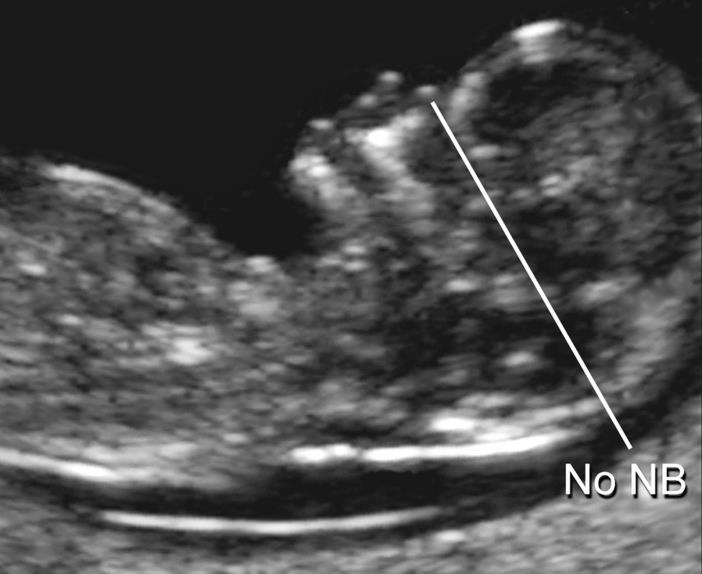
— носовая кость. У плодов с синдромом Дауна носовая кость может отсутствовать, либо быть уменьшенной (гипоплазированной). Очень редко такое может встречаться и у совершенно здоровых детей. Точный диагноз устанавливается только при помощи генетического анализа.
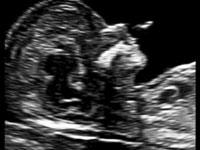
Нормальная носовая кость Отсутствие носовой кости
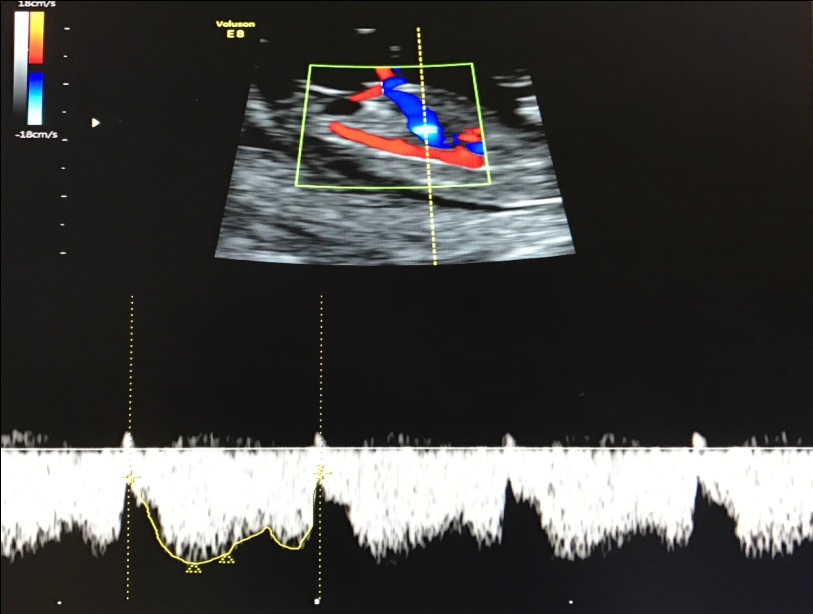
— кровоток в венозном протоке – это маленький сосуд в печени плода. При обратном (ретроградном) токе крови в данном сосуде можно предположить, что у плода хромосомный синдром, либо врожденный порок сердца.
Нормальный кровоток в венозном протоке
Но важно правильно получить этот кровоток и дать ему оценку. Для этого требуются определенные навыки и квалификация врача, которые подтверждаются ежегодной сертификацией FMF.
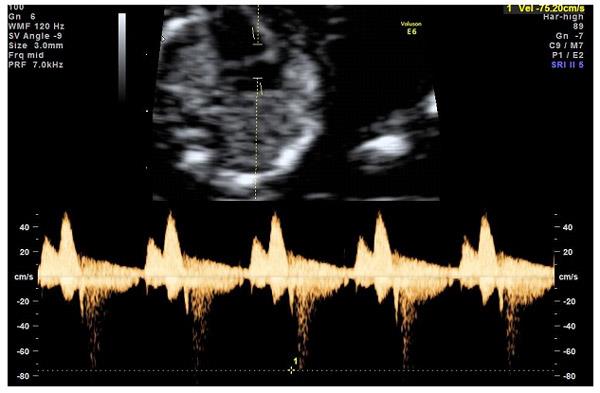
— кровоток через трикуспидальный клапан в сердце плода. Здесь ретроградный (обратный) кровоток тоже указывает на хромосомную патологию, либо может проявляться при врожденных пороках сердца.
3. Анатомические структуры плода и исключение крупных врожденных пороков
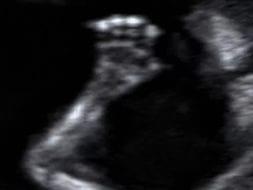
Ручка плода Мозг плода в виде “бабочки” в норме
4. Длина шейки матки
5. Стенки матки и придатков (яичников)
6. Кровоток в маточных артериях
УЗИ может проводиться как трансабдоминально, так и трансвагинально.
Что делать при высоком риске хромосомной патологии у плода
Если комплекс раннего пренатального обследования указывает на высокий риск врожденной патологии у плода, Вам будет рекомендована консультация генетика с последующей инвазивной диагностикой (биопсия ворсин хориона на сроке до 14 недель или амниоцентез, проводимый после 16 недель) и генетическим анализом. Именно генетический анализ точно определяет хромосомные заболевания и врожденные патологии у плода.
Что представляет собой скрининг во втором триместре беременности
Согласно приказу № 572н от 1.11.2012 г., второй скрининг состоит из ультразвукового исследования плода на сроке 18-21 неделя беременности. В этом возрасте кровь на биохимические маркеры уже не сдается. Плод имеет массу около 300-500 грамм и длину 20-25 см, и УЗИ позволяет детально проанализировать все анатомические структуры плода и выявить большинство пороков развития. Тогда же оценивается количество околоплодных вод, расположение и структура плаценты, длина шейки матки и др.
После проведения УЗИ на данных сроках беременности большинство вопросов пренатальной диагностики считаются закрытыми.
Надеемся, что эта информация поможет Вам лучше понять важность и необходимость скрининга в первом и втором триместрах беременности. В нашей клинике у Вас есть уникальная возможность пройти качественное обследование и получить максимально объективные данные о состоянии Вашего плода.
Лечение плацентарной недостаточности
Предсказание риска задержки внутриутробного развития и/или гипоксии плода либо их своевременное выявление чрезвычайно важны для предупреждения и коррекции этих осложнений. Для оценки состояния плаценты особенно широко используется определение в крови пептидных гормонов и специфических белков беременности.
Совместно с НИИ морфологии человека РАМН мы исследуем динамику плацентарных белков у женщин с герпесвирусными инфекциями.
При подготовке к беременности в сыворотке крови с 26 дня менструального цикла до 2 дня менструации и/или во время менструации в менструальной крови определяется концентрация АМГФ (альфа-2-микроглобулин фертильности, РР14).
Во время беременности в первом триместре определяются:
Во втором триместре определяются:
В третьем триместре определяются:
АМГФ (альфа-2-микроглобулин фертильности, РР14)
Определение содержания АМГФ в кровянистых выделениях матки после ранних самопроизвольных абортов показало, что при потере беременности концентрация АМГФ в 50-100 раз превышает уровень белка в нормальной менструальной крови. Поэтому тест на АМГФ может быть использован для дифференциальной диагностики маточных кровотечений и установления причины женского бесплодия. Резкое увеличение содержания АМГФ в сыворотке крови отмечается при тяжелом эндометриозе. При хроническом эндометрите отмечено уменьшение содержания АМГФ в эндометриальном секрете в среднем в 5 раз по сравнению с нормой. Это уменьшение было особенно выраженным при хроническом эндометрите с недостаточностью лютеиновой фазы (более чем в 20 раз по сравнению с нормой). При ановуляторном цикле АМГФ в секрете эндометрия не обнаружен.
При наступлении беременности содержание АМГФ в сыворотке быстро увеличивается, достигая максимума между 6 и 12 неделями. После 16 недель концентрация АМГФ уменьшается и выходит на плато начиная с 24 недель беременности. В первом триместре уровень АМГФ в сыворотке крови матери перестает нарастать или падает при угрозе невынашивания беременности еще до начала клинических проявлений. Так как уровень АМГФ чрезвычайно индивидуален, целесообразно его исследование в первом триместре в динамике 2-3 раза с интервалом в 2-3 недели.
ТБГ(трофобластический бета-1-гликопротеин)
ТБГ – специфический белок беременности и связанных с нею заболеваний (пузырный занос, хорионэпилиома), синтезируется клетками цито- и синцитиотрофобласта и секретируется в кровоток матери. ТБГ обнаруживается в сыворотке крови на протяжении всей беременности, начиная с самых ранних сроков. По мере развития физиологической беременности уровень ТБГ в сыворотке крови постоянно возрастает, достигая максимума к 35-38 неделям. Наблюдается отсутствие положительной динамики или снижение концентраций ТБГ в сыворотке крови беременных женщин по сравнению с нормой:
Уровень ТБГ в сыворотке крови матери резко возрастает при многоплодии, сахарном диабете, гемолитической болезни плода, перенашивании беременности.
В связи с широким диапазоном индивидуальных концентраций ТБГ, рекомендуется его исследование в динамике 2-3 раза с интервалом в 1-2 недели.
Плацентарный альфа-1-микроглобулин (ПАМГ)
Повышенный уровень ПАМГ-1 является:
Задержка внутриутробного роста плода при повышенном уровне ПАМГ-1 может быть обусловлена нарушениями развития и созревания плаценты. Ряд исследователей рассматривают ПАМГ-1 как естественный «материнский» регулятор инвазивности трофобласта. Вероятно, что в аномально высоких концентрациях ПАМГ препятствует нормальному внедрению цитотрофобласта в спонгиозный слой эндометрия и ограничивает рост трофобласта ворсинчатого хориона.
Концентрация ПАМГ-1 в материнской сыворотке в норме не превышает 40 нг/мл на протяжении всей беременности. Для выявления фетоплацентарных нарушений рекомендуется исследовать сыворотку крови матери, начиная с 16-17 недели беременности до 33-35 недель беременности.
Наш медицинский центр оказывает самый широкий спектр услуг. Вы всегда можете обратится к нам по вопросам ведения беременности. Мы готовы оказать вам услуги ведения беременности после эко и ведения поздней беременности.
Миома матки
Миома матки – доброкачественная опухоль матки, довольно часто встречающееся заболеванием. Диагностируется заболевание у 20% тридцатилетних женщин. Длительное время миому было принято считать опухолью доброкачественного характера, которая может стать злокачественной исключительно при определенных условиях. Единственным методом лечения при диагностировании миомы до недавнего времени считалось удаление опухоли вместе органом, то есть с маткой. Сегодня специалисты рассматривают миому как реакцию организма на причиненные матке повреждения. Факторами болезни являются:
Формируется миома из соединительной или мышечной ткани. Размер ее может составлять от пары миллиметров до 1-8 сантиметров. Локализоваться опухоль может на шейке матки или на теле. При обследовании нередко выявляется несколько узлов разной величины.
Возникает миома по причине активного деления клеток матки, которое стимулируют эстрогены. Одной из особенностей данного заболевания является то, что выявление в результате анализа крови нормального баланса содержания прогестерона и эстрогенов не является гарантией того, что миома отсутствует. Для того чтобы быть уверенным в отсутствии данного заболевания, требуется серьезное обследование с использованием современных методов диагностики. Диагностика позволяет также выявить место расположения образования: в полости матки, в брюшной полости, в стенке матки.
Миома практически никогда не диагностируется у девушек до 25 лет и у женщин после 50 лет. Наибольшей опасности подвергаются женщины после 25 и до 50. Особенно высока вероятность развития миомы в периоды общего снижения иммунитета, во время воспалений половой сферы, во время беременности. В последние годы диагноз «миома матки» нередко ставят девушкам 17-18 лет.
Симптомы миомы матки
О том, что у женщины развивается миома матки, она может и не подозревать, поскольку внешние признаки могут и не проявляться. Нередко случается так, что осмотр пациентки гинеколог проводит по совершенно другим причинам (например, профосмотр) и во время обследования выявляет новообразование. Симптомы проявляются активно в случаях, когда матка вырастает до больших размеров, но если опухоль небольшая, симптомов может и не быть.
Миома матки схожа симптоматикой со многими болезнями репродуктивных органов. Среди наиболее частых симптомов, по которым можно определить образование и развитие миомы, являются:
Своевременное обращение к специалисту позволяет выявить проблему на ранних стадиях, избежав таким образом необходимости в оперативном вмешательстве.
Причины возникновения миомы
Основная причина – гормональные сбои по причине увеличения концентрации эстрогенов. Во время менопаузы концентрация эстрогена понижается, и миома может самостоятельно исчезнуть, без какого-либо лечения. Но рассчитывать на такой результат специалисты не рекомендуют, советуя женщинам при появлении первых симптомов как можно скорее обращаться к врачу.
Спровоцировать появление болезни может целый ряд факторов:
Некоторые факторы, являющиеся причиной появления миозных новообразований, заслуживают более пристального внимания.
В группу риска входят женщины до 35 лет, у которых диагностирована гипертония или наличествуют проблемы ожирением (обмен веществ). Также причиной могут стать воспаление, принявшее форму хронического, травмы и применение контрацептивов орально.
Вероятность развития заболевания зависит в немалой степени от того, сколько и как часто женщина рожала, продолжительности и наличия грудного вскармливания, сколько было доношенных и сколько было прерванных беременностей. У рожавшей хоть единожды женщины вероятность развития миомы значительно меньше, чем у нерожавшей.
Неправильное питание или несбалансированный рацион. Недостаточное количество волокон в пище, высокий процент жирных кислот и избыточная калорийность продуктов питания значительно повышают шансы на возникновение новообразования. Если в организме процент жира значительно превышает норму, гормональный баланс может сместиться и числа эстрогенов увеличится, что, в свою очередь, повышает риск образования опухолей.
Диагностика миомы матки
Самый простой и надежный способ своевременно выявить миому – ежегодно посещать осмотры врача-гинеколога. Установлено наличие развивающейся миомы может быть во время влагалищного гинекологического исследования – матка определяется как бугристая, плотная, увеличенная. При обнаружении заболевания для подтверждения диагноза может быть проведено диагностическое выскабливание, после чего соскоб исследуют гистологическими методами. Диагностирование опухоли возможно также с применением следующих методов:
В некоторых случаях специалист, при наличии некоторых симптомов, но при отсутствии узлов миомы, рекомендует пациентке пройти УЗИ через 6 месяцев.
Какой врач лечит миому матки
При проявлении определенных симптомов, указывающих на наличие новообразования (тянущие боли внизу живота, нестабильные месячные, длительные кровотечения и пр.), женщины задумываются о том, к какому специалисту им следует обратиться. Лечением миомы занимаются гинекологи и гинекологи-хирурги. Гинекологи проводят первичный осмотр, дают назначения на диагностику и по результатам диагностирования определяют способ (метод) наиболее эффективный для восстановления здоровья женщины. В случае если по результатам анализов, показана операция, ее проводят гинекологи-хирурги.
Клиника АО «Медицина» в Москве оказывает услуги диагностики и лечения миомы матки. К услугам пациенток высококвалифицированные специалисты, владеющие самыми современными методиками лечения и эффективно использующие традиционные методики. Клиника оснащена современным оборудованием диагностическим и лечебным, что позволяет специалистам медицинского заведения успешно излечивать самые сложные случаи.
Для того чтобы удостовериться в высокой квалификации специалистов в области гинекологии, работающих в клинике АО «Медицина», достаточно посетить раздел «Наши врачи» на официальном сайте клиники.
Методы лечения миомы матки
При выборе метода гинеколог учитывает множество факторов, основными из которых являются:
возраст пациентки (если пациентка вышла из детородного возраста, специалист может порекомендовать медикаментозное лечение);
Пациентки с диагнозом «миома матки» в обязательном порядке наблюдаются у гинеколога, в большинстве случаев частота визитов составляет раз в три месяца.
В зависимости от состояния опухоли и других факторов гинеколог выбирает один из двух способов лечения:
Лечение миомы без хирургии
Консервативное или терапевтическое лечение может быть назначено специалистом, если:
Консервативное лечение заболевания предусматривает применение лекарственных препаратов. В перечне базовых мероприятий, проведение которых позволяет устранить миому без операции, действия, направленные на достижение следующих целей:
Нормализация обмена веществ путем коррекции диеты пациентки.
Нормализация менструального цикла для того, чтобы исключить вероятность длительных кровотечений.
Предотвращение проявления симптомов анемии.
Восстановление иммунитета в целях повышения защитных свойств организма.
Восстановление микрофлоры половых органов и лечение диагностированных заболеваний.
Консервативное лечение применяется в случаях, если диагностирована миома небольших размеров при отсутствии четко выраженных симптомов. Наиболее распространенным способом лечения является назначение гормональных препаратов. Данные препараты представляют собой производные прогестерона и действуют следующим образом: одновременно нормализуют функцию яичников и препятствуют дальнейшему развитию новообразования. Препараты вводятся путем инъекций раз в месяц на протяжении 6 месяцев. Прием препаратов позволяет уменьшить размеры матки на 55% и более.
Данная методика используется в большинстве случаев при диагностировании миомы у женщин старшего возраста, поскольку о молодых женщин вероятно развитие остеопороза. Недостаток методики в том, что консервативные методы могут только затормозить развитие болезни, но не устранить ее полностью. При лечении таким способом женщин старшего возраста высока вероятность того, что при наступлении менопаузы миома рассосется самостоятельно.
Ультразвуковой метод
Методика ФУЗ-абляции относится к прогрессивным методам лечения. Основой методики является коагуляция узлов миомы путем направленных импульсов ультразвука фокусированного. Контролируется процесс с помощью МРТ. Данная процедура имеет множество преимуществ по сравнению с удалением миомы путем операции, но эффективна она только при наличии определенных характеристик, поэтому решение о применении ФУЗ-абляции принимается исключительно в индивидуальном порядке после тщательного обследования.
Применение метода ФУЗ-абляции имеет множество преимуществ:
Операбельное лечение миомы матки
Проведение операций при постановке диагноза «миома матки» возможно в тех случаях, когда все другие способы лечения неэффективны. Наиболее щадящим вариантом операбельного лечения является проведение лапароскопии, щадящей для организма и позволяющей полностью сохранить репродуктивную функцию. Среди преимуществ данной методики:
Метод эмболизации маточных артерий (ЭМА)
ЭМА начали применять сравнительно недавно. Методика заключается в том, что питание миоматозного узла прекращается, поскольку останавливается кровоток по артериям. После того, как хирург обнаруживает сосуд, в него вводится препарат, останавливающий кровоток. После прекращения кровоснабжения узлы миомы полностью исчезают или значительно уменьшаются в размерах. Одним из преимуществ операции является полное исчезновение симптомов. Кроме того, после проведения операции полностью отсутствует риск рецидива.
Хирургия миомы
Хирургия показана, если:
В зависимости от результатов обследования, возраста пациентки и других факторов гинеколог может назначить:
Молодым нерожавшим женщинам назначается консервативное хирургическое лечение.
Миомэктомия, представляющая собой процедуры, направленные на вылущивание миозных узлов, позволяет сохранить репродуктивную функцию:
Если пациентка не намерена рожать, а результаты обследования указывают на полное удаление органа, гинекологи используют одну из методик радикальной хирургии:
Показания к операционному лечению миомы матки
Хирургическое вмешательство является единственным способом излечения при следующих факторах:
Способ миэктомии определяется хирургом в зависимости от локализации новообразования, тяжести заболевания, типа миомы, индивидуальных особенностей пациентки.
Противопоказания при диагностировании миомы матки
Существует несколько противопоказаний, в частности, категорический запрет на посещение саун, бань, пляжа – то есть, любого места, где вероятен перегрев.
При выборе метода лечения противопоказаны следующие способы:
Стоимость обследования, диагностики и лечения миомы матки
Клиника АО «Медицина» предлагает услуги первичного обследования, диагностики и лечения по ценам, ознакомиться с которыми можно в таблице ниже или в соответствующем разделе сайта клиники.
Общая стоимость лечения определяется после первичного обследования и выбора наиболее эффективного курса лечения. Специалисты АО «Медицина» (клиника академика Ройтберга) в Москве используют наиболее эффективные методики, современное высокоточное диагностическое оборудование, безопасные материалы и эффективные препараты.
Преимущества лечения миомы в клинике АО «Медицина»
АО «Медицина» (клиника академика Ройтберга) в Москве предлагает услуги специалистов высокой квалификации, имеющих богатый опыт в области лечения миомы матки и располагающих современным оборудованием. Весомыми факторами в пользу выбора клиники АО «Медицина» для лечения миомы матки являются:
Обратившись в клинику АО «Медицина» в Москве, вы гарантированно получите высокопрофессиональную медицинскую помощь и первоклассное обслуживание.