Левофлоксацин при ангине у взрослых можно принимать или нет
(1) ФГБУ НКЦ оториноларингологии ФМБА России, Москва (2) ФГБОУ ДПО РМАНПО Минздрава России, Москва
Впрактике врача-оториноларинголога бывают ситуации, когда стартовая эмпирическая антибактериальная терапия не приводит к быстрому эффекту. В этом случае, оценивая состояние пациента через 72 часа, врачу необходимо сменить антибиотик на более сильный, с широким спектром действия. При этом нередко смену осуществляют на антимикробные средства класса хинолонов – фторхинолоны. Препаратам этой группы присущи хорошие фармакокинетические свойства, высокая степень проникновения в ткани и клетки как человека, так и микроорганизма.
Фторхинолоны выгодно отличаются от других антибиотиков своими свойствами: ингибированием фермента ДНК-гиразы – фермента бактериальной клетки, с широким спектром антимикробного действия (грамотрицательные и грамположительные аэробные бактерии, микобактерии, Mycoplasma pneumonia, Chlamydia pneumoniae); высокой степенью бактериальной активности; возможностью создания в тканях и клетках человека концентраций препаратов, близких к сывороточным или их превышающих; хорошей переносимостью и небольшой частотой побочных эффектов. Кроме того, длительный период полувыведения определяет удобный режим дозирования – 1–2 раза в сутки. Так, препарат этой группы левофоксацин при приеме внутрь имеет большой объем распределения и достигает высоких концентраций в тканях, фагоцитах и жидкостях организма, в частности в тканях околоносовых пазух, а также в макрофагах [1].
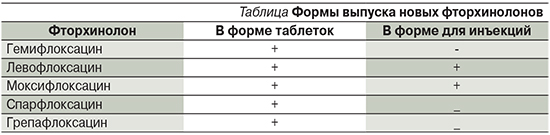
В настоящее время синтезированы новые препараты группы фторхинолонов, проявляющие более высокую активность в отношении грамположительных бактерий, прежде всего пневмококков, что позволило выделить их в отдельную подгруппу – 2-го поколения, или новые фторхинолоны (см. таблицу). При этом левофлоксацин и моксифлоксацин выпускают в двух формах: в таблетках и для внутримышечного введения, что позволяет использовать их в виде ступенчатой терапии, что снижает стоимость лечения.
Препараты этой группы оказывают выраженное действие на грамотрицательные бактерии (Moraxella catarrhalis, Legionella spp.), Haemophilus influenzae (включая штаммы, продуцирующие β-лактамазы) [2].
Препараты группы новых фторхинолонов обладают более высокой природной активностью в отношении Streptococcus pneumoniae по сравнению с ранними фторхинолонами (например, левофлоксацин – 1 мг/л). В связи с этим их целесообразно назначать при внебольничных инфекциях дыхательных путей. При этом активность новых фторхинолонов не различается в отношении пенициллинчувствительных и пенициллинрезистентных штаммов пневмококка. В настоящее время установлено, что резистентность пневмококков к новым фторхинолонам минимальная (менее 1%). Высокая активность фторхинолонов 2-го поколения в отношении S. pneumoniae крайне важна, т.к. острые и хронические заболевания в настоящее время достаточно часто вызывает этот патоген.
Препараты группы новых фторхинолонов превосходят ранние по активности в отношении других стрептококков (группы А и С) и стафилококков (Staphylococcus aureus). В отношении Pseudomonas aeruginosa самым активным фторхинолоном остается ципрофлоксацин, из новых фторхинолонов реальной антипсевдомонадной активностью обладает лишь левофлоксацин.
Установлено, что совместный прием ряда препаратов (антациды, сукральфат, соли висмута, кальция, препараты железа) уменьшает биодоступность фторхинолонов при их пероральном приеме, что может приводить к снижению эффективности последних. Следует иметь в виду, что прием пищи замедляет всасывание фторхинолонов.
Имеются ограничения применения препаратов этой группы для беременных и кормящих женщин, детей и подростков в возрасте до 16–18 лет. Это выявлено в эксперименте о повреждающем действии фторхинолонов в отношении хрящевой ткани неполовозрелых животных. Однако эти данные не подтверждены в клинике. Но такое противопоказание оправданно, т.к. строго ограничивает широкое нерациональное использование фторхинолонов в педиатрии до получения надежных доказательств их безопасности для пациентов этой категории.
Анализ базы данных фармаконадзора Италии показал, что относительный риск развития побочных эффектов при применении левофлоксацина не отличался от такового у пероральных антибиотиков других классов [3].
К наиболее частым побочным эффектам при применении фторхинолонов относятся симптомы со стороны желудочно-кишечного тракта (тошнота, рвота, диарея, боли в животе, изменения вкуса), однако в большинстве случаев они носят умеренный характер и не требуют отмены лечения.
В клинических исследованиях левофлоксацина наиболее распространенным побочным эффектом была диарея, встречавшаяся с частотой 4–6%, что существенно ниже, чем при применении пероральных пенициллинов или цефалоспоринов [4]. Побочные эффекты со стороны центральной нервной системы – ЦНС (головная боль, головокружение и нарушения сна), являющиеся классовым эффектом фторхинолонов, при лечении левофлоксацином (1%) наблюдались реже.
Все фторхинолоны примерно с одинаковой частотой вызывают реакции со стороны ЦНС (5–8%), минимальная нейротоксичность отмечена у офлоксацина и левофлоксацина. Реакции со стороны ЦНС характерны для всех препаратов этого класса. Однако их наблюдают нечасто, они, как правило, проявляются головной болью, головокружением, сонливостью, расстройством сна (эти симптомы обычно возникают в 1-й день лечения и исчезают сразу после отмены). Развитие судорог описано значительно реже. Они возникают в основном на 3–4-й день лечения у больных, имеющих предрасполагающие факторы (эпилепсию, мозговую травму, гипоксию, пожилой возраст, сочетанное применение с теофиллином или нестероидными противовоспалительными средствами) и саморазрешаются при отмене препарата [5].
Частота возникновения кожных сыпей при применении левофлоксацина составляет 0,2% [6]. Частота анафилактоидных реакций при лечении левофлоксацином сопоставима с таковой у большинства препаратов этой группы – 1,8–23,0 на 1 млн дней лечения [6]. Частота развития анафилаксии на 1 млн суточных доз составила для левофлоксацина 0,6 [7].
В клинических исследованиях левофлоксацина гепатобилиарные поражения встречались в 0,1–1,0% случаев [6]. Частота гепатита, некроза печени и печеночной недостаточности при лечении левофлоксацином, согласно данным Фармаконадзора Франции, составляет 500 мс, а также избегать сочетанного применения фторхинолонов с другими лекарственными средствами, вызывающими удлинение интервала QT [10, 11].
В эпидемиологических исследованиях частота развития тендинопатий при применении фторхинолонов составила 1:2000 [10], по данным FDA (Food and Drug Administration), 1,3–5,6 на 10 тыс. пациенто-лет [12]. Пятилетнее наблюдение за детьми (n=6000), принимавшими антибиотики, показало, что частота поражений сухожилий или суставов при применении левофлоксацина, составляет
1. Torres A., Liapikou A. Levofloxacin for the treatment of respiratory tract infections. Expert. Opin. Pharmacother. 2012;13(8):1203–12.
2. Яковлев С.В. Место фторхинолонов в лечении бактериальных инфекций. РМЖ. 2003;8:434–49.
3. Salvo F., Polimeni G., Cutroneo P.M., Leone R., Confortic A., Moretti U., Motola D., Tuccori M., Caputi A.P. Allergic reactions to oral drugs: a case/non-case study from an Italian spontaneous reporting database (GIF). Pharmacol. Res. 2008;58:202–7.
4. Stahlmann R., Lode H.M. Risks associated with the therapeutic use of fluoroquinolones. Expert. Opin. Drug. Saf. 2013;12(4):497–505.
5. Lipsky B.A., Baker C.A. Fluoroquinolone toxicity profiles: a review focusing on newer agents. Clin. Infect. Dis 1999;28(2):352–64.
6. Liu H.H. Safety profile of the fluoroquinolones: focus on levofloxacin. Drug. Saf. 2010;33:353–69.
7. Blanca-López N., Andreu I., Torres Jaén M.J. Hypersensitivity reactions to quinolones. Curr. Opin. Allergy. Clin. Immunol. 2011;11:285–91.
8. Carbon C. Effets indésirables de la lévofloxacine: données des études cliniques et de la pharmacovigilance. Therapie. 2001;56:35–40.
9. Owens R.C., Ambrose P.G. Antimicrobial safety: focus on fluoroquinolones. Clin. Infect. Dis. 2005;41(Suppl. 2):144–57.
10. Stahlmann R., Lode H.M. Risks associated with the therapeutic use of fluoroquinolones. Expert. Opin. Drug. Saf. 2013;12(4):497–505.
11. Zipes D.P., Camm A.J., Borggrefe M., et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death-еxecutive summary: A report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death) Developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Eur. Heart J. 2006;27(17):2099–114.
12. Arabyat R.M., Raisch D.W., McKoy J.M., Ben-nett C.L. Fluoroquinolone-associated tendon-rupture: a summary of reports in the Food and Drug Administration’s adverse event reporting system. Expert. Opin. Drug. Saf. 2015;14(11):1653–60.
13. Yee C.L., Duffy C., Gerbino P.G., Stryker S., Noel G.J. Tendon or joint disorders in children after treatment with fluoroquinolones or azithromycin. Pediatr. Infect. Dis. J. 2002;21(6):525–29.
14. Gilbert P., J. Das and I. Foley. Biofilms susceptibility to antimicrobials. Adv. Dent. Res. 1997;11:160–67.
15. Brooun A., Liu S., Lewis K. A dose-responsestudy of antibiotic resistance in Pseudomonas aeruginosa biofilms. Antimicrob. Agents Chemo-ther. 2000;44:640–46.
16. Lewis K., Spoering A.L., Kaldalu N., et al. Persisters: specialized cells responsible for biofilm tolerance. Biofilms, infection and antimicrobial therapy. Ed. by Pace J.L., Rupp M., Finch R.G. Taylor & Francis Group. 2005. P. 241–57.
17. Goto T., Nakame Y., Nishida M., Ohi Y. In vitro bactericidal activities of beta-laktamases, amikacin and fluoroquinolones against Pseudomonas aeruginosa biofilm in artificial urine. Urology. 1999;53(5):1058–62.
18. Bjarnsholt T. Biofilm infections. Springer. 2011. 314 p.
19. Trampuz A., Zimmerli W. Diagnosis and treatment of infections associated with fractu-refixation devices. Injury. 2006;37:59–66.
20. Costerton J.W., Montanaro L., Arciola C.R. Biofilm in implant infections: its production and regulation. Int. J. Artif. Organs. 2005;11:1062–68.
21. Catheter-Related Infections (Infectious Disease and Therapy). Ed. by Seifert H., Bernd J., Farr B.M. Marcel Dekker. 2005. 519 p.
22. Мележик И.А., Яворская Н.В., Шепелевич В.В., Кокозей В.Н. Роль боипленок Pseudomonas aeruginosa в развитии эндогенных инфекций. Бюллетень Оренбургского научного центра УрО РАН (электронный журнал)., 2013;3.
23. Бузолева Л.С., Пузь А.В., Синебрюхов С.Л., Гнеденков С.В., Ким А.В., Еськова А.И., Пономарева А.Л. Имптантат-ассоцииро-ванные инфекции, связные с проблемой биопленкообразования. Современные проблемы науки и образования. 2016;5. URL: https://science-education.ru/ru/article/view?id=25430.
24. Shehab N., Patel P.R., Srinivasan A., Budnitz D.S. Emergency department visits for antibiotic-associated adverse events. Clin. Infect. Dis. 2008;47:735–43.
25. Крюков А.И., Кунельская Н.Л., Гуров А.В., Туровский А.Б., Изотова Г.Н. Клиника, диагностика и лечение бактериального синусита. Метод. рекомендации №23. М., 2013. 27 с.
26. IMS Health National Sales Perspective (NSP), Y2014. Source File: NSP_2015-896 FQ AC 2014.
Регистрационный номер:
Торговое наименование препарата:
Международное непатентованное или группировочное наименование:
Лекарственная форма:
Состав:
1 капсула 250 мг содержит:
Действующее вещество: Левофлоксацина гемигидрата 256,23 мг, в пересчете на безводный левофлоксацин 250 мг.
Вспомогательные вещества: целлюлоза микрокристаллическая, тип 101 84,86 мг, гипромеллоза 1,2 мг, повидон К30 4,71 мг, кальция стеарат 3,0 мг.
Состав оболочки капсул:
корпус: титана диоксид (Е171) – 2,0%, желатин – до 100%.
крышечка: титана диоксид (Е171) – 1,00%, индигокармин (Е132) – 0,13330%, желатин – до 100%.
1 капсула 500 мг содержит:
Действующее вещество: Левофлоксацина гемигидрата 512,46 мг, в пересчете на безводный левофлоксацин 500 мг.
Вспомогательные вещества: целлюлоза микрокристаллическая, тип 101 71,07 мг, гипромеллоза 2,4 мг, повидон К30 8,07 мг, кальция стеарат 6,0 мг.
Состав оболочки капсул:
корпус: титана диоксид (Е171) – 2,0%, желатин – до 100%.
крышечка: титана диоксид (Е171) – 1,00%, индигокармин (Е132) – 0,13330%, желатин – до 100%.
Описание
Капсулы 250 мг: твердые желатиновые капсулы № 0 с непрозрачным корпусом белого цвета и непрозрачной крышечкой голубого цвета. Содержимое капсул – смесь гранул и порошка светло-желтого цвета.
Капсулы 500 мг: твердые желатиновые капсулы № 00 с непрозрачным корпусом белого цвета и непрозрачной крышечкой голубого цвета. Содержимое капсул – смесь гранул и порошка светло-желтого цвета.
Фармакотерапевтическая группа:
противомикробное средство, фторхинолон.
Код ATX:
Фармакологические свойства
Фармакодинамика
Препарат Левофлоксацин – синтетический антибактериальный препарат широкого спектра действия из группы фторхинолонов, содержащий в качестве действующего вещества левофлоксацин – левовращающий изомер офлоксацина. Левофлоксацин блокирует ДНК-гиразу и топоизомеразу IV, нарушает суперспирализацию и сшивку разрывов ДНК, ингибирует синтез ДНК, вызывает глубокие морфологические изменения в цитоплазме, клеточной стенке и мембранах микробных клеток.
Левофлоксацин активен в отношении большинства штаммов микроорганизмов, как в условиях in vitro, так и in vivo.
Чувствительные микроорганизмы (МПК ≤2 мг/л, зона ингибирования >17 мм)
Умеренно чувствительные микроорганизмы (МПК = 4 мг/л, зона ингибирования 16-14 мм)
Резистентные к левофлоксацину микроорганизмы (МПК ≥8 мг/л, зона ингибирования ≤13 мм)
Другие микроорганизмы: Mycobacterium avium.
Резистентность
Резистентность к левофлоксацину развивается в результате поэтапного процесса мутаций генов, кодирующих обе топоизомеразы типа II: ДНК-гиразу и топоизомеразу IV. Другие механизмы резистентности, такие как механизм влияния на пенетрационные барьеры микробной клетки (механизм, характерный для Pseudomonas aeruginosa) и механизм эффлюкса (активного выведения противомикробного средства из микробной клетки), могут также уменьшать чувствительность микроорганизмов к левофлоксацину.
В связи с особенностями механизма действия левофлоксацина обычно не наблюдается перекрестной резистентности между левофлоксацином и другими противомикробными средствами.
Клиническая эффективность (эффективность в клинических исследованиях при лечении инфекций, вызываемых перечисленными ниже микроорганизмами)
Фармакокинетика
Левофлоксацин быстро и практически полностью всасывается после приема внутрь, прием пищи мало влияет на его абсорбцию. Абсолютная биодоступность при приеме внутрь составляет 99-100%. После однократного приема 500 мг левофлоксацина максимальная концентрация (Сmax) в плазме крови достигается в течение 1-2 ч и составляет 5,2±1,2 мкг/мл. Фармакокинетика левофлоксацина является линейной в диапазоне доз от 50 мг до 1000 мг. Равновесная концентрация левофлоксацина в плазме крови при приеме внутрь 500 мг левофлоксацина 1 или 2 раза в сутки достигается в течение 48 ч.
На 10 день приема внутрь левофлоксацина 500 мг 1 раз в сутки Сmax левофлоксацина составляла 5,7±1,4 мкг/мл, а минимальная концентрация левофлоксацина (концентрация перед приемом очередной дозы) (Cmin) в плазме крови составляла 0,5 ± 0,2 мкг/мл.
На 10 день приема внутрь левофлоксацина 500 мг 2 раза в сутки Сmax в плазме крови составляла 7,8±1,1 мкг/мл, a Cmin – 3,0±0,9 мкг/мл.
Связывание с белками сыворотки крови составляет 30-40%. После однократного и повторного приема внутрь 500 мг левофлоксацина объем распределения левофлоксацина составляет в среднем 100 л., что указывает на хорошее проникновение левофлоксацина в органы и ткани организма человека.
Проникновение в слизистую оболочку бронхов, жидкость эпителиальной выстилки, альвеолярные макрофаги
После однократного приема внутрь 500 мг левофлоксацина Сmax в слизистой оболочке бронхов и жидкости эпителиальной выстилки достигались в течение 1 ч или 4 ч и составляли 8,3 мкг/г и 10,8 мкг/мл, соответственно, с коэффициентами пенетрации в слизистую оболочку бронхов и жидкость эпителиальной выстилки по сравнению с концентрацией в плазме крови, составляющими 1,1-1,8 и 0,8-3,0 соответственно.
После 5 дней приема внутрь 500 мг левофлоксацина средние концентрации левофлоксацина через 4 ч после последнего приема препарата в жидкости эпителиальной выстилки составляли 9,94 мкг/мл и в альвеолярных макрофагах – 97,9 мкг/мл.
Проникновение в легочную ткань
Сmax в легочной ткани после приема внутрь 500 мг левофлоксацина составляли приблизительно 11,3 мкг/г и достигались через 4-6 ч после приема препарата с коэффициентами пенетрации 2,0-5,0 по сравнению с концентрацией в плазме крови.
Проникновение в альвеолярную жидкость
После 3 дней приема 500 мг левофлоксацина 1 или 2 раза в сутки Сmax левофлоксацина в альвеолярной жидкости достигались через 2-4 ч после приема препарата и составляли 4,0 мкг/мл и 6,7 мкг/мл, соответственно, с коэффициентом пенетрации 1,0 по сравнению с концентрациями в плазме крови.
Проникновение в костную ткань
Левофлоксацин хорошо проникает в кортикальную и губчатую костную ткань, как в проксимальных, так и в дистальных отделах бедренной кости, с коэффициентом пенетрации (костная ткань/плазма крови) 0,1-3,0. Сmax левофлоксацина в губчатой костной ткани проксимального отдела бедренной кости после приема 500 мг препарата внутрь составляли приблизительно 15,1 мкг/г (через 2 ч после приема препарата).
Проникновение в спинномозговую жидкость
Левофлоксацин плохо проникает в спинномозговую жидкость.
Проникновение в ткань предстательной железы
После приема внутрь 500 мг левофлоксацина 1 раз в сутки в течение 3-х дней, средняя концентрация левофлоксацина в ткани предстательной железы составляла 8,7 мкг/г, среднее соотношение концентраций предстательная железа/плазма крови составляло 1,84.
Концентрации в моче
Средние концентрации в моче через 8-12 ч после приема внутрь дозы 150 мг, 300 мг и 600 мг левофлоксацина составляли 44 мкг/мл, 91 мкг/мл и 162 мкг/мл, соответственно.
Левофлоксацин метаболизируется в незначительной степени (5% принятой дозы). Его метаболитами являются дезметиллевофлоксацин и N-оксид левофлоксацин, которые выводятся почками. Левофлоксацин является стереохимически стабильным и не подвергается хиральным превращениям.
После приема внутрь левофлоксацин относительно медленно выводится из плазмы крови (период полувыведения [Т1/2] – 6-8 ч). Выведение преимущественно почками (более 85% принятой дозы). Общий клиренс левофлоксацина после однократного приема 500 мг составлял 175±29,2 мл/мин.
Отсутствуют существенные различия в фармакокинетике левофлоксацина при его внутривенном введении и приеме внутрь, что подтверждает, что прием внутрь и внутривенное введение являются взаимозаменяемыми.
Фармакокинетика у отдельных групп пациентов
Фармакокинетика левофлоксацина у мужчин и женщин не различается.
Фармакокинетика у пациентов пожилого возраста не отличается от таковой у молодых пациентов, за исключением различий фармакокинетики, связанных с различиями в клиренсе креатинина (КК).
При почечной недостаточности фармакокинетика левофлоксацина изменяется. По мере ухудшения функции почек выведение через почки и почечный клиренс (CIR) уменьшаются, а Т1/2 удлиняется.
Фармакокинетика при почечной недостаточности после однократного приема внутрь 500 мг левофлоксацина
Режим дозирования у пациентов с нарушением функции почек (КК ≤50 мл/мин)
Левофлоксацин выводится преимущественно почками, поэтому при лечении пациентов с нарушенной функцией почек требуется снижение дозы препарата (см. таблицу ниже).
Боль в горле
Подбор ЛС для лечения тонзиллита
Роза Исмаиловна Ягудина, д. ф. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Одной из наиболее распространенных жалоб в осеннее-зимний и, как ни странно, в летний периоды является боль в горле. Причинами возникновения болезненных ощущений могут стать различные патогенетические процессы, происходящие в организме человека, а летом – еще и нарушение экологической обстановки (влажный, запыленный воздух, кондиционеры). Наиболее частыми разновидностями поражений горла являются ларингит, фарингит и тонзиллит. Последнее из перечисленных заболеваний – это воспаление небных миндалин. Тонзиллит является самой распространенной причиной болей в горле, более того, нередко воспаление имеет хроническую форму течения.
Причины и механизм возникновения тонзиллита
Боль в горле, как считают сами пациенты, всегда связана с переохлаждением. Однако этиология развития поражений ротоглотки весьма разнообразна: от бактерий до вирусов. Возникновение болевого синдрома в этих случаях практически всегда связано с поражением небных миндалин, располагающихся на боковых стенках ротоглотки – стыке респираторного и пищеварительного трактов. Миндалины имеют множество лакун, в которые открываются крипты, или мешки, имеющие дихотомическое деление и погруженные в глубину миндалин. Такое строение миндалин способствует скоплению в них различных экссудатов. Небные миндалины не имеют приводящих лимфатических сосудов, так как сами активно продуцируют лимфоциты. Также небные миндалины принимают активное участие в формировании местного и общего иммунитета.
NB! Нельзя путать ангину и хронический тонзиллит (точнее, его обострение, которое при схожих симптомах требует иного лечения).
Ангина – общее инфекционное заболевание, с острым воспалением компонентов лимфаденоидного глоточного кольца (чаще именно небных миндалин). Ангины разделяют на: первичные, вторичные и специфические.
Хронический тонзиллит – хронический воспалительный, периодически обостряющийся очаг инфекции в небных миндалинах с общей инфекционно-аллергической реакцией.
Механизм распространения инфекции – воздушно-капельный, в основном происходит при кашле, чихании, поцелуе, пользовании одной посудой, полотенцами и пр. Наиболее частой причиной развития хронического тонзиллита является β-гемолитический стрептококк группы А, другими возбудителями – St. Aureus, H. influenzae, M. Catarrhalis, N. Gonorrhoeae, C. haemolyticum, M. Pneumoniae, C. pneumoniae, Toxoplasma, анаэробы, аденовирусы, цитомегаловирусы, вирусы герпеса и др. Хронический тонзиллит не всегда является следствием перенесенной ангины. В большинстве случаев он развивается незаметно, маскируясь под другие заболевания (ОРВИ, стоматит и др.). При прогрессировании тонзиллита медленно происходит замещение паренхимы миндалин соединительной тканью, образуются инкапсулированные очаги некроза, в воспаление вовлекаются регионарные лимфатические узлы. Выделяют несколько форм и видов хронического тонзиллита с различными симптомами.
Наличием только местных признаков характеризуется тонзиллит простой формы (начальная стадия)
Также на этой стадии могут обостряться другие, не связанные с тонзиллитом заболевания, которые могут иметь серьезные последствия.
Токсико-аллергическая форма I (ТАФ I) – обусловлена неоднократно перенесенными ранее ангинами. Помимо местных признаков (таких же, как и на начальной стадии), развиваются общие токсико-аллергические явления:
Сопутствующие заболевания в этом случае такие же, как при простой форме, но они не имеют единой инфекционной основы с хроническим тонзиллитом.
Токсико-аллергическая форма II (ТАФ II) – характеризуется местными признаками, присущими простой форме, и общими токсико-аллергическими реакциями:
Сопутствующие заболевания могут быть такими же, как при простой форме (не связаны с инфекцией). Течение данной стадии хронического тонзиллита может сопровождаться развитием тяжелых осложнений: паратонзиллярного абсцесса, тонзиллогенного сепсиса и др.
Лечение тонзиллита
Как избавиться от тонзиллита? Небные миндалины играют большую роль в нормальном функционировании иммунной системы, поэтому лечение заболевания в первую очередь должно предусматривать восстановление защитных функций организма. Фармакотерапия хронического тонзиллита включает в себя комплекс мер, направленных на устранение бактериальный среды, купирование воспаления и устранение гнойных пробок со слизистой оболочки глотки. Лечение хронического тонзиллита проходит в соответствии с формой и фазой заболевания (острый тонзиллит, латентный).
NB! Консервативная терапия проводится на начальной стадии заболевания и ТАФ I вне периода обострения и не ранее 1 месяца после него. Больным с ТАФ II показана тонзилэктомия!
Принципы фармакотерапии хронического тонзиллита:
Иммуномодуляторы
Антисептики
Растворы для полоскания
Важным этапом лечения боли в горле является санация ротоглотки с помощью разнообразных антисептиков. Лучшим вариантом санации является систематическое (до 8–10 раз в сутки) полоскание горла при тонзиллите антисептическими и противовоспалительными растворами фурацилина, настойки листьев эвкалипта (оказывают противомикробное действие), календулы, прополиса (оказывают антисептическое и противовоспалительное действие), препаратами, содержащими НПВП средство бензидамин и т. п.
Упомянутый выше бензидамин выпускается не только в форме раствора, но и в виде спрея, обеспечивающего так называемую «точечную» санацию ротоглотки. Другие спреи, применяющиеся при боли в горле, содержат гексэтидин, повидон-йод, смеси камфоры, левоментола, хлоробутанол и масла эвкалипта.
Другой удобной местной формой санации горла являются таблетки для рассасывания и пастилки на основе тех же антисептиков (комбинация сухого экстракта шалфея с эфирным маслом, амбазон, хлоргексидин в комбинации с тетракаином и витамином C). Как правило, помимо обезболивающего эффекта, таблетки и леденцы оказывают бактерицидное, местно-анестетическое и иммуномодулирующее действие. Основой для местных препаратов для рассасывания также могут быть препараты группы ПНВП: флурбипрофен, ацетиламинонитропропоксибензол, бензидамин.
Антиоксиданты
Антиоксиданты при лечении боли в горле применяются для улучшения метаболизма, восстановления работы ферментных систем и уменьшения разрушительного действия свободных радикалов и перекисных соединений, а также для повышения иммунитета (рутинсодержащие комплексы, витамины группы А, Е, С, микроэлементы Zn, Mg, Si, Fe, Ca, биодобавки, и др.).
Критерии эффективности лечения
Показателями того, что проводимое лечение обладает достаточной эффективностью, являются:
Но даже в этом случае курсы лечения лучше проводить не менее трех раз в год, особенно в период межсезонья.
Однако если у больного даже с простой формой хронического тонзиллита или ТАФ I возникает рецидив, то после первого курса лечения в небных миндалинах сохраняется гной, происходит образование казеозных масс, поэтому необходимо обсудить с пациентом возможность проведения тонзиллэктомии.
Таким образом, консервативное лечение хронического тонзиллита должно в какой-то мере рассматриваться как этап подготовки больного к тонзиллэктомии при хроническом тонзиллите ТАФ I, а при простой форме (при наличии положительного результата лечения) нужно научить пациента поддерживать миндалины в удовлетворительном состоянии – то есть проводить профилактику хронического тонзиллита. Многих интересует, как вылечить хронический тонзиллит раз и навсегда. К сожалению, универсальных рецептов для лечения хронического тонзиллита нет, так как это очаговая инфекция, которая постоянно снижает иммунитет и в любой момент может вызвать обострение состояния больного.
Таблица 1. Список лекарственных препаратов для лечения хронического тонзиллита у взрослых и детей (группа Rx)