мутация de novo что это
Мутация de novo
Впервые возникшее изменение генетической последовательности (последовательности нуклеотидов в ДНК), в отличие от унаследованного.
Это совсем не редкое событие и значение таких мутаций в медицине велико. Генетические заболевания, проявляющиеся расстройствами аутистического спектра (РАС), возникают обычно из-за de novo мутаций — например, синдром Ретта.
Существует предположение, что именно de novo мутации вызывают значительную часть генетически обусловленных случаев аутизма. Такая гипотеза объясняет и то, почему риск аутизма возрастает с возрастом отца. Дело в том, что точечные мутации, возникающие при каждом делении клеток, в большей степени накапливаются с возрастом у мужчин (чьи половые клетки постоянно делятся в течение жизни), чем у женщин (чьи половые клетки не делятся, а пребывают в состоянии покоя вплоть до овуляции). Это значит, что у отцов в позднем репродуктивном возрасте выше вероятность передать потомству возникшие de novo точечные мутации. Правда, стоит отметить, что у женщин с возрастом увеличивается частота другого типа мутаций — изменений числа хромосом, что приводит, например, к синдрому Дауна.
По существующим оценкам, точечные de novo мутации объясняют до 15% случаев РАС, и более протяженные de novo мутации (микроделеции, микродупликации) объясняют еще 3-6%. Однако эти оценки пока нужно рассматривать как предварительные.
Термин мутация в медицинской генетике сейчас рекомендовано заменять на «генетический вариант» — это более нейтральное название (под мутациями многие понимают «нечто вредное», но большинство генетических вариантов нейтральны).
Текст: Екатерина Померанцева, кандидат биологических наук, врач-генетик, заведующая лабораторией Genetico
Медицинские интернет-конференции
Языки
Детекция мутации de novo в гене дистрофина и её значение для медико-генетического консультирования при мышечной дистрофии Дюшенна (клиническое наблюдение)
Муравлева Э.А., Стародубова А.В, Пышкина Н.П., Дуйсенова О.С.
Резюме
Ключевые слова
Статья
Детекция мутации denovo в гене дистрофина и её значение для медико-генетического консультирования при мышечной дистрофии Дюшенна
(клиническое наблюдение)
Муравлева Э.А., Стародубова А.В, Пышкина Н.П., Дуйсенова О.С.
Научный руководитель: д.м.н. доц. Колоколов О.В.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ
Кафедра неврологии ФПК и ППС им. К.Н. Третьякова
Введение. Мышечная дистрофия Дюшенна (МДД) относится к наиболее часто встречающимся наследственным нервно-мышечным болезням. Распространенность её составляет 2-5 : 100000 населения, популяционная частота – 1 : 3500 новорожденных мальчиков. Эта форма мышечной дистрофии впервые описана Edward Meryon (1852г.) и Guillaume Duchenne (1861г.).
Заболевание характеризуется Х-сцепленным рецессивным типом наследования и тяжелым, прогрессирующим течением. МДД обусловлена мутацией в гене дистрофина, локус которого локализован на Xp21.2. Около 30% случаев обусловлены мутациями de novo, 70% – носительством мутации матерью пробанда. Дистрофин отвечает за соединение цитоскелета каждого мышечного волокна с основной базальной пластинкой (внеклеточного матрикса) через белковый комплекс, который состоит из многих субъединиц. Отсутствие дистрофина приводит к проникновению избыточного кальция в сарколему (клеточную мембрану). Мышечные волокна подвергаются некрозу, происходит замещение мышечной ткани жировой, а также соединительной.
Современная диагностика МДД основана на оценке соответствия проявлений болезни клинико-анамнестическим и лабораторно-инструментальным (креатин-киназа сыворотки крови (ККС), электронейромиография (ЭНМГ), гистохимическое исследование мышечного биоптата) критериям, генеалогическом анализе и данных молекулярно-генетического исследования.
Проведение медико-генетического консультирования в настоящее время во многих семьях позволяет предупредить рождение больного ребенка. Пренатальная ДНК диагностика на ранних сроках беременности в семьях, имеющих ребенка, страдающего МДД, позволит выбрать дальнейшую тактику для родителей и, возможно, досрочно прекратить беременность в случае наличия заболевания у плода.
В ряде случаев клиническая картина наблюдается у женщин – гетерозиготных носительниц мутантного гена в виде увеличения икроножных мышц, умеренно выраженной мышечной слабости, снижения сухожильных и периостальных рефлексов, по данным параклинических исследований повышается уровень ККС. Кроме того, классические клинические проявления МДД могут возникать у женщин с синдромом Шерешевского-Тернера (генотип 45, ХО).
Клинический пример. В нашей клинике наблюдается мальчик К., 7 лет, который предъявляет жалобы на слабость в мышцах рук и ног, утомляемость при длительной ходьбе. Мама ребенка отмечает у него периодические падения, затруднения при подъеме по лестнице, нарушение походки (по типу «утиной»), трудности при вставании из положения сидя, увеличение икроножных мышц в объеме.
Раннее развитие ребенка протекало без особенностей. В возрасте 3-х лет окружающие заметили нарушения двигательных функций в виде появления трудностей при ходьбе по лестнице, при вставании, ребенок не принимал участия в подвижных играх, стал быстро уставать. Затем изменилась походка по типу «утиной». Наросли трудности при вставании из положения сидя или из положения лежа: поэтапное вставание «лесенкой» с активным использованием рук. Постепенно стало заметным увеличение икроножных и некоторых других мышц в объеме.
В неврологическом осмотре ведущим клиническим признаком является симметричный проксимальный периферический тетрапарез, более выраженный в ногах (мышечная сила в проксимальных отделах верхних конечностей – 3-4 балла, в дистальных – 4 балла, в проксимальных отделах нижних конечностей – 2-3 балла, в дистальных – 4 балла). Походка изменена по типу «утиной». Использует вспомогательные («миопатические») приемы, например вставание «лесенкой». Мышечный тонус снижен, контрактур нет. Гипотрофия мышц тазового и плечевого пояса. «Миопатические» черты, например в виде широкого межлопаточного пространства. Имеется псевдогипертрофия икроножных мышц. Сухожильные и периостальные рефлексы – без достоверной разницы сторон; биципитальные – низкие, триципитальные и карпорадиальные – средней живости, коленные и ахилловы – низкие. На основании клинических данных заподозрена МДД.
Помимо пробанда осмотрены его родители и старшая родная сестра. Ни у кого из родственников пробанда клинических проявлений МДД не наблюдалось. Однако у матери замечено некоторое увеличение икроножных мышц в объеме. По данным генеалогического анализа пробанд является единственным заболевшим в семье. При этом нельзя исключить, что мать ребенка и родная сестра пробанда являются гетерозиготными носительницами мутантного гена (рис. 1).
В рамках медико-генетического консультирования семья К. была обследована на предмет наличия/отсутствия делеций и дупликаций в гене дистрофина. Молекулярно-генетический анализ в лаборатории ДНК-диагностики МГНЦ РАМН выявил у пробанда К. делецию 45 экзона, что окончательно подтверждает установленный клинический диагноз МДД. У матери делеция 45 экзона, выявленная у сына, не обнаружена. У сестры в результате анализа делеция 45 экзона, выявленная у брата, не найдена. Следовательно, у исследуемого мутация, скорее всего, имеет происхождение de nоvo, однако также она может явиться результатом герминального мозаицизма у матери. Соответственно, при мутации de novo риск рождения больного ребенка у матери будет определяться популяционной частотой данной мутации (1:3500, ‹‹1%), что значительно меньше, нежели при Х-сцепленном рецессивном типе наследования (50% мальчиков). Поскольку невозможно полностью исключить, что мутация может явиться результатом герминального мозаицизма, при котором наследование по законам Менделя нарушается, рекомендуется проведение пренатальной диагностики при последующей беременности у матери и сестры пробанда.
Заключение. В настоящее время у врача есть широкий арсенал симптоматических средств, используемых в лечении МДД, однако, несмотря на достижения науки, этиологическое лечение МДД до сих пор не разработано, эффективных препаратов для заместительного лечения при МДД не существует. Согласно недавним исследованиям стволовых клеток, существуют перспективные векторы, которые могут заменить поврежденные мышечные ткани. Однако, в настоящее время, возможно лишь симптоматическое лечение, направленное на улучшение качества жизни больного. В этой связи ранняя диагностика МДД играет важнейшую роль для своевременного проведения медико-генетического консультирования и выбора дальнейшей тактики планирования семьи. Для пренатальной ДНК диагностики исследование с помощью биопсии хориона (CVS) можно проводить на 11-14 неделях беременности, амниоцентез можно использовать после 15 недели, забор крови плода возможен примерно на 18 неделе. Если тестирование будет осуществлено на ранних сроках беременности, возможно досрочное прекращение беременности в случае наличия заболевания у плода. В ряде случаев целесообразно проведение преимплантационной ДНК диагностики с последующим экстракорпоральным оплодотворением.
Выводы. Для обеспечения раннего выявления и профилактики МДД необходимо шире использовать методы молекулярно-генетической диагностики; повысить настороженность практикующих врачей в отношении данной патологии. При мутации de novo риск рождения больного ребенка у матери определяется популяционной частотой мутации гена дистрофина. В случаях носительства мутации матерью пробанда требуется пренатальная или перимплантационная ДНК диагностика с целью планирования семьи.
Мутации de novo в человеческом геноме связаны с кроссинговером
Наибольшее количество мутаций de novo — тех, которые есть у ребенка, но не было у родителей — происходит вблизи точки рекомбинации при кроссинговере. Это показало исследование геномов более 150 000 человек, проведенное исландской биотехнологической компанией deCODE Genetics.
При образовании яйцеклеток и сперматозоидов во время мейоза происходит кроссинговер — обмен протяженными гомологичными участками между парными хромосомами. Поэтому ребенок получает хромосомы, не идентичные родительским, а «мозаичные», состоящие из участков парных хромосом. В основе кроссинговера лежит гомологичная рекомбинация. Она начинается с двухцепочечных разрывов, которые чаще встречаются в определенных участках генома, называемых горячими точками рекомбинации.
Теперь выяснилось, что рекомбинационные события могут влиять на интенсивность мутагенеза. Исследователи из deCODE Genetics, находящейся в Рейкьявике дочерней компании Amgen, получили геномные данные для 155 250 исландцев — родительских пар и детей (полногеномное секвенирование и ДНК-микрочипирование). Изучив различия в ДНК родителей и детей, они обнаружили более 4,5 млн рекомбинаций и около 200 000 мутаций de novo. Местоположение мутационных событий в этой работе определяется с разрешением 682 п.н.; в предыдущих подобных работах точность была не лучше тысяч пар нуклеотидов.
Результаты исследования «указывают на тот факт, что генерация генетического разнообразия — нечто большее, чем просто случайность», — говорит Кари Стефанссон, генеральный директор deCODE Genetics и один из ведущих авторов статьи.
Оказалось, что мутации гораздо чаще происходят вблизи точек рекомбинации. Для почти 3000 трио родителей и детей сделали полногеномное секвенирование и обнаружили 200 435 мутаций de novo. Частота таких мутаций в пределах 1000 от точки рекомбинации была в 50 раз выше, чем в среднем по геному, а при удалении она уменьшалась. Предыдущие исследования показывали аналогичные результаты, но менее детально. Интересно, что характеристики «отцовских» и «материнских» мутаций несколько отличались, вероятно, из-за различной организации мейоза при оогенезе и сперматогенезе.
В свою очередь, и расположение горячих точек рекомбинации в геноме, как уже говорилось, не случайно: они находятся преимущественно в регуляторных областях и в участках, богатых GC. По данным авторов работы, кроссинговер реже происходит в транскрибируемых областях, в том числе отмеченных сигнатурами гистонов H3K36me3 и H4K20me1, и чаще — в энхансерных областях, маркированных сигнатурами гистонов H3k27ac и H3K4me1.
Кроме того, число мутаций в ДНК ребенка увеличивается с возрастом родителей — по оценкам авторов, прибавляется 1, 39 мутации на каждый год возраста отца и 0,38 на каждый год матери. С возрастом матери увеличивается и число кроссинговеров в хромосомах яйцеклетки. Отмечено, что точки рекомбинации и мутации de novo у женщин с возрастом смещаются к областям с более поздней репликацией и более низким содержанием GC.
Исследователи выявили гены (в том числе несколько ранее не известных), которые могут быть связаны с рекомбинацией. Всего они нашли 47 вариантов в 35 локусах, влияющих на скорость рекомбинации и/или местоположение рекомбинационных событий.
Авторы работы высказывают предположение, что эволюция направляла события кроссинговера (и мутагенеза) к регуляторным областям и от кодирующих: таким образом уменьшалось количество вредных мутаций, затрагивающих регионы кодирования, и стимулировались регуляторные вариации. Это важно для лучшего понимания того, как создается генетическое разнообразие у вида, а также для понимания природы заболеваний, вызванных мутациями. Кроме того, эти результаты могут быть полезны для эволюционных исследований. Например, данные по мутациям в ДНК используется в качестве «молекулярных часов» — для определения временного расстояния между эволюционными событиями.
ДНК-диагностика: всем ли пациентам с БАС нужен генетический анализ?
Анализ каких генов делать при семейной и спорадической формах БАС в первую очередь? Что такое мутация de novo, и как она появляется в родословной? Если мутантных генов у болеющего БАС не обнаружено, что это значит? Публикуем доклад биолога, руководителя Лаборатории клинической биоинформатики, к.б.н. Федора Коновалова на Пятой общероссийской пациентской конференции по БАС с международным участием.
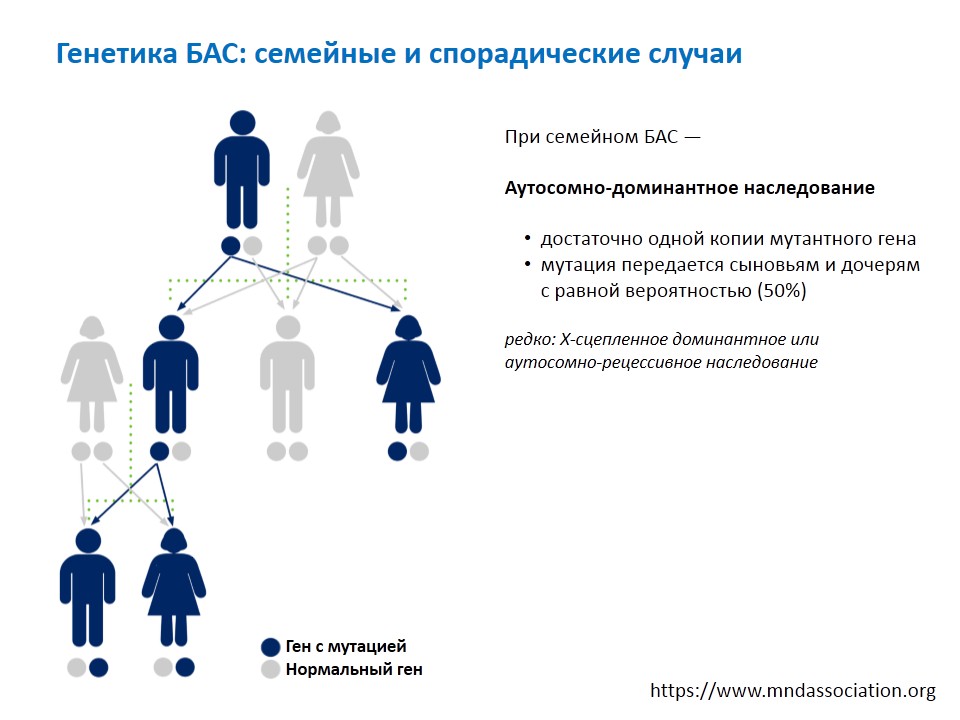
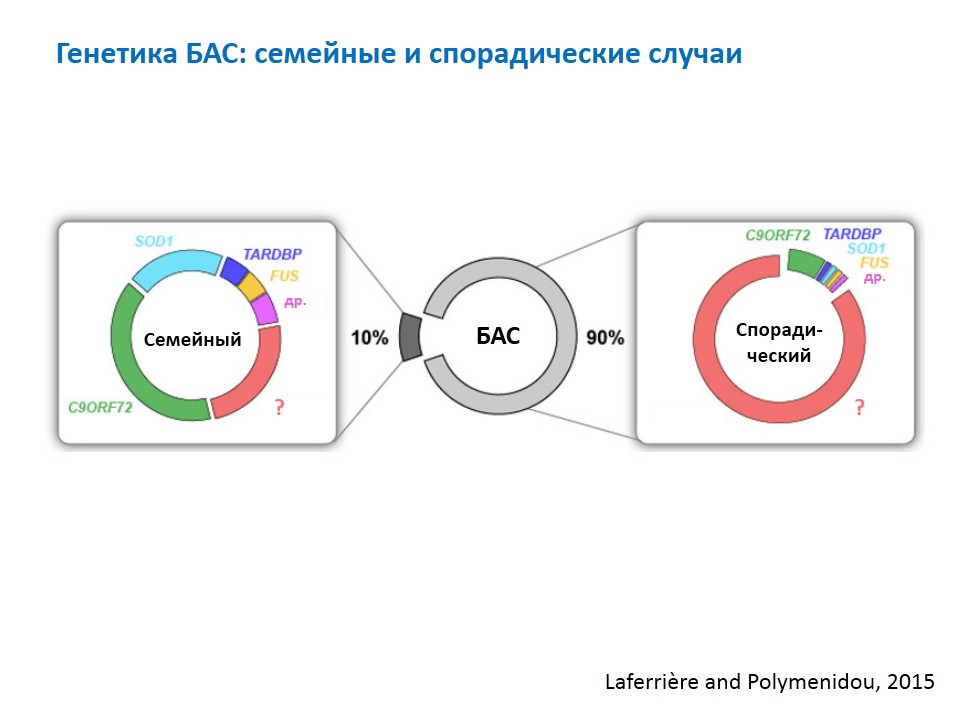
Когда речь идет о генетике БАС имеются в виду, конечно, семейные случаи, которых около 10%. При семейном БАС основной тип наследования — аутосомно- – процесс, при котором болезнь проявляется при наследовании хотя бы одного « дефектного» гена от любого из родителей.
» >доминантный : это прямая передача потомкам без перескока через поколение с вероятностью 50% от больных к больным. Причем это не зависит от пола: мальчики и девочки болеют с одинаковой частотой. Откуда берутся эти 50%?!
У больного в одной из хромосом — а мы помним, что их у нас по две — есть мутантный ген. Вторая такая же хромосома — нормальная. Каждому ребенку родитель передает только одну из каждой пары хромосом. Поэтому и получается, что больной с определенной вероятностью 50% на 50% передаст дефектную хромосому любому из потомков. Что здесь важно?! Допустим, что у больного два ребенка. Это не значит, что один ребенок унаследовал мутацию, а второй нет: вероятность 50% для каждого из детей равноценна и не зависит от того, есть уже в семье ребенок с мутантным геном или нет. При этом мутация передается с равной вероятностью сыновьям и дочерям больных. Крайне редко, но бывают Х-сцепленные доминантные рецессивные наследования. В таких случаях принцип передачи генов немного отличается. Его в рамках доклада мы рассматривать не будем.
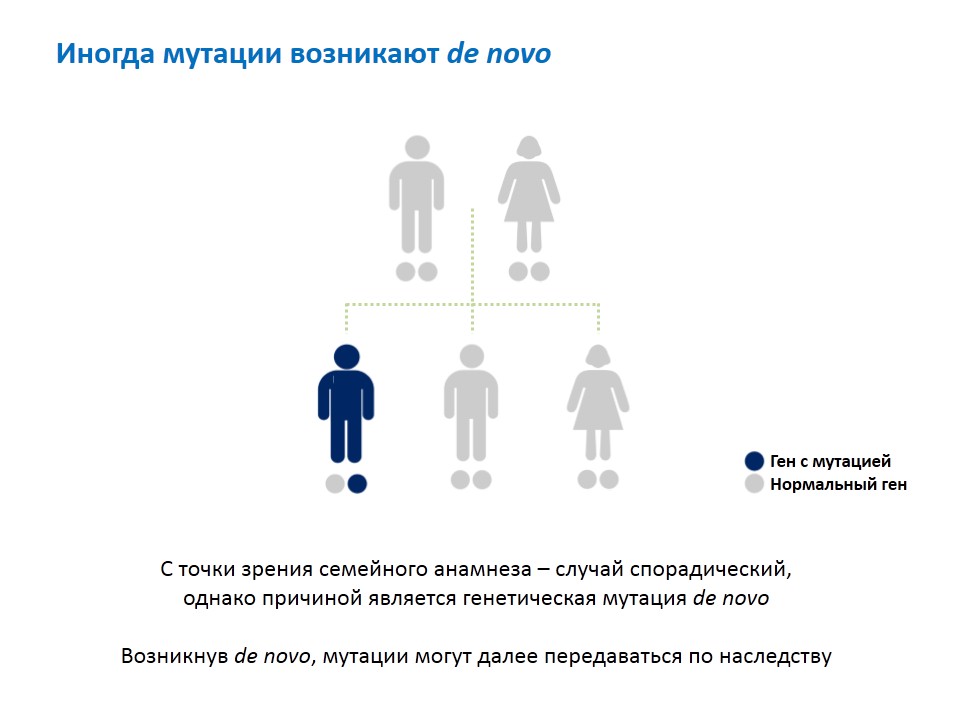
Как появляется мутация в родословной
Иногда изменения в гене возникают de novo (де ново). Например, в семье, где оба родителя здоровые, у ребенка во взрослом возрасте развивается БАС. С точки зрения врача и самого пациента при изучении его семейного анамнеза (совокупности сведений о больном и его заболевании — здесь и далее прим. ред.) случай носит спорадический характер. Но де-факто он имеет наследственную причину: мутация появилась либо в ходе эмбриогенеза (процесс образования и развития эмбриона) этого человека при копировании генетической информации, либо при формировании половых клеток у родителей. Такое встречается чаще, при этом самих родителей и даже их последующих детей болезнь нисколько не затрагивает. Важно, что когда произошли такие мутантные изменения в гене, они будут передаваться по наследству, и спорадический БАС становится семейным. Такие случаи происходят с определенной частотой, которая соответствует как минимум той доле случаев, где установлена спорадическая форма заболевания.
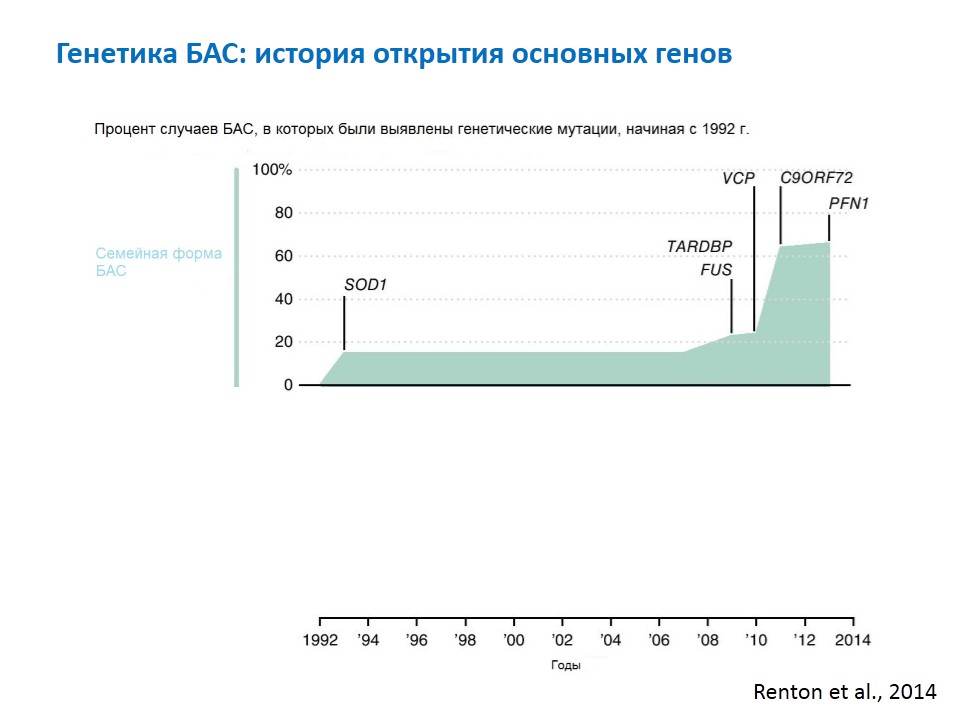
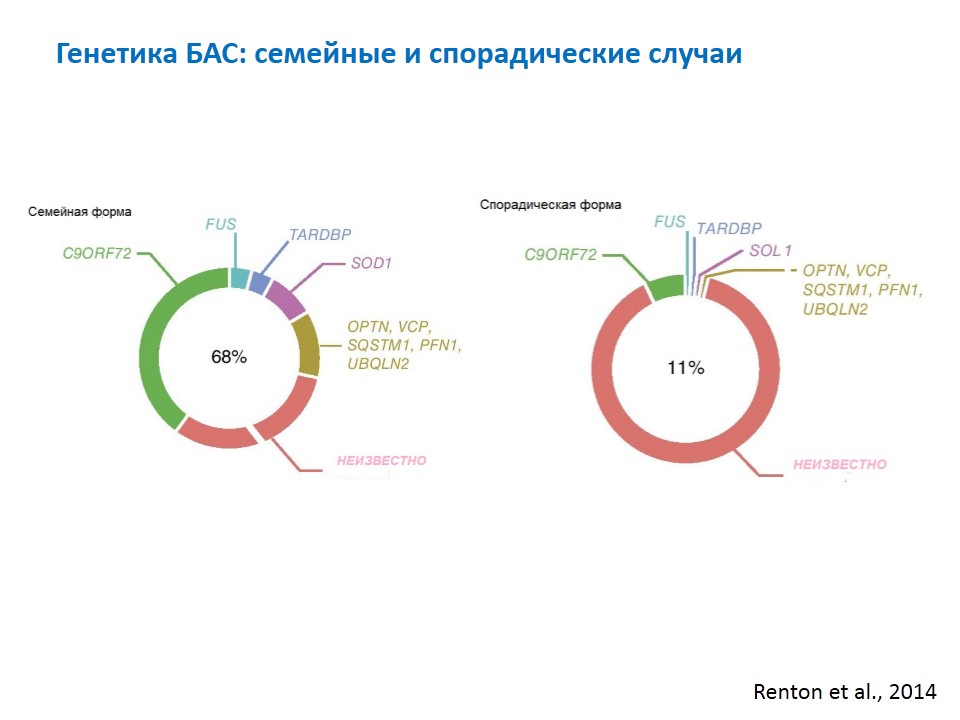
Какие гены вызывают БАС
Все остальные гены при семейном БАС составляют в сумме меньше, чем два вышеуказанных.
Что же со спорадической формой? Здесь на страже тоже генетика: мутация de novo возникает в тех же самых генах, которые люди могут унаследовать от больных родителей. Единственное исключение — ген SOD1, в котором выявляются как и мутации de novo в спорадических случаях, так и унаследованные, но не проявившиеся у родителей мутации. Это явление называется неполной пенетрантностью, когда при наличии мутантного гена заболевание не всегда развивается.
При доминантном типе наследования спорадическая форма БАС при анализе гена SOD1 выявляется примерно в 10% случаев. При этом в российской популяции он превалирует над геном C9orf72: при анализе последнего спорадическая форма выявляется гораздо реже, чем при SOD1.
Всего известно примерно 20 генов, мутантные изменения в которых так или иначе вызывают БАС.
Проводить или не проводить генетическое тестирование
В первую очередь, надо ответить на вопрос: для кого? Для пациента с БАС — понятно, что это уточнение диагноза и прогноза при наличии заболевания. Зная молекулярную причину, врач знает с чем это сопоставить в литературе, с мировым опытом. Назначенное лечение, например, при конкретной форме БАС может быть скорректировано. В частности, для БАС, вызванного мутациями в гене C9orf72, существуют определенные разработки патогенетической терапии (устранения и подавления механизмов развития болезни).
То же касается и вопроса о планировании семьи. Если, например, вы хотите обеспечить рождение детей гарантированно без БАС с помощью ЭКО и прибегаете к преимплантационной генетической диагностике (выявление заболеваний у эмбриона перед имплантацией в матку, сокращенно — ПГД), то вам нужно знать какой мутантный ген обнаружен у болеющего. ПГД не делается на поиск болезни: причина должна быть выявлена до того, как планировать ЭКО.
Очевидно, что для тех, кто является родственником при семейном БАС, необходимость тестирования — это возможность знать будет ли болезнь. Этот вопрос каждый взрослый человек решает сам для себя.
Если же речь идет о здоровых людях, которые еще не знают будет ли у них заболевание, то нужно понимать, что возможен существенный психологической эффект от результатов исследования. Генетические анализы имеют одно очень важное свойство: они делаются раз и навсегда, это путь в одну сторону. В отличие, например, от МРТ или биохимических анализов, которые отслеживают динамику. Поэтому перед тем, как делать любое генетическое исследование — и речь здесь не только о БАС — нужно хорошо подумать.
Методы анализа ДНК
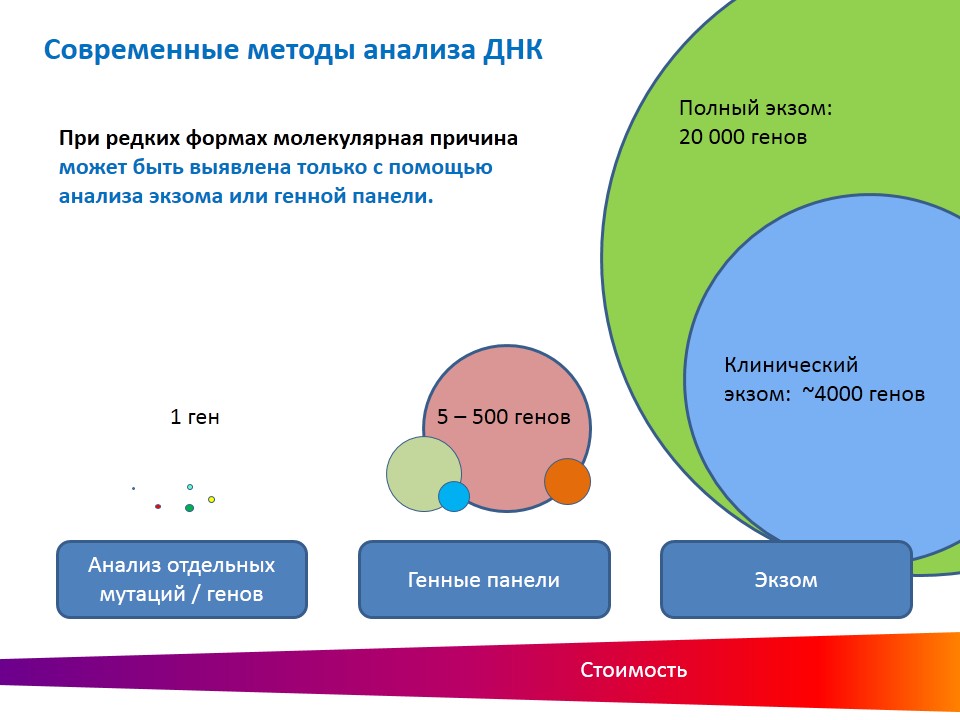
Современные методы анализа ДНК позволяют читать сразу десятки и сотни генов в рамках одного исследования за разумные деньги. Доступны для анализа даже так называемые «полные экзомы» (полноэкзомное секвенирование ДНК ) — кодирующие участки всех 20 000 генов человека, или его клинически значимую часть (около 4000 генов). Такой анализ помогает при редких формах БАС, когда, за исключением генов SOD1 и C9orf72, молекулярная причина может быть установлена только через анализ экзома или генной панели. Естественно, стоимость анализа возрастает, но оно не пропорционально увеличению объема исследования. Поэтому, в особых случаях, оправданны.
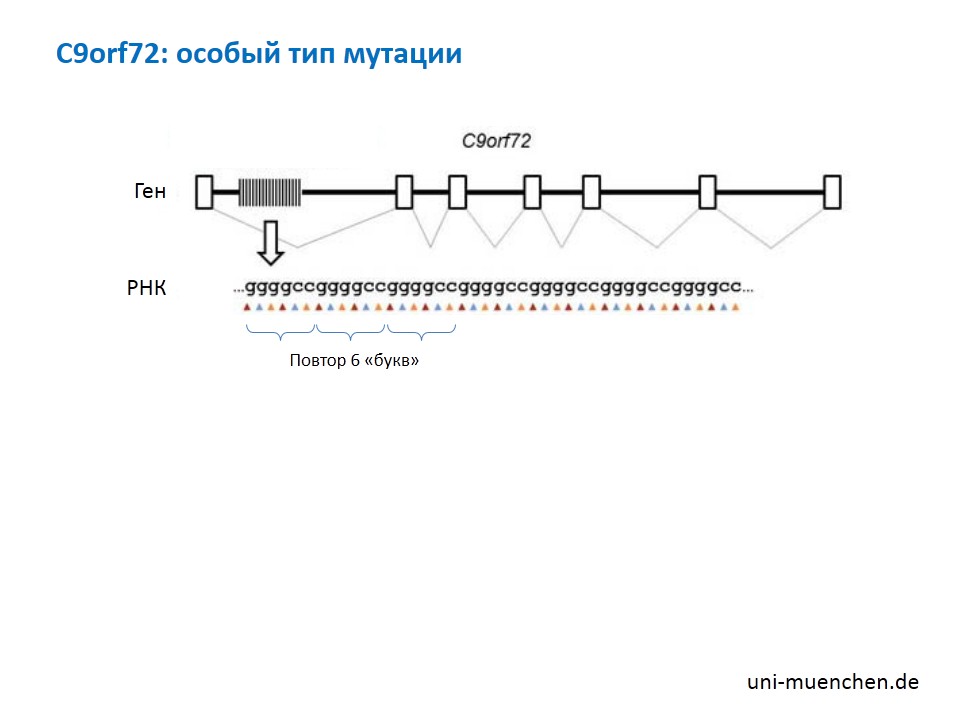
Генетические тесты можно разделить по их принципу. Поисковые — когда в определенном месте генома мы ищем любые мутации. Подтверждающие тесты — это когда мы в ДНК ищем конкретную мутацию. Например, анализ повтора в гене C9orf72. Тест делается специальными наборами и не входит ни в одно другое исследование, даже в дорогостоящие полногеномные. Тест на поиск мутаций в гене C9orf72 всегда нужно делать отдельно. По стоимости он доступен большинству.
То же и анализом гена SOD1. Его ещё можно назвать комбинированным. Почему? Тест проводится классическим методом секвенирования по Сэнгеру, доказавшим свою эффективность. Это подтверждающий тест одновременно с поиском мутации. Его стоимость чуть выше теста гена C9orf72, но в пределах разумного.
Тест на анализ вышеуказанных генов имеет смысл делать при обеих генетических формах БАС. Только при семейном БАС в первую очередь лучше начинать с анализа гена C9orf72, а при спорадической форме — SOD1. Можно сразу оба сделать: зависит от возможностей.
Если в этих двух исследованиях ничего не было найдено, то тогда можно переходить к более масштабным — полноэкзомному секвенированию или генным панелям «Нейродегенеративные заболевания». Их проводит ряд лабораторий, которые владеют современным методом секвенирования нового поколения. Какая именно генная панель подойдет для пациента с БАС в лабораториях должны сообщать при первичном консультировании по телефону. Если лаборатория затрудняется ответить на этот вопрос, то, наверно, не стоит ей доверять, потому как организация должна знать, какие исследования проводит и какие услуги оказывает.
Любая генетическая панель ограничена известными генами. В ней могут отсутствовать гены, открытые совсем недавно. В таком случае можно делать секвенирование экзома. По стоимости исследование экзома ненамного превышает стоимость проведения генных панелей.
Последние два метода объединяются в группу NGS — секвенирование нового поколения. Несмотря на это, их результаты нужно подтверждать. Когда найдена мутация с помощью панелей, секвенирования экзомов и геномов, врач подтвердил причину, нужно подтверждать конкретную мутацию секвенированием по Сэнгеру. Допустим, секвенировали вы экзом, нашли там мутацию НЭК1, нужно подтвердить ее наличие другим методом — классическим и надежным, таким как метод Сэнгера. Будет проведен тест конкретно выявленной мутации, а не всего экзома.
Вопросы из зала
Если больной сдает первые два анализа, БАС подтверждается, стоит ли родственникам тоже сдать эти анализы?
Важный момент: каким может быть результат генетического теста. С одной стороны, есть классический «плюс»: выявлена известная патогенная мутация. Например, при анализе C9orf72 выявлено больше сотни повторов, а при анализе SOD1 — классическая 91-я мутация. Вроде, все понятно, нашли причину, но не нужно из этого ставить знак равенства в отношении развития заболевания, если тестируется родственник. Вероятность развития БАС и прогноз течения заболевания зависит не от самого факта результата, а от гена, особенно это касается SOD1 и конкретной мутации. Даже в пределах одного гена некоторые мутации иногда дают разный эффект. И хорошо, если этот эффект описан в литературе на большой когорте пациентов, тогда всё можно сопоставить. А иногда бывает, что нет. Здесь всегда нужно давать определенный запас на вариабельность проявлений даже мутации в одном и том же гене.
Если, допустим, проверили мужа, у которого БАС, на SOD1 и C9orf72, мутаций выявлено не было. Значит ли это, что дети унаследуют БАС, надо ли их проверять?
Коновалов Ф. А.: Нет, не факт, что это наследственное. Поскольку результата положительного, по молекулярной причине, пока нет и в семье это первый случай, то это может быть спорадический случай. Для детей это будет иметь актуальность, если такая причина будет найдена. Если это действительно спорадический случай, то БАС на нем закончится. Потому что это не генетическая причина. Если же это на самом деле наследственная причина — мутация de novo —, тогда может не закончиться на муже, да. Здесь зависит от того, есть мутация или нет. Правильно, что сделали первые два теста сделали. Здесь еще по вашему клиническому случаю нужно смотреть.
При генетическом анализе надо учитывать еще один момент: промежуточный вариант этих тестов. Поисковые исследования потому так и называются, потому они такие сложные и современные, что иногда выявляют мутации, которые ранее никем в мире не были описаны. Это не делает эти мутации плохими, но мы их вынуждены «вариант с неопределенной значимостью», есть такой термин. Что это значит? Эти мутации являются либо патогенными либо ни на что не влияющими. Мы просто не знаем это до конца. По международным стандартам их рекомендовано все равно сообщать. Чтобы выяснить патогенная мутация или нет, могут потребоваться дополнительные исследования, например, анализ ДНК родителей. Тогда можно подтвердить, например, статус de novo, если у родителей мутации нет, а у потомка есть. С учетом возраста манифестации БАС это не всегда возможно. Нужны научные эксперименты, функциональный анализ мутации, который не всегда возможен. К сожалению, некоторые результаты таких поисковых исследований так и остаются в неопределенном статусе. Такова реальность. Для болеющего такие варианты не повод делать выводы ни в плюс, ни в минус.
И наконец, отрицательный результат, когда мутации не выявлены. Во-первых, это ни в коем случае не исключает клинический диагноз. Если врач поставил БАС, а в генах мутации не обнаружено, это не означает, что болезни нет. Это важно. Почему результат может быть отрицательным?
Первая причина — конкретный случай БАС не является наследственным. Он истинно спорадический и не имеет генетической причины. Вторая причина — мутация есть, но она в каком-то новом, еще не открытом гене. Все гены, которые сейчас нам известны, были когда-то в неопределенном статусе. Еще несколько лет назад мутацию в НЭК1, найдя даже ее в экзоме, нельзя было сообщить и интерпретировать. И самый коварный момент: мутация может быть и есть в геноме, но она не выявилась из-за технических ограничений метода.
Скажите, пожалуйста, известны ли причины спорадических мутаций науке или нет. Из-за чего это возникает? Есть причины?
Коновалов Ф. А.: Каждый из нас является носителем каких-то мутаций, в том числе de novo. У каждого — в среднем 80 отличий, которые есть только у нас, а у наших родителей нет. У большинства они случайным образом не попадают в какие-то значимые участки генома. ДНК в каждой клетке и в каждом организме все время копируется все время. Этот процесс не идеален: копирование подвержено ошибкам. Для этого нет никакой внешней причины. Естественно, бывают такие сильные мутагенные воздействия, если живешь, например, в зоне радиационного облучения. Естественный мутагенный фон на самом деле не так сильно влияет на частоту мутации de novo. Поэтому точную причину назвать затрудняюсь.
Когда, с Вашей точки зрения, можно надеяться на переход от простой констатации факта, что мутации такого-то гена приводят к БАС, к пониманию механизма почему это происходит? Как Вы думаете, когда это может быть?
Коновалов Ф. А.: Здесь нет такой точной даты. Такие механизмы ученые будут постепенно открывать для каждого гена в отдельности. Потому что механизмы будут разными в этих случаях. Например, для мутации C9orf72 таких механизмов уже предложено как минимум четыре. Данные есть в пользу всех. Исследования ведутся чрезвычайно активно. Думаю, в ближайшие 10 лет, какие-то новые механизмы тоже появятся, а в ближайшие 20—25 лет будет уже известно их существенное количество.
Благодарим за помощь в расшифровке видеозаписи доклада конференции волонтера БФ «Живи сейчас» Елену Петросян.