нити киари в полости пп что это
Нити киари в полости пп что это
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ ФНЦ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФНЦ трансплантологии и искусственных органов им. акад. В.И. Шумакова, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
Тромбоз сети Киари правого предсердия после коррекции врожденного порока сердца
Журнал: Кардиология и сердечно-сосудистая хирургия. 2013;6(6): 99-101
Иванов А. С., Гламазда С. В., Родионов А. С., Лебедева А. В., Кузьмин В. В., Абрамова Н. Н., Ильинский И. М., Можейко Н. П. Тромбоз сети Киари правого предсердия после коррекции врожденного порока сердца. Кардиология и сердечно-сосудистая хирургия. 2013;6(6):99-101.
Ivanov A S, Glamazda S V, Rodionov A S, Lebedeva A V, Kuz’min V V, Abramova N N, Il’inskiĭ I M, Mozheĭko N P. Chiari network thrombosis of the right atrium after correction of congenital heart disease. Kardiologiya i Serdechno-Sosudistaya Khirurgiya. 2013;6(6):99-101.
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ ФНЦ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФНЦ трансплантологии и искусственных органов им. акад. В.И. Шумакова, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
ФГБУ «Федеральный научный центр трансплантологии и искусственных органов им. акад. В.И. Шумакова» Минздрава России, Москва
Тромбозы камер сердца после хирургических вмешательств в условиях искусственного кровообращения (ИК) — редкая и малоизученная патология. Чаще всего данные состояния встречаются при антифосфолипидном синдроме (АФС) и других тромбофилиях.
Основными предрасполагающими факторами для тромбообразования в полостях сердца являются наличие препятствия кровотоку, септальные дефекты (врожденные и приобретенные пороки сердца и магистральных сосудов), нарушения ритма сердца (мерцание, трепетание предсердий), наличие интравенозного катетера, эндокардиальных электродов, изменения свертывающей системы крови, в том числе транзиторные. В ряде наблюдений причина остается не выявленной [5]. К одной из механических причин тромбообразования и патологических тромбоэмболий относят развитую сеть Киари (не полностью редуцированные остатки клапана венозного синуса в правом предсердии (ПП) в области устья нижней полой вены). Она может служить «ловушкой» для тромбоэмболов и в последующем местом формирования тромба [6].
Разные авторы [1—3, 5] для лечения пациентов с тромбозами полостей сердца предлагают использовать консервативную (тромболитическую, антиагрегантную и антикоагулянтную) терапию с разной степенью эффективности, а также хирургическую коррекцию.
В доступной литературе [3, 4] мы нашли описания 4 наблюдений тромбоза ПП с местом фиксации тромба к сети Киари, возникших в отсроченный период после коррекции врожденного порока сердца — дефекта межпредсердной перегородки (МПП) в условиях ИК.
Приводим собственное описание редкого наблюдения тромбоза ПП в области сети Киари после коррекции врожденного порока сердца.
Пациентка К., 14 лет, поступила в ФГБУ ФНЦ трансплантологии и искусственных органов с диагнозом: врожденный порок сердца — дефект МПП. Предъявляла жалобы на слабость, быструю утомляемость при физической нагрузке.
По данным рентгенографии, сердце увеличено в объеме за счет правых отделов, признаки гиперволемии малого круга кровообращения.
На ЭКГ ритм синусовый, частота сердечных сокращений до 80 уд/мин, нормальное положение электрической оси сердца, неполная блокада правой ножки пучка Гиса.
По данным эхокардиографии (масса тела 53 кг, рост 160 см, площадь поверхности тела 1,54 м2): конечный диастолический размер (КДР) правого желудочка (ПЖ) 3,3 см; ПП 3,7×3,6 см; КДР левого желудочка (ЛЖ) 4,3 см, конечный систолический размер (КСР) 2,8 см, фракция изгнания (ФИ) 66%; толщина межжелудочковой перегородки (МЖП) 0,8 см; толщина задней стенки левого желудочка (ЗСЛЖ) 0,8 см; диаметр аорты на уровне фиброзного кольца 1,7 см; давление в легочной артерии (ЛА) 30 мм рт.ст.; скорость кровотока в аорте 0,96 м/с; скорость кровотока в ЛА 1,36 м/с. В области МПП у ее нижнего края при цветовом допплеровском картировании лоцируется турбулентный косонаправленный поток в полость ПП, диаметром до 2,1 см со сбросом крови слева направо.
Коагулограмма до операции: активированное частичное тромбопластиновое время (АЧТВ) 32 с, протромбиновый индекс 86%, фибриноген 2600 мг/л, растворимые комплексы фибрин-мономера (РКФМ) 5 мг%. Агрегация тромбоцитов с адреналином 97% против 72%, c АДФ — 99% против 87%.
Общий анализ крови, общий анализ мочи, биохимический анализ крови без особенностей.
Порок являлся гемодинамически значимым и подлежал хирургической коррекции.
10.01.13 выполнена операция — пластика дефекта МПП заплатой из ксеноперикарда в условиях ИК. Интраоперационно при ревизии дефект МПП без нижнего края, размером 1,8×3,0 см. В области устья нижней полой вены (НПВ) перегородка шириной 5 мм, истончена, с множественными фенестрациями. Выполнено иссечение перфорированной части перегородки. Дефект закрыт заплатой из ксеноперикарда, фиксированной четырьмя П-образными швами (пролен 4/0) по задней полуокружности НПВ и непрерывным обвивным швом по остальному периметру. При проверке МПП герметична.
Послеоперационный период протекал без осложнений. Проводилась антибактериальная, противовоспалительная, десенсибилизирующая терапия. На 8-е сутки в удовлетворительном состоянии пациентка выписана под наблюдение педиатра и кардиолога по месту жительства. По данным контрольного обследования: на ЭКГ ритм синусовый, правильный, частота сердечных сокращений 91 уд/мин, неполная блокада правой ножки пучка Гиса. При эхокардиографии КДР ПЖ 1,8 см; ПП 2,9×3,2 см; КДР ЛЖ 4,3 см, КСР ЛЖ 2,8 см; ФИ 66%; МЖП 0,8 см; давление в ЛА 25 мм рт.ст.; скорость кровотока в аорте 1,1 м/с; скорость кровотока в ЛА 1,12 м/с. Патологические потоки в области МПП не определяются. Рекомендована консультация в клинике через 6 мес.
Дома через 2 мес после выписки в течение 2 дней отмечались эпизоды повышения температуры до 37,3 °С на фоне катаральных явлений. Проводилась симптоматическая терапия с положительным эффектом.
При плановой контрольной эхокардиографии через 6 мес после операции выявлено КДР ПЖ 1,8 см, ПП 4,4×3,8 см, ФИ 67%, область МПП интактна, визуализируется подвижное объемное образование ПП на ножке (2,5×1,7 см), пролабирующее в трехстворчатый клапан (рис.1). 
Пациентка в срочном порядке госпитализирована. При поступлении состояние удовлетворительное, жалоб нет. По данным рентгеновской мультиспиральной компьютерной томографии и магнитно-резонансной томографии органов грудной клетки в полости ПП определяется дополнительное мягкотканное образование неправильной «гроздевидной» формы размером 45×30×25 мм, подвижное, нависающее над устьем НПВ и пролабирующее в трехстворчатый клапан (рис. 2). 
Проводилась дифференциальная диагностика между тромбом и новообразованием ПП.
Коагулограмма: АЧТВ 32 с, протромбиновый индекс 82%, фибриноген 3090 мг/л, РКФМ 22 мг%, агрегация тромбоцитов с адреналином 88% против 44%, c АДФ — 86% против 57%, с ристомицином — 94% против 72%, антитромбин-3 97% (норма 75—125%), плазминоген 99% (норма 75—150%), D-димер 523 нг/мл (норма ≤500 нг/мл), протеин C 94% (норма 70—130%).
Повышение уровня D-димера могло указывать на возможное наличие в организме организованного тромба в стадии лизиса. Образование было расценено как флотирующий тромб ПП и пациентка по витальным показаниям (в связи с возможной тромбоэмболией легочной артерии) была оперирована.
Интраоперационно: в связи с риском разрушения тромба и тромбоэмболии легочной артерии канюляция НПВ произведена под контролем зрения через вскрытое ПП. Вмешательство выполняли на работающем сердце (длительность ИК 17 мин) и нормотермии. При ревизии ПП в области устья НПВ выражена сеть Киари, к которой фиксировано многодольчатое образование (4,2×2,9×1,2 см) плотной консистенции, имеющее вид цветной капусты (см. рис. 3 на цв. вклейке). 
По данным патоморфологического исследования, иссеченное во время операции образование имело на разрезе пестрый вид от розового до серо-белого цвета с отходящим от него тонким тяжом сети Киари.
При гистологическом исследовании (см. рис. 4 на цв. вклейке) 
Послеоперационный период протекал без осложнений. Со 2-х суток после операции профилактически начата антикоагулянтная (фрагмин) и антиагрегантная (кардиомагнил) терапия, с 4-х суток начат прием варфарина. При достижении целевого значения международного нормализованного отношения (МНО) 2,0—2,5 фрагмин отменен. На 7-е сутки удален центральный венозный катетер, сняты швы.
Пациентка обследована для выявления АФС и наследственных тромбофилий. Титры антител к фосфолипидам IgG, фосфолипидам IgM, кардиолипину, IgG, кардиолипину, IgM, b2 гликопротеину I, IgG, b2 гликопротеину I, IgM, аннексину V, IgG, аннексину V, IgM были ниже референсных значений, что позволило исключить АФС. Данных, подтверждающих генетическую патологию (лейденовская мутация, мутация гена протромбина), не получено.
При ультразвуковом исследовании вен нижних конечностей и таза данных, свидетельствующих о тромбозе, не получено.
На 10-е сутки пациентка в удовлетворительном состоянии выписана из стационара под наблюдение кардиолога и гематолога по месту жительства. При выписке АЧТВ 34 с, протромбиновый индекс 59%, фибриноген 3102 мг/л, РКФМ 28 мг%, агрегация тромбоцитов с адреналином 25% против 20%, с АДФ — 78% против 40%, D-димер 1082 нг/мл (
Мальформация Арнольда–Киари
Клиническая картина мальформации Киари
Клинические проявления АК – I типа проявляются чаще всего в юношеском либо в зрелом возрасте. Эти проявления укладываются в такие неврологические синдромы, как церебеллобульбарный, ликворогипертензионный, сирингомиелический, синдромы повреждения черепных нервов. Ликворогипертензионный синдром проявляется головной болью, обычно субокципитальной, и болью в шее, усиливающейся при кашле, чихании и напряжении, застойными дисками зрительных нервов. Стволовые нарушения и расстройства функций черепных нервов проявляются в виде неустойчивых осциллопсий, тригеминальной дизестезии, снижения слуха, шума в ушах, головокружения, дисфагии, остановки дыхания во время сна, периодических обмороков (часто связанных с кашлем), нарушения контроля над ЧСС, АД при переходе из горизонтального положения в вертикальное, могут наблюдаться атрофия половины языка, паралич голосовых связок, стридор, спастический или комбинированный (больше в верхних конечностях) тетрапарез. Мозжечковые расстройства — нистагм, дизартрия, атаксия. Симптомы, связанные с сирингомиелическими кистами — онемение, расстройство чувствительности, обычно по диссоциированному типу, а также нейроартропатия, нарушение функций тазовых органов, отсутствие брюшных рефлексов, мышечная гипотрофия. При этом ряд авторов отмечают несоответствие между локализацией, протяженностью кисты, кистозным индексом (отношение переднезаднего размера кисты к таковому размеру поперечника спинного мозга на уровне кисты), с одной стороны, и зоной гипестезии, распространенностью сегментарных расстройств поверхностной чувствительности, выраженностью мышечной гипотрофии и степенью пареза — с другой.
АК II типа манифестирует у новорожденных и в раннем детском возрасте такими симптомами, как апноэ, стридор, билатеральный парез голосовых связок, нейрогенная дисфагия с назальной регургитацией, цианоз во время кормления, нистагм, гипотония, слабость, спастика в верхних конечностях, что может прогрессировать вплоть до тетраплегии.
Мальформация Киари III типа встречается редко, клинические проявления ее такие же, как при АК II.
Диагностика мальформации Киари
Широкое внедрение МРТ в клиническую практику позволило решить большинство проблем, связанных с диагностикой аномалии Киари. Этому способствовали хорошая визуализация структур задней черепной ямки, краниовертебрального перехода, спинного мозга, отсутствие артефактов от костных структур.
Лечение мальформации Киари
Лечение мальформации Киари и сопутствующей сирингомиелии возможно хирургическим путем. Операция заключается в декомпрессии задней черепной ямки с пластикой твердой мозговой оболочки.
Эффективность хирургической декомпрессии составляет от 50 до 85% по данным разных авторов. Необходимо помнить, что хирургическое лечение лучше проводить до развития грубых неврологических нарушений, так как после проведения хирургического лечения восстановление функций происходит не полностью или не происходит вовсе, и основной задачей хирургии является стабилизация неврологического статуса пациента и недопущение дальнейшего прогрессирования заболевания.
Синдром Арнольда — Киар
Педиатр Анна Колинько о патологии развития головного мозга, которая может встречаться у 30 % населения
Синдром хронической усталости, головокружения и боль в шее могут быть следствием мальформации (аномалии) Арнольда — Киари. После начала широкого использования МРТ стало понятно, что болезнь встречается у 14–30 % популяции
Все первые описания мальформации были посмертными. В 1883 году шотландский анатом Джон Клеланд (J. Cleland, 1835–1925 гг.) впервые описал удлинение ствола и опущение миндалин мозжечка в большое затылочное отверстие у 9 умерших новорожденных. В 1891 году австрийский патолог Ганс фон Киари (H. Chiari, 1851–1916 гг.) подробно охарактеризовал 3 типа мальформации у детей и взрослых. А в 1894 году немецкий патолог Юлиус Арнольд (J. Аrnold, 1835–1915 гг.) подробно описал синдром Киари 2 типа, в сочетании со спинномозговой грыжей (spina bifida). В 1896 году Киари дополнил свою классификацию четвертым типом. В 1907 году ученики Арнольда использовали термин «мальформация Арнольда — Киари» по отношению к аномалии 2 типа. Теперь это название распространилось на все типы. Некоторые врачи справедливо отмечают, что вклад Арнольда несколько преувеличен и верным будет термин «мальформация Киари».
Версии о причинах
Этиология и патогенез синдрома Арнольда — Киари остаются неуточненными. Киари предположил, что смещение мозжечка и продолговатого мозга происходит из‑за внутриэмбриональной гидроцефалии, которая возникает как следствие стеноза сильвиева водопровода — узкого канала длиной 2 см, который соединяет III и IV желудочки мозга.
Типы мальформаций
1 тип — опущение миндалин мозжечка в позвоночный канал ниже уровня большого затылочного отверстия с отсутствием спинномозговой грыжи. У 15–20 % пациентов этот тип сочетается с гидроцефалией, а у 50 % больных — с сирингомиелией — заболеванием, при котором в спинном и продолговатом мозге образуются полости. В 1991 году было предложено подразделить аномалии Арнольда — Киари 1 типа на тип А — с сирингомиелией и тип В — без сирингомиелии.
Сирингомиелии при Арнольде — Киари 1 степени.
Энцефаломенингоцеле — врожденная грыжа головного мозга и его оболочек, содержащая цереброспинальную жидкость.
Спинальная дизрафия — порок развития, заключающийся в отсутствии слияния по средней линии парных закладок кожи, мускулатуры, позвонков, спинного мозга
2 тип — опущение нижних отделов червя мозжечка, продолговатого мозга и IV желудочка. Отличительным признаком данного типа является сочетание со спинномозговой грыжей (spina bifida) в поясничном отделе, отмечается прогрессирующая гидроцефалия, часто — стеноз водопровода мозга. Среди детей с менингомиелоцеле до 90 % случаев сопровождается аномалией Арнольда — Киари 2 степени.
0, 1 и 2 степени синдрома Арнольда — Киари наиболее распространены в популяции. III и IV типы обычно несовместимы с жизнью.
Симптоматика
Терапия
Лечение аномалий Арнольда — Киари зависит от выраженности неврологической симптоматики. Консервативная терапия включает в себя нестероидные противовоспалительные препараты и миорелаксанты. Если в течение 2–3 месяцев консервативная терапия безрезультатна или у пациента имеется выраженный неврологический дефицит, показано оперативное вмешательство. В процессе операции устраняется сдавление нервных структур и нормализуется ликвороток путем увеличения объема (декомпрессии) задней черепной ямки и установки шунта. Оперативное лечение эффективно, по разным источникам, в 50–85 % случаев, в оставшихся случаях симптоматика регрессирует не полностью. Операцию рекомендуется выполнять до развития тяжелого неврологического дефицита, поскольку восстановление происходит лучше при минимальных изменениях неврологического статуса. Подобное оперативное лечение выполняется почти в каждом федеральном нейрохирургическом центре России и проводится в рамках высокотехнологичной медицинской помощи по системе ОМС.
Эхографическая диагностика порока Арнольда-Киари у плода
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
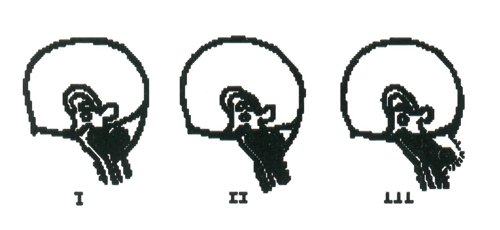
Рис. 1. Схема различных типов порока Арнольда-Киари в сагиттальной плоскости.
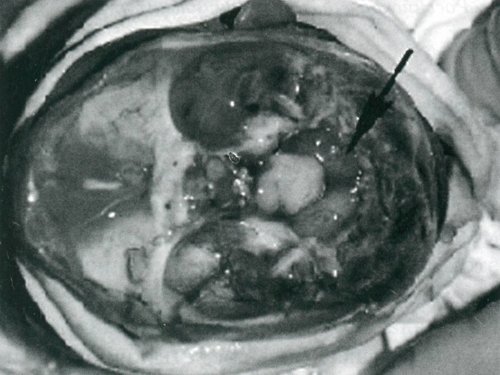
Рис. 2. Беременность 23 недели. Порок Арнольда-Киари II типа. Вид задней черепной ямки у плода после элиминации (отмечено стрелками).
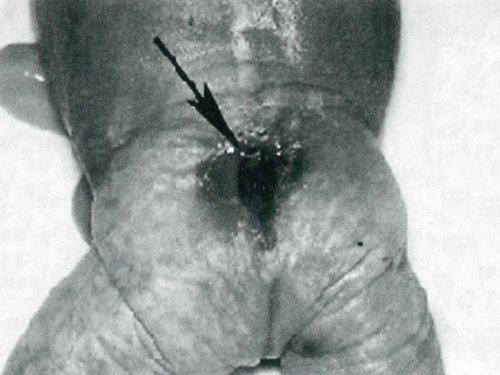
Рис. 3. Плод с пороком Арнольда-Киари в 19 недель. Менингоцистоцеле в крестцовой области у плода после элиминации.
Точная частота синдрома Арнольда-Киари неизвестна, однако менингомиелоцеле встречается в 1-4 случаях на 1000 рождений [4, 5], занимая одно из первых мест в структуре аномалий ЦНС. Отрицательные результаты в попытках лечения детей с менингомиелоцеле, возможно, объясняются наличием дизонтогенеза головного мозга [2]. В связи с этим возрастает роль пренатального определения не только грыжи спинного мозга, но и оценки развития головного мозга у плода с целью выявления или исключения порока Арнольда-Киари.
В большинстве публикаций как отечественных, так и зарубежных авторов, посвященных уьтразвуковой диагностике пороков ЦНС у плода, отмечаются значительные сложности в выявлении менингомиелоцеле, особенно во II триместре беременности 8. При упоминании об аномалии Арнольда-Киари также обычно указывается на значительные трудности в типировании и диагностике порока [8, 9]. На современном этапе к возможным эхографическим признакам аномалии Арнольда-Киари относят внутреннюю гидроцефалию [8, 9], а также типичную форму мозгового черепа типа «лимон» и изображение мозжечка в виде «банана» [4, 9]. Однако по мнению некоторых исследователей эти признаки не отличаются высокой специфичностью по отношению к пороку Арнольда-Киари [7]. Целью настоящего исследования являлось определение надежных ультразвуковых критериев диагностики аномалии Арнольда-Киари у плода, а также разработка рациональных методических приемов сканирования при подозрении на этот порок.
Материалы и методы
Эхографическое обследование плодов производилось при помощи различных ультразвуковых приборов с использованием как трансабдоминального, так и трансвагинального доступов датчиками частотой 3,5-7,5 МГц. После проведения рутинного акушерского ультразвукового обследования у всех плодов производилось сканирование головного мозга с использованием трех взаимно перпендикулярных плоскостей (горизонтальной, фронтальной, сагиттальной), при этом в каждой плоскости отмечались особенности эхографической картины.
Результаты
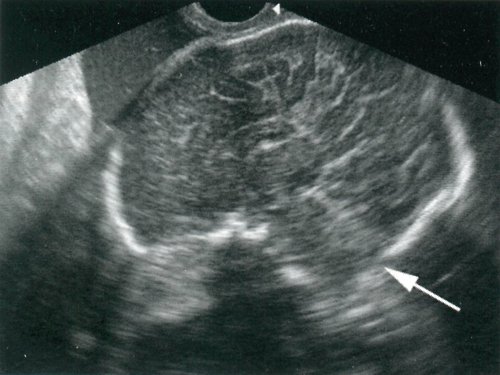
Рис. 4. Беременность 37 недель. Порок Арнольда-Киари I типа. Сагиттальное сканирование. Отсутствие большой цистерны (отмечено стрелкой).
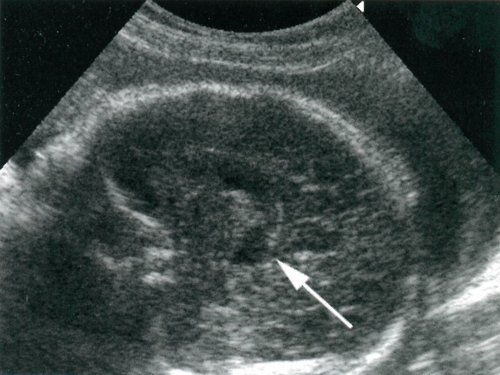
Рис. 5. Беременность 23 недели. Порок Арнольда-Киари II типа. Расширенные задние отделы 3-го желудочка (отмечено стрелкой).
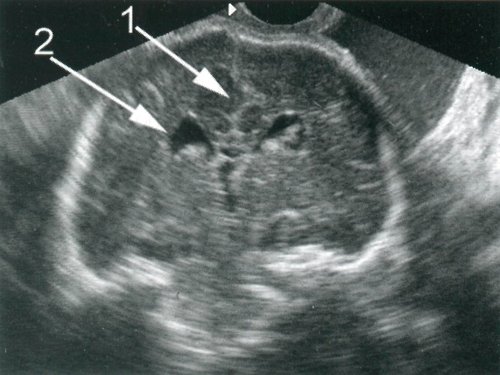
Рис. 6. Беременность 17 недель. Порок Арнольда-Киари II типа. Фронтальное сканирование. Деформация межполушарной щели (1). Наличие дополнительной латеральной стенки бокового желудочка(2).
В результате эхографических обследований головного мозга плодов с пороком Арнольда-Киари в горизонтальных плоскостях (см. табл. 1) вентрикуломегалия, а именно увеличение ширины задних отделов тела бокового желудочка, обнаружена в 41 случае. Следует отметить, что расширение тел боковых желудочков в наших исследованиях не всегда сопровождалось расширением 3-го желудочка при сроках беременности 36-40 недель. Во всех наблюдениях расширение передних отделов 3-го желудочка сочеталось с расширением ширины задних отделов тела бокового желудочка более 2 см.
| Признак порока (особенность) | Число случаев и процент к числу наблюдений в группах | ||
|---|---|---|---|
| 1 (n=18) | 2 (n=17) | 3 (n=20) | |
| «Банан» | 3 (16,6%) | 2 (11,7%) | 0 (0%) |
| «Лимон» | 5 (27,7%) | 2 (11,7%) | 0 (0%) |
| «Банан» + «Лимон» | 3 (16,6%) | 0 (0%) | 0 (0%) |
| Вентрикуломегалия (ширина задних отделов тела бокового желудочка > 1,0 см) | 11 (61,0%) | 13 (76,4%) | 17 (85,0%) |
| Расширение 3-го желудочка: передних отделов задних отделов | 0 (%) 9 (50,0%) | 1 (5,8%) 7 (41,1%) | 5 (25,0%) 10 (50,0%) |
| Ланцетовидная форма задних отделов тела желудочка | 8 (44,0%) | 7 (41,1%) | 11 (55,0%) |
| Затрудненная визуализация мозжечка | 12 (66,0%) | 15 (88,2%) | 19 (95,0%) |
Расширение задних отделов 3-го желудочка в настоящем исследовании обнаружено у 26 плодов. Выявление ромбовидной структуры в области цистерны четверохолмия (см. рис. 5), соответствующее расширению надшишковидного кармана 3-го желудочка, сочеталось либо с полным отсутствием гидроцефалии, либо с вентрикуломегалией, когда ширина задних отделов тела бокового желудочка была менее 2 см. Следует отметить, что расширение задних отделов 3-го желудочка у плодов с пороком Арнольда-Киари отмечено в половине случаев в каждой из групп (см. табл. 1).
Без четкой корреляции со сроком беременности у плодов с пороком Арнольда-Киари при горизонтальных сканированиях выявлена характерная, заостренная кзади («ланцетоподобная»), форма задних отделов тела бокового желудочка, которая в абсолютном числе наблюдений коррелировала с характерными изменениями формы боковых желудочков при фронтальных сканированиях.
При обследованиях мозга плодов во фронтальных плоскостях тело бокового желудочка на протяжении от отверстия Монро до треугольника приобретало дополнительную латеральную стенку. Следует отметить тенденцию к учащению появления этого признака у плодов с увеличением гестационного срока (см. табл. 2). Подобная тенденция наблюдалась также в эхографическом выявлении асимметрии расположения сосудистых сплетений боковых желудочков (рис. 6). Искривления мозолистого тела и асимметрия борозд медиальных поверхностей полушарий чаще отмечались у плодов во 2 и 3 группах. Отсутствие прозрачных перегородок не коррелировало с гестационным возрастом.
| Признак порока (особенность) | Число случаев и процент к числу наблюдений в группах | ||
|---|---|---|---|
| 1 (n=18) | 2 (n=17) | 3 (n=20) | |
| Атипичность субарахноидальных пространств лобных долей | 6 (33,3%) | 13 (76,4%) | 16 (80,0%) |
| Изменение формы боковых желудочков | 8 (44,4%) | 12 (70,5%) | 19 (95,0%) |
| Асимметрия расположения сосудистых сплетений боковых желудочков | 11 (61,1%) | 13 (76,4%) | 15 (75,0%) |
| Искривление молозистого тела и асимметрия борозд медиальных поверхностей полушарий | 3 (16,6%) | 5 (29,4%) | 9 (45,0%) |
| Отсутствие прозрачной перегородки | 2 (11,1%) | 3 (17,6%) | 3 (15,0%) |
При фронтальных сканированиях через лобные доли у плодов с синдромом Арнольда-Киари во 2 и 3 группах (см. табл. 2) выявлено частое атипичное изображение латеральных субарахноидальных пространств лобных долей, которое проявлялось в резком сужении или даже в полном их отсутствии при сроках беременности менее 34 недель.
Резкое удлинение ножек мозга и моста, отмеченное при сагиттальных сканированиях у плодов с пороком Арнольда-Киари, в подавляющем большинстве случаев (см. табл. 3) характеризовалось увеличением расстояния (2 см или более) между задней поверхностью валика мозолистого тела и верхней поверхностью червячка мозжечка (см. рис. 5). Следует отметить, что при наличии порока Арнольда-Киари I типа удлинение ножек мозга и моста было незначительным (см. рис. 4). Во всех случаях диагностики порока Арнольда-Киари I типа выявлялось, прежде всего, отсутствие большой цистерны, а также отмеченные выше другие признаки этой аномалии.
| Признак порока (особенность) | Число случаев и процент к числу наблюдений в группах | ||
|---|---|---|---|
| 1 (n=18) | 2 (n=17) | 3 (n=20) | |
| Отсутствие большой цистерны вследствие смещения мозжечка | 12 (66,6%) | 16 (94,1%) | 19 (95,0%) |
| Резкое удлинение ножек мозга и моста | 17 (94,4%) | 15 (88,2%) | 19 (95,0%) |
Обсуждение
Анализируя результаты настоящего исследования (см. табл. 1), при использовании горизонтальных плоскостей сканирования совокупная выявляемость таких признаков порока Арнольда-Киари, как «лимон» и «банан», составила не более 45% при сроке гестации до 22 недель и 24% при беременности до 28 недель. Вентрикуломегалия (увеличение ширины задних отделов тела бокового желудочка или atrium более 1,0 см) встретилась в 61, 76 и 85% (в 1,2 и 3 группах соответственно). Однако по данным Американского института ультразвука в медицине вентрикуломегалия при ширине задних отделов тела бокового желудочка более 1,5 см абсолютно точно устанавливается лишь в 53% случаев [10]. Затруднительное выявление или полное отсутствие визуализации мозжечка в сочетании с выявлением «ланцетовидной» формы задних отделов тела боковых желудочков и расширения надшишковидного кармана 3-го желудочка, по нашему мнению, по своей информативности значительно превосходят другие критерии порока Арнольда-Киари и менингомиелоцеле при горизонтальных сканированиях (см. табл. 1). Достаточную помощь в постановке диагноза порока Арнольда-Киари может также оказать определение вентрикуломегалии с отсутствием признаков расширения передних отделов 3-го желудочка. На это указывают как данные настоящего исследования, так и результаты ультразвуковых обследований у новорожденных с менингомиелоцеле [12].
Отсутствие в литературе данных по применению фронтальных и сагиттальных плоскостей сканирования у плодов с Spina Bifida или синдромом Арнольда-Киари несколько затрудняет интерпретацию результатов, полученных в ходе настоящего исследования (см. табл. 2, 3). Однако они не противоречат как патоморфологическим представлениям о макроскопической организации порока, так и данным постнатальных исследований мозга с применением различных визуальных методов [2, 3,11,12].
Результаты эхографических обследований, приведенные в табл. 2, указывают на наличие ряда особенностей мозга, которые могут быть выявлены при использовании фронтальных сканирований у плодов с менингомиелоцеле. Несмотря на высокую выявляемость (см. табл. 2) таких признаков, как атипичность субарахноидальных пространств лобных долей, изменение формы боковых желудочков и асимметрию сосудистых сплетений и борозд, эти критерии, по-видимому, отражают больше вторичные общие дизонтогенетические изменения мозга, связанные с различными вариантами аномального развития ЦНС [14]. Вместе с тем выявление таких особенностей может способствовать более точной диагностике аномального головного мозга и дополнять картину прогноза в каждом конкретном случае.
Обнаружение признаков аномалии Арнольда-Киари у плода может явиться показанием к исключению дефектов развития позвоночника (включая инвазивные), при этом даже полное отсутствие ультразвуковой информации о состоянии позвоночника указывает на наличие Spina Bifida более чем в 95% случаев.
Таким образом, выполненное исследование показало, что использование не только горизонтальной, но и других плоскостей сканирования (фронтальной, сагиттальной), позволяет выявить ряд высокоинформативных критериев аномалии Арнольда-Киари у плода. Эхографический диагноз этого порока при использовании совокупности плоскостей и учета перечисленных выше признаков не должен представлять затруднений в подавляющем большинстве случаев после 16-й недели гестации.
Литература
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.