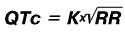нормоадаптация qt к rr интервалу что это
Синдром удлиненного интервала QT и псевдогипопаратиреоз. клинический случай
Опубликовано в журнале: «ПРАКТИКА ПЕДИАТРА»; июнь; 2016; стр. 40-48.
Ключевые слова: дети, синдром удлиненного интервала QT, псевдогипопаратиреоз, наследственная остеодистрофия Олбрайта, гипокальциемия, диагностика, резистентность к паратиреоидному гормону.
Keywords: children, syndrome long QT interval, pseudohypoparathyroidism, Albright hereditary osteodystrophy, hypocalcemia, diagnostics, parathyroid hormone resistance.
В течение последних двух десятилетий значительный прогресс в понимании электрофизиологических основ внезапной аритмической смерти во многом был обусловлен интенсивными исследованиями синдрома удлиненного интервала QT (СУИQT), при котором имеется высокий риск внезапной сердечной смерти (ВСС) вследствие развития жизнеугрожающих желудочковых аритмий. Для клиницистов, помимо выявления синдрома удлиненного интервала QT, чрезвычайно важным является установить первичную или вторичную его формы. От этого полностью зависит выбор тактики лечения и прогноз.
Синдром удлиненного интервала QT (СУИQT) встречается в виде первичного (наследственные синдромы Романо-Уорда, Джервелла-Ланге-Нильсена и спорадические формы, обусловленные специфическими генными мутациями) и вторичного вариантов. Наследственный СУИQT является заболеванием с высоким риском внезапной сердечной смерти, относится к генетически детерминированным первичным электрическим заболеваниям сердца и характеризуется удлинением интервала QT на электрокардиограмме (ЭКГ) покоя, приступами потери сознания вследствие развития тахикардии типа «пируэт» и фибрилляции желудочков. С момента открытия синдрома до настоящего времени это заболевание служит уникальной моделью для изучения патофизиологии, электрокардиографических проявлений, молекулярногенетических механизмов, а также факторов риска внезапной аритмической смерти [1, 2].
В патогенезе СУИQT ведущая роль принадлежит генам, кодирующим трансмембранные ион-селективные каналы. При СУИQT мутации найдены в генах, кодирующих калиевые, натриевые и кальциевые каналы, мембранные переносчики, а также некоторые структурные белки, локализованные на 3, 4, 7, 11, 12, 17, 20 и 21-й хромосомах. Большинство идентифицированных генетических дефектов при СУИQT относится к мутациям, нарушающим структуру кодируемого белка [3, 4]. Молекулярно-генетические варианты синдрома и характер мутаций определяют электрофизиологические особенности и клиническую картину заболевания. В то же время, несмотря на различия, все варианты СУИQT объединяются общими фенотипическими проявлениями. Клиническая диагностика синдрома основана на критериях, впервые предложенных в 1985 г. P. Schwartz и уточненных автором в 1993 г. [5]. Диагноз складывается из: 1) анализа предшествующей истории обмороков («синкопальных эпизодов»); 2) семейного анамнеза, включающего случаи ВСС в возрасте моложе 40 лет; 3) оценки специфических изменений ЭКГ [6, 7, 8].
Для клиницистов, помимо выявления синдрома удлиненного интервала QT, чрезвычайно важным является установить первичную или вторичную его формы. От этого полностью зависит выбор тактики лечения и прогноз.
Вторичный синдром удлиненного интервала QT провоцируется приемом лекарственных препаратов, может развиваться на фоне низкокалорийной диеты, при психогенных заболеваниях, заболеваниях ЦНС, при нарушениях метаболизма, вегетативной дисфункции, вследствие нарушения функции паращитовидных желез, электролитных нарушениях, токсического действия лекарственных препаратов [8].
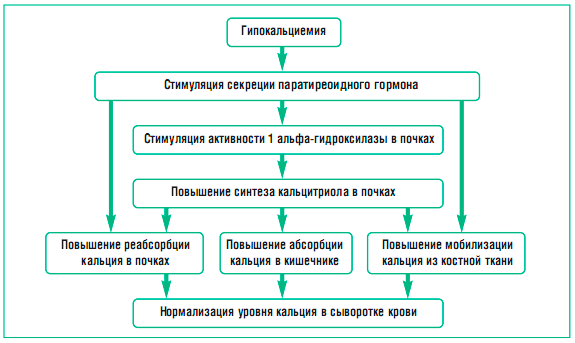
Нормальное протекание всех жизненно важных процессов в организме обеспечивается за счет поддержания кальция в плазме крови в очень узких пределах, контролируемых паратгормоном (ПГТ) и метаболитами витамина D. Мишенями этих гормонов являются: костная ткань, почки и тонкая кишка. Концентрации кальция и фосфора во внеклеточной жидкости взаимосвязаны: любые изменения одного из ионов приводят к обратному изменению концентрации другого. Регуляция фосфорно-кальциевого обмена и эффекты паратиреоидного гормона представлены на схеме 1. Клинические проявления гипокальциемии:
Схема 1
Регуляция фосфорно-кальциевого обмена (эффекты паратиреоидного гормона)
Заболевание описано впервые швейцарским терапевтом Eric Martin с соавторами в 1940 г. и американским врачом-эндокринологом Fuller Albright с соавторами в 1942 г. Характеризуется аутосомно-доминантным типом наследования [13].
Известен ген, ответственный за развитие заболевания. Ген GNAS1 (Guanine Nucleotide-binding protein, Alpha-Stimulating activity polypeptide 1) локализован на хромосоме 20 в регионе 20q13, содержит 13 экзонов; кодирует стимулирующую aльфа-субъединицу G-белка (Gsa). Патогенез: белок Gs-альфа является посредником между рецепторами гормонов на поверхности клеток-мишеней и аденилатциклазой, которая катализирует синтез циклического аденозинмонофосфата, запуская реакцию клеток на воздействие гормонов. Мутантные белки Gs-альфа не активируют аденилатциклазу либо их активность сильно снижена. У больных ПГПТ типа 1А активность Gs-aльфа в 2 раза ниже, чем у здоровых людей, поэтому реакция клеток-мишеней на ПГТ ослаблена [14, 15].
Дифференциальная диагностика различных типов ПГПТ представлена в табл. 1.
Таблица 1
| 28 01 2016 | 02 02 2016 | норма | |
| Кальций общий | 1,51 | 1,66 | 2,02-2,60 мМоль/л |
| Са 2 + (ионизированный) | 0,66 | 0,74 | 1,13-1,32 мМоль/л |
| Фосфор неорганический | 3,21 | 3,23 | 1,30-2,26 мМоль/л |
Псевдогипопаратиреоз, критерии диагноза:
Лечение при псевдогипопаратиреозе:
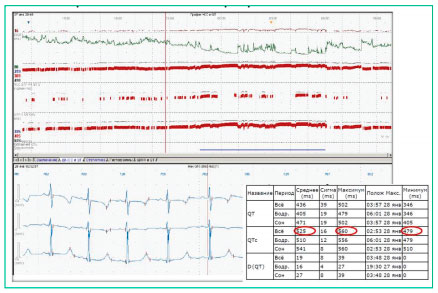
По данным холтеровского мониторирования (рис. 3) имеет место незначительная тахикардия в течение суток; отмечено удлинение интервала QT в течение всего времени исследования; QTmax = 475 мс, meanQTс = 525, maxQTc = 580 мс.
Рисунок 3
Холтеровское мониторирование ЭКГ
По данным ЭХО-КГ структурной патологии не выявлено; имеет место тенденция к снижению систолической функции левого желудочка; обращает внимание отсутствие ускоренного электромеханического проведения и удлинение ВИР, типичных для первичного синдрома удлиненного интервала QT
По данным тредмил-теста функциональная способность снижена, ответ ЧСС на нагрузку снижен; отмечено удлинение интервала QTc в исходе QTc = 466-475 мс без динамики продолжительности интервала QTc на нагрузке, нарушений ритма и проводимости в течение времени исследования не зарегистрировано.
Таблица 2
Дифференциальная диагностика различных типов псевдогипопаратиреоза
| Типы ПГПТ | Гипокальциемия Гиперфосфатемия | Паратгормон крови | Дефицит субъединицы альфа Gбелка | Экскреция цАМФ с мочой (тест Элсворса-Говарда) | Резистентность к другим гормонам (кроме ПТГ) |
| IA | + | ↑ | + | ↓ | + |
| IB | + | ↑ | — | ↓ | — |
| IC | — | N | + | N | + |
| II | + | ↑ | — | N | — |
УЗИ щитовидной железы без патологии.
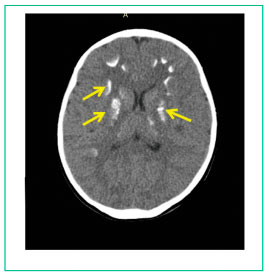
Рисунок 4
Множественные кальцинаты в веществе головного мозга (желтые стрелки).
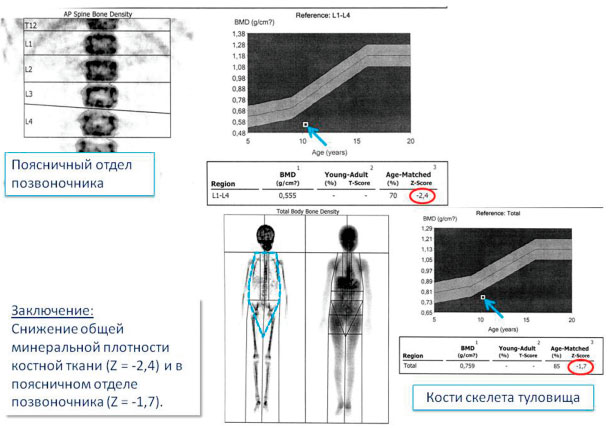
Рисунок 5
Денситометрия (снижение минеральной плотности костной ткани).
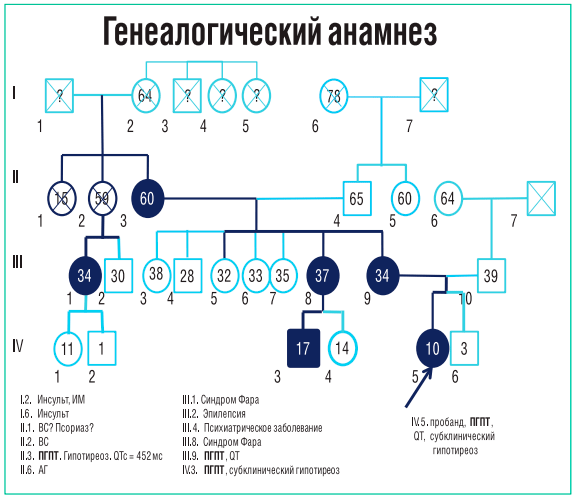
Проведено комплексное обследование родственников пробанда. У матери и бабушки по линии матери выявлены аналогичные изменения: гипокальциемия, гиперфосфатемия, гиперпаратиреоз, синдром удлиненного интервала QT. Родословная после уточнения диагноза представлена на рис. 6.
Рисунок 6
Фрагмент родословной Софьи Т., 10 лет (после обследования родственников и уточнения диагноза)
Сходство ряда клинических и биохимических признаков, которые имелись у пробанда, обуславливали необходимость проведения дифференциального диагноза с рядом патологических состояний, сопровождающихся гипокальциемией:
1. Гипопаратиреоз (с которым в первую очередь проводился дифференциальный диагноз) был исключен в связи с высоким уровнем ПГТ у нашей пациентки (при гипопаратиреозе уровень ПТГ снижен).
2. Рахитоподобные заболевания (РПЗ) (при которых часто отмечается гипокальциемия) были исключены, ввиду отсутствия у пробанда типичных для РПЗ рахитических деформаций скелета и характерных лабораторных и рентгенологических изменений.
На основании совокупности критериев:
ребенку выставлен основной диагноз: псевдогипопаратиреоз (МКБ X: Е20.1). Первичный гипотиреоз. Осложнение основного диагноза: синдром удлиненного интервала QT, синкопальная форма (МКБ X: 145.8)
Заключение: представленное клиническое наблюдение демонстрирует сложности дифференциально-диагностического поиска, важность своевременного исследования простых биохимических параметров (при синдроме удлиненного интервала QT, эпилепсии, выявлении эктопических кальцинатов обязателен скрининг показателей фосфорно-кальциевого обмена); необходимость интегрировать отдельные признаки в общий фенотип патологического состояния для целенаправленной своевременной диагностики наследственных заболеваний. Своевременная и ранняя диагностика позволяет найти оптимальный подход к лечению, профилактике осложнений и предупреждению повторного возникновения заболевания в семье (медико-генетическое консультирование). Это диктует необходимость врачам различных специальностей четко ориентироваться в потоке наследственно обусловленной патологии.
Синдром укороченного интервала QT
Синдром укороченного интервала QT — это новый и еще недостаточно изученный вариант нарушения ритма, который сегодня выделяется как важный проаритмогенный фактор и предиктор внезапной сердечной смерти. Развитие этого состояния связывают с несколькими генетическими мутациями. У большинства больных синдром протекает без клинических проявлений, реже он манифестирует головокружениями, предобморочными и синкопальными состояниями. С диагностической целью проводятся ЭКГ, суточное мониторирование по Холтеру, другие инструментальные методы (Эхо-КГ, кардиальное ЭФИ). Единственный эффективный вариант лечения — установка дефибриллятора-кардиовертера.
МКБ-10
Общие сведения
В клинической кардиологии более известен синдром удлиненного QT, который зачастую связан с внезапной смертью молодых людей. Обратное состояние ‒ синдром укороченного интервала QT ‒ было описано только в 2000 г., а детальные клинические наблюдения за пациентами с такой патологией проведены в 2005 г. Истинная частота встречаемости этого типа расстройств ритма не установлена из-за сложности диагностики и отсутствия ярких клинических признаков, однако ученые предполагают большую распространенность проблемы в популяции.
Причины
Большинство ученых сходятся во мнении, что развитие синдрома укороченного QT связано с генетически детерминированными нарушениями процесса возбуждения в проводящей системе сердца. Это объясняет частые семейные случаи внезапной смерти при отсутствии органических кардиальных патологий. Мутации наследуются по аутосомно-доминантному типу. Выделяют следующие типы поврежденных генов, ответственных за возникновение синдрома:
Помимо генетических мутаций, уменьшению интервала могут способствовать внешние факторы. Наиболее опасными считаются учащение сердцебиения, повышение температуры тела, увеличение содержания калия и кальция в крови. Независимым фактором риска является дисбаланс вегетативной нервной системы с преобладанием тонуса симпатических нервов.
Патогенез
Электрофизиологическая основа синдрома укороченного интервала QT — ускорение второй фазы потенциала действия в миокарде правого желудочка. Патология возникает вследствие генетически обусловленного дефекта калиевых каналов, что приводит к усиленному выходу калиевых ионов из внутриклеточной жидкости, ионному дисбалансу. Роль в патогенезе синдрома играет гиперсимпатикотония, которая угнетает работу кальциевых каналов и усугубляет имеющиеся нарушения.
Чтобы определить, насколько укороченным является интервал, существует специальная формула, которая выглядит как «656/(1+ЧСС/100)». По этой формуле рассчитывается нормальный интервал в миллисекундах (мс) при соответствующей частоте сердечных сокращений. Синдром укороченного интервала устанавливается, если показатель составляет менее 88% от нормы. Выделено 2 варианта заболевания: постоянное идиопатическое укорочение, парадоксальное (брадизависимое) уменьшение интервала QT.
Симптомы
Главным клиническим проявлением синдрома служат синкопальные состояния — кратковременные эпизоды потери сознания, возникающие в сочетании с аритмией, нарушениями кровоснабжения головного мозга. Несмотря на быстроту развития симптоматики, при синкопе выделяется 3 последовательных фазы: пресинкопальное состояние, собственно синкопе постсинкопальное состояние. Большинство случаев начинаются в момент физической нагрузки или сразу после ее прекращения.
Пресинкопальная (липотимическая) фаза длится до нескольких минут. Пациенты ощущают внезапную нарастающую слабость, тошноту, головокружение и мелькание «мушек» перед глазами. Как правило, беспокоят шум и заложенность в ушах, человек предчувствует, что скоро он потеряет сознание. Кардиогенному обмороку могут предшествовать стеснение в грудной клетке, чувство нехватки воздуха, ощущение замирания сердца.
Второй этап представляет собой обморок — потерю сознания с резким снижением мышечного тонуса, вследствие чего человек падает. Объективно отмечается бледность кожных покровов, снижение АД, слабая наполненность пульса. Кардиогенное синкопе продолжается несколько минут, после чего сознание возвращается к больному. Постсинкопальный период длится от нескольких минут до нескольких часов, проявляется слабостью, повышенной потливостью, неуверенностью движений.
Осложнения
Диагностика
При физикальном обследовании врачу-кардиологу не удается обнаружить признаки, патогномоничные для синдрома укороченного QT. Исключение составляет сочетание патологии с фибрилляцией предсердий или желудочков, которая характеризуется выраженными объективными симптомами. Для диагностики нарушения длины интервала пациенту назначается расширенное обследование, куда входят следующие методы:
Генетическое исследование. При секвенировании генома можно обнаружить типичные для данного синдрома мутации, однако ввиду недостаточного объема данных по этому заболеванию и сложности исследования генетические тесты используются ограниченно.
Лечение синдрома укороченного интервала QT
При укороченном интервале QT стандартные противоаритмические препараты не демонстрируют должной эффективности, поэтому их применение нецелесообразно. Современные научные данные показывают позитивное действие алкалоидов коры хинного дерева на удлинение рефрактерного периода желудочков, предупреждения вентрикулярных аритмий. Основным методом остается хирургическое лечение — имплантация кардиовертера-дефибриллятора, которая проводится при:
Кардиовертер-дефибриллятор (ИКД) устанавливается малоинвазивным методом с использованием эндоваскулярного доступа. Такой способ сокращает период реабилитации пациентов, снижает риск послеоперационных осложнений. В периоде восстановления больным необходимо выполнять рекомендации по двигательному режиму и физическим нагрузкам, регулярно посещать кардиолога для контроля сердечной деятельности.
Прогноз и профилактика
Прогноз зависит от того, насколько укороченным при расчётах является QT, наличием или отсутствием клинических симптомов болезни, состоянием сердечно-сосудистой системы. При ранней диагностике и постановке ИКД прогноз относительно благоприятный. Для снижения риска жизнеугрожающих нарушений ритма пациентам с синдромом укороченного QT рекомендовано избегать тяжелых физических нагрузок, сильных эмоциональных стрессов. Эффективные меры первичной профилактики пока не разработаны.
Удлинение интервала QT
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
МГМСУ имени Н.А. Семашко
В последние годы в клинической кардиологии проблема удлинения интервала QT привлекает к себе пристальное внимание отечественных и зарубежных исследователей как фактор, приводящий к внезапной смерти. Установлено, что как врожденные, так и приобретенные формы удлинения интервала QT являются предикторами фатальных нарушений ритма, которые, в свою очередь, приводят к внезапной смерти больных.
Синдром удлинения QT интервала представляет собой сочетание удлиненного интервала QT стандартной ЭКГ и угрожающих жизни полиморфных желудочковых тахикардий (torsade de pointes – «пируэт»). Пароксизмы желудочковых тахикардий типа «пируэт» клинически проявляются эпизодами потери сознания и нередко заканчиваются фибрилляцией желудочков, являющихся непосредственной причиной внезапной смерти.
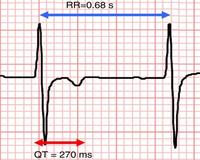
Длительность интервала QT зависит от частоты сердечных сокращений и пола пациента. Поэтому используют не абсолютную, а корригированную величину интервала QT (QTc), которую расчитывают по формуле Базетта
где: RR – расстояние между соседними зубцами R на ЭКГ в сек.;
К = 0,37 для мужчин и К = 0,40 для женщин.
Удлинение интервала QT диагностируют в том случае, если длительность QTc превышает 0,44 с.
Наиболее распространенная методика выявления дисперсии QT – регистрация стандартной ЭКГ в течение 3–5 минут при скорости записи 25 мм/час. Используют также холтеровское мониторирование ЭКГ, что позволяет анализировать колебания дисперсии QTс (QTcd) в течение суток. Однако ряд методологических аспектов данного метода находятся в стадии разработки. Так, отсутствует единое мнение о верхней границе нормальных значениях дисперсии корригированного интервала QT. По мнению одних авторов, предиктором желудочковых тахиаритимий является QTcd более 45, другие исследователи предлагают считать верхней границей нормы QTcd 70 мс и даже 125 мс.
Cуществуют два наиболее изученных патогенетических механизма аритмий при синдроме удлиненного QT интервала. Первый – механизм «внутрисердечных нарушений» реполяризации миокарда, а именно, повышенная чувствительность миокарда к аритмогенному эффекту катехоламинов. Второй патофизиологический механизм – дисбаланс симпатической иннервации (снижение правосторонней симпатической иннервации вследствие слабости или недоразвития правого звездчатого ганглия). Эта концепция подтверждается на моделях с животными (удлинение QT интервала после правосторонней стеллэктомии) и результатами левосторонней стеллэктомии в лечении резистентных форм удлинения QT интервала.
Этиология синдрома удлинения интервала QT
У здоровых людей в покое имеется лишь незначительная вариабельность процессов реполяризации, поэтому дисперсия интервала QT минимальна. Причины удлинения интеврала QT условно делят на 2 группы – врожденные и приобретенные [1].
Врожденные формы синдрома удлинения QT интервала становяся одной из причин смерти детей. Смертность при нелеченных врожденных формах данного синдрома достигает 75%, при этом 20% детей умирают в течение года после первой потери сознания и около 50% – в первое десятилетие жизни. К врожденным формам синдрома удлиненения интервала QT относят синдром Gervell и Lange–Nielsen и синдром Romano–Ward. Синдром Gervell и Lange–Nielsen – редкое заболевание, имеет аутосомно–рецессивный тип наследования и представляет собой сочетание врожденной глухонемоты с удлинением интервала QT на ЭКГ, эпизодами потери сознания и нередко заканчивается внезапной смертью детей в первое десятилетие жизни. Синдром Romano–Ward имеет аутосомно–доминантный тип наследования с популяционной частотой 1:10 000–1:15 000 и пенетрантностью гена 0,9. Он имеет сходную клиническую картину: нарушения ритма сердца, в ряде случаев с потерей сознания на фоне удлиненного интервала QT у детей без нарушения слуха и речи.
Частота выявления удлиненного интервала QT у детей школьного возраста с врожденной глухонемотой на стандартной ЭКГ достигает 44%, при этом почти у половины из них (около 43%) отмечались эпизоды потери сознания и пароксизмы тахикардии. При суточном мониторировании ЭКГ почти у 30% из них зарегистрированы пароксизмы наджелудочковой тахикардии, примерно у каждого пятого – «пробежки» желудочковой тахикардии типа «пируэт» [1].
Для диагностики врожденных форм синдрома удлинения QT интервала в случае пограничного удлинения и/или отсутствия симптомов предложен набор диагностических критериев. «Большие» критерии – это удлинение QT интервала более 0,44 мс, наличие в анамнезе эпизодов потери сознания и наличие синдрома удлинения QT интервала у членов семьи. «Малые» критерии – это врожденная нейросенсорная тугоухость, эпизоды альтернации Т–волн, медленный сердечный ритм (у детей) и патологическая желудочковая реполяризация. Наибольшее диагностическое значение имеют достоверное удлинене QT–интервала, пароксизмы тахикардии torsade de pointes и эпизоды синкопе.
Врожденный синдром удлинения интервала QT – генетически гетерогенное заболевание, в которое вовлечены более 5 различных локусов хромосом. Установлено, как минимум, 4 гена, определяющих развитие врожденного удлинения интервала QT.
Наиболее распространенной формой синдрома удлинения интервала QT у молодых лиц является сочетание данного синдрома с пролапсом митрального клапана. Частота выявления удлинения интервала QT у лиц с пролапсами митрального и/или трикуспидального клапанов достигает 33% [2]. По мнению большинства исследователей, пролапс митрального клапана является одним из проявлений врожденной дисплазии соединительной ткани. Среди других проявлений «слабости соединительной ткани» – повышенная растяжимость кожи, астенический тип телосложения, воронкообразная деформация грудной клетки, сколиоз, плоскостопие, синдром гипермобильности суставов, миопия, варикозное расширение вен, грыжи. Рядом исследователей выявлена взаимосвязь увеличенной варибельности QT интервала и глубины пролабирования и/или наличия структурных изменений (миксоматозная дегенерация) створок митрального клапана. Одной из главных причин формирования удлинения интервала QT у лиц с пролапсом митрального клапана является генетически предопределенный или приобретенный дефицит магния [1, 2].
Приобретенное удлинение QT интервала может возникнуть при атеросклеротическом или постинфарктном кардиосклерозе, при кардиомиопатии, на фоне и после перенесенного мио– или перикардита. Увеличение дисперсии интервала QT (более 47 мс) может также являться предиктором развития аритмогенных синкопальных состояний у больных с аортальными пороками сердца.
Отсутствует единое мнение о прогностическом значении увеличения дисперсии интервала QT у больных постинфарктным кардиосклерозом: часть авторов выявили у этих пациентов четкую взаимосвязь между увеличением продолжительности и дисперсии интервала QT (на ЭКГ) и риском развития пароксизмов желудочковой тахикардии, другие исследователи подобной закономерности не обнаружили. В тех случаях, когда у пациентов с постинфарктным кардиосклерозом в покое величина дисперсии интервала QT не увеличина, следует оценить этот параметр при проведении пробы с физической нагрузкой. У больных постинфарктным кардиосклерозом оценку дисперсии QT на фоне нагрузочных проб многие исследователи считают более информативной для верификации риска желудочковых нарушений ритма.
Удлинение интервала QT может наблюдаться и при синусовой брадикардии, атриовентрикулярной блокаде, хронической цереброваскулярной недостаточности и опухоли головного мозга. Острые случаи удлинения интервала QT могут также возникать при травмах (грудной клетки, черепно–мозговых).
Автономная нейропатия также увеличивает величину интервала QT и его дисперсию, поэтому данные синдромы имеют место у больных сахарным диабетом I и II типов.
Удлинение интервала QT может иметь место при нарушениях электролитного баланса с гипокалиемией, гипокальциемией, гипомагнезиемией. Подобные состояния возникают под воздействием многих причин, например, при длительном приеме диуретиков, особенно петлевых (фуросемид). Описано развитие желудочковой тахикардии типа «пируэт» на фоне удлинения интервала QT cо смертельным исходом у женщин, находившихся на малобелковой диете с целью снижения массы тела.
QT интервал может удлиняться при применении терапевтических доз ряда лекарственных средств, в частности, хинидина, новокаинамида, производных фенотиазина. Удлинение электрической систолы желудочков может наблюдаться при отравлении лекарствами и веществами, оказывающими кардиотоксическое действие и замедляющими процессы реполяризации. Например пахикарпин в токсических дозах, ряд алкалоидов, которые блокируют активный транспорт ионов в клетку миокарда, а также оказывают ганглиоблокирующее действие. Известны также случаи удлинения интервала QT при отравлениях барбитуратами, фосфороорганическими инсектицидами, ртутью.
Представляют интерес данные о суточных ритмах дисперсии QT, полученных при холтеровском мониторировании ЭКГ. Обнаружено достоверное увеличение дисперсии интервала QT в ночные и ранние утренние часы, что, возможно, и повышает риск внезапной смерти в это время у больных с различными сердечно–сосудистыми заболеваниями (ишемия и инфаркт миокарда, сердечная недостаточность и др.). Полагают, что увеличение дисперсии интервала QT в ночные и утренние часы связано с повышенной симпатической активностью в данное время суток.
Общеизвестно удлинение QT при острой ишемии миокарда и инфаркте миокарда. Стойкое (более 5 дней) увеличение интервала QT, особенно при сочетании с ранними желудочковыми экстрасистолами, прогностически неблагоприятно. У этих пациентов выявлено значительное (в 5–6 раз) повышение риска внезапной смерти.
При развитии острой ишемии миокарда также достоверно повышается дисперсия интервала QT. Установлено, что дисперсия интервала QT увеличивается уже в первые часы острого инфаркта миокарда. Отсутствует единое мнение о величине дисперсии интервала QT, которое является четким предиктором внезапной смерти у больных острым инфарктом миокарда [3]. Установлено, что при передних инфарктах миокарда дисперсия более 125 мс – прогностически неблагоприятный фактор, свидетельствующий о высоком риске летального исхода. Ряд авторов выявили еще более значительное повышение дисперсии QT при реперфузии (после коронарной ангиопластики). Однако другие исследователи, наоборот, обнаружили уменьшение дисперсии QT во время реперфузии у больных острым инфарктом миокарда, а увеличение дисперсии QT отметили в тех случаях, когда реперфузия не была достигнута. Поэтому некоторые авторы рекомендуют использовать снижение дисперсии QT интервала в качестве маркера успешной реперфузии. У больных с острым инфарктом миокарда также нарушается циркадный ритм дисперсии QT: она повышена в ночные и утренние часы, что повышает риск внезапной смерти в это время суток.
В патогенезе удлинения QT при остром инфаркте миокарда, несомненно, играет роль гиперсимпатикотония, именно этим многие авторы объясняют высокую эффективность b–блокаторов у этих пациентов. Кроме того, в основе развития данного синдрома лежат и электролитные нарушения, в частности, дефицит магния. Результаты многих исследований свидетельствуют о том, что до 90% больных с острым инфарктом миокарда имеют дефицит магния. Выявлена также обратная корреляционноая взаимосвязь уровня магния в крови (сыворотке и эритроцитах) с величиной интервала QT и его дисперсией у пациентов с острым инфарктом миокарда [1].
Прежде всего следует устранить этиологические факторы, которые привели к удлинению интервала QT в тех случаях, где это возможно. Например, следует отменить или уменьшить дозу медикаментов (диуретики, барбитураты и др.), которые могут увеличивать продолжительность или дисперсию интервала QT. Адекватное лечение сердечной недостаточности, согласно международным рекомендациям, и успешное хирургическое лечение пороков сердца также приведет к нормализации величины интервала QT. Известно, что у больных с острым инфарктом миокарда фибринолитическая терапия уменьшает величину и дисперсию интервала QT (хотя и не до нормальных величин). Среди групп препаратов, которые способны влиять не патогенез данного синдрома, особо следует отметить две группы – b–блокаторы и препараты магния.
Врожденный синдром удлинения интервала QT
Пациентам с синдромами Romano–Ward и Gervell и Lange–Nielsen необходим постоянный прием b–блокаторов в сочетании с пероральными препаратами магния (Магния оротат по 2 табл. 3 раза в день). Левосторонняя стеллэктомия и удаление 4 и 5 грудных ганглиев может быть рекомендовано пациентам, у которых фармакологическая терапия не дала положительного результата. Имеются сообщения об успешном сочетании лечения b–блокаторами с имплантацией искусственного водителя ритма сердца [1].
Для пациентов, нуждающихся в неотложной терапии, препаратом выбора является пропранолол внутривенно (со скоростью 1 мг/мин, максимальная доза – 20 мг, средняя доза – 5–10 мг под контролем АД и ЧСС) либо болюсное внутривенное введение 5 мг пропранолола на фоне внутривенного капельного введения магния сульфата (Кормагнезина) (из расчета 1–2 г сульфата магния (200–400 мг магния) в зависимости от массы тела (в 100 мл 5% раствора глюкозы в течение 30 мин).
У пациентов с идиопатическим пролапсом митрального клапана лечение следует начинать с применения пероральных препаратов магния (Магнерот по 2 табл. 3 раза в день в течение не менее 6 месяцев), поскольку тканевой дефицит магния считают одним из основных патофизиологических механизмов формирования как синдрома удлинения QT интервала, так и «слабости» соединительной ткани. У этих лиц после лечения препаратами магния не только нормализуется величина интервала QT, но и уменьшаются глубина пролабирования створок митрального клапана, частота желудочковых экстрасистол, выраженность клинических проявлений (синдрома вегетативной дистонии, геморрагических симптомов и др.). Если лечение пероральными препаратами магния через 6 месяцев не оказало полного эффекта показано добавление b–блокаторов.
Приобретенный синдром удлинения интервала QT
Должны быть отменены все препараты, способные удлинить QT интервал. Необходима коррекция электролитов сыворотки крови, особенно калия, кальция, магния. В ряде случаев этого бывает достаточно для нормализации величины и дисперсии интервала QT и профилактики желудочковых нарушений ритма.
При остром инфаркте миокарда фибринолитическая терапия и b–блокаторы уменьшают величину дисперсии интервала QT [3]. Эти назначения, согласно международным рекомендациям, являются обязательными у всех больных острым инфарктом миокарда с учетом стандартных показаний и противопоказаний.
Однако даже при адекватном ведении пациентов с острым инфарктом миокарда у немалой части из них величина и дисперсия QT интервала не достигают нормальных величин, следовательно, сохраняется риск внезапной смерти. Поэтому активно изучается вопрос об эффективности применения препаратов магния в острой стадии инфаркта миокарда. Длительность, дозировки и способы введения препаратов магния у этих больных окончательно не установлены. Имеются следующие схемы: внутривенное введение Кормагнезина–400 из расчета 0,5–0,6 г магния в 1 час в течение первых 1–3х суток с последующим переходом на пероральный прием Магнерота (2 табл. 3 раза в течение не менее 4–12 недель). Имеются данные, что у больных острым инфарктом миокарда, получавших подобную терапию, отмечены нормализация величины и дисперсии интервала QT и частоты желудочковых нарушений ритма [1].
При купировании желудочковых тахиаритмий у пациентов с приобретенными формами удлинения интервала QT в схему лечения рекомендуется также добавление внутривенное капельное введение Кормагнезина из расчета 2–4 г сульфата магния (400–800 мг магния) в 100 мл 5% раствора глюкозы в течение 30 минут. В случае необходимости возможно его повторное введение [1].
Таким образом, удлинение интервала QT является предиктором фатальных нарушений ритма и внезапной кардиогенной смерти как у больных с сердечно–сосудистыми заболеваниями (в том числе с острым инфарктом миокарда), так и у лиц с идиопатическими желудочковыми тахиаритмиями. Своевременная диагностика удлинения QT и его дисперсии, в том числе при холтеровском мониторировании ЭКГ и при проведении нагрузочных проб, позволят выделить группу больных с повышенным риском развития желудочковых аритмий, синкопальных состояний и внезапной смерти. Эффективными средствами профилактики и лечения желудочковых нарушений ритма сердца у больных с врожденными и приобретенными формами синдрома удлинения интервала QT являются b–блокаторы в сочетании с препаратами магния.
Магнерот (торговое название)
1. Шилов А.М., Мельник М.В., Санодзе И.Д. Диагностика, профилактика и лечение синдрома удлинения QT интервала. // Методические рекомендации – Москва, 2001 – 28с.
2. Степура О.Б., Мельник О.О., Шехтер А.Б., Пак Л.С., Мартынов А.И. Результаты применения магниевой соли оротовой кислоты «Магнерот» при лечении больных с идиопатическим пролапсом митрального клапана. // Российские медицинские вести, 1999, №2, С.74–76.
3. Макарычева О.В., Васильева Е.Ю., Радзевич А.Э., Шпектор А.В. Динамика дисперсии QT при остром инфаркте миокарда и ее прогностическое значение // Кардиология – 1998 – №7 – С.43–46.